脾硬化性血管瘤样结节性转化6例临床病理分析
2020-12-30叶丹丽刘映文赖续文闫广宁宗嘉雯罗锦霞何文源王卓才
叶丹丽,刘映文,赖续文,闫广宁,宗嘉雯,罗锦霞,何文源,王卓才
脾硬化性血管瘤样结节性转化(sclerosing angiomatoid nodular transformation, SANT)属于罕见的发生在脾脏红髓的结节性病变。1993年Hida等[1]首次提出,2004年Martel等[2]详细描述其病理特征并定义。迄今为止,文献报道不足200例[3]。本文回顾性分析6例脾SANT的临床病理学特征、免疫表型、诊断及鉴别诊断等并复习相关文献,旨在进一步提高临床与病理医师的认识水平,以防误、漏诊。
1 材料与方法
1.1 材料收集2009~2018年中国人民解放军南部战区总医院病理科确诊的6例脾SANT标本。男女各3例,年龄19~50岁,中位年龄31.5岁。1例因肝内占位检查发现,3例有腹部不适或呕血,2例体检发现。5例行B超检查,3例提示实性占位或恶性变(图1),2例提示脾肿大。CT检查4例患者有3例为血管瘤(图2),1例为巨脾。2例行PET/CT检查仅考虑低度恶性和良性病变。肝内占位患者B超检查示脾脏恶性变,PET/CT稍低密度影,代谢未见明显增高,考虑良性病变(表1)。
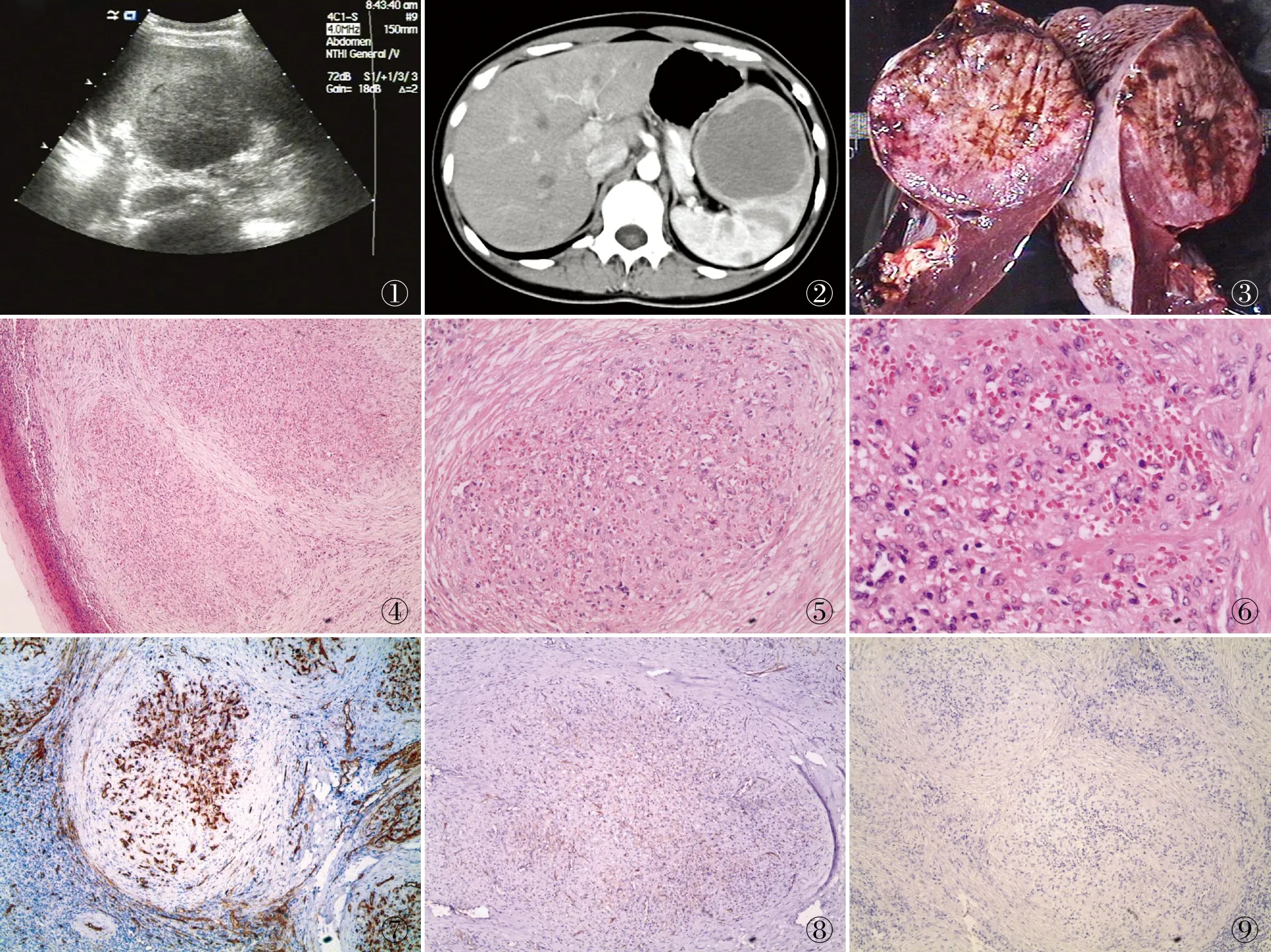
图1 B超检查:脾脏见实性等回声,边界清,形态规则 图2 CT检查:脾脏见一稍低密度肿块影,边界不清,增强后边缘呈强化趋势 图3 灰红色肿物,边界清楚 图4 镜下病变境界清楚,呈结节状分布 图5 结节见形态不一、大小不一的毛细血管 图6 管壁内衬肥胖的上皮,无明显异型 图7 肉芽肿样结节中血管内皮CD34呈弥漫强阳性,EnVision两步法 图8 肉芽肿样结节中血管内皮CD31呈弥漫强阳性,EnVision两步法 图9 原位杂交检测EBER阴性

表1 脾SANT的临床特征
1.2 方法标本均经10%中性福尔马林固定18~24 h,经脱水、浸蜡,常规石蜡包埋并切片,行HE染色、免疫组化染色和原位杂交检测。免疫组化染色采用EnVision两步法,一抗包括CD31、CD34、FⅧRAg、CD8、CD68、SMA、CD21、CD23和IgG4,均购自爱必梦生物公司。
1.3 结果判断免疫组化标记FⅧRAg、SMA、CD68和IgG4定位于细胞质,CD31和CD34定位于细胞质/细胞膜,CD8、CD21和CD23定位于细胞膜,以棕黄色颗粒为阳性。阴性对照采用PBS缓冲液代替一抗。原位杂交检测采用EBER法,试剂盒和胃酶工作液购自爱必梦生物公司,以细胞核着色为阳性;阳性对照为鼻咽癌组织。
2 结果
2.1 眼观脾脏质量190~500 g,大小11 cm×8.5 cm×3.5 cm~13.5 cm×11 cm×4.5 cm。4例单发结节,2例多发,直径0.7~6.5 cm,平均2.8 cm(表1)。切面呈灰红色或灰白色,边界尚清楚(图3),实性,质软或中等硬度,局部可见出血,未见明显坏死。
2.2 镜检低倍镜下病变与周围正常脾脏实质界限清楚,呈圆形或不规则多结节状,其大小不一。高倍镜下结节呈肉芽肿样,由裂隙样、圆形或不规则管腔的血窦样毛细血管构成,腔内可有或无红细胞,有不等量红细胞外渗,少数扩张的毛细血管。血管内皮肥胖,呈短梭形或立方状,无异型性,核分裂象罕见。纤维细胞呈洋葱皮样包绕、分隔结节,纤维细胞无明显异型性及核分裂象,可伴胶原化或黏液样变(图4~6),散在不等量的中性粒细胞、淋巴细胞、浆细胞及吞噬含铁血黄素的组织细胞浸润。
2.3 免疫表型肉芽肿样结节中血管内皮CD34(图7)和CD31(图8)均呈弥漫强阳性,3例CD8呈阳性;脾索样血管中CD34、CD31均呈阳性,CD8呈阴性;裂隙样血管中CD31、CD8均呈阳性,CD34呈阴性;小静脉样血管中CD31呈阳性,CD34、CD8均呈阴性;4例FⅧRAg呈阳性,肉芽肿样结节内血管管壁平滑肌和间质纤维细胞SMA阳性,结节内和结节附近的组织细胞CD68呈阳性。CD21和CD23呈阴性。散在IgG4阳性的浆细胞(<10个/400 HPF)(表2)。

表2 脾SANT免疫表型及原位杂交检测
2.4 EBER检测6例原位杂交检测EBER均阴性(图9)。
3 讨论
SANT是发生于脾脏红髓的罕见病变。1993年由Hida等[1]首次提出,2004年Martel等[2]建议使用“SANT”命名,或称脾非肿瘤性血管瘤样结节性反应性增生、脾结节性血管增生及多结节性血管瘤等。2014年Rosai[4]为了与血管瘤区分,将其归属于脾脏其他原发性肿瘤和瘤样病变。
3.1 临床特点女性略多,年龄3~82岁,中位年龄45岁,多为体检或其他疾病治疗时发现,少有腹痛或其它症状[5]。少数病例可合并结肠癌、恶性黑色素细胞瘤、肾透明细胞癌、血小板减少症等[5-6]。影像学检查:B超示不同的回声信号,提示脾脏占位[7];CT扫描示进行性中央显像,“车辐状”和延迟成像,这种成像模式的特征与SANT病变中纤维结缔组织分割程度有关[8];PET/CT示高代谢活性,可能与SANT的肉芽肿样组织间质富有含铁血黄素巨噬细胞、纤维细胞和慢性炎细胞有关[8]。本组患者无性别差异,中位年龄31.5岁,比文献报道的患者年轻,可能与体检普及和保健意识增强有关,提示脾SANT发病隐匿,无临床特征,实际发病时间可能更早。B超检查与文献报道[7]一致;CT扫描示低密度影,边界不清,密度尚均匀及PET/CT检查低密度占位,边界欠清,放射性摄取未见明显增强,与文献报道[8]不一致。本组中1例合并肝内胆管细胞癌,脾脏的病变可认为是肝肿瘤转移。因此,SANT合并恶性肿瘤时需引起重视,避免误、漏诊。
3.2 病理特征脾脏质量为68~2 720 g,结节直径1.0~17.0 cm,边界清楚,切面灰褐色,白色相间。低倍镜下病变与周围脾脏界限清,呈多结节状,大小不一,形态各异。高倍镜下见结节为肉芽肿样,由裂隙样、圆形或不规则管腔的血窦样毛细血管构成,腔内可含红细胞,可外渗,管腔可扩张。血管内皮细胞肥胖,呈短梭形或立方状,无异型,核分裂象罕见。结节被纤维细胞呈洋葱皮样包绕、分隔,纤维细胞无明显异型及核分裂象,可伴胶原化或黏液变,散在不等量中性粒细胞、淋巴细胞、浆细胞及吞噬含铁血黄素的组织细胞浸润[9-10];免疫组化表达模式有3种,脾索样血管CD34和CD31阳性、CD8阴性;裂隙样血管CD31和CD8阳性、CD34阴性;小静脉样血管CD31阳性,CD34和CD8阴性[2]。 IgG4阳性的浆细胞>10个/400 HPF。本组2例肿瘤为多发结节,大体形态及组织结构和免疫表型与文献报道[2]相似。在2例脾脏多发结节中有1例合并肝胆管细胞癌为首次报道。IgG4阳性的浆细胞<10个/400 HPF,与文献报道[11]不一致。
3.3 发病机制Kuo等[11]认为SANT与EB病毒感染、IgG4相关硬化性疾病[9]、血管增生有关[2,8]。本组病例的组织学缺乏EB病毒感染后淋巴细胞增殖现象,且原位杂交检测EBER阴性,这可能与实验方法的灵敏度或病毒一过性感染有关。虽然组织图像表现为围血管“洋葱皮”样硬化性结构及散在浆细胞浸润,但是IgG4阳性的浆细胞<10个/400 HPF,与文献报道[9,12-13]不一致。因此,单纯认为脾SANT与IgG4相关硬化性疾病有关值得质疑。本组血管内皮中CD34、CD31和CD8的表达与文献报道[2]脾SANT的3个模式相似,但CD34在病变及其周边表达与肝癌中肝窦毛细血管化的内皮表达一致。推测SANT属于肿瘤性病变或与类肿瘤综合征累及相关血管内皮系统有关,但是血管内皮系统的检测未能推测血管周的改变,而IgG4相关硬化性疾病则不能解释血管内皮的病变,另病毒感染影响因素太多。因此,明确其机制需收集更多病例进行深入探讨。
3.4 诊断及鉴别诊断脾SANT临床罕见,常在体检或其他疾病治疗中发现,诊断需排除以下疾病。(1)毛细血管瘤:与脾SANT相似,具有分叶状结构,但免疫组化标记CD8阴性及间质缺乏纤维组织增生,可资鉴别。(2)错构瘤:病变完全由红髓组成,可见窦状裂隙。免疫表型虽有重叠,但脾SANT具有明显的血管瘤样结节和间质洋葱皮样结构。(3)炎性假瘤:梭形的纤维母细胞或肌纤维母细胞增生,但无血管瘤样结构且血管内皮标记CD34、CD31等阴性,易于鉴别。(4)脾贫血性梗死:病变为大片出血坏死,伴纤维化或机化,无结节状的血管瘤样改变。(5)异位胰腺组织:病变腺腔内可有分泌物,无红细胞,免疫组化标记血管内皮标志物阴性。(6)与肠套叠和黏膜脱垂相关的结肠旺炽型血管增生:有肠套叠或黏膜脱落病史,血管呈浸润性生长,但周围无增生的纤维细胞包绕。(7)反应性血管增生:血管内皮细胞以纤维蛋白为中心形成乳头结构,乳头与增生的纤维结缔组织相互吻合成血管网,病变弥漫未形成类似SANT境界清楚的结节,间质也无增生的成纤维母细胞、浆细胞、淋巴细胞及吞噬含铁血黄素的组织细胞。
3.5 治疗及预后SANT属于良性的肿瘤样病变,常行手术切除,术后随访患者未见复发及转移。因脾SANT预后良好且不明确病变性质,对无症状或病变较小者,常采取随访;对有症状或病变较大者,目前推荐手术切除。
