水产养殖环节“非规范药品”使用质量安全风险隐患分析
2020-12-28宋金龙甘金华穆迎春张洪玉韩刚刘璐李晔
宋金龙,甘金华,穆迎春*,张洪玉,韩刚,刘璐,李晔
(1.中国水产科学研究院,农业农村部水产品质量安全控制重点实验室,北京 100141; 2.中国水产科学研究院长江水产研究所,湖北 武汉 430223)
渔药在降低水产养殖发病率和死亡率、提高饵料利用率和促进生长等方面有重要作用,科学合理使用渔药是保证水产品安全的重要措施。2005年渔药地标升级为国标后,经过不断废止更新,目前允许使用的渔药以中草药为主,杀真菌药仅1种,抗菌药12种,驱虫和杀虫药共15种[1],现有的国标渔药无法满足产业需求。加之经过多年使用,多数病原菌、寄生虫等病原体已对国标渔药产生耐药性[2],渔药企业不得不寻求更好的代替途径。
近年来,个别未参加“升标协作组”的企业将没有升为国家标准的原渔药等产品以“非规范药品”名义进行销售[3]。由于“非规范药品”销售企业只需根据企业注册标准进行生产销售,没有明确管理法规监管,市场迅速扩大,呈逐年增长趋势,年销售额估算超过100亿元,占渔药销售总值70%以上,涉及生产企业1 000余家,商品名称10 000余种[4-5]。化学类水质底质改良剂、微生物制剂及免疫增强剂等水产养殖用“非规范药品”的市场规模远大于国标渔药,甚至一些杀虫药、除草剂等 “国标药品”中的主要成分也被包装成“非规范药品”在市场上销售,形成了“乱象多、禁不住、管不了、不清楚”的特殊产业形态[6-7]。
当前,“非规范药品”使用中存在风险研究缺失、成分不明、无生产技术及质量检测标准、产品质量良莠不齐等现象,加之无明确管理法规,监管缺位,水产“非规范药品”市场安全隐患突出,给水产品质量安全带来较大风险[8-10]。近年来,对国家产地水产品兽药残留监控计划中发现的阳性样品进行溯源,多数养殖户均表示未使用过违禁药品,推测有可能是来自“非规范药品”的使用[11]。
2019年,在农业农村部农产品质量安全监管司部署下,中国水产科学研究院质量与标准研究中心牵头组织开展了养殖环节“非规范药品”使用质量安全风险隐患排查和水产养殖用兽药及其它投入品安全隐患排查,共采集样品397个,通过实地调研、测试分析和综合研判,初步掌握了水产养殖环节“非规范药品”安全隐患基本情况,以期为制订更加科学的监管措施提供支撑。
1 材料与方法
1.1 实验材料
供试“非规范药品”通过实地或网络购买,共采集华北、东北、华东、华中及华南等5个水产养殖主产区“非规范药品”样品397个,涵盖北京、天津、河北、黑龙江、辽宁、吉林、湖北、湖南、江苏、安徽、广东及广西等12个省、自治区、直辖市的淡水、海水养殖环节。按照“非规范药品”性质差异分为化学类和微生物类“非规范药品”,其中化学类样品295个,微生物类样品102个。
1.2 化学类“非规范药品”检测方法
1.2.1 样品预处理
将固态、半固态样品“非规范药品”充分均质,称取(5.00 ± 0.05)g于50 mL离心管中,加入500 mg MgSO4(无水),再加入10 mL 含1%甲酸的乙腈溶液,涡旋1 min后超声提取10 min,5 ℃,10 000 r/min 冷冻离心10 min,取出上清液;残渣再加入10 mL 含1%甲酸的乙腈溶液,重复上述提取步骤,合并上清液;上清液经40 ℃旋蒸至干后用1 mL 含1%甲酸的乙腈溶液复溶,取500 μL复溶液加500 μL水混匀,5 ℃、10 000 r/min 离心10 min,再取200 μL上清液加800 μL水混匀,过0.22 μm水相滤膜后上机检测。
液态样品直接准确吸取1 mL于15 mL的离心管中,用超纯水稀释10倍后,5 ℃、10 000 r/min离心10 min,取上清过0. 22 μm水相滤膜后上机检测。
1.2.2 液相色谱/质谱联用检测条件
色谱柱采用Thermo C18柱(150 mm × 2.1 mm,5 μm);柱温:30 ℃;进样量:10 μL;流速:0.2 mL/min;流动相:(A)甲醇,(B)5 mmol乙酸铵+0.1%甲酸水溶液,洗脱梯度:0~2 min,30%~90%A;2~8 min,90%;8~10 min,30%。
电喷雾源正负离子模式(ESI); 检测方式: 飞行时间质谱(TOF-MS)全离子扫描;TOF-MS扫描范围:m/z100~800;电离电压(IS):5 500 V; 雾化气(GS1):55 kPa; 辅助加热气(GS2):55 kPa; 气帘气(CUR):25 kPa; 辅助加热气温度: 550 ℃; 去簇电压(DP):70 V; 在上述质谱条件下,增加信息相关二级全扫描(Information dependent acquisition,IDA),监测响应值超过1 000的化合物,得到其子离子信息,扫描范围:m/z50~800; 碰撞能量(CE):35 eV; 扩展碰撞能量(CES):15 eV。
1.2.3 “非规范药品”成分筛查与定量分析
在确定的色谱-质谱条件下获得化合物飞行时间全扫描和二级质谱图,建立化合物的高分辨二级质谱数据库,包括化合物名称、分子式、CAS 编号、保留时间、相对分子质量及结构式等信息。用Peak View软件中的Master View功能处理采集后的数据,根据各化合物的保留时间、一级精确质量数和质量偏差、同位素峰分布及高分辨二级质谱数据库检索结果进行定性分析,以一级提取离子的峰面积进行定量测定。
1.3 微生物类“非规范药品”检测方法
1.3.1 有效菌和杂菌检测方法
参照《农用微生物菌剂标准》(GB 20287—2006)中农用微生物菌剂产品的技术标准对有效活菌数、霉菌数、粪大肠菌群数和溶血性的检测结果进行判定(表1)[12]。
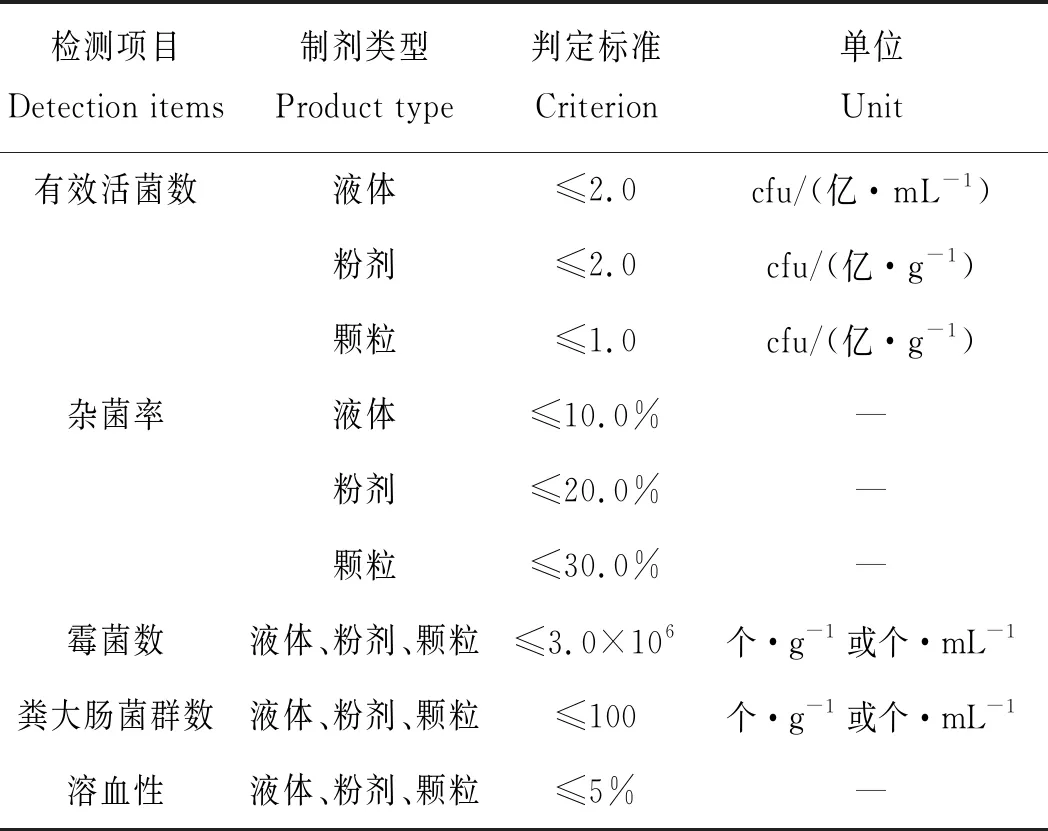
表1 检测项目及判定标准Tab.1 The detection items and the criterion
1.3.2 溶血性检测方法
颗粒或粉剂样品取1 g加入1 mL无菌生理盐水中,制成受试物。每个样品取3支试管,加入无菌脱纤维抗凝兔血和无菌生理盐水(表2),设置阴性对照和阳性对照组。混匀后置于(37.0±0.5) ℃恒温水浴锅中60 min,10 000 r/min离心5 min后取上清,在545 nm波长处测定上清液吸光度。溶血率计算公式为:

式(1)
2 结果
2.1 化学类“非规范药品”检测结果
共评估水产养殖环节化学类“非规范药品”295个,采用高分辨率质谱建立“非规范药品”成分快速筛查平台,该平台可同时对194种抗生素、78种杀虫剂、59种除草剂及58种抗菌剂进行检测。结果显示,化学类“非规范药品”存在添加药品甚至违禁用药情况,检出药品添加样品51个,整体检出率17.29%。
2.1.1 “非规范药品”中药品成分检出和浓度情况
根据《水产养殖用药明白纸》(农业农村部渔业渔政管理局发布,以下简称“明白纸”)中药品类别进行判定,检出禁用药2种(孔雀石绿和克百威),占检出样品总数的3.92%。检出批准用水产兽药4种(甲霜灵、恩诺沙星、辛硫磷和敌百虫),占检出样品总数的31.38%。其他未明确的杀菌剂、除草剂和甚至人用抗生素种类27种,分别为:二甲戊灵、鱼藤酮、敌草隆、红霉素、马拉硫磷、西草净、喹烯酮、替米考星、扑灭津、西玛津、莠灭净、敌敌畏、甲胺磷、啶虫脒、环丙沙星、扑草通、噻嗪酮、苯噻草胺、异丙威、双氯芬酸、扑草净、醚菊酯、己唑醇、吡虫啉、林可霉素、吡蚜酮和特丁净,占检出样品总数的78.43%。
从检出浓度上看,隐性添加药品浓度范围较大,为2.02~28 060.00 mg/kg,其中33个样品超过1 000 mg/kg,涉及药品种类9种,包括红霉素、西草净、鱼藤酮、敌草隆、辛硫磷、替米考星、敌百虫、喹烯酮和二甲戊灵等。
2.1.2 不同类型“非规范药品”检出情况
根据化学类“非规范药品”使用功能上的差异,将其初步分为11类,包含水质或底质改良剂、免疫增强剂、中草药制剂、外用消毒剂、杀菌剂、杀藻与除草剂、化学增氧剂、诱食剂、着色或增色剂、促生长剂及酶制剂。其中杀菌剂检出率最高26.67%,检出样品4个,其次为外用消毒剂检出率26.09%,检出样品6个,中草药制剂检出率25.00%,检出样品7个(图1)。
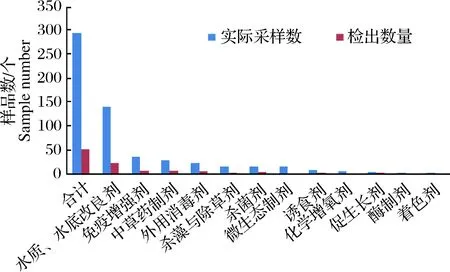
图1 化学类“非规范药品”不同类别的检出情况Fig.1 The detection of different types in chemical “nonspecification drugs”
2.2 微生物类“非规范药品”检测结果
共采集102个微生物类“非规范药品”,参考《农用微生物菌剂标准》(GB 20287—2006)[12],对其检测结果进行判定。从产品质量上看,微生物类“非规范药品”质量问题主要体现在标注微生物与内含菌种不符、有效活菌数不足。从产品安全性上看主要体现在粪大肠菌群、霉菌超标以及具有溶血性。
2.2.1. “非规范药品”质量检测情况
从质量上看,102个样品中24个有效活菌数不足,不合格率23.53%;杂菌超标的36个,不合格率35.29%,其中2个样品未检测到活菌。对照样品包装标注信息,37个样品包装未标注菌含量,未标注率36.27%,16个样品实测菌含量低于包装标注量的60%以上,占包装标注样品总数的24.62%。从实际内含微生物种类上看,36个样品杂菌率超标,不合格率35.29%。102个样品包装标注了数十种微生物,但是仅检出11种具有明确功能的微生物(图2)。
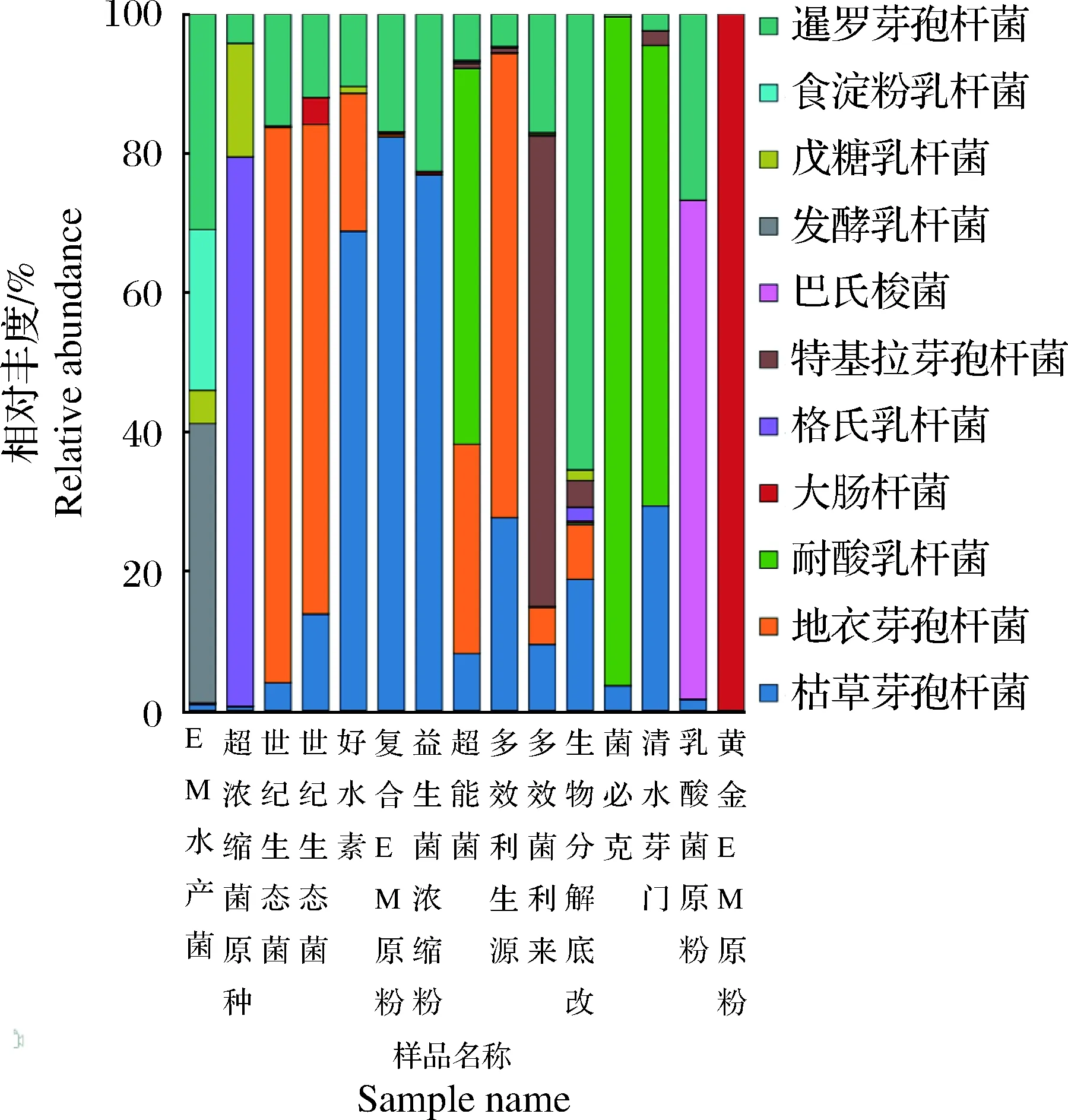
图2 微生物类“非规范药品”菌种种类检测情况Fig.2 The detection of different bacterial species in microbial “nonspecification drugs”
2.2.2 “非规范药品”安全性检测情况
从安全性上看,102个“非规范药品”中,16个样品霉菌超标(复合微生态制剂7个、芽孢杆菌制剂5个及乳酸菌制剂4个),不合格率15.69 %。霉菌最高检出量1.23×107个/g,为标准限量40倍。从粪大肠菌群数上看,11个样品粪大肠菌群数检出量超标,不合格率10.78%。超标样品均为复合微生态制剂,占复合微生态制剂总数32.35%。虽粪大肠菌群样品检出个数相对较少,但检出量严重超标,其中产品名称为“EM水产菌”的样品,粪大肠菌群数2.56×105MPN/mL,为标准限量的2 560倍。8个样品检测出具有溶血性,不合格率7.84%。其中4个乳酸菌制剂检测结果超标,占不合格样品总数50%。从致病菌检测结果上看,本次排查检出2种疑似致病菌,分属弓形杆菌属(Arcobacter)和拟杆菌属(Bacteroides)。
3 风险分析
3.1 化学类 “非规范药品”风险隐患分析
3.1.1 隐形添加禁用药物对水产品质量安全的隐患
从检出药品类别上看,共检出2种禁用药,其中孔雀石绿是一种化工染料,曾一度用于治疗水霉病和对原虫病的控制,其代谢产物无色孔雀石绿在鱼体内和环境中残留时间长,具有潜在的致癌、致畸和致突变等危害[13-14];克百威(呋喃丹)是一种杀虫剂,根据中国农药毒性分级标准,属高毒农药,且持效期长,因此,原农业部第193号公告明确禁止在所有食品动物养殖过程中使用孔雀石绿和克百威[15-18]。禁用药物的隐形添加不仅对养殖环境造成污染,同时对水产动物及人类的健康安全构成风险隐患。
3.1.2 隐形添加其他药品对水产品质量安全的隐患
除禁用药检出以外,其他药品的隐性添加对水产品质量安全的风险隐患也不容小觑。检出的杀藻与除草剂中,二甲戊灵含量最高,其属于苯胺类除草剂,在水产养殖中用于防治车轮虫病害,但易在鱼体肝脏中富集,导致肝脏发生病变,且持效期长[19-21]。其次是敌草隆,其虽属低毒除草剂,但对水生生物有极高毒性,具有潜在致癌风险[22]。二甲戊灵和敌草隆如在水产养殖环节长期使用,可能对养殖水环境、水生生物及人体健康构成安全隐患。检出的抗菌药中,红霉素、环丙沙星、恩诺沙星和替米考星含量均较高,其在水产品中残留会危害人体健康,产生细菌耐药性,加大防治难度[23-25]。检出的杀虫剂中,部分药品对水生生物具有一定的毒性,如鱼藤酮、醚菊酯、敌敌畏、甲胺磷和辛硫磷等[26-29]。其中鱼藤酮对水生生物有极高毒性,多数鱼类的致死浓度为0.025 mg/L[30-31]。
由于检出的所有隐性添加药物均未在产品标签上标识,并且部分“非规范药品”药物成分添加浓度较高,养殖者在不知情的情况下使用,经养殖环境不断蓄积,很容易给水产品和人类健康带来隐患。
3.2 微生物类“非规范药品”风险分析
3.2.1 致病菌对水产品质量安全的隐患
水产养殖业常见致病菌和条件致病菌有副溶血性孤菌(Vibrioparahaemolyticus)、创伤孤菌(Vibriovulnificus)、霍乱孤菌(Vibriocholerae)、沙门氏菌(Salmonella)、气单胞菌(Aeromonas)和大肠埃希氏菌(Escherichiacoli)等。本次排查有2种疑似致病菌(弓形杆菌属、拟杆菌属)和大肠杆菌被检出,其中11个样品大肠杆菌检测结果超标,不合格率10.78%。弓形杆菌主要分离于水体环境、畜禽制品中,可通过水体环境介导到人体肠道环境中,为水源性致病菌,与人类胃肠炎和菌血症有关[32-33]。拟杆菌可寄居于人和动物肠道内,过量寄生会引起人类颅内、腹腔和盆腔内感染[34]。大肠杆菌主要分布在水体环境及人和动物的肠道中,可引起出血性肠炎、溶血性贫血和溶血尿毒症等疾病[35]。
3.2.2 霉菌对水产品质量安全的隐患
霉菌是形成分枝菌丝的真菌的统称,有着极强的繁殖能力,其可通过寄生或分泌有毒代谢产物,使水产养殖动物感染真菌性疾病、产生急性或慢性中毒、严重损伤多种脏器、有致畸或致癌作用[36-38]。霉菌毒素为霉菌分泌的有毒代谢产物,通过饲料或养殖环境进入水产养殖动物体内,通过抑制水产动物免疫机能,引起继发性感染,或引起动物体急性或慢性毒性,严重损害肝脏、肾脏及肠道组织等多种器官[36-37]。本次排查发现16个样品霉菌检测结果超标,不合格率15.69%。本次排查出的水霉病为霉菌寄生在水生动物体表引起的典型真菌类疾病之一,感染部位主要为体表受伤组织,病症表现为早期无明显症状,中期于病灶部位形成灰白色如棉絮状覆盖物,晚期可导致养殖生物细胞组织黏附、皮肤溃烂和肌肉组织大量坏死,严重时可导致死亡[38-39]。
3.2.3 微生物溶血性对水产品质量安全的隐患
溶血性试验是观察受试物是否能够引起细胞溶血和红细胞凝聚等反应,是药物安全性评价的重要组成部分[40-41]。本次排查发现8个样品溶血性检测结果超标,不合格率7.84%。水产养殖病原菌可产生细菌性溶血素,引起红血球细胞溶解,产生溶血性[42]。其中溶血性链球菌(Streptococcushemolyticus)在自然界中分布较广(水、空气、尘埃及粪便),通过直接接触或食用对人类(上呼吸道、下消化道和泌尿生殖道)造成化脓性感染,食用后易引起急性肠胃炎,严重时会引起脱水及其他并发症[43-44]。
4 对策建议
4.1 对“非规范药品”进行分类管理,“应药则药,宜非则非”
考虑到中国水产养殖生产实际,对水产“非规范药品”管理既不能一禁了之,也不能放任其无序发展。建议根据“应药则药,宜非则非”原则,对“非规范药品”实施分类管理使用。对于确有治疗功能除抗菌药以外的“非规范药品”,应加快开展研究和评估工作,建议实施“先登记注册并逐步过渡到审批”的管理政策。如鱼藤酮(杀虫剂)、二硫氰基甲烷(消毒剂)及硫醚沙星(消毒剂)等。
对于环境改良类和微生态制剂类等“非规范药品”,建议组织相关技术力量深入研究,规范使用方法,降低市场准入门槛,借鉴农用肥料登记管理制度进行管理。如有机肥、无机肥类产品,研究建立质量标准和使用规范;微生态制剂类产品,研究建立可以用于水产微生态制剂的微生物菌种名单,加强上市前的质量标准检测和安全性审查。
4.2 继续深入开展“非规范药品”排查和评估工作,将红霉素等纳入国家投入品风险排查计划
在前期排查的基础上,聚焦“非规范药品”排查种类,更加精准地确定筛查目录和范围,增加先锋类、百草枯、草甘膦、沙拉沙星、亚甲基蓝、代森铵和代森锰锌等药品的排查。对已经发现的使用量大、范围广、危害大的药品,如西草净、特丁净和二甲戊灵等开展深入评估,掌握其代谢消除规律,提出防控措施。同时开展抗生素类水产“非规范药品”管控措施研究,掌握主要国家和国际组织对此类物质的管控措施,提出适合国情的管控措施建议。
4.3 规范产品标识说明,加强宣传和技术指导
依据《中华人民共和国产品质量法》、《农产品质量安全法》和《兽药管理条例》等法律法规要求,严格“非规范药品”包装标识。对于产品成分标识不明确、功能标注不实、使用方法不详、成分含量不准或者不标明有效成分的产品等,依法依规进行处罚。同时,借助国家实施食用农产品合格证的历史机遇,通过推行水产品合格证制度,强化落实生产经营者的主体责任,不断加大对养殖户的科普宣传和技术培训,引导养殖生产者科学认识和规范使用“非规范药品”,防范降低盲目用药给水产品造成的安全隐患。
