MgCo2O4超级电容器电极材料的制备及其电化学性能研究
2020-12-21刘万能毛志鹏朱小龙
倪 航,刘万能,毛志鹏,田 玉,朱小龙,郑 广
(江汉大学 光电化学材料与器件教育部重点实验室,化学与环境工程学院,湖北 武汉 430056)
0 引言
能源匮乏和环境污染等问题日益严重,开发可持续的绿色再生能源及相关储能装置亟不可待[1],基于此,研究者们致力于寻找并开发出一种能源节约型、环境友好型、实用便捷的储能器件。超级电容器因拥有充放电速率快、循环寿命长及安全性高等特点,已成为目前研究较多的储能装置。然而超级电容器能量密度低等缺点限制了其应用[2]。由于低容量、低倍率等瑕疵电极材料是引起超级电容器低能量密度的核心因素,解决这一问题的关键在于对兼具较高容量及倍率性能、优异循环稳定性能的电极材料进行研发[3−4]。
在诸多电极材料中,尖晶石型钴基金属氧化物ACo2O4(A= Mg、Cu、Mn、Ni 等)在科学领域中是一类研究普遍的法拉第电容电极材料,因为该尖晶石型钴基金属氧化物中富含两种金属离子,具备良好的电化学性能以及优异的倍率性能。在这类尖晶石型电极材料中,MgCo2O4材料的理论容量可达3 122 F/g,远高于其他钴基金属氧化物[4],但MgCo2O4材料的实际容量比起理论相差甚远,这大部分归于其纳米材料的较低电子电导率、较小的比表面积、是否存在多孔结构等因素。研究表明,尖晶石类型的纳米材料所具备的电容性能主要取决于其颗粒尺寸、比表面积、微观形貌及其结构等[4−5]。在众多纳米结构的材料研究中,具有多孔结构的材料能够极大地增加自身的比表面积,有效地让电解液中更多的离子大幅度接触材料表面,从而提高电极材料的能量密度[4,6]。但传统的超级电容器电极制备工艺使得导电剂、粘结剂以及多孔活性材料三者紧密地聚积,让材料的多孔性结构在一定程度上丧失了本质作用,在宏观上表现为内阻增大,大大削弱了材料的比电容。
本文针对MgCo2O4纳米材料在实际中的应用而展开研究,在传统工艺的基础上,采用尿素水热合成法在泡沫镍上成功地“生长”出片层花状的MgCo2O4材料,直接将其作为工作电极,避免了导电剂、粘结剂粉体的杂乱堆积,有效地增加比表面积、降低内阻,基于此详细地分析了其纳米形貌的优点,论述了其电化学性能。
1 实验材料与方法
1.1 实验试剂
本实验所采用的药品均为分析纯,主要药品信息见表1。

表1 药品信息表Tab.1 Chemical list
1.2 实验方法
先称取 0.444 g 的 Mg(NO3)2·6H2O、1.028 g 的 Co(NO3)2·6H2O 和 1.092 g 的 CO(NH2)2固 体溶解在60 mL 的蒸馏水中,磁力均匀搅拌30 min,形成均匀的深粉红色溶液。把泡沫镍(2 cm ×4 cm)放入超声装置中,3 mol/L 盐酸侵蚀泡沫镍30 min 以去除表面的NiO,分别用丙酮、无水乙醇和去离子水超声10 min,并将其放入真空干燥箱里,60 ℃的条件下干燥5 h。然后将上述溶液转入100 mL 的不锈钢反应釜中,将干燥过的泡沫镍倾斜插入其内胆,拧紧密封,放入真空干燥箱中,在120 ℃的条件下反应6 h。之后分别用去离子水和无水乙醇对粉红色的泡沫镍进行离心洗涤数次,再次置入真空干燥箱中干燥8 h 以后,将样品在空气氛围中350 ℃(升温速率5 ℃/min)煅烧2 h,取出样品。
1.3 实验仪器
X 射线衍射仪(XRD,Xpert Powder)用于产物的纯度和物相分析。产物的形貌表征使用的是场发射扫描电子显微镜(SEM,SU8000),其加速电压为3 kV。材料的电化学性能测试设备为上海辰华仪器公司的CHI660E 型电化学工作站。
如图1 所示,采用三电极体系对所制备的MgCo2O4纳米材料进行电化学性能测试。以“生长”有活性物质的泡沫镍(NF−MgCo2O4,1 cm × 2 cm)直接作为工作电极(WE),其中泡沫镍所承载的活性材料质量约为1 mg,饱和甘汞(Hg/HgO)和铂片(Pt)分别作为参比电极(RE)和对电极(CE)。整个测试在2 mol/L 的KOH 溶液中进行。电化学性能测试包括循环伏安法(CV)、恒电流充放电法(GCD)以及交流阻抗图谱(EIS)。CV 的电压工作范围为0 ~0.5 V,扫描速率为2、8、10 mV/s;GCD 的工作电压区间是 0 ~ 0.5 V,电流密度是 10、8、6、4、2、1 A/g。EIS 的频率是0.001 Hz ~ 100 kHz。

图1 实验三电极体系测试示意图Fig.1 Schematic diagram of the three-electrode test system
2 结果与分析
2.1 晶体表征
图2(a)为MgCo2O4纳米材料的晶体衍射峰图谱即XRD 图谱,图2(b)为以镁原子为棱边的MgCo2O4单 位 晶 胞 。从 图 2(a)中 可 以 看出 ,MgCo2O4纳 米 材料 的 XRD 图谱 在 2θ= 18.71°、31.31°、36.79°、38.67°、44.79°、55.53°、59.29°、65.21°、77.79°分别对应于 MgCo2O4尖晶石晶面(111)、(220)、(311)、(222)、(400)、(422)、(511)、(440)、(533)处的衍射峰,此外所有衍射峰均可与图谱下方的MgCo2O4标准卡片(JCPDS No.81−0667)中的衍射峰位置相吻合,表明在晶体形成过程中晶化强度良好,成功制备出了较纯的MgCo2O4晶体。

图 2 (a)MgCo2O4 晶体衍射峰图谱;(b)MgCo2O4 单位晶胞示意图Fig.2 (a) XRD pattern of MgCo2O4 crystal; (b) Schematic diagram of MgCo2O4 unit cell
2.2 形貌表征
通过对MgCo2O4纳米材料的晶体理论分析,为了进一步对其进行物理表征,采用SEM 观察其微观形貌。图3(a)为MgCo2O4样品的整体形貌,可以看出MgCo2O4是由块型的纳米片层组合而成的片层花状结构,并且它们的大小各异,片层形态单一而又较为均匀。这些片层花状结构较小的尺寸约为7.34 μm,较大的尺寸约为15.38 μm,整体呈现较大尺寸。为了进一步探究图3(a)中的“花层”结构,放大观测倍率得到如图3(b)所示的片层纳米花,“花”的直径数值相当,合成的花状大小较为类似。将图3(a)和图3(b)联合分析可知,若所合成的花状纳米材料的尺寸较大,片与片的空隙较多,材料所具备的比表面积就高,这为提升材料本身容量提供了一个重要的理论依据。为了观察其片层结构中片层厚度以及所形成的空隙具体情况,进一步放大该片层结构(见图3(c)),在图3(c)中可以清晰地发现在每一“朵”花状的材料里,每个纳米片的厚度较为相同,并且纳米片的片层较为光滑,纳米片与纳米片之间相互交叉、交叠,即空隙形成的概率较大,以致于该花状的材料内部留有诸多空隙,这些花状结构里的纳米片厚度相似。同时对图3(c)中的区域里某一纳米片的厚度继续放大进行观察(见图3(d)),在图3(d)中已标出该纳米片层的厚度约为63.9 nm。因此,该片层花状结构中每个片层花结构趋于张开的状态,所具有的片层表面积较大,且在张开的状态下,纳米片与纳米片之间两两相互交叠而展现出了一定的空隙;很明显这样的材料结构在电解液中发生法拉第氧化还原反应时,材料的表面可以大量地吸附溶液中的OH−,以及部分OH−有较大概率能够渗透到空隙中,进而有助于提高该材料的电化学性能。从微观形貌和结构可以推断,较高的比表面积和多空隙是由纳米片层花状组成的MgCo2O4纳米材料的特征,有利于活性材料在进行氧化还原反应时提高材料的比电容。
MgCo2O4纳米材料的整个合成在Mg/Co 盐−CO(NH2)2−H2O 的三元体系中完成。在水热合成过程中,尿素在反应中级阶段发生水解并缓慢释放出NH3和OH−,该过程可协调溶液中的金属离子在泡沫镍上形成Mg、Co 双氢氧化物的微小“种子”。此形成的“种子层”可以看作电镜图中片层花状的MgCo2O4阵列成核的中枢,随着容器内反应的进行,最终在泡沫镍上形成了Mg、Co 双氢氧化物纳米片层花状结构。然后将其通过高温氧化生成尖晶石型的MgCo2O4纳米材料。MgCo2O4纳米材料形成的化学反应式如下:

为了更好地表述SEM 图中在泡沫镍上水热法制备3D 片层花状MgCo2O4的生长过程,采用多孔矩形板替代泡沫镍,给出了其形成示意图(见图4)。

图3 片层花状MgCo2O4 微观形貌Fig.3 Micromorphology of lamellar flower-like MgCo2O4

图4 片层花状MgCO2O4 形成示意图Fig.4 Schematic illustration of lamellar flower-like MgCo2O4
2.3 电化学性能
2.3.1 比电容的计算 本文采用恒电流充放电曲线(GCD)公式计算电极材料的比电容[7],

式中,C是活性物质的比电容(F/g),I是放电电流(A),Δt是放电时间(s),ΔV是测试的电压窗口(V),m是电极片上所承载的活性物质的质量(g),而I m就是通常所说的电流密度J,单位为A/g。
2.3.2 循环伏安性能 在盛有2 mol/L KOH 溶液的三电极体系中,通过运用循环伏安曲线(CV)、恒电流充放电曲线(GCD)以及交流阻抗图谱(EIS)对MgCo2O4纳米材料的电化学性能进行测试。
尖晶石型钴基氧化物具有较高的理论比电容,因其富含两种不同的金属原子。但是绝大部分情况下,具有尖晶石型的晶体结构中占有四面体的金属原子不参与氧化还原反应,是因为其价态无变化[8],对电容量的贡献来自占有八面体的金属原子。CV 测试是一种了解电极材料的电化学活跃性以及洞察其材料氧化还原反应活跃性的强有力的技术手段。图5 是MgCo2O4纳米材料的循环伏安曲线图,从图5(a)中可以清晰地观察到在低扫描速率2 mV/s 下,曲线出现两对很明显的氧化还原峰,说明该纳米材料的电容行为基于法拉第氧化还原反应,是典型的法拉第赝电容行为方式。在图5(b)中,较低扫描速率下呈现的两对氧化还原峰相比于较高扫描速率要规整,其主要是由OH−扩散较怠慢引起的[9],以至于OH−不仅可以与材料的表面发生化学反应,还能够渗透到其内部进行作用[10],这也诠释了材料利用率更高的原因。另一方面,该CV 曲线中出现两对氧化还原峰,说明发生了两种价态变化。图5(a)中的第一组氧化还原峰(X1、X2)和第二组氧化还原峰(X3、X4),可用化学方程式来表示这段CV 曲线的Mg+/Mg2+与Co3+/Co4+之间的相互变化[11−15]:

如图5(b)所示,随着扫描速率的增大,其对应的CV 曲线的面积也随之增大,相应的峰位置也随之改变,即对应的氧化还原峰值增大,其中氧化峰逐渐向坐标的正方向移动,还原峰逐渐向坐标的负方向移动,表明该材料具有快速的氧化还原能力,而出现这种明显的电位分歧现象与电极的欧姆内阻和极化效应以及OH−的扩散有关[16]。值得注意的是,在扫描速率增大的过程中,CV 曲线不能保持原有的形状,其原因的可能有两点:第一,存在一定的极化效应[17],同时又表明了该合成的纳米材料的活跃可逆性一般;第二,在扫描速率较大的情况下,因为较缓慢地扩散导致离子的迁移被限制[10],致使电极材料与之接触不完全。
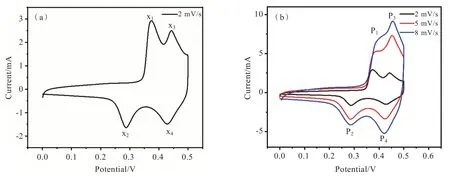
图5 (a)扫描速率2 mV/s 和(b)不同扫描速率的MgCo2O4 循环伏安曲线Fig.5 MgCo2O4 cyclic voltammetry curves of (a) scan rate 2 mV/s and (b) different scan rates
2.3.3 充放电性能 为了进一步探究该材料的电化学行为,采用恒电流充放电功能进行测试。图6(a)为经过该功能测试后所得曲线,称为恒流充放电曲线(GCD)。在GCD 图中所有的曲线均呈现出较为完美的对称性,说明该纳米材料的可逆性良好,具有良好的赝电容性能[4]。随着测试电流密度的增大,所有的GCD 曲线形状无较大改变,说明该MgCo2O4电极具备较高的库仑效率[10]。另外,在GCD 图中,0.2 ~ 0.35 V 处的曲线段基本呈垂直,这是由于电极/电解液之间界面电荷隔离所引起的双电层电容行为所导致的,而图中出现的略微电势平台,起缘于该纳米材料所发生的法拉第氧化还原反应,在这一化学过程中,体系内的纳米材料的表面以及内部与吸附/嵌入的OH−相互作用,这与CV 分析结果一致[10]。值得一提的是,在整个充放电曲线中都没有明显的电压降现象,说明了在电极内部几乎不存在阻抗的抑制行为。GCD 测试最能直观地映射出纳米材料的比电容量值,如图6(b)所示为该材料的倍率性能图,其所展示的深蓝色部分代表不同电流密度下实际电容量值,而红色部分则是相对于最大电容量值所未达到的部分,根据图6(b)及公式(1)可对比电容量进行计算,在电流密度为1、2、4、6、8、10 A/g 的情况下,对应的比电容量值分别为 315.6、148、69.8、44.8、32.2、24.7 F/g,之所以出现这样的趋势可能与材料与 OH−接触的快慢有关。在低电流密度下,MgCo2O4纳米材料与OH−的接触较为迟缓,纳米材料的利用率高[9−10],这与 CV 曲线的分析结果相吻合。
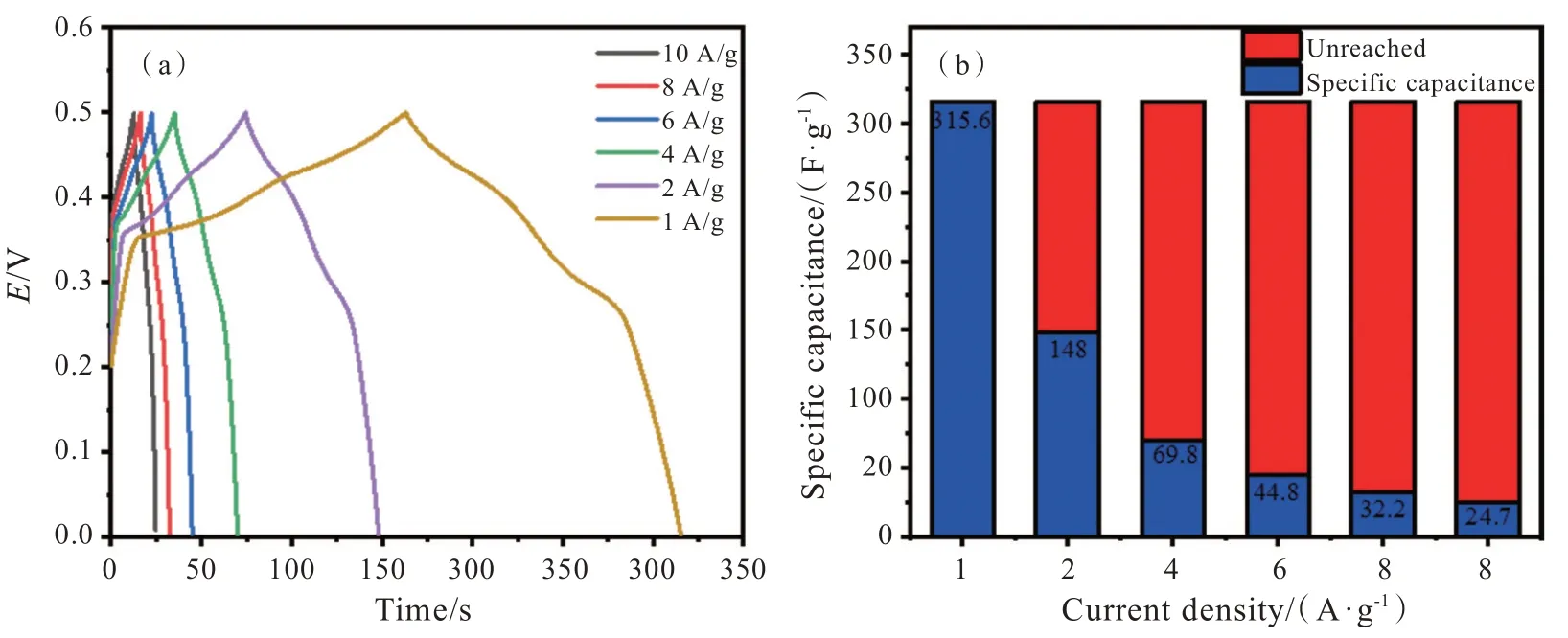
图6 (a)不同电流密度下的MgCo2O4 恒流充放电曲线;(b)MgCo2O4 纳米材料的倍率性能图Fig.6 (a) MgCo2O4 galvanostatic charge/discharge curves at different current densities; (b) Rate performance of MgCo2O4 nanomaterial
2.3.4 循环性能 循环性能测试是一种评价纳米材料是否具备优秀稳定性质的重要技术手段。图7 为MgCo2O4纳米材料的循环性能示意图。图7 中插图分别是在电流密度为1 A/g 的情况下循环充放电曲线中间某时刻的波形图,及在循环4 000 圈后对应比电容保留率的柱状图,其中蓝色部分为保留的容量,红色部分则为损耗的容量。循环测试部分在电流密度为1 A/g 下将样品进行循环4 000 圈,计算得出比电容仅损失了26.5%,保持了73.5%原始容量,这种循环结果说明该MgCo2O4纳米材料具有长期的卓越稳定性[4]。
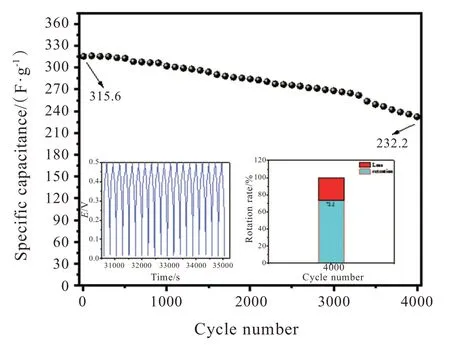
图7 在电流密度1 A/g 下循环4 000 圈MgCo2O4 纳米材料的循环性能图Fig.7 Cycle performance of MgCo2O4 nanomaterial at the current density of 1 A/g up to 4 000 cycles
2.3.5 阻抗性能 图8(a)为MgCo2O4纳米材料的EIS,其中插图为高频区域半圆的放大图,图8(b)为最常用的等效RC 电路图。表2 为阻抗图循环4 000 圈前后的对比结论。EIS 测试也是衡量纳米材料是否具有优良特性的重要指标之一。EIS 是由弧形曲线组成,弧形曲线又包含具有各自特征的高频半圆区域和低频直线区域。高频区域的半圆直径受电化学极化控制[18],对应于电极材料与电解液之间的电荷接触以及传递阻抗的大小,半圆直径越大,则阻抗越大,成正比。低频区域的直线斜率受物理扩散控制[18],对应于电解液中的离子在电极材料内部传递和扩散的阻抗大小,直线斜率越大,则阻抗越小,成反比。图8 中红色代表未循环前的阻抗谱图,黑色表示循环后的阻抗谱图。
在图8(b)中,Rs代表电解液、活性材料的内阻、活性材料与集流体表面接触的电阻的总和;Rct代表电极与电解液表面的电荷转移的电阻;Cd表示双电层电容;Zw表示电极−电解液界面OH−的扩散阻力;而CPEp则为恒相位角元的代替。高频区半圆包含Rs与Rct,低频区直线斜率K代表瓦尔堡阻抗(Zw),其中Rs电阻值可由高频区域的实轴截距所得知,Rct电阻值可从高频区域中的半圆直径中计算[19−20]。
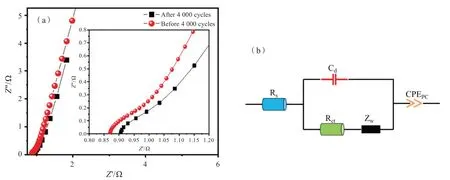
图 8 (a)MgCo2O4 纳米材料的交流阻抗谱;(b)等效 RC 电路图Fig.8 (a) EIS of MgCo2O4 nanomaterial;(b) The equivalent RC circuit diagram

表2 阻抗谱循环4 000 圈前后的对比结论Tab.2 Contrastive conclusion of impedance spectra before and after 4 000 cycles
图9 中展示了片层花状3D MgCo2O4电化学反应机理,其中图9(a)以图3(b)所示的MgCo2O4“花”作为参考,图9(b)展示的是该“花”俯视角度的3D 片层花状结构,其所示生动形象地描述了“花”在参与OH−反应时的机理与电子随机输出的情况,而图9(c)的红色箭头指代该整体的花状纳米材料的电子可能输出路径。一般来说,可通过两个核心的因素提高纳米材料的电容量性能:一是增大比表面积,构造多孔结构纳米材料,该类材料均能在实验测试中表现出优越的电化学性能;二是与所制备纳米材料的晶体结晶度有关,比如材料的结构等,晶体具备良好的结构能够让离子/电子快速迁移。普遍的情况下,活性材料拥有高度结晶的前提下,具有有效的循环稳定性及其电导率。本文中涉及到的片层花状结构可以较好地让溶液中的OH−离子渗入MgCo2O4纳米材料的内部,使得该纳米材料不仅表面可以发生化学反应,其内部也能有一定的概率充分地与电解液中的OH−离子发生化学反应,导致对纳米材料的利用率较高。通过组装形成的多孔结构有利于抑制电化学反应过程中的体积形变,保证电极的循环稳定性。此外,在传统电极制备的工艺基础上,通过一步水热法将活性材料直接“生长”在泡沫镍导电骨架上,以免让导电剂和粘黏剂的粉体累积直接影响到材料比表面积暴露在电解液中的概率,以致于让材料的比表面积接触率大大降低,提供更少的反应活性位点,从而增大其内部的欧姆电阻。

图9 片层花状的3D MgCo2O4 电化学反应机理Fig.9 Electrochemical reaction mechanism of 3D MgCo2O4 with lamellar flower-like structure
3 结论
1)本实验通过一步简单的尿素水热法所制备的MgCo2O4纳米结构呈现片层花状,片与片之间留有空隙。该花状材料尺寸、直径大小不一,较小的约为7.34 μm,较大的约为15.38 μm,且纳米片厚度匀称,约63.9 nm。
2)通过对晶体结构分析表明该材料是较纯的MgCo2O4,活性材料确保了良好的结晶度,保证了材料的电导率及其电极的循环稳定性。
3)对获得的MgCo2O4材料进行电化学性能测试,显示该材料是较为良好的电极材料,在电流密度1 A/g 的情况下其比电容可达315.6 F/g。在循环4 000 圈之后,比容量仅损失了26.5%,呈现出良好的循环性能。
