4-乙烯基-1-环己烯二环氧化物阳离子单体光聚合性能研究
2020-12-18周金娣陆炳宇
周金娣,陆炳宇
(海门市自来水有限公司 分析实验室,江苏 南通 226100)
光固化技术是一种利用紫外光产生活性种,使体系发生聚合和交联反应而固化的一种涂层固化技术[1]。与热固性涂层相比,其利用光源实现固化,具有高效、节能、环保等优势。固化速度相对而言较快,反应效率高[2-4]。按其固化聚合机理,可分为自由基光固化体系和阳离子光固化体系。阳离子光固化体系中,阳离子引发剂在光照条件下分解产生超强质子酸,在其作用下,活性基团发生阳离子聚合,链增长、交联固化成膜[2]。与自由基光固化体系相比,阳离子体系对氧气阻聚不敏感,但是对空气中水汽敏感;通常固化速度相对较低,并会发生一定的暗反应[3,4]。
常用的阳离子型光固化活性基团包括氧杂环类和乙烯基醚类的官能团[5,6]。其中乙烯基醚和环氧基化合物较为常用。通常的双酚A型环氧树脂可用于阳离子光固化体系,但其具有粘度高、施工不便、反应活性低、固化慢等不足。因此开发使用低粘度、高官能度、高活性的阳离子光固化单体或树脂,对阳离子光固化体系至关重要。如黄笔武等[7,8]以多种多元醇为骨架,合成并研究了多种缩水甘油醚的阳离子固化性能。此类单体粘度低、官能度高,可用于调节阳离子体系的粘度和固化速率。此外,相对于缩水甘油醚或缩水甘油酯体系,脂环族环氧体系固化速率较快,且无明显诱导期[9-14]。因此,对脂环族环氧单体的阳离子固化过程进行研究,合成制备具有高反应活性、快速固化的阳离子光固化单体或树脂,具有较大的应用前景。如Crivello等[12,13]设计合成了系列含乙烯基醚的脂环族阳离子固化单体,显示具有较高的阳离子固化反应活性。采用双环戊二烯环氧化制备的阳离子固化单体也具有较高潜在应用价值。
本文考察了4-乙烯基-1-环己烯二环氧化物的阳离子光固化过程,采用实时红外光谱监测其固化过程中环氧基团的转化率随光照时间的变化关系,分析了不同的光强、不同光源、引发剂浓度下的光固化过程。并以3,4-环氧环己基甲酸- 3′,4′-环氧环己基甲酯为参照,考察了其分子结构中不同环氧基团的反应活性差异,并对固化后材料进行了红外光谱和热稳定性分析。
1 实验部分
1.1 主要原料
4-乙烯基-1-环己烯二环氧化物(TTA22)、3,4-环氧环己基甲酸-3′,4′-环氧环己基甲酯(TTA21):江苏泰特尔新材料科技有限公司;二苯基碘六氟锑酸盐(PAG30202)、增感剂PSS303:常州强力电子新材料股份有限公司。
1.2 分析测试与表征
傅里叶变换红外光谱(FT-IR)分析:将质量浓度为4%的阳离子光引发剂单体涂布在压制好的KBr盐片上,测试红外光谱。测试结束后,将同一盐片于60 mW/cm2光强下固化,并将固化后的盐片再次进行红外光谱分析。测试条件:用 Nicolet5700 型傅里叶变换红外光谱仪对产物结构进行表征。扫描波长范围设置为 4000~500 cm-1,分辨率设为4 cm-1,扫描32次。
热重(TGA)分析:将质量浓度为4%的阳离子光引发剂单体在90 mW/cm2光强下充分光照固化后进行TGA分析。测试条件:采用Q500型热重分析仪进行测试,样品质量为 6~10 mg,设置升温速率为 10 ℃/min,设置温度测试范围为25~600 ℃,N2氛围下进行。
采用实时红外(Real-Time IR Nicolette iS5)监测环氧单体的光固化过程[5,6,9]。将固化样品涂布于溴化钾盐片上,UV光源辐射样品使之固化,同时监测样品红外谱图中908~922 cm-1环氧基团相关特征吸收峰的峰面积变化。树脂固化过程的环氧基团转化率按下式计算:
式中,A0与At分别是未光照和光照t时间的环氧基团吸收峰面积。
Photo-DSC分析:采用photo-DSC分析不同单体聚合时放热量[15]。将溶解有4%光引发剂的单体加入到分析测试坩埚中,并放置参比坩埚,光强60 mW/cm2, 温度40 ℃,以20 mL/min的速度通入N2。
2 结果与讨论
2.1 光聚合性能分析
在不同的引发剂浓度以及汞灯光强下,考察了4-乙烯基-1-环己烯二环氧化物(TTA22)的紫外光聚合性能。此外,还分析了其在LED光源下与汞灯光源下光聚合性能差异,以及LED光源下不同增感剂浓度对光聚合性能的影响。TTA22具有两种不同的环氧基——脂环族环氧基和脂肪族环氧基,将之与含有两个脂环族环氧基的3,4-环氧环己基甲酸-3′,4′-环氧环己基甲酯(TTA21)进行比较,考察了不同环氧基的光聚合性能。
2.1.1不同引发剂浓度下光聚合性能
图1是不同的光引发剂浓度下,光强为60 mW/cm-2时,TTA22的环氧基转化率随时间的变化关系和相应的转化速率。图1a可以看出,随引发剂浓度增加,环氧基的最终转化率逐渐增大。当引发剂浓度为1%时,其环氧最终转化率(C100%)仅为48%,随着引发剂浓度增加到4%时,环氧转化率增加到70%。光照45 s(总光照时间的5%)时的环氧基转化率(C5%)占最终环氧基转化率(C100%)的比例大于50%,说明反应前期聚合速率较快。当引发剂浓度为1%时,C5%/C100%为58%,光引发剂浓度增加到4%时,C5%/C100%增加到85%,说明具有较快的固化速率。当光照时间大于45 s时,转化率随时间增长缓慢,这是由于体系固化导致分子运动受限,造成聚合速率快速降低。
从光聚合的环氧基转化速率图(图1b)可以看出,其主要的聚合反应发生在光照的前20 s内,20 s后其聚合速率接近0。光聚合的反应速率随着光引发剂浓度的增加而增加,当引发剂浓度从1%增加到2%时,其聚合速率增加较小,而从2%增加到4%时,聚合速率增加明显。
2.1.2不同光强下的光聚合性能
图2a显示的结果表明,随着光强增加,固化体系的最终环氧转化率(C100%)逐渐增大。当光强为30 mW/cm2时,体系的最终环氧转化率仅为45%,当光强增加到60 mW/cm2时,最终环氧转化率显著增加至65%,而进一步增加光强至90 mW/cm2时,转化率增加幅度减小,仅从65%增加至72%。这是由于高光强下,单位时间内光引发剂分解速率大,产生的超强质子酸浓度相对较高,使得聚合初期大量环氧基参与聚合反应,显著提高了环氧基转化率。此外,高光强下引起温度升高,使得固化时分子运动受限程度降低,亦有可能是导致环氧基转化率的提高的影响因素之一。因此可以观察到不同光强下,光照45 s内的环氧基转化率占最终环氧基转化率的比例大于80%。
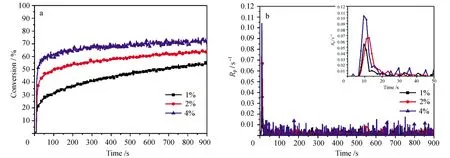
图1 不同光引发剂浓度(质量分数)对光聚合性能影响a. 转化率随时间变化; b. 转化速率随时间变化
反应速率随时间的变化图(图2b)可以看出,随着光强的增加,聚合速率逐渐增加,但是差异较小。当光照时间大于30 s时,聚合速率接近0,光照10 s时达到最大聚合速率。
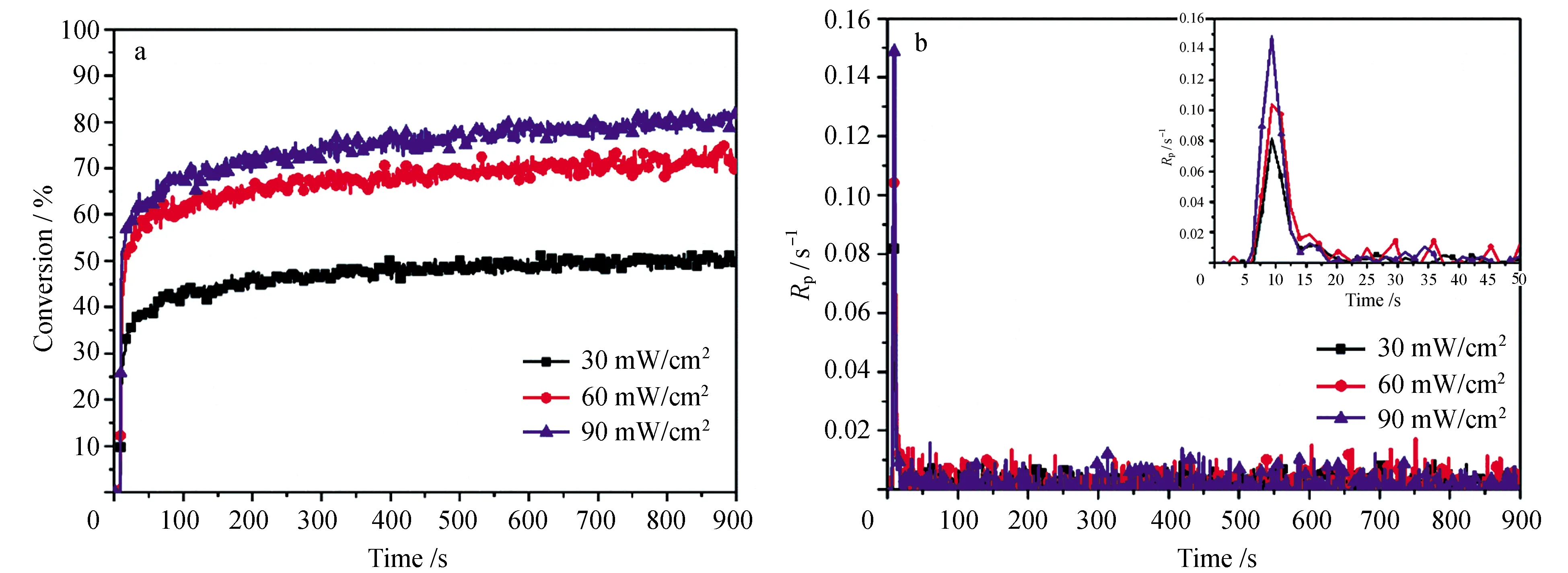
图2 不同光强对光聚合性能影响a. 转化率随时间变化; b. 转化速率随时间变化
2.1.3不同光源下光聚合性能
从图3a中可以看出,不加增感剂时,LED光源下环氧基光聚合性能明显低于汞灯条件下的聚合。这是由于阳离子光引发剂二苯基碘六氟锑酸盐的吸收波长显著小于LED光源的发射波长,光源波长不匹配导致光引发剂分解速率慢,不能有效地引发环氧基的开环聚合反应。当向固化体系中加入1%增感剂PSS303后,LED光源下的环氧基转化率和转化速率明显增加,但仍低于汞灯下不加增感剂的固化体系,说明加入增感剂后,聚合体系对LED光能利用效率增加,但相比汞灯条件下,其利用效率仍然较低。这是由于体系中加入增感剂后,增感剂吸收光能形成激发态,激发态的增感剂与光引发剂作用,使其分解而产生质子酸引发环氧基聚合。增感剂的加入使体系可吸收并利用长波长的紫外光,但由于涉及双分子相互作用,激发态增感剂不能将光能100%传递给光引发剂使其分解,故而引发效率相对较低。而汞灯光聚合体系中加入增感剂后,环氧基转化率和转化速率差异不大,仅略有增加,说明相比于通过增感剂间接吸收光能而分解,光引发剂直接吸收光能分解引发环氧基聚合具有显著高效率。
2.1.4不同增感剂浓度下的LED光聚合性能
图4a中可以看出,随增感剂浓度增加,环氧基的转化率和聚合反应速率相应增加。当增感剂浓度为1%时,最终环氧转化率为50%,当增感基浓度提高到2%时,环氧基的转化率达到65%。由反应速率图(图4b)可以看出,随着增感剂浓度增加,反应速率随之增加,达到最大反应速率的时间逐渐缩短。相比汞灯的光聚合体系,LED光源下的聚合速率较低,这可能是由于光引发剂通过增感剂对光源的利用效率相对较低。
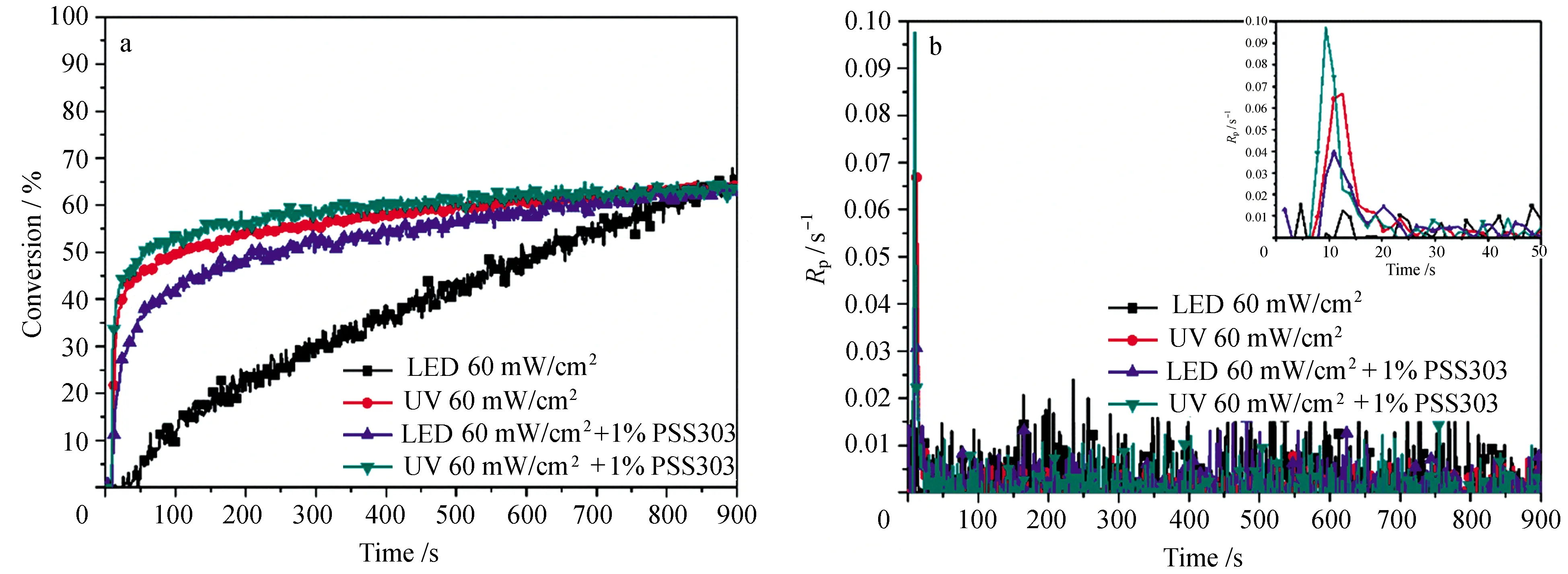
图3 不同光源对光聚合性能的影响a. 转化率随时间变化; b. 转化速率随时间变化

图4 LED光源下不同浓度(质量分数)增感剂对光聚合性能影响a. 转化率随时间变化; b. 转化速率随时间变化
2.1.5不同单体的光聚合性能
4-乙烯基-1-环己烯二环氧化物(TTA22)分子结构中含有两种不同的环氧基——脂环族环氧基和脂肪族环氧基。为了比较两种环氧基的光聚合性能,选用了一种含有两个脂环族环氧基的单体3,4-环氧环己基甲酸-3′,4′-环氧环己基甲酯(TTA21)作对比,二者分子结构式见式1。
图5是两种不同的单体光聚合的转化率和时间关系图以及转化速率随时间变化关系图。图5a中可以看出TTA22具有更快的反应速率及环氧基转化率,聚合反应前期即达到较高的转化率,固化快。而TTA21 光聚合转化速率较慢,前期环氧基转化率较低,固化慢。图5b中TTA22的光聚合速率达到0.105 s-1,而TTA21光聚合速率仅为0.027 s-1,差异显著,说明TTA22分子结构中脂肪族环氧基具有相对较高的反应活性。这可能是环氧基的空间位阻效应所致。
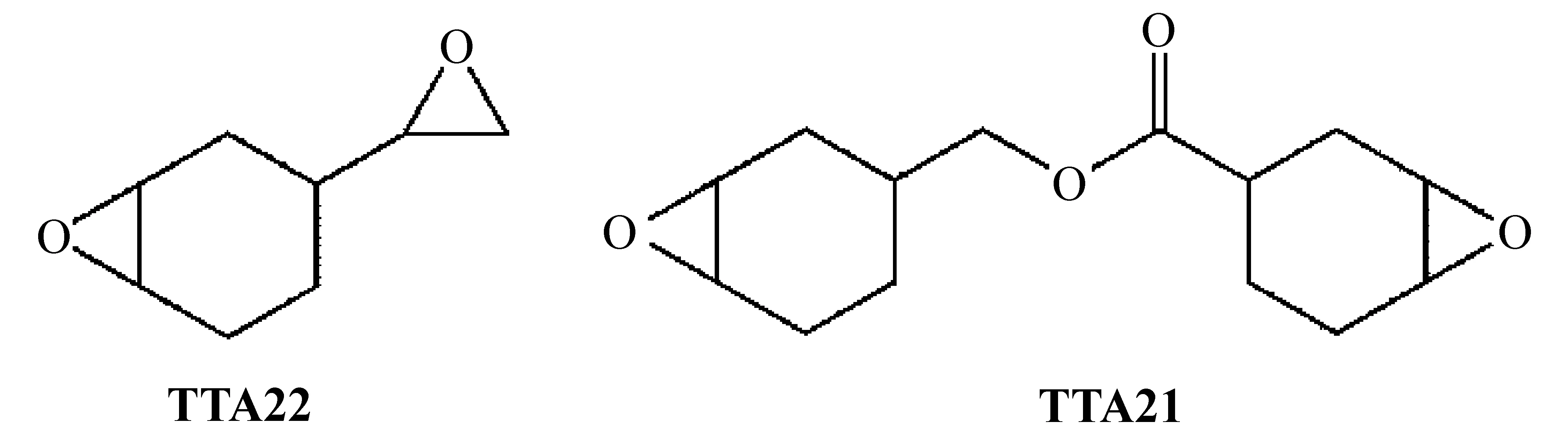
式1 TTA22和TTA21分子结构式
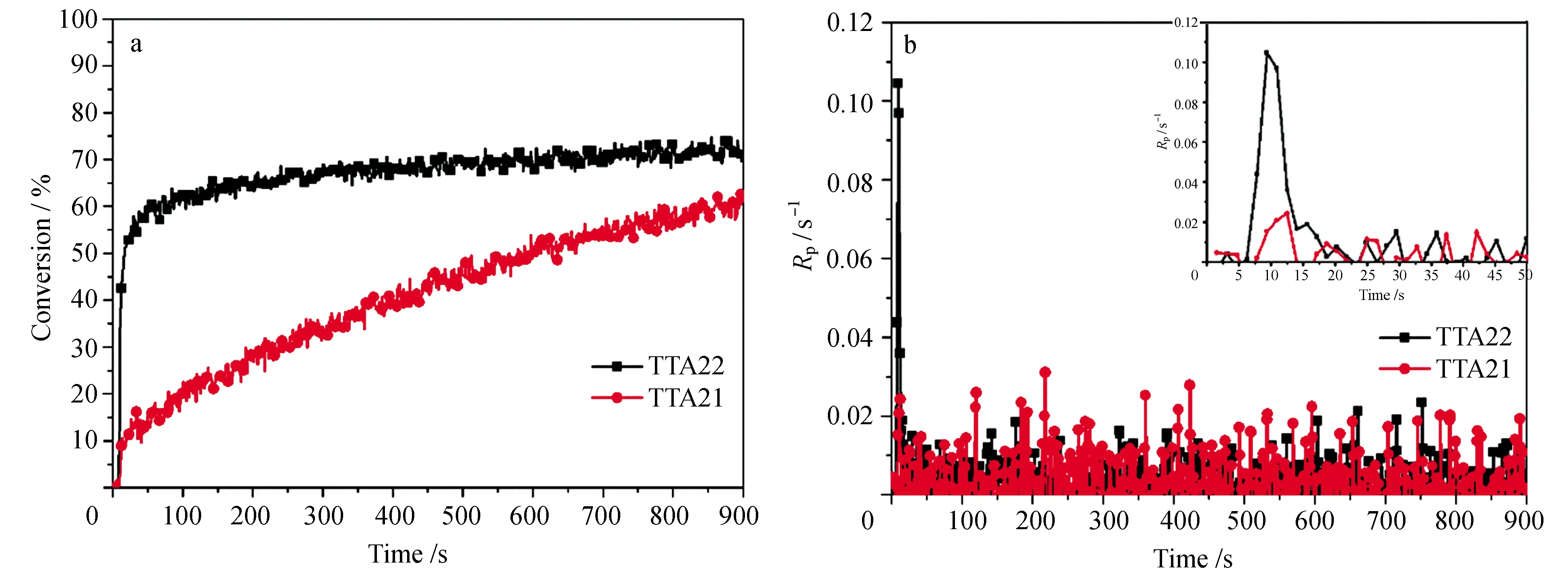
图5 不同单体的光聚合性能a. 转化率随时间变化; b. 转化速率随时间变化
图6是采用了photo-DSC分析4-乙烯基-1-环己烯二环氧化物(TTA22)和3,4-环氧环己基甲酸-3′,4′-环氧环己基甲酯(TTA21)光聚合性能的结果。图中可以看出,TTA22最大聚合速率时放热达到2480 W/mol,而TTA21最大聚合速率时放热仅为720 W/mol。TTA22的反应放热显著大于TTA21。比较TTA22和TTA21的分子结构,可认为光聚合时TTA22分子结构中的两种环氧基具有不同的活性,其中脂肪族环氧基放热大于脂环族的放热。由于阳离子聚合过程链增长速率受温度影响较大,故而高放热速率可促进阳离子聚合反应,从而促进放热速率进一步增大。
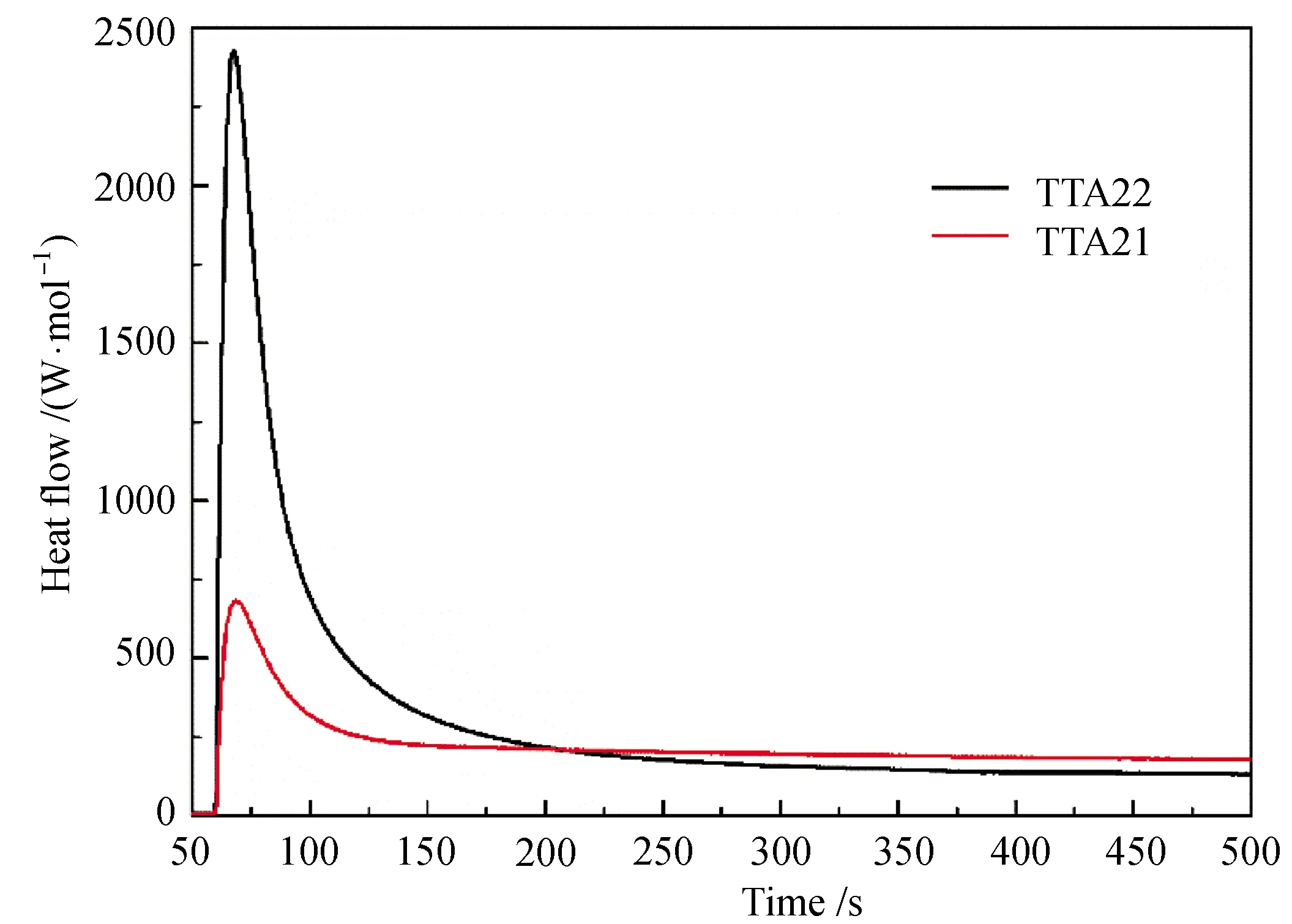
图6 不同单体光聚合性能的photo-DSC分析
2.2 固化后材料性能分析
分别对4-乙烯基-1-环己烯二环氧化物(TTA22)和3,4-环氧环己基甲酸-3′,4′-环氧环己基甲酯(TTA21)固化后的材料进行了红外光谱分析及TGA热稳定性分析。
2.2.1固化前后红外光谱分析
图7a、b分别为4-乙烯基-1-环己烯二环氧化物(TTA22)和3,4-环氧环己基甲酸-3′,4′-环氧环己基甲酯(TTA21)光固化前后的红外光谱谱图。图7a中可以看出TTA22固化后,在3450 cm-1处出现了明显的羟基伸缩振动吸收峰,这是由于环氧基开环反应生成的羟基所致。同时1073 cm-1处出现了C—O—C的伸缩振动吸收峰,而922 cm-1处的环氧基团吸收峰明显减小,表明环氧阳离子聚合生成聚醚链。图7b显示了TTA21光固化前后的红外光谱图,图中同样在3450 cm-1和1072 cm-1处出现由于环氧基阳离子聚合而生成的羟基和聚醚的红外光谱吸收峰。但是926 cm-1处的环氧基吸收峰在固化后略有减小,但并未消失,这说明TTA21在PAG30202光引发剂下聚合转化率较小,聚合固化效率低。
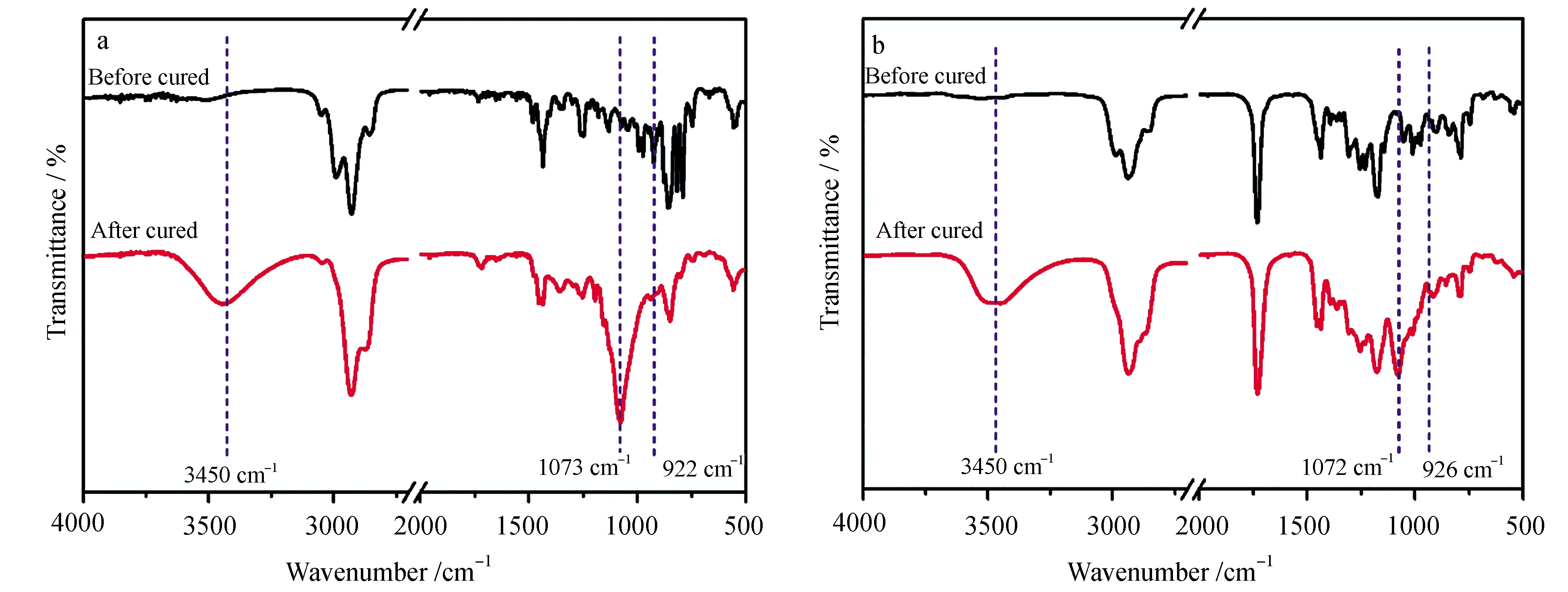
图7 不同单体光固化前后红外光谱分析a. TTA22; b. TTA21
2.2.2固化后材料热稳定性分析
图8为不同单体固化后材料的TGA热稳定性分析。从图中可以看出,TTA22和TTA21两种环氧单体光固化后材料的开始分解温度分别为305 ℃和315 ℃,十分接近。当温度继续升高,材料开始热分解,可以看出TTA21的分解速率小于TTA22,且最终固体份残留TTA21为20%而TTA22为5%,说明TTA21的热稳定性略优于TTA22。在TGA升温过程中,材料中未反应的环氧基可能会在热作用下进一步固化,从而使TTA22和TTA21可能由环氧基转化率差异导致的热稳定性差异消除或减小。从TTA22和TTA21的分子结构计算,TTA21分子结构中含氧量为19.0%而TTA22分子结构中含氧量为22.8%,故而TTA22的最终固体残留低于TTA21。另一方面,TTA21分子结构中的环己基含量较高,高温下可能脱氢,形成苯环而增加热稳定性。
3 结论
本文采用实时红外光谱分析考察了4-乙烯基-1-环己烯二环氧化物(TTA22)在不同光引发剂浓度、不同光强以及不同光源下的光聚合性能。
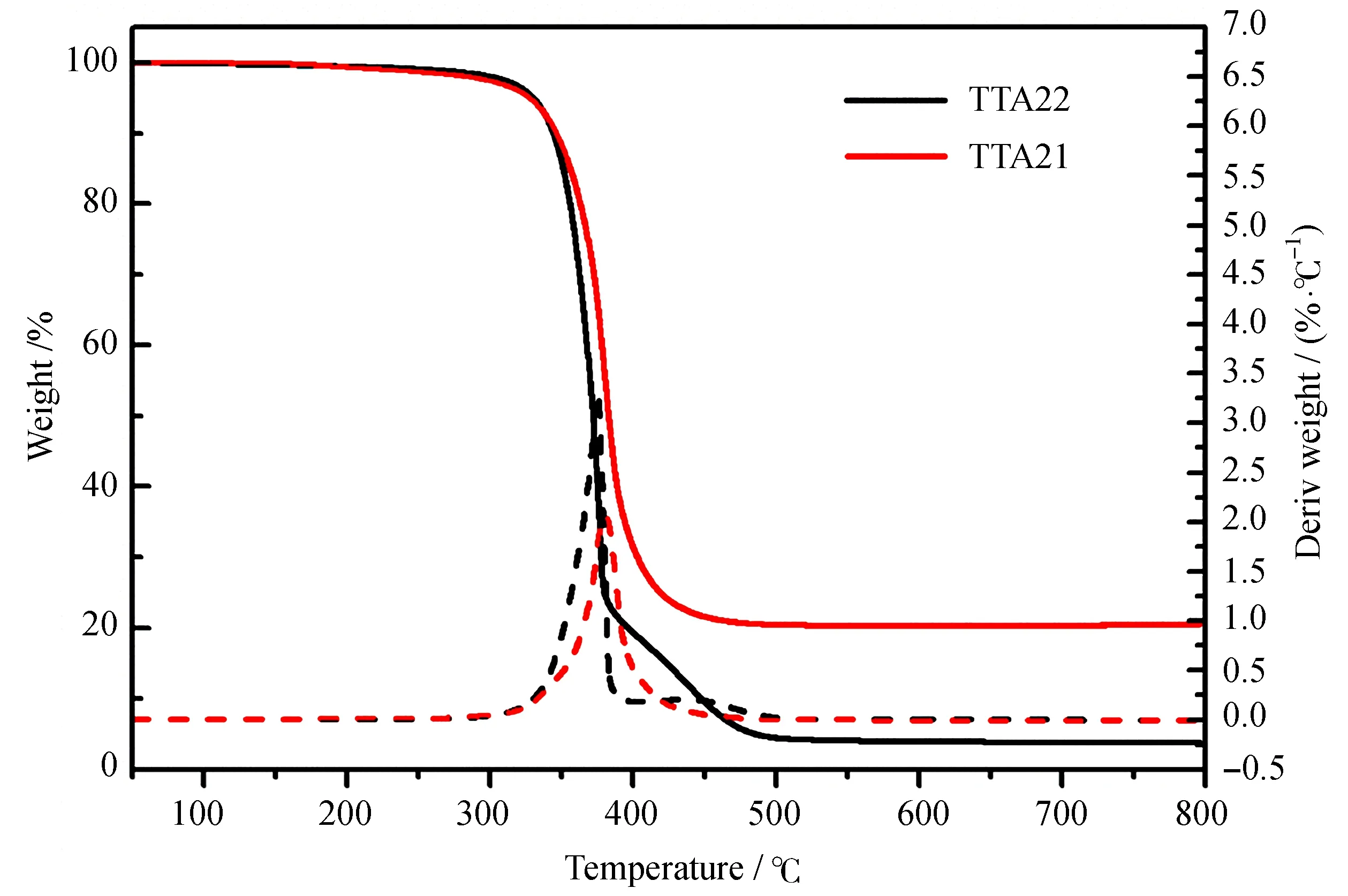
图8 不同单体光固化后的TGA分析
随着引发剂浓度增大、光强的增加,单体环氧基转化率和转化速率随之增加。LED光源下单体的环氧基转化率和转化速率低于汞灯下的转化率及转化速率。随着增感剂浓度增加,单体在LED光源下的转化率和转化速率增加。以3,4-环氧环己基甲酸- 3′,4′-环氧环己基甲酯(TTA21)为参照,比较了其与TTA22的阳离子光聚合活性,结果显示,TTA22光聚合过程中的放热量、环氧基转化率、转化速率显著大于TTA21,表现出较高的光聚合活性,而TTA21固化后材料的热稳定性优于TTA22。
