金连菊复方制剂对小鼠的 急性毒性试验
2020-12-15黄全明周剑辉杨昭远兰宗宝俸祥仁
黄全明 周剑辉 杨昭远 兰宗宝 俸祥仁


摘 要: 以健康昆明种小鼠为动物模型,一次性经口灌服不同剂量(10.00、7.76、6.03、4.68、3.63和2.82g·kg-1 )的金连菊复方制剂,通过开展小鼠急性毒性试验评价其用药安全性。结果表明:灌服不同剂量金连菊复方制剂后,小鼠首先呈现安静、趴卧不动、腹式呼吸,随着时间推移部分小鼠出现被毛竖立、眼球突出、尾部血管发蓝等症状,严重者腹部急剧收缩、行动不稳、抽搐死亡,但至给药后第4 d小鼠毒性反应基本消失;小鼠死亡现象主要发生在给药后24 h内,且呈明显的量效关系;剖檢死亡小鼠发现其肺脏充血或有出血点,同时伴有胸腔积液;试验结束后将剩余小鼠全部处死剖检,发现各处理组小鼠的内脏器官均无明显病理变化,与正常小鼠的内脏器官一致。通过改良寇氏计算公式得到金连菊复方制剂对小鼠的半数致死量(LD 50 )为6.299g·kg-1 ,其标准误差(Sx 50 )为 0.035 5 ,95%置信区间为7.394~5.367,属于实际无毒性物质。
关键词: 金连菊复方制剂;小鼠;急性毒性试验;半数致死量(LD 50 )
中图分类号: S853.74文献标志码: A文章编号: 0253-2301(2020)06-0017-05
DOI:10.13651/j.cnki.fjnykj.2020.06.004
Acute Toxicity Test of Compound Preparation of Jinlianju on Mice
HUANG Quan-ming 1, ZHOU Jian-hui 2, YANG Zhao-yuan 3, LAN Zong-bao4* , FENG Xiang-ren5*
(1. Yongfu County Agriculture and Rural Bureau, Guilin, Guangxi 541800, China; 2. Guilin Animal
Husbandry Station, Guilin, Guangxi 541000, China; 3. Institute of Animal Health in Jiangnan District
of Nanning, Nanning, Guangxi 530001, China; 4. Institute of Agricultural Science and Technology
Information, Guangxi Academy of Agricultural Sciences, Nanning, Guangxi 530007, China;
5. Guangxi Baipeng Livestock Breeding Station, Liuzhou, Guangxi 541502, China)
Abstract:By taking the healthy Kunming mice as the animal model, the compound preparation of Jinlianju was given different doses ( 10.00 ,7.76 ,6.03 ,4.68 ,3.63 and2.82 g·kg-1 ) by oral administration at one time. The acute toxicity test of mice was carried out to evaluate the drug safety. The results showed that after filling different doses of the compound preparation of Jinlianju, the mice showed quiet, laying still and abdominal breathing at first; As time went on, some mice showed clothing hair erection, protruding eyes and blue blood vessels in the tail. In the severe cases, the abdomen contracted sharply, the movement was unstable, and the mice twitched and died, but the toxic reaction of the mice basically disappeared at the 4th day after medication. The death of mice mainly occurred within 24 h after medication, and showed an obvious dose-effect relationship. The dead mice were found to have congestion in the lungs or bleeding points, as well as pleural effusion. After the end of the test, all the remaining mice were sacrificed for autopsy, and it was found that the internal organs of the mice in each treatment group had no obvious pathological changes, which was consistent with the internal organs of normal mice. By using the Karber method, theLD 50 andSx 50 of Jinlianju compound preparation for mice were obtained, being6.299 g·kg-1 and0.035 5 , respectively. And the confidence interval of 95% was7.394- 5.367 , indicating that the compound preparation of Jinlianju belonged to the actual non-toxic substance.
Key words:Jinlianju compound preparation; Mice; Acute toxicity test; Median lethal dose
西药在畜禽疫病防治上虽然具有疗效快的优势,但易产生耐药性,或对动物机体产生一定损伤,且存在药物残留的风险,进而对人类健康产生间接的不利影响。中药具有天然的保健及药用成分,可提高机体免疫力,同时具有抗病毒及抗应激等活性作用,毒副作用小,不易诱发病原菌产生耐药性[1-2] ;且我国中药历史发展悠久,具有上千年的应用實践,因此中药在兽医临床应用中优势巨大。复方中药制剂是由两种或两种以上的中药材组方而成,相对于单方药物,复方中药制剂具有提高药物疗效、减少不良反应、改善服用药品依从性、降低用药成本等优势,目前在畜禽养殖生产上已得到广泛应用[3-4] 。中药复方制剂安全性是进一步研究其药理、毒理作用的基本保障,同时对评价新药是否具备研发价值具有重要意义,即开展急性毒性试验和亚慢性毒性试验是评价中药复方制剂安全性的必要环节[2,5] 。其中,根据急性毒性试验结果可初步了解试验药物的毒性强度和可能的靶器官,为药物进行其他方面的试验研究提供依据[6] 。本课题组前期研究发现,金银花、连翘、野菊花、乌梅和五倍子等中药对大肠杆菌 Escherichia coli 、巴氏杆菌 Pasteurella sp.、链球菌 Streptococcus sp.、沙门氏菌 Salmonella sp.、金黄色葡萄球菌 Staphylococcus aureus 和放线杆菌 Actinobacillus sp.等 6 种猪场常见病原菌高度敏感[7] ,并在此基础上研发出金连菊复方制剂(金银花∶ 连翘∶ 野菊花∶ 乌梅∶ 五倍子=3∶ 5∶ 5∶ 3∶ 4)[2] 。因此,需进一步开展金连菊复方制剂对昆明种小鼠的急性毒性试验,评价用药安全性,为其兽医临床用药提供理论依据。
1 材料与方法
1.1 试验材料
金银花、连翘、野菊花、乌梅和五倍子等中药原材料购自广西玉林市中药材专业市场。健康昆明种小鼠购自广西医科大学实验动物中心,购回后先适应暂养5 d,体重18.0~22.0 g·只-1 。
1.2 试验方法
1.2.1 中药材处理 精确称取金银花60.0 g,以95%乙醇浸泡6~8 h,收集浸提液,药渣再用95%乙醇浸泡4~6 h,合并2次浸提液后80℃加热回流2 h,收集浸提液,过滤,浓缩至生药含量为1.0g·mL-1 ,装瓶备用。同时按组方配比精确称取连翘100.0 g、野菊花100.0 g、乌梅60.0 g和五倍子80.0 g,煎煮前以5倍蒸馏水浸泡2 h,煎煮30 min后收集药液,再加入5倍蒸馏水继续煎煮30 min,合并2次药液,浓缩至生药含量为1.0g·mL-1 。室温下 4 000 r·min-1 离心20 min,收集上清液装瓶备用。按3∶ 17比例合并上述两种药液,采用手提式压力蒸汽消毒器灭菌30 min,即获得金连菊复方制剂。试验前浓缩或稀释至设计的用药浓度。
1.2.2 试验分组设计 选取健康昆明种小鼠共60只,雌雄各半,试验期间饲喂小鼠全价饲料,室温控制在25~28℃,相对湿度为40.0%~70.0%,采用自然光照,自由饮水。用药前禁食12 h,称重,将小鼠随机分为6组,每组10只,雌雄各半;采用中性红染色标记对小鼠进行常规标记。根据寇氏法按等比级数设计6个剂量组,分别一次性经口灌服不同剂量(10.00、7.76、6.03、4.68、3.63和2.82g·kg-1 ),对应为Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ和Ⅵ组。给药后每天注意观察记录小鼠的精神状况、采食饮水情况和死亡情况。
1.2.3 观察指标 观察给药后0~16 h各组小鼠的反应及死亡情况,包括小鼠的行为、动作、呼吸等是否出现异常,以及分泌物及排泄物情况,详细记录小鼠中毒症状和症状出现时间及死亡时间;对死亡小鼠进行剖检,肉眼观察各脏器有无异常,如有明显病变,取病变组织器官制作病理组织切片作进一步观察。在给药当天及给药后第4、8、12和16 d称重,称重前禁食12 h,最后一次称重后将小鼠全部处死,剖检,观察组织器官有无病变。
1.2.4 测定指标依据 小鼠体重采用差量法测定其平均值。半数致死量(LD 50 )采用改良寇氏法进行计算[5,8-9] :当包含0和100%死亡率时,LD 50 =lg-1 [ X m i (∑ P -0.5)];当不包含0和100%死亡率时,LD 50 =lg-1 { X m-i [∑ P -1/4(3- P m- P n)]}。
LD 50 的标准误差:Sx 50 = i (∑ PQ/n )0.5
LD 50 的95%可信限=lg-1 (lgLD 50 ±1.96×Sx 50 )
式中: i 为组距; X m为最大剂量对数; P 为各剂量组死亡率(用小数表示); Q 为各组剂量存活率, Q =1- P ; P m为最高死亡率; P n为最低死亡率;∑ P 为各剂量组死亡率之和; n 为各组动物数。
1.3 统计分析
试验数据采用Excel 2007进行整理,利用DPS进行单因素方差分析(One-wag ANOVA),并以Duncan′s新复极差法进行多重比较。
2 结果与分析
2.1 灌服不同剂量金连菊复方制剂对小鼠体重 变化 的影响
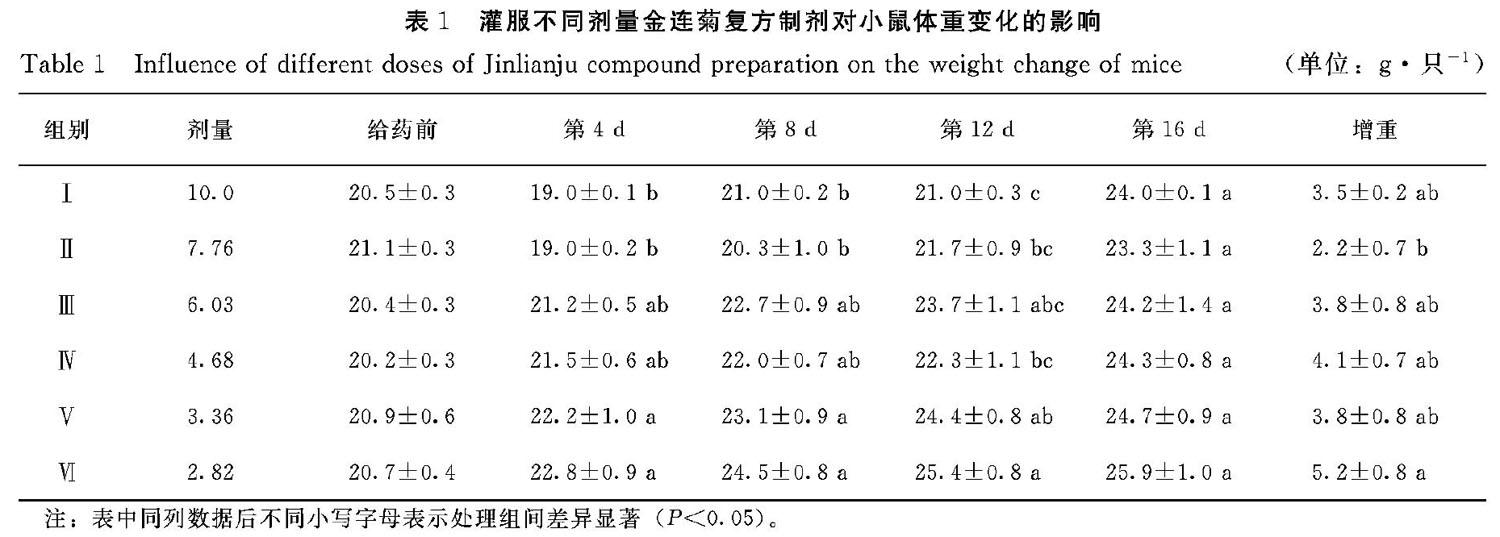
由表1可知,经口灌服金连菊复方制剂后第4 d,Ⅰ组和Ⅱ组小鼠的体重较给药前分别减轻7.32%和9.95%,而Ⅲ组、Ⅳ组、Ⅴ组和Ⅵ组小鼠的体重比给药前分别增重3.92%、6.44%、6.22%和10.14%,其中Ⅴ组、Ⅵ组分别显著高于Ⅰ组和Ⅱ组( P <0.05),Ⅲ组和Ⅳ组与其他处理组间的差异均不显著( P >0.05)。给药后第8 d,Ⅰ组、Ⅱ组、Ⅲ组、Ⅳ组、Ⅴ组和Ⅵ组小鼠的体重较给药后第 4 d 的体重分别增加10.53%、6.84%、7.08%、2.33%、4.05%和7.46%,其中Ⅴ组、Ⅵ组分别显著高于Ⅰ组和Ⅱ组( P <0.05),但与Ⅲ组和Ⅳ组的差异不显著( P >0.05)。至给药后第12 d,除Ⅰ组小鼠的体重无增长外,Ⅱ组、Ⅲ组、Ⅳ组、Ⅴ组和Ⅵ组小鼠的体重较给药后第 8 d 的体重分别增加6.90%、4.41%、1.36%、5.63%和3.67%,其中Ⅵ组显著高于除Ⅲ组和Ⅴ组外的其他3个处理组( P <0.05)。至给药后第16 d,各处理组小鼠的体重差异均不显著( P >0.05)。在整个试验周期内,以Ⅵ组小鼠体重的增重最明显,平均增重5.2g·只-1 ,显著高于Ⅱ组小鼠(平均增重2.2g·只-1 ),但与其他处理组间无显著差异( P >0.05)。
2.2 灌服不同剂量金连菊复方制剂后小鼠的毒性反应症状
经口灌服不同剂量金连菊复方制剂后,各处理组小鼠首先呈现安静、趴卧不动、腹式呼吸,随着时间推移部分小鼠出现被毛竖立、眼球突出、尾部血管发蓝等症状,严重者腹部急剧收缩、行动不稳、抽搐死亡;一些小鼠死前伴有神经兴奋症状,表现为攀爬、惊跳或鸣叫等。小鼠死亡主要发生在给药后24 h内,至给药后第4 d小鼠毒性反应基本消失,且高剂量处理组小鼠死亡率较高,呈明显的量效关系,其中,Ⅰ组累计死亡小鼠9只,Ⅱ组累计死亡小鼠5只,Ⅲ组和Ⅳ组累计死亡小鼠均为4只,Ⅴ组累计死亡小鼠2只,Ⅵ组小鼠未出现死亡现象(表2)。对死亡小鼠及时进行剖检,观察发现部分死亡小鼠的肺脏充血或有出血点,同时伴有胸腔积液。在试验结束后将剩余小鼠全部处死,剖检发现各处理组小鼠的内脏器官均无明显病理变化,与正常小鼠的内脏器官一致。
2.3 金连菊复方制剂对小鼠的LD 50 及95%置信 区间
对小鼠灌服不同剂量金连菊复方制剂后的死亡情况如表3所示。将表3中的试验数据代入改良寇氏计算公式中,可得到金连菊复方制剂对小鼠的LD 50 为6.299g·kg-1 ,Sx 50 为 0.035 5 ,95%置信区间为7.394~5.367。按照毒理學对药物毒性的分级标准[10-11] ,LD 50 > 5 000 mg·kg-1 属于实际无毒性物质,因此,可确定金连菊复方制剂对小鼠安全无毒。
3 讨论
急性毒性试验是药物毒理学评价的常用方法,可根据LD 50 对试验药物的毒性进行分级,初步了解其毒性强度,为药物进行临床用药试验提供参考依据[6,12-13] 。本研究结果表明,经口一次性灌服不同剂量金连菊复方制剂后,小鼠首先呈现安静、趴卧不动、腹式呼吸,随着时间推移部分小鼠出现被毛竖立、眼球突出、尾部血管发蓝等症状,严重者腹部急剧收缩、行动不稳、抽搐死亡,但至给药后第4 d小鼠毒性反应基本消失;小鼠死亡现象主要发生在给药后24 h内,且高剂量处理组小鼠死亡率较高,呈明显的量效关系;剖检死亡小鼠发现其肺脏充血或有出血点,同时伴有胸腔积液,试验结束后将剩余小鼠全部处死剖检,发现各处理组小鼠的内脏器官均无明显病理变化,与正常小鼠的内脏器官一致;此外,通过改良寇氏计算公式得到金连菊复方制剂对小鼠的LD 50 为6.299g·kg-1 ,Sx 50 为 0.035 5 ,95%置信区间为7.394~5.367,属于实际无毒性物质,与本课题组前期开展的大鼠亚慢性毒性试验结果[2] 基本一致,说明金连菊复方制剂安全性好。
由于组成金连菊复方制剂的5 味中药(金银花、连翘、野菊花、乌梅和五倍子)均对大肠杆菌、巴氏杆菌、链球菌、沙门氏菌、金黄色葡萄球菌和放线杆菌等 6 种猪场常见病原菌具有高度的敏感性[7] ,因此该复方中药制剂可作为饲料添加剂应用于断奶仔猪的育肥养殖,但其给药剂量需要通过临床试验进一步探究确认。
参考文献:
[1] 陈培军.中兽医药与畜牧业的健康养殖[J].中国动物保健,2017,19(3):37-38.
[2]兰宗宝,俸祥仁,张鑫,等.金连菊复方制剂对大鼠的亚慢性毒性试验[J].江西农业学报,2019,31(4):82-86.
[3]邓鑫,陆彦蓉,覃兰迁,等.复方苦玄参颗粒急性毒性和亚慢性毒性试验[J].南方农业学报,2018,49(9):1873-1879.
[4]肖蕊,施君,谢小东,等.柴桂感寒口服液急性毒性和长期毒性试验[J].南方农业学报,2018,49(11):2327-2334.
[5]张明.中药复方多糖的急性毒性研究[J].安徽农业科学,2010,38(25):13707-13708.
[6]王利,杨艳玲.伤力草水提物对肉鸡急性毒性试验[J].黑龙江畜牧兽医,2019(24):133-135.
[7]姜源明,俸祥仁,兰宗宝,等.中药对猪场常见病原菌的药敏特性及联合抑菌活性评价[J].江西农业学报,2019,31(2):80-85.
[8]张亚君,刘文利,林明明,等.中药复方制剂“归芪饮”的急性毒性研究[J].山东畜牧兽医,2018,39(1):9-10.
[9]张吉丽,李冰,司鸿飞,等.小鼠口服五氯柳胺的急性毒性研究[J].安徽农业科学,2016,44(12):148-149.
[10] 徐叔云,卞如濂,陈修.药理实验方法学 [M]. 第2版.北京:人民卫生出版社,1981.
[11] 刘昌孝,孙瑞元.药物评价实验设计与统计学基础[M].北京:军事医学科学出版社,1998.
[12]韦芊含,雷伟伟,陈昕,等.饲用黄丝藻粉的急性毒性和亚慢性毒性试验[J].中国畜牧兽医,2020,47(5):1602-1610.
[13]洪伟鸣,左伟勇,宋亮,等.鸡支康口服液的亚慢性毒性试验研究[J].中国畜牧兽医,2013,40(9):140-143.
(责任编辑:柯文辉)
