乙炔选择性加氢:催化剂结构敏感性分析及调控
2020-12-07李雨柔葛小虎曹约强段学志周兴贵袁渭康
李雨柔,葛小虎,曹约强,段学志,周兴贵,袁渭康
(华东理工大学化学工程联合国家重点实验室,上海200237)
石脑油蒸汽裂解是工业上获得乙烯和丙烯等重要化工基础原料的主要途径[1]。然而,这种方式得到的烯烃中通常含有炔烃和二烯烃的杂质,比如裂解得到的碳二组分中通常含有0.5%~3%的乙炔[2]。这些高度不饱和化合物会降低下游烯烃聚合催化剂的活性,并影响聚合物产品的物理性能。因此,工业上需要将这一类杂质除去,控制其含量小于5μg/g。目前,催化选择性加氢被认为是这一过程中炔烃等杂质分离转化的最为有效的方法[3]。此外,煤基路线获得的乙炔通过催化选择性加氢制乙烯,在一定程度上可缓解我国乙烯市场过度依赖石油资源的局势,也能充分发挥我国富煤少油的资源优势[4-5]。
关于乙炔选择性加氢催化剂的研究已经有几十年的历史了,其中Pd 基催化剂因其较高的加氢活性而受到最广泛的关注。目前工业上普遍采用的也是高度优化的Pd 基催化剂[3]。但是,Pd 基催化剂容易导致乙炔深度加氢生成乙烷[6],且催化剂表面乙炔易聚合生成“绿油”,覆盖催化剂活性位点和堵塞催化剂孔道,从而导致催化剂失活。已有研究结果表明,副反应的发生是由于反应物在催化剂表面多齿构型的强吸附导致的。因此,基于反应特性分析的催化剂活性位结构的精准设计和调控对于抑制副反应发生、提升催化剂性能具有重要意义。
近年来,研究者们分别从乙炔选择性加氢催化剂的粒径效应、形貌效应和电子效应进行了一系列研究,阐明了催化剂的活性金属粒径、形貌和电子结构对于反应性能的重要作用,为催化剂的结构调控与优化明确目标。此外,研究者们通过构筑合金及金属间化合物催化剂,实现了催化剂活性位几何结构和电子结构的理性调控,并开展了关于新发展的单原子及其合金催化剂相关研究,优化了乙炔、乙烯等关键物种在催化剂表面的吸附构型及动力学行为,显著提升了乙炔选择性加氢反应性能。本文从以上方面综述了近年来乙炔选择性加氢催化剂的研究进展,重点关注了催化剂的结构敏感性分析及调控策略,并介绍了新兴的单原子及其合金催化剂在该体系的应用进展,最后展望了乙炔选择性加氢催化剂的未来研究方向。
1 单金属催化剂的结构敏感性
1.1 粒径效应
活性金属粒径大小在多相催化反应中具有非常重要的作用。将活性金属颗粒粒径从纳米尺度减小到原子级分散尺度,可能显著改变金属表面位点类型、数目和电子性质,从而改变其催化性能[7],即所谓的结构敏感性反应。Pd 催化乙炔选择性加氢反应是一个典型的结构敏感性反应[8],其活性与金属粒径有显著的依赖关系。因此,深入理解乙炔选择性加氢反应活性和产物选择性对Pd 纳米颗粒粒径的依赖,对催化剂的设计和优化具有重要意义。
Cao 等[7]将多晶面动力学分析与晶体模型计算相结合(图1),探究了Pd 催化乙炔选择性加氢反应的结构敏感性。首先通过动力学实验发现,在Pd纳米粒子粒径大于3.1nm时,乙炔加氢反应的表观活化能不随粒径变化而变化。此外,催化剂电子结构分析表明Pd 纳米粒子粒径大于3.1nm 时其电子性质相似,这预示着存在一种主导活性位。进一步结合催化剂表征和晶体模型计算,将乙炔转化速率和产物生成速率对不同类型的表面原子数目归一,基于此发现Pd 催化乙炔加氢反应中乙炔消耗反应和C4副产物的主导活性位为Pd(111)面,深度加氢产物乙烷生成的主导活性位为Pd 的角位。此外,粒径小于3.1nm 时,该催化反应过程由Pd 电子性质决定。Ruta 等[8]利用反相微乳液方法制备了高分散Pd 纳米粒子,并负载在CNF/SMFInconel载体上,研究了乙炔加氢过程中Pd 纳米粒子的粒径效应。研究结果表明,在反应初期金属表面上形成的积炭减少了可用于吸附乙炔的活性位点,积炭和Pd-Cx表面相的形成是结构敏感性反应。在较小的Pd 纳米颗粒上,表面C 与Pd 的比值较高,因此可用于反应的表面位点减少,从而实验测得TOF 较小。对比11nm 和13nm 粒径大小的Pd 催化剂的TOF 大小,发现二者几乎相同。据此,作者认为11nm 是一个“临界”粒径大小,高于此粒径的Pd催化剂的活性与粒径大小不相关。

图1 多晶面动力学分析和晶体模型计算示意图[7]
除了Pd 之外的其他活性金属催化乙炔加氢反应也是结构敏感性反应。Shi等[9]采用原子层沉积法在氧化铝载体上可控制备了一系列粒径大小不同的Cu/Al2O3催化剂。粒径大小分布从Cu单原子到粒径大小为9.3nm 的Cu 纳米颗粒。实验结果表明,Cu/Al2O3催化剂的乙炔加氢活性随着铜粒径的减小显著降低,主要是由于铜粒径减小弱化了H2解离和乙炔吸附活化。动力学研究表明,随着铜粒径从9.3nm 减小到7.3nm、3.4nm 和Cu 单原子,H2反应级数对应从1.07 逐渐增加到1.21、1.63和1.89,意味着氢气活化变得更加困难。此外,由于在小粒径的Cu 催化剂上的乙烯脱附更容易,乙烯选择性随着Cu粒径减小显著提升,在Cu单原子催化剂上乙炔接近100%转化时乙烯选择性增加到91%。Pt 催化乙炔加氢反应性能也与金属Pt 纳米粒子粒径大小相关。Kuo等[10]研究了不同Pt粒径的Pt/TiO2催化剂的乙炔选择性加氢反应性能,发现随着Pt 纳米颗粒平均粒径的增大,表观活化能降低,催化剂的比活性增加。单原子Pt 催化剂的加氢活性很弱甚至可忽略,而当Pt 物种从单原子尺度增加到亚纳米团簇尺度时,其加氢活性显著增加。此外,粒径大小在亚纳米尺度范围内,Pt催化剂的乙烯选择性明显高于对大粒径纳米Pt 颗粒的催化剂。这主要是随着Pt 粒径的减小其电子密度降低,导致C2H4吸附减弱,从而更易从催化剂表面上脱附下来,避免进一步加氢生成乙烷。
可见,Pd、Cu 和Pt 催化乙炔选择性加氢反应均表现显著的结构敏感性,即活性金属的粒径大小显著影响到其催化性能。关于催化剂的粒径效应的研究不仅有助于深入理解催化剂的结构敏感性,还可以辨识出乙炔催化选择性加氢反应中的活性和目标产物选择性的主控尺度,指导高效加氢催化剂的可控构筑。
1.2 形貌效应
除了粒径效应外,金属纳米颗粒的形貌效应是催化反应过程结构敏感性的另一种体现。比如,表面暴露(100)面的立方体Pd纳米颗粒的催化活性与暴露(111)面的八面体Pd 纳米颗粒的显著不同,可能是由于暴露的不同活性金属表面的几何和电子结构不同导致[8]。近年来,随着纳米合成技术的快速发展,金属纳米粒子的形貌可控制备及其催化性能的研究受到了广泛的关注[11-12]。Kim 等[13]制备氧化铝负载的立方体和由大量Pd(111)面组成的球形形貌Pd纳米催化剂,发现立方体形貌Pd催化剂在乙炔选择性加氢反应中的活性和乙烯选择性明显高于球形纳米颗粒催化剂,进而认为Pd(100)面对于该反应更为重要。Yarulin等[14]采用类似的方法制备了立方体、立方八面体[由Pd(111)和Pd(100)面]和八面体形貌的Pd纳米颗粒(分别为Pdcub、Pdco和Pdoct),并通过臭氧和紫外辐射处理除去制备过程中残留在金属颗粒表面的表面包裹剂。在乙炔选择性加氢反应中,不同形貌的Pd 纳米颗粒催化剂的乙烯选择性几乎相同,但加氢活性按Pdoct>Pdco>Pdcub顺序依次减小,故认为Pd(111)面的活性比Pd(100)面更高。可见,不同活性金属晶面对于加氢反应活性和乙烯选择性的影响还存在争议,这可能是在纳米金属颗粒制备中引入的表面稳定剂及其在表面的残留带来的。
理论计算作为实验研究的补充,可研究理想晶面上催化反应过程。Yang 等[15]通过密度泛函理论(DFT)计算探究了Pd(211)、Pd(100)和Pd(111)面上乙炔选择性加氢反应过程,揭示了表面结构对活性和选择性的影响。研究结果表明,台阶面这种更开放的表面上乙炔容易发生深度加氢形成乙烷,而密堆积表面Pd(111)是乙烯选择性较高的活性表面。不同表面乙炔加氢活性依次为Pd(211)>Pd(111)>>Pd(100),表明加氢活性由表面原子的排列方式决定而不是由配位数决定,Pd(100)面相对较低的加氢活性可能是由于乙炔在其上的强吸附而导致的。
此外,由于乙炔在Pd催化剂表面的吸附很强,在反应过程可能会导致催化剂的结构改变,从而影响催化加氢性能。Niu 等[16]制备了立方体形貌的Pd纳米颗粒并负载在多层石墨烯上作为乙炔选择性加氢催化剂,并研究了其在反应过程中催化剂结构的稳定性及其对反应的影响。该催化剂经过127h 反应后,乙炔转化率基本保持不变,维持在90%左右。但是,随着反应的进行,催化剂的乙烯选择性逐渐从77%降到3%。反应的碳平衡和热重分析结果排除了催化剂表面积炭的存在。此外,催化剂结构表征发现,Pd 纳米颗粒未出现聚集,且仍是暴露(100)晶面的立方体形貌。然而,高倍透射电镜表征结果表明,随着反应的进行,立方体Pd 纳米颗粒的(100)面从平坦变粗糙,意味着缺陷位和台阶位数目的增加。已有的实验和理论计算结果表明,缺陷位、角位和台阶位等低配位位点易导致乙烷生成。因此,作者认为可能是由于反应过程中立方体形貌的Pd 纳米颗粒表面微观结构的改变导致了乙烯选择性的降低。
随着研究的深入,Teschner 等[17]通过实验研究发现在乙炔加氢反应过程中,Pd 催化剂中会出现渗碳现象,生成次表面碳掺杂Pd 的新相(PdCx)。次表面碳的存在能够显著抑制Pd 催化剂上次表面氢物种的生成,从而减少乙烷的生成,提高Pd 催化剂的选择性。值得指出的是,次表面碳的生成也存在显著的形貌效应,即暴露不同晶面的活性金属纳米颗粒上,次表面碳的生成速率显著不同。通过实验发现,在Pd(111)面上不易形成PdCx,而在Pd(100)面上乙炔分解形成PdCx物相从热力学上很容易进行。Crespo-Quesada等[18]通过原位XRD和理论计算研究也发现,立方体形貌的Pd 上渗碳的速率比八面体形貌的Pd 上高六倍。Yang 等[15]通过理论计算表明存在次表面碳原子时,平坦表面的乙炔加氢活性增加,而台阶表面的活性降低。此外,他们发现在存在次表面氢物种的情况下,乙炔加氢的活性均高于洁净的Pd表面和具有次表面碳的Pd表面上的乙炔加氢活性,而选择性低于后两者。
目前已有的关于乙炔选择性加氢催化剂的形貌效应的研究主要是围绕活性金属Pd 展开,对于其他活性金属如Ni和Cu等未见报道。在未来的研究工作中,尤其是寻找贵金属Pd基催化剂替代品中,关于非贵金属的形貌效应的研究是重要的,这将对催化剂活性位的设计和调控具有一定的指导意义。
除了活性金属的晶面对于乙炔选择性加氢反应有影响之外,载体暴露的晶面及其表面性质也会对催化剂的加氢性能有显著影响。比如,He 等[20]对比研究了暴露不同晶面的γ-Al2O3负载的CrOx催化乙炔选择性加氢性能,发现CrOx/(110)γ-Al2O3与CrOx/(111)γ-Al2O3相比具有更好的加氢性能。催化剂结构表征结果表明,这可能是由于在CrOx/(110)γ-Al2O3表面上,存在相对较多的低价态的活性Cr物种,有利于H2分子的活化。而在(111)γ-Al2O3表面,该Cr 物种的形成较难。另一方面,载体表面酸碱性等性质也会对其负载的活性金属催化性能产生影响。He 等[20]将Pd 负载在具有酸碱性不同的水滑石、MgO 和Al2O3载体,研究三种催化剂的反应性能。结果表明,碱性载体增加了Pd的电子密度,而酸性使得Pd处于缺电子状态且有利于Pd原子的重新分散,从而提高了Pd催化乙炔加氢活性。
1.3 电子效应
如前文所述,在纳米粒子的粒径尺寸大小改变时,有时也会伴随着纳米粒子电子性质的改变,从而影响催化剂的活性及选择性。Cao等[7]在研究Pd/CNT 催化剂时,发现Pd 纳米粒子平均粒径小于3.1nm 时,XPS 测得的Pd03d 峰向低结合能方向偏移,表明Pd 电子密度随粒径的减小而增大。乙炔在Pd 催化剂上的强吸附通常导致表面含碳物种的覆盖率较高,因而用于氢气活化的表面位点大大减少,从而使得氢的活化变得困难,抑制加氢反应的发生。已有研究结果表明,乙炔在富电子Pd 表面的吸附会明显减弱。因此,当粒径减小时,乙炔在表面吸附减弱后,有更多的活性位点用于氢气活化,进而促进加氢反应过程,提高催化剂活性。
进一步,Cao 等[21]提出了通过氮掺杂碳纳米管优化Pd 催化剂的电子性质,调控其催化乙炔加氢反应动力学,见图2。研究结果表明,当N掺杂量不同时,其负载的Pd催化剂电子性质也显著不同。与Pd/N1.4-CNT(数字为N 掺杂分数)和Pd/CNT 相比,Pd/N2.1-CNT 和Pd/N3.5-CNT 催化剂的Pd03d XPS 结合能明显降低,表明Pd 表面电子密度显著提高。对应地,Pd/N2.1-CNT 和Pd/N3.5-CNT 催化剂的吸附能力也明显减弱,乙烯更易从催化剂表面脱附,因而它们比Pd/N1.4-CNT 和Pd/CNT 催化剂具有更高的乙烯选择性。此外,Pd/N3.5-CNT 活性明显低于Pd/N1.4-CNT 和Pd/N2.1-CNT 催化剂。这很可能是因为Pd/N3.5-CNT 催化剂上Pd03d5/2结合能过低(即Pd电子密度过高)导致吸附能力大大减弱,不利于反应物乙炔吸附活化。而且,Pd/N3.5-CNT 催化剂的Pd 纳米粒子也明显大于其他催化剂,对应地Pd(111)活性中心较少,这可能是其活性较低的另一方面原因。因此,适宜的Pd电子结构和Pd纳米粒子的粒径对催化剂的活性、选择性和稳定性非常关键。

图2 反应动力学和乙烯/乙炔程序升温脱附实验结果[21]
针对Pt 催化剂,Kuo 等[10]通过原位XPS 研究发现,随着Pt粒径的减小,Pt 4f7/2峰向高结合能方向移动,意味着Pt电子密度降低。这可能是由于不同的Pt纳米颗粒的粒径效应以及金属与TiO2表面的相互作用而导致。Pt单原子、亚纳米团簇和<1.5nm纳米粒子(PtSA-0.7nm和Pt0.9nm)中Pt 物种价态偏高,介于0 和+2 之间。对于更大粒径的纳米粒子(Pt1.5nm和Pt2.1nm),Pt 物种化学状态接近Pt0。研究结果表明,Pt电子密度的降低减弱了乙烯在催化剂上的吸附,使其更易从催化剂表面脱附,从而提高了乙烯的选择性。值得指出的是,在Pd催化剂上Pd电子密度减小有利于乙烯的吸附,这可能是由于乙烯在不同金属表面的吸附机制不同而导致。
2 第二金属对催化剂结构的调控
引入第二种金属对活性金属的合金化,能够调变活性金属几何和电子结构,进而提高催化反应性能[22-23]。近年来,在乙炔加氢催化剂的研究中,合金化也受到广泛关注。通过加入另一组分金属形成合金,可隔离活性金属位点并调变其电子性质,改变乙炔和乙烯在催化剂表面的吸附构型以及反应动力学行为等,实现乙炔选择性加氢反应催化剂设计与优化。
Cao等[24]采用金属In实现Pd合金化,制备了双金属Pd-In/Al2O3催化剂。在Pd 中加入In 隔离了Pd位点,向Pd转移电子形成富电子的Pd表面,并抑制了氢化钯的形成,提高了乙烯选择性。乙炔在Pd-In/Al2O3上的吸附较弱,促进了氢气的活化,另一方面减小了催化剂粒径,共同促进了Pd-In/Al2O3活性的提高。动力学实验表明(图3),In 的引入显著改变了乙炔选择性加氢反应动力学行为。乙炔反应级数随催化剂中In 含量的增加而增加,说明随着In 含量的增加,乙炔吸附减弱。但在较高的C2H2分压下,反应速率降低,乙炔呈现负反应级数,表明乙炔在催化剂表面覆盖度较大,从而缺乏吸附和解离氢的表面空位,不利于加氢反应。在较高的C2H2分压下,Pd-In/Al2O3的负反应级数绝对值比Pd/Al2O3的小,说明乙炔在双金属表面的吸附较弱,表面空位更多,有利于氢气的活化。这与Pd-In/Al2O3高的乙炔加氢活性一致。此外,Pd-In合金催化剂的性能很大程度上取决于合金组成。结构表征和动力学研究表明,这主要是由于合金催化剂中Pd 活性中心的电子和几何修饰程度的不同导致。针对PdIn 双金属催化剂,Markov 等[25]通过CO-DRIFTS 表征发现,在2000cm-1以下的区域没有明显的吸收峰,意味着催化剂表面Pd 原子被In原子完全隔离形成了完全孤立的Pd 位点。XPS 分析表明,In 不仅孤立了Pd 位点,还改变了其电子性质,降低了费米能级附近d态的密度。这使得乙炔和目标产物乙烯吸附变弱,降低了催化剂加氢活性,但提高了其乙烯选择性。

图3 乙炔分压和氢气分压对催化剂上乙炔加氢反应速率影响[24]
除了常规的合金外,金属间化合物催化剂由于其活性金属和客体金属均匀排列,可以对活性金属实现定向调控的特点而逐渐受到研究者的关注。Feng 等[26]采用DFT 计算研究了金属间化合物PdIn的(110)表面和Pd3In 的(111)表面上乙炔加氢反应过程。结果表明,在PdIn(110)表面上,单个Pd 原子被4个近邻的In原子隔离。C2H2倾向于吸附在相邻的两个Pd 原子上,有利于其通过类乙烯C2H3Pd 中间体加氢制C2H4。C2H4通过弱π 键吸附在Pd 原子上,更易从表面脱附,预示着PdIn(110)表面在反应中应具有较高的选择性。在Pd3In(111)表面上,C2H2和C2H3最有利的吸附位点是三原子Pd 位点上的三齿空位,而C2H4以di-σ 构型吸附不易从表面脱附,易导致副产物乙烷的生成。因此,对乙炔选择性加氢反应而言,PdIn(110)表面比Pd3In(111)表面具有更高的催化选择性。作者进一步通过实验制备了对应的金属间化合物催化剂,验证了DFT 计算研究的结果。
Zn 和Ga 也常作为合金组分被用于炔烃加氢反应中。Zhou等[27]报道了在Pd-Zn金属间化合物的单个Pd 活性位点上,乙烯只存在π 键吸附模式,这使得乙烯更易从Pd-Zn表面脱附下来,而不会过加氢成为副产物乙烷。Pd-Zn-Pd 中结构特点为乙炔以中等强度的σ键吸附提供了两个相邻的Pd位点,这使C C 通过类乙烯中间体活化并易于转化为乙烯,保证了催化剂的反应活性。另外,这些孤立的Pd 活性位点仍能促进H2解离成活性H 物种。H2吸附的微量热实验表明,尽管Zn对Pd的稀释作用导致H2吸附量和吸附能均比Pd 纳米催化剂低,但在初始吸附能为45kJ/mol的情况下,氢仍可能发生解离吸附,Pd-Zn合金催化剂能在含氢反应中为乙炔加氢反应提供所需的活性H物种。Shao等[28]制备碳纳米管负载的纳米Pd2Ga金属间化合物催化剂,发现纳米金属间化合物催化剂表面具有丰富的低配位位点(边、台阶和扭结),因而具有较高的活性。在Ga加入后,Pd与Ga的共价相互作用抑制了反应过程中“绿油”的生成。与Pd/CNT 相比,Pd2Ga/CNT 对β-氢化物和PdCx有抑制作用。Glyzdova 等[29]制备了碳材料为载体的PdGa 催化剂,并研究了其催化乙炔选择性加氢反应性能。他们发现由于Ga 的引入,Pd 颗粒的平均粒径减小了4/5,Pd 的金属分散度较高,因而乙炔加氢活性较高。然而,X 射线吸收光谱表征发现Ga 原子引入后,只有10%的Pd 原子转化为PdxGay相,因此对乙炔加氢反应的选择性改变不明显,乙烯选择性仅提高了3%左右。
此外,Ag和Cu也常作为第二金属用于调变Pd催化剂结构。Riyapan 等[30]通过强静电吸附和电化学沉积联用制备了不同表面Ag 覆盖度(θAg)的PdAg/TiO2催化剂,Ag 的引入使得乙炔以π 吸附模式在Pd 位点上吸附,有利于乙烯的生成而抑制了乙烷的生成。此外,他们发现不同θAg时PdAg催化乙炔选择性加氢性能显著不同。当θAg=0.92ML 时,PdAg/TiO2催化剂加氢活性和乙烯选择性最佳。Zhang等[31]采用理论计算研究了PdCu(0)和PdCu(I)催化剂对乙炔选择性加氢的活性和选择性的影响,其中(0)和(Ⅰ)代表Cu组分的不同价态,分别为0价和正一价。他们发现C2H4在PdCu(0)催化剂上的吸附强度远低于C2H2,而在PdCuガ催化剂上C2H2和C2H4的吸附相当,这表明富含C2H4的反应组分中C2H4相较于C2H2更易吸附在PdCuガ催化剂上。因此,PdCuガ催化剂的选择性比PdCu(0)催化剂差。此外,计算结果还表明加氢反应的活性中心在Pd 及其周围的Cu 位点上,并非是H2在Pd 上解离,溢流到Cu上对炔烃分子加氢。
除了Pd 系合金催化剂,非贵金属Ni 催化剂作为Pd 催化乙炔选择性加氢反应潜在替代品引起广泛关注。Yang 等[32]用密度泛函理论计算了Au、Ag和Cu掺杂Ni表面的活性和选择性的总体趋势,发现单金属Ni 活性较低的主要是由于其较高的乙炔吸附能,通过Au、Ag和Cu等惰性金属的掺杂可以减弱乙炔的吸附,从而提高加氢活性。双金属催化剂的活性大小依次为Au-Ni>Ag-Ni>Cu-Ni。在这些体系中,乙炔的加氢活性与吸附能的关系都是在火山型曲线的强吸附侧。因此,掺杂金属的惰性越强,催化剂表面加氢活性越高。Studt等[33]通过DFT计算预测NiZn 催化剂是性能优异的乙炔选择性加氢反应非贵金属催化剂,并通过实验制备得到了MgAl2O4尖晶石负载的NiZn催化剂,其选择性随着Zn 含量的增加而增加,比同样条件下测试的Pd-Ag 合金的选择性更高。Spanjers 等[34]采用同位素标记和DFT计算研究了乙炔在Ni-Zn金属间化合物催化剂上的加氢和齐聚反应机理。DFT 计算表明,在Ni 中添加Zn 有助于降低乙炔对低聚物的选择性,Ni-Zn 表面C—C 键减少是由于乙炔吸附能及表面覆盖率的降低。动力学实验结果也证实纯Ni金属和Ni-Zn合金表面覆盖率不同。该作者提出乙炔的吸附能可作为C—C 键形成的一个描述符,因为高吸附能导致C2物种的覆盖率增加,C—C键形成的速率增加。
Cao 等[35]通 过DFT 计 算 发 现,相 比 于Ni 和Ni5Ga3金属间化合物催化剂,NiGa金属间化合物催化剂中Ni活性位点被Ga完全隔离,使得乙炔和乙烯分子以π键模式择优吸附,表现出显著提高的乙烯选择性。考虑到非贵金属Ni 电负性低于贵金属Pd,传统的浸渍法和液相还原法难以得到颗粒尺寸均匀的非贵金属金属间化合物纳米催化剂。该作者进一步发展了一种简单、高效的制备方法,即基于层状双金属氢氧化物(LDHs)层板阳离子的可调性,实现粒径相似的Ni、Ni5Ga3和NiGa纳米金属间化合物催化剂的可控制备,并结合球差电子显微镜和X 射线吸收光谱等先进催化剂结构表征技术,解析了催化剂的原子结构和电子性质,发现NiGa金属间化合物催化剂中Ni 活性位点处于完全孤立的状态,且乙炔和乙烯分子通过π键构型吸附,证实了上述理论预测的结果。此外,性能评价结果也表明NiGa 金属间化合物是一种良好的乙炔选择性加氢催化剂,一方面能显著提高乙烯选择性,另一方面能减少“绿油”的生成。类似地,Liu 等[36]开发了一种新型的液相共还原策略制备了粒径均一的Ni-Ga 和Ni-Sn 纳米金属间化合物催化剂,发现由于Ga和Sn对Ni位点隔离和电子结构的调变,使得Ni3Ga 和Ni3Sn2表现出优良的乙炔选择性加氢性能。Li 等[37]使用α-Al2O3作为载体,通过等体积共浸渍的方法制备了NiGa/α-Al2O3催化剂,并与单金属Ni催化剂对比研究了其乙炔选择性加氢反应性能。他们发现晶格中Ga 的存在抑制了解离后的H 物种的移动,限制了乙炔的深度加氢,并可能导致催化剂表面的乙烯吸附减弱,从而使得NiGa/α-Al2O3催化剂具有更高的乙烯选择性。
3 新型单原子(合金)催化剂
随着催化剂制备和表征方法的持续发展,越来越多的研究开始关注将催化剂活性贵金属颗粒从纳米尺度减小到原子尺度,制得单原子催化剂,以期最大化贵金属的利用效率[38-40]。此外,由于原子级分散贵金属催化剂的独特结构特性,单原子催化剂也会显著改变关键物种吸脱附行为和反应机理,有望成为调变催化反应性能的有效途径之一[41-43]。与单原子催化剂类似,将活性金属原子级分散在另一金属中可制得单原子合金催化剂。这是金属催化剂分散的一个极端情况,同样可以大幅提高贵金属的利用效率。近年来,单原子和单原子合金催化剂在乙炔选择性加氢催化剂的研究中引起研究者的关注。
Huang 等[44]采用缺陷纳米金刚石-石墨烯为载体制备原子分散的Pd 催化剂(Pd1/ND@G),Pd 通过与C原子结合形式嵌入到石墨烯的缺陷中,形成的Pd—C键结构抑制了非选择性次表面氢物种的形成。与Pd 纳米团簇催化剂相比,Pd 单原子催化剂的表面C2H4物种更易脱附,抑制其加氢生成乙烷。类似地,Huang 等[45]合成了负载在缺陷纳米石墨烯上的Cu 单原子催化剂(Cu1/ND@G)。Cu 原子通过与3个C原子的键合作用锚定在石墨烯的缺陷位置上。通过DFT 计算发现,Cu1上乙烯加氢的能垒(1.27eV)高于乙烯脱附能垒(1.08eV),表明乙烯在催化剂表面更易脱附而非进一步加氢,预示催化剂具有较高的乙烯选择性。此外,如图4所示,动力学研究结果表明,单原子催化剂Cu1/ND@G和Cu团簇催化剂Cun/ND@G 的表观活化能分别为41.9kJ/mol 和54.3kJ/mol,Cu1催化剂活性明显高于Cu团簇催化剂。此外,Huang等[46]利用原子层沉积法在石墨碳氮化物上合成了原子分散的Pd 催化剂Pd1/g-C3N4,其比Pd 纳米催化剂(Pd-NP)具有更高的乙烯选择性。作者还发现在单原子催化剂上碳二物种聚合反应过程被抑制,因而具有更高的抗结焦性能。Zhou等[47]通过冷冻干燥法制备了负载在N掺杂石墨烯上的Pd 单原子催化剂。单原子催化剂中的Pd-N4结构的强局部配位作用抑制了Pd 的聚集,即使在高温条件下也可以稳定存在。该催化剂在125℃反应温度下表现出优异的乙炔选择性加氢性能,这是由于催化剂表面高浓度的Pd 活性位点以及乙烯在孤立的Pd原子表面吸附能较弱导致的。Zhuo 等[48]研究了缺陷石墨烯(DG)负载的单原子Ni催化剂(Ni1-DG),发现其对乙炔的选择性加氢产物表现出较高的选择性。DFT计算结果表明,Ni单原子在双空位的缺陷石墨烯载体上倾向于与周围未配位的C 形成4 个Ni—C 键。加氢过程中,乙炔经两步加氢通过类乙烯中间体C2H3Ni生成C2H4。第一和第二步的加氢势垒分别为0.89eV 和0.60eV,低于相应的Pd 单原子催化剂(加氢势垒分别为1.54eV 和0.82eV),说明其具有良好的催化加氢活性。深度加氢形成C2H5*中间体需要克服0.80eV 的势垒,高于乙烯脱附的能垒,表明Ni1-DG 催化剂具有高的乙烯选择性,与实验结果相互印证。
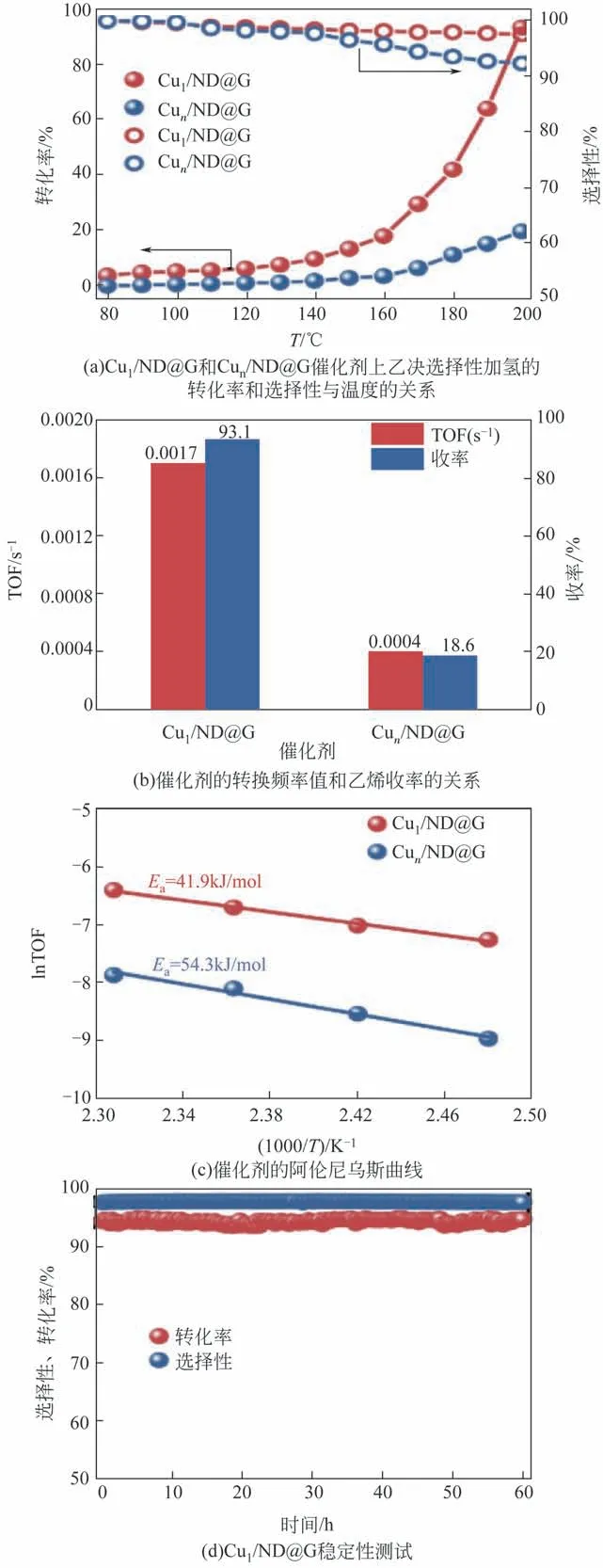
图4 Cu1/ND@G和Cun/ND@G的反应性能[45]
针对单原子合金(SAA)催化乙炔选择性加氢反应,Pei等对比研究了Pd单原子分散的Ag-Pd[49]、Au-Pd[50]和Cu-Pd[51]合金催化剂。Ag-Pd 单原子合金催化剂中电子从Ag向Pd转移,使得Pd表面的电子密度变大,进而弱化了乙烯的吸附。动力学实验结果表明,Ag-Pd单原子合金催化剂上的活化能比单金属Pd/SiO2催化剂高12kJ/mol,说明单原子合金催化剂即使在表面Pd 浓度极低的情况下仍能保持较高的加氢活性。Liu[52]为了解释这种二元合金催化剂的反应机理,利用密度泛函理论研究了Pd-Ag合金纳米团簇上的乙炔加氢反应。结果表明,无论是在Ag 团簇的顶点还是边缘位点,H2和C2H2都能同时与单个Pd 原子结合。此外,加氢生成的C2H4分子位于Pd 原子的顶部位,占据了H2的唯一吸附点,因而C2H4分子无法进一步加氢生成乙烷。Cu-Pd 单原子合金催化剂中,Cu 对单原子Pd 位点的隔离以及电子作用不仅促进了H2的解离,而且减弱了C2H4的吸附,因而催化剂在高乙炔转化率下依然具有高乙烯选择性。对比Au-Pd、Ag-Pd和Cu-Pd 单原子合金催化剂,发现IB 金属在隔离单原子Pd 中起到相似的作用,并且三种催化剂的活化能相似,这表明三种催化剂都具有相似的活性中心或者相似的催化机理。进一步通过DFT 计算研究了不同IB 金属对Pd 单原子合金催化剂作用的差异,结果表明当Cu 或Ag 与单原子Pd形成合金时,电子从Cu或Ag转移到Pd,使其电子密度增大。这与它们的电负性顺序相对应:Au(2.54)>Pd(2.20)>Ag(1.93)≈Cu(1.90)。因此,三种单原子合金催化剂乙烯选择性不同可能是由电子作用的差异导致的。
Cao 等[53]制备了Pd-Cu 单原子合金催化剂,作者发现加入Cu 之后,催化剂对于H2的吸附能力几乎可以忽略不计,这与Batista等[54]观察到的现象相同,可能是由于Cu对Pd的稀释作用所导致。H2在Pd-Cu单原子合金催化剂上的化学吸附应包括H2分子在Pd 原子上解离、H 原子溢流到Cu 上、H 原子回流到Pd 原子再结合以及H2从Pd 原子脱附。Pd-Cu 催化剂中痕量的Pd 可以激活周围原本不活跃的Cu 原子,成为乙炔加氢的活性中心。故即使H2在Pd-Cu 单原子合金催化剂上的吸附比单金属Pd 弱得多,但其对过量乙烯中乙炔加氢仍表现出良好的活性和选择性。Jørgensen等[55]通过基于DFT计算的动力学蒙特卡洛模拟计算对比研究了在Pd(111)、Pd/Cu(111)和Pd/Cu 单原子合金纳米颗粒上的乙炔选择性加氢过程。研究结果表明,乙炔在Pd连续位点上比在Cu位点上更易发生深度加氢反应,单原子合金Pd/Cu(111)表面因而表现出更高的乙烯选择性。但是,Pd/Cu 单原子合金纳米颗粒的选择性比Pd/Cu(111)表面明显低。这主要是由于纳米颗粒上有一些角位、边位等强吸附位点,使得乙烯难以脱附,导致其进一步加氢。该作者还指出,在金属纳米颗粒上存在多种不同类型的位点会导致复杂的动力学耦合现象,使得加氢反应的基元步骤在不同位点上进行,因而常用的展延表面无法作为一个充分的模型表面描述纳米颗粒上的催化反应过程。
活性金属除了原子级分散在惰性的载体和第二金属上,还可以分散在活性金属氧化物载体上,利用单原子独特的结构特性与反应性能,弥补载体催化性能的不足。比如,CeO2(111)上氧空位的形成十分困难,因而其催化加氢活性较弱。为了提高其催化活性,Riley 等[56]基于密度泛函理论的研究,提出在CeO2(111)上掺杂镍原子,从而形成氧空位和暴露单Ce原子位。隔离的O和Ce位点促进了H2在氧空位处的异裂解离,由此产生的O—H 和Ce—H 物种有效地催化乙炔加氢反应,避免了C2H3*中间体的深度加氢。其中,Ni 的掺杂降低了反应决速步骤的能垒,但并不直接参与催化反应,而是创建了新的活性位点。由此可见,单原子或单原子合金的作用机理并不唯一,与不同活性金属以及载体的相互作用有关。
4 结语
理解乙炔选择性加氢催化剂结构敏感性,可阐明主副反应活性位点以及金属纳米颗粒的形貌和电子结构对反应性能的影响机制,为催化剂结构调控指明方向。通过合金及金属间化合物催化剂赋予的几何结构和电子结构的精准调控,可优化关键物种的吸脱附和反应动力学行为,调变目标产物乙烯的脱附速率与其进一步加氢反应速率,并抑制表面碳二物种的耦合生成“绿油”前体,提高催化剂的选择性和稳定性。新型单原子(合金)催化剂由于其独特的结构特征,可抑制关键物种在活性位上不理想的吸附构型,同样可以促进目标产物乙烯的及时脱附,并减少“绿油”前体的生成。目前关于催化剂的失活机理及动力学的研究较少,已有的研究结论也主要是基于催化剂反应前后的统计结果的对比得到初步结论。此外,低负载量的贵金属单原子催化剂和非贵金属及其合金催化剂的质量活性低于现有的工业Pd 基催化剂,乙炔完全转化所需的反应温度较高。然而,高温在热力学上更有利于催化剂表面“绿油”的生成。因此,在下一步的研究工作中,如何构筑高效、稳定且低成本的乙炔选择性加氢催化剂以替换目前工业贵金属Pd 基催化剂将会是研究的重点和难点。
