丁硫克百威在豇豆不同时期施用的降解代谢研究
2020-12-02狄珊珊王新全张昌朋王祥云
王 娣,狄珊珊,王新全,张昌朋,王祥云,*,王 萌
(1.农产品质量安全危害因子与风险防控国家重点实验室(筹),农业农村部农药残留检测重点实验室,浙江省农业科学院 农产品质量标准研究所,浙江 杭州 310021;2.海南大学 园艺学院,海南 海口 570228;3.海南大学 植物保护学院,海南 海口 570228)
豇豆(Vignaunguiculata),俗称豆角、长豆角、带豆、裙豆等[1-2],是我国重要的蔬菜品种之一。豇豆富含维生素B1、维生素B2、维生素C等多种维生素和植物蛋白质等营养成分[3],口感清脆,味道鲜美,深受消费者喜爱。豇豆易栽培,经济效益稳定,在全国范围内广泛种植[1,4]。但豇豆属于花果同期作物,生产过程中极易受到病虫为害[5],菜农常常在豇豆收获期施用农药,以控制病虫害、提高产量,这使得豇豆喷施农药后的安全间隔期难以保证,加重了农药残留隐患[4]。
丁硫克百威(carbosulfan,CAS登录号55285-14-8),分子式为C20H32N2O3S,是一种广谱的氨基甲酸酯类杀虫剂[6],适用于蚜虫[7]、蓟马[8]等虫害防治。丁硫克百威在杧果[9]、苹果[10]、白菜[11]、韭菜[7]等植物体可以代谢成为毒性较高的克百威和3-羟基克百威[12](其主要代谢途径如图1所示),会导致更高的膳食摄入风险。近年来,豇豆中克百威超标的案例也时有报道,如2010年的海南豇豆质量安全事件[13]。此外,在2013年对陕西省10个市的农贸市场、超市和批发市场市售蔬菜的抽样调查[14]和2017上半年对安徽省部分地区批发市场的抽样调查中[15],均有克百威检出。据调查,丁硫克百威也是潜在的克百威残留来源之一。因此,对丁硫克百威及其代谢产物——克百威和3-羟基克百威进行膳食风险评估是非常有必要的。
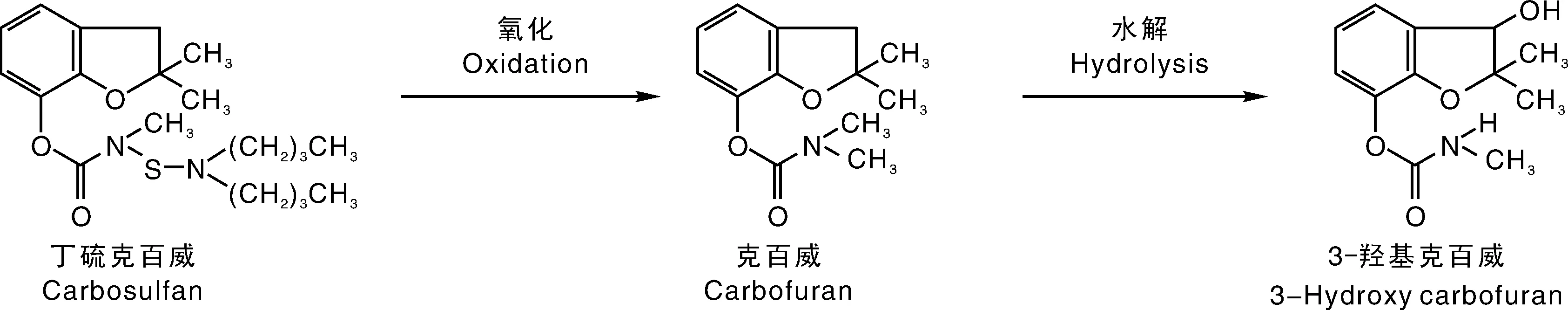
图1 丁硫克百威的主要代谢途径Fig.1 Major metabolism pathways of carbosulfan
为明确丁硫克百威在豇豆不同生长时期的使用风险,特开展相关研究。针对豇豆的生长特点,设置播种期、苗期、结荚期2次施药和结荚期3次施药4种情景,以及不同施药剂量的田间试验,按照一定的时间间隔采集成熟豇豆样品,以液相色谱串联质谱(LC-MS/MS)的方法测定丁硫克百威、克百威和3-羟基克百威的残留量。同时,针对丁硫克百威在结荚期2次和3次施药进行了慢性膳食摄入风险和急性膳食摄入风险评估。总体上,本研究旨在对安全合理使用农药提供实用性依据,通过对丁硫克百威的降解代谢进行研究,以掌握豇豆中丁硫克百威、克百威和3-羟基克百威的残留水平,通过评估其膳食摄入风险水平,探究消费者因食用豇豆而摄入丁硫克百威、克百威和3-羟基克百威的潜在健康风险,从而为豇豆生产的质量安全风险管理提供科学依据。
1 材料与方法
1.1 仪器与试剂
LC-30AD液相色谱仪,日本岛津公司;Triple Quad 4500质谱仪,美国AB SCIEX公司;Heraeus biofuge primo R型离心机,美国Thermo Scientific公司;BSA2202S型电子天平,北京塞多利斯科学仪器有限公司;QT-2型旋涡混合器,上海琪特分析仪器有限公司;0.22 μm滤膜,天津博纳艾杰尔科技有限公司;Millipore-Q超纯水系统,美国Millipore公司。
丁硫克百威、克百威和3-羟基克百威标准溶液(1 000 mg·L-1),农业农村部环境质量监督检验测试中心(天津);35%丁硫克百威种子处理粉剂,美国富美实公司;200 g·L-1丁硫克百威乳油,江苏蓝丰生物化工股份有限公司;乙腈(色谱纯),德国Merck公司;无水硫酸镁(分析纯),永华化学科技(江苏)有限公司;醋酸钠(分析纯),广东光华科技股份有限公司;C18净化材料,天津博纳艾杰尔科技有限公司。试验用水均系由Millipore-Q超纯水系统制得的超纯水,25 ℃条件下电阻率18.2 MΩ·cm。
1.2 分析方法
1.2.1 样品前处理
准确称取10 g样品(精确至0.01 g)至50 mL离心管,加入20 mL乙腈,涡旋提取3 min,加入6 g无水硫酸镁和1.5 g醋酸钠后立即手动剧烈振摇1 min,随后以5 000 r·min-1离心5 min。取上清液1.5 mL至装有50 mg C18净化材料和200 mg无水硫酸镁的2 mL离心管中,涡旋混匀30 s后以5 000 r·min-1离心5 min,取1.0 mL上清液经0.22 μm滤膜过滤至进样小瓶,待LC-MS/MS测定。
1.2.2 仪器条件
液相色谱条件:Inertsil ODS-3色谱柱(75 mm×2.10 mm,2 μm,日本岛津公司);流动相,V(甲醇)∶V(水)=90∶10;流速,0.25 mL·min-1;柱温,35 ℃;进样时间,8 min;进样体积,5 μL。
质谱条件:多反应监测模式(MRM);离子源,正离子源模式(ESI+);气帘气,40 psi(1 psi=0.070 3 kg·cm-2);离子化电压,+5 500 V;温度,450 ℃;喷雾气,30 psi;辅助加热气,30 psi。丁硫克百威、克百威和3-羟基克百威的监测离子对和相关参数见表1。

表1 丁硫克百威、克百威和3-羟基克百威的MRM参数Table 1 MRM parameter of carbosulfan,carbofuran and 3-hydroxycarbofuran
1.2.3 基质标准溶液配制和基质标准曲线绘制
经预试验验证,基质抑制效应较强,为了保证数据的准确性,本试验采用基质标准曲线进行计算。具体方法简述如下:依次准确吸取1 000 mg·L-1的丁硫克百威、克百威和3-羟基克百威标准溶液各1.00 mL,以乙腈定容,配制为100 mg·L-1的混合标准储备液。以1.2.1节获得的空白豇豆提取液分别配制0.005、0.010、0.020、0.100、0.200、0.500 mg·L-1的丁硫克百威、克百威和3-羟基克百威基质标准溶液。以质量浓度为横坐标(x),相应的峰面积为纵坐标(y),绘制标准曲线,外标法定量。
1.2.4 添加回收试验
在空白豇豆样品中添加0.01、0.05、0.20、1.00 mg·kg-1的丁硫克百威、克百威和3-羟基克百威,每个处理5个重复,涡旋混匀后静置30 min,使化合物被豇豆样品充分吸收。样品前处理和仪器测定同1.2.1和1.2.2节,计算该方法的平均回收率和相对标准偏差(RSD)。
1.3 田间试验
田间试验于2016年7—9月在浙江省农业科学院基地进行。豇豆露地种植,土壤肥沃疏松,灌排方便。试验期间以晴好天气为主,54 d的试验周期内仅有18 d出现降雨。根据土壤墒情,适时通过沟灌的方式补水。该基地试验前3 a未种植过豆类作物。根据豇豆的生长特点,分别设置4块试验田,分为播种期、苗期、结荚期2次施药和结荚期3次施药4种施药情景,每种施药情景下仅在对应时期施药。参照丁硫克百威农药产品的标签信息,播种期设最低剂量(2 250 g·hm-2,以有效成分计,下同)、最高剂量(3 750 g·hm-2)和最高剂量的1.5倍(5 625 g·hm-2)3个施药剂量;苗期、结荚期2次施药和结荚期3次施药分别设最低剂量(225 g·hm-2)、最高剂量(375 g·hm-2)和最高剂量的1.5倍(562.5 g·hm-2)3个施药剂量。每个处理重复3次。
播种期施药情景下,采用土施的施药方式,于播种后43、47、51 d采集豇豆样品;苗期施药情景下,于豇豆出苗10 d后,每隔7 d喷雾施药1次,始花期最后1次施药(共4次),分别于距最后一次施药后10 (豇豆成熟)、14 、18 d采集豇豆样品。结荚期2次施药情景下,于始花期第1次施药,间隔5 d施第2次,分别于距最后一次施药后1、3、5、7、10 d采集豇豆样品。结荚期3次施药情景下,于始花期第1次施药,每间隔5 d依次施第2、3次,分别于距最后一次施药后1、3、5、7、10 d采集豇豆样品。
每个小区的边行和每行两边0.5 m内不进行采样,在小区内设置10个以上的采样点,随机采集豇豆样品,每个小区采集1 kg样本装入容器中包扎妥当,带回实验室处理。样品用不锈钢刀具切成2~4 cm的小段,用四分法缩分样本,分取500 g样品,经匀浆后装入封口样品容器中,贴好标签,放入低温冰箱(-20 ℃)中待测。
1.4 慢性膳食摄入风险和急性膳食摄入风险评估
农药的慢性膳食摄入风险(%ADI)和急性膳食摄入风险(%ARfD)参照GB 2763—2019《食品安全国家标准 食品中农药最大残留限量》进行评估,其中,某类食品一餐的最大消费量、以可食部分计的产品单个质量、变异因子,以及丁硫克百威、克百威、3-羟基克百威的急性参考剂量参照联合国粮食及农业组织(FAO)的报告[16],分别取值为0.5 487 kg、0.083 kg、3、0.02 mg·kg-1·d-1、0.001 mg·kg-1·d-1、0.001 mg·kg-1·d-1。
当%ADI或%ARfD≤100%时,表示其风险为可接受,值越小,风险越小;当%ADI或%ARfD>100%时,表示有不可接受的风险,值越大,风险越大。
2 结果与分析
2.1 方法的线性范围、准确度和精密度
在0.005~0.500 mg·L-1范围内,丁硫克百威、克百威和3-羟基克百威的峰面积(y)与质量浓度(x)间具有良好的线性相关性,线性回归方程分别为y=223 002x+28 710、y=106 142x+106和y=4 254.8x-19 699,相关系数(r)均大于0.99,方法定量限(LOQ)均为0.01 mg·kg-1。
添加回收试验结果(表2)显示,0.01~1.00 mg·kg-1添加水平下:丁硫克百威的平均回收率为73%~105%,相对标准偏差(RSD)低于20.1%;克百威的平均回收率为72%~94%,RSD低于12.5%;3-羟基克百威的平均回收率为82%~103%,RSD低于17.3%。以上指标均符合NY/T 788—2018《农作物中农药残留试验准则》中关于添加回收试验的要求。
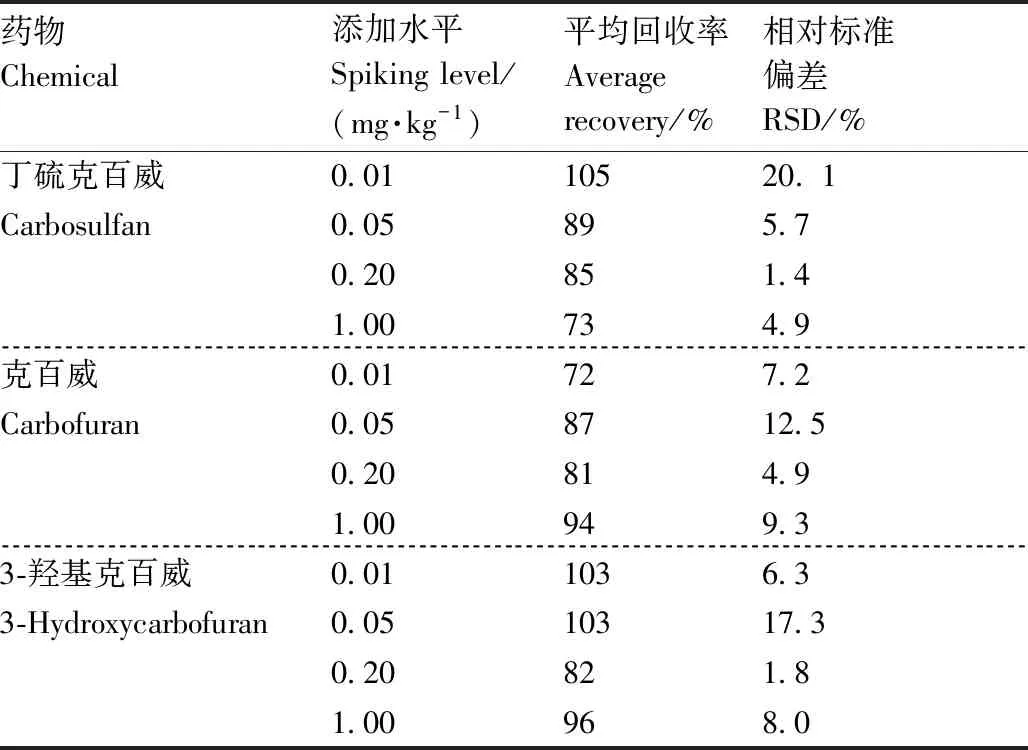
表2 丁硫克百威、克百威和3-羟基克百威在豇豆中的平均添加回收率和相对标准偏差(n=5)Table 2 Average recovery and relative standard deviation (RSD) of carbosulfan,carbofuran and 3-hydroxycarbofuran in cowbean under different spiking levels (n=5)
2.2 丁硫克百威在豇豆播种期使用后的残留
按照推荐剂量的最低剂量、最高剂量和最高剂量的1.5倍在播种期使用丁硫克百威后,药后43、47、51 d采集的豇豆中均无丁硫克百威及其代谢物检出。
2.3 丁硫克百威在豇豆苗期使用后的残留
据GB 2763—2019《食品安全国家标准 食品中农药最大残留限量》:丁硫克百威在豇豆上无最大残留限量(MRL),克百威在豇豆上的MRL为0.02 mg·kg-1,3-羟基克百威以克百威计。
豇豆始花期最后一次使用丁硫克百威后,于药后10、14、18 d分别采集成熟的豇豆样品,测定结果显示:药后10 d的豇豆中无丁硫克百威检出,最高剂量药后10 d克百威(含3-羟基克百威,将3-羟基克百威的残留量乘以换算系数0.93折算成克百威的残留量)的残留量达0.019 mg·kg-1,最高剂量的1.5倍药后10 d 克百威(含3-羟基克百威)的残留量达0.040 mg·kg-1,高于MRL。
2.4 丁硫克百威在结荚期使用后的残留及其风险评估
2.4.1 丁硫克百威在结荚期使用后的残留
在结荚期2次使用丁硫克百威,在药后1、3、5、7、10 d采集的豇豆中,丁硫克百威、克百威和3-羟基克百威均有检出,检出浓度随时间推进而降低。药后1 d采集的豇豆中,丁硫克百威的残留值较高;药后1、3、5 d采集的豇豆中克百威(含3-羟基克百威)残留量均高于GB 2763—2019规定的MRL;以最高剂量和最高剂量的1.5倍施药后7 d,豇豆中的克百威(含3-羟基克百威)残留量仍高于GB 2763—2019规定的MRL;直至药后10 d,3种剂量下豇豆中的克百威(含3-羟基克百威)残留量才降至GB 2763—2019规定的MRL以下(表3)。
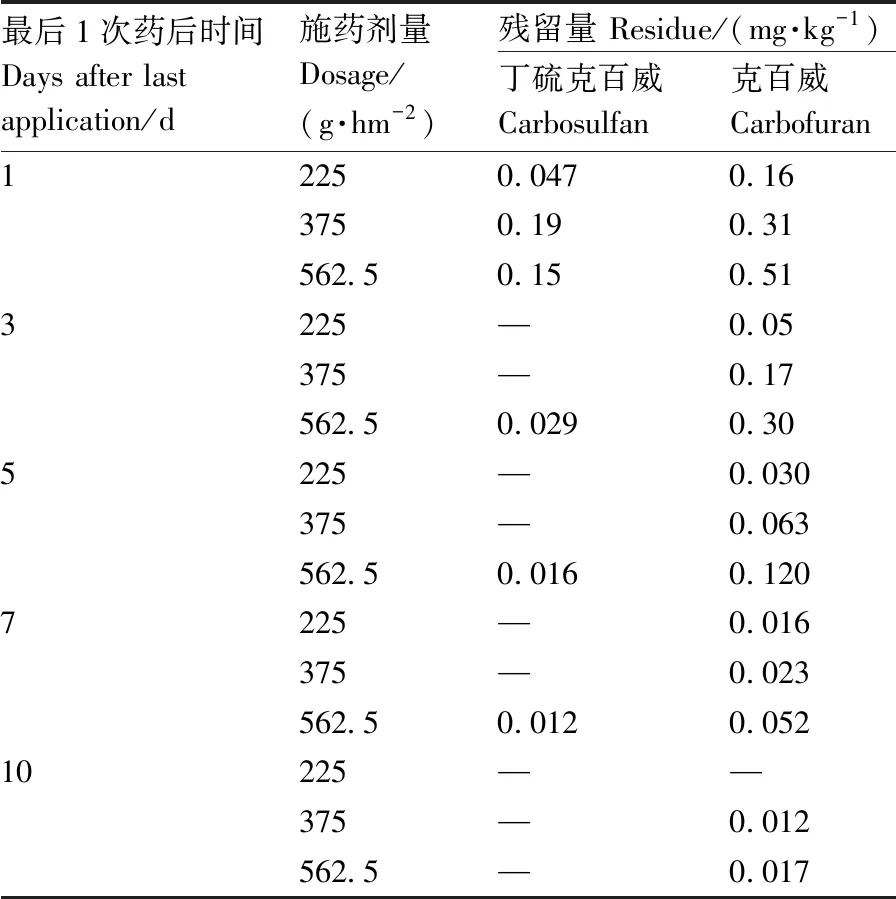
表3 丁硫克百威结荚期2次施用后在豇豆中的残留动态Table 3 Residue dynamics of carbosulfan after double application during fruiting stage
在结荚期3次使用丁硫克百威,在药后1、3、5、7、10 d采集的豇豆中,丁硫克百威、克百威和3-羟基克百威均有检出,且检出浓度随时间推进而降低。药后1 d和3 d采集的豇豆中丁硫克百威的残留量较高;药后1、3、5 d的豇豆中克百威(含3-羟基克百威)残留量均高于GB 2763—2019规定的MRL;最高剂量和最高剂量1.5倍药后7 d,豇豆中的克百威(含3-羟基克百威)残留量仍高于MRL;最低剂量和最高剂量药后10 d,豇豆中的克百威(含3-羟基克百威)残留量已低于MRL,但最高剂量1.5倍药后10 d的豇豆中克百威(含3-羟基克百威)残留量仍高于MRL(表4)。
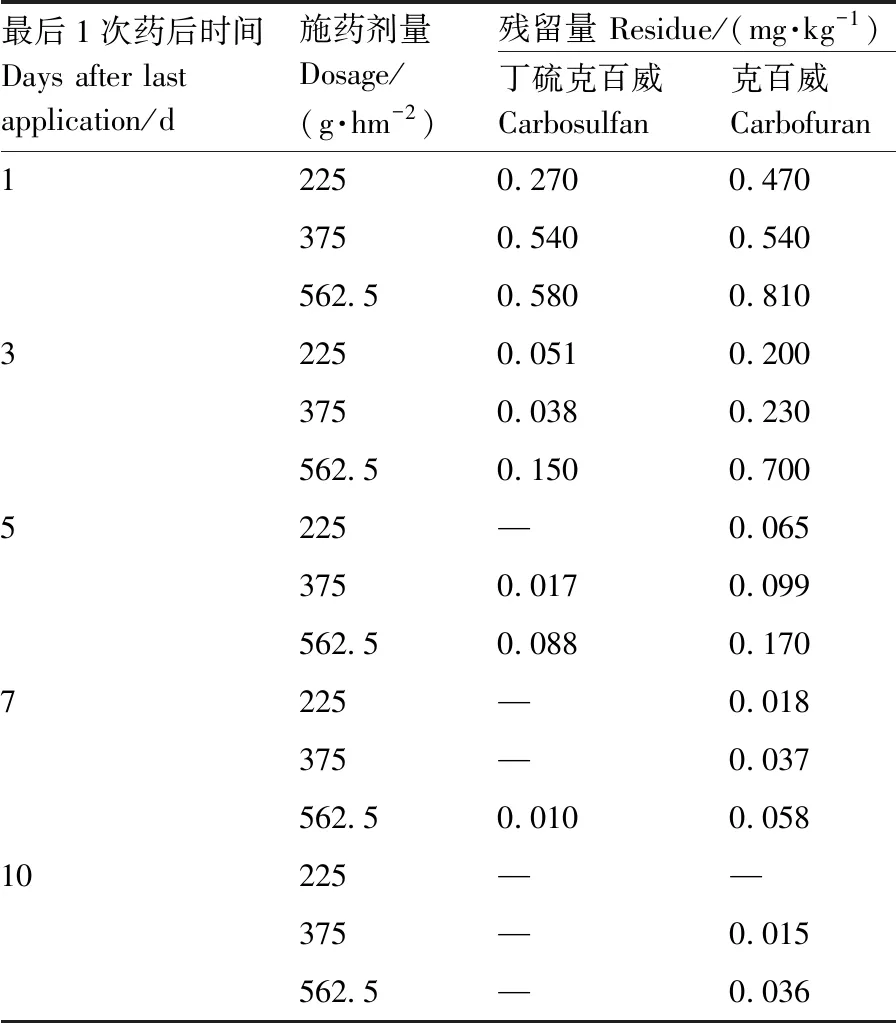
表4 丁硫克百威结荚期3次施用后在豇豆中的残留动态Table 4 Residue dynamics of carbosulfan after triple application during fruiting stage
2.4.2 丁硫克百威在结荚期使用后的风险评估
由于结荚期2次和3次施药后丁硫克百威、克百威(含3-羟基克百威)残留量较高,所以进一步开展风险评估。如图2、3所示,丁硫克百威的%ADI和%ARfD均在药后1 d最高,分别为1.37%~16.9%和1.74%~19.6%;克百威(含3-羟基克百威)的%ADI和%ARfD也表现为药后1 d最高,分别为45.8%~239%和110%~555%。结荚期2次施药和3次施药后丁硫克百威的%ADI和%ARfD均低于100%,表明其慢性膳食摄入风险和急性膳食摄入风险均可接受。但是,当施用剂量为最高剂量的1.5倍时,结荚期2次施药情景下,克百威(含3-羟基克百威)的%ADI在药后1 d高于100%,其慢性膳食摄入风险不可接受;克百威(含3-羟基克百威)的%ARfD,在最低剂量施药后1 d、最高剂量施药后前3 d、最高剂量的1.5倍施药后前5 d均高于100%,其急性膳食摄入风险均不可接受。结荚期3次施药情景下,最低剂量和最高剂量施药后1 d,最高剂量的1.5倍施药后前3 d,克百威(含3-羟基克百威)的%ADI均高于100%,其慢性膳食摄入风险不可接受;最低剂量和最高剂量施药后前3 d、最高剂量1.5倍施药后前5 d,克百威(含3-羟基克百威)的%ARfD均高于100%,其急性膳食摄入风险不可接受。
3 讨论
丁硫克百威使用后的超标风险主要源于其代谢物——克百威(含3-羟基克百威)。本试验表明,苗期以最高剂量的1.5倍施用丁硫克百威将导致药后10 d的豇豆中克百威(含3-羟基克百威)残留量超标,以最高剂量施药后10 d的豇豆中克百威(含3-羟基克百威)残留量也已接近GB 2763—2019规定的MRL;结荚期2次或3次施药后7 d内克百威(含3-羟基克百威)的残留量超标;结荚期以最高剂量的1.5倍3次施药10 d后豇豆中克百威(含3-羟基克百威)的残留量仍高于GB 2763—2019规定的MRL。这与宋禹等[11]的研究结果一致:在白菜中喷施丁硫克百威后,代谢产生的克百威和3-羟基克百威含量随时间延长均呈现先升高后降低趋势,且半衰期远大于丁硫克百威。因此,从安全监管的角度,播种期使用丁硫克百威不会导致豇豆中残留超标,可以安全使用;但苗期和结荚期使用丁硫克百威存在极高的风险,应考虑禁止其在播种期之外使用。此外,结荚期3次施药情景的残留量显著高于2次施药,其原因可能包括:一是部分来自于3次施药残留的叠加;二是2次施药时豇豆正处于快速生长期[17],而3次施药时豇豆生长已较为缓慢,农药残留代谢较慢。
膳食风险评估结果显示:结荚期施药,2次施药和3次施药后的膳食摄入风险主要源于丁硫克百威的代谢物——克百威(含3-羟基克百威)。其中,丁硫克百威的慢性膳食摄入风险和急性膳食摄入风险均较低,小于100%。但当以最高剂量的1.5倍在结荚期2次施药后1 d,克百威(含3-羟基克百威)的%ADI高于100%,其慢性膳食摄入风险不可接受;在最低剂量施药后1 d、最高剂量施药后前3 d、最高剂量的1.5倍施药后前5 d,克百威(含3-羟基克百威)的%ARfD均高于100%,其急性膳食摄入风险不可接受。结荚期3次施药情景下,以最低剂量和最高剂量施药后1 d、最高剂量的1.5倍施药后前3 d,克百威(含3-羟基克百威)的%ADI均高于100%,其慢性膳食摄入风险不可接受;以最低剂量和最高剂量施药后前3 d、最高剂量的1.5倍施药后前5 d,克百威(含3-羟基克百威)的%ARfD均高于100%,其急性膳食摄入风险不可接受。因此,丁硫克百威在豇豆结荚期使用会产生极高的急性膳食摄入风险,应禁止丁硫克百威在结荚期的使用。
与其他类似的文献相比,大部分研究丁硫克百威或者其他农药残留的文献只涉及农药的降解代谢[7,11],而本文在分析降解代谢的基础上加入了膳食风险评估,旨在从食品安全的角度引起人们的重视,从而为农药的合理使用提供参考。
根据本研究的残留数据和风险评估结果,丁硫克百威在豇豆中的使用存在较大的质量安全和膳食风险,应对其使用加以严格的限制:建议不允许在豇豆播种期之外使用。
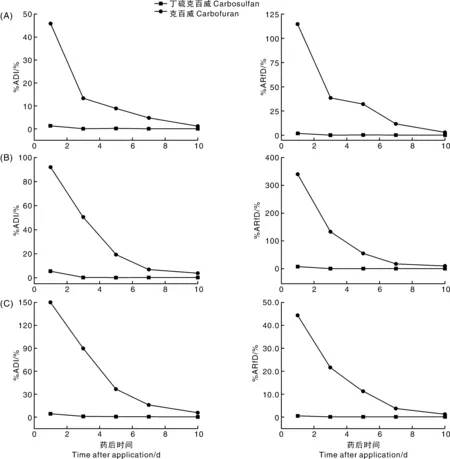
A~C的施药剂量分别为最低剂量、最高剂量和最高剂量的1.5倍。图中克百威的数据包含3-羟基克百威。下同。The application dosage in A-C was the lowest dose,the maximum dose,and 1.5 times the maximum dose according to the registration,respectively.The data for carbofuran included 3-hydroxycarbofuran.The same as bleow.图2 结荚期2次施药场景豇豆样本的膳食摄入风险Fig.2 Risk assessment of cowpea samples after double application during fruiting stage
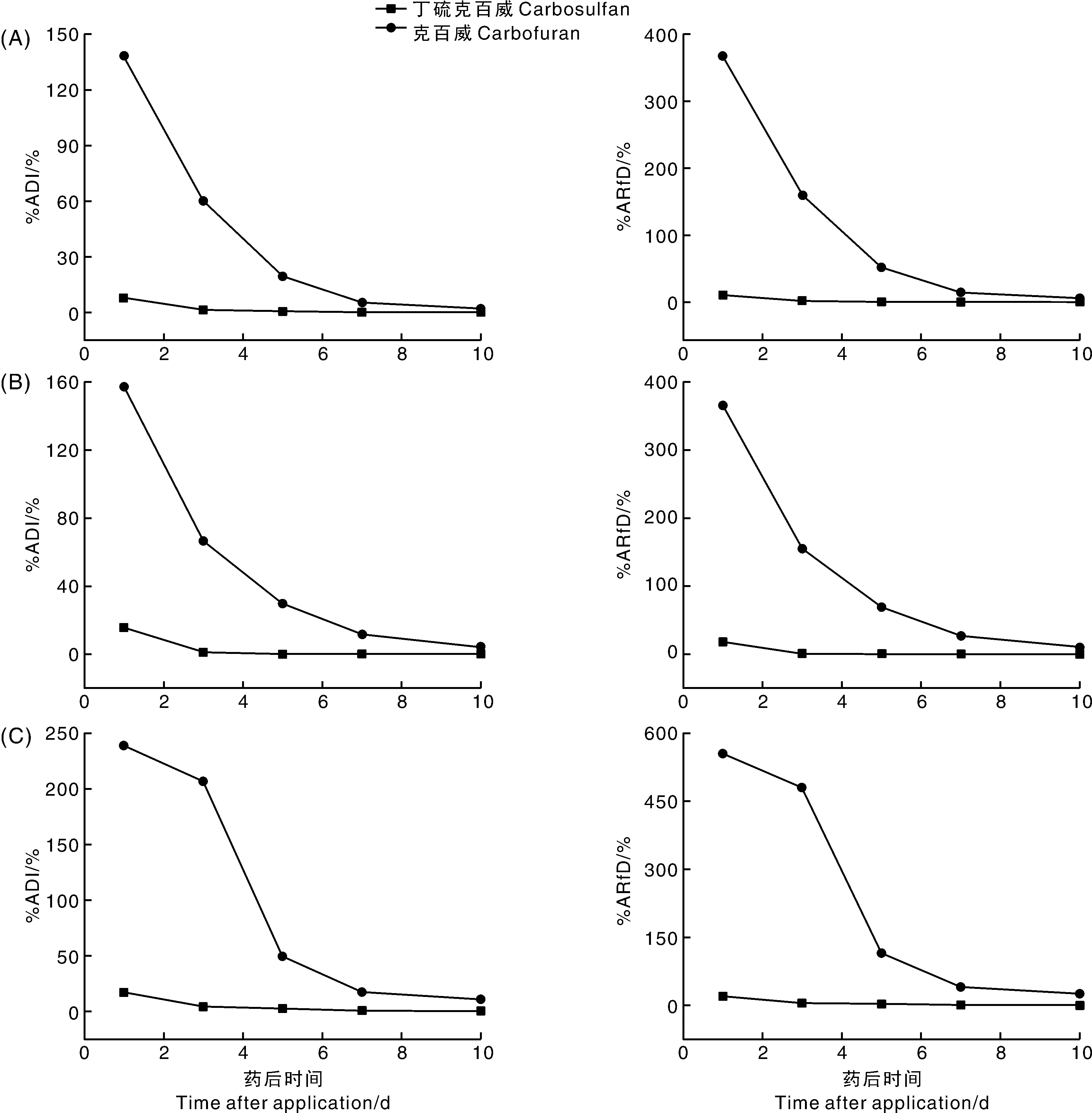
图3 结荚期3次施药后豇豆样本的膳食摄入风险Fig.3 Risk assessment of cowpea samples after triple application during fruiting stage
