微水固相法对皂荚多糖的阳离子化改性工艺研究
2020-12-01朱昌玲张锋伦
朱昌玲, 雷 鹏, 张锋伦
(中华全国供销合作总社南京野生植物综合利用研究所,江苏 南京 211111)
皂荚(GleditsiasinensisLam.)又名皂荚树、皂角、猪牙皂等,皂荚树是理想的木本植物多糖原料资源[1-3]。皂荚多糖是存储性多糖,存在于种子胚乳细胞壁。皂荚种子的内胚乳质量占种子组成的30%~40%,而内胚乳中聚糖(主要为半乳甘露聚糖)质量分数高达70%左右[4-5]。半乳甘露聚糖中每个糖单体平均有 3个活性羟基,可以在一定的条件下通过羟基官能团进行化学反应。化学改性在半乳甘露聚糖分子中引入亲水基团,提高了亲水性和溶胀速度,同时降低了水不溶物含量,使半乳甘露聚糖性能更加优良,应用更加广泛[6]。
微水固相法是基于半乳甘露聚糖吸水膨胀特点提出的一种创新性化学改性方法,是将皂荚多糖微水吸胀的过程与反应试剂的渗入过程进行耦合,也就是在吸水膨胀过程中同步进行化学改性反应。该工艺对微水吸胀后的皂荚种子胚乳片进行压延破壁和挤压质构处理,胚乳片呈蓬松多孔雪花片状,解决了溶剂法或干法反应中试剂与物料接触面小等缺点,大幅度提高了反应效率,降低了生产成本[7]。本研究以皂荚种子胚乳片为原料,以3-氯-2-羟丙基三甲基氯化铵为醚化剂,考察了氢氧化钠质量分数、醚化剂质量分数、反应温度及反应时间对阳离子皂荚多糖黏度和取代度的影响,以期为阳离子皂荚多糖的工业化生产提供参考,从而推进皂荚多糖的高效应用。
1 材料与方法
1.1 材料、试剂与仪器
皂荚种子胚乳片,由河北涉县供销社提供;NaOH,工业级;95%(体积分数)乙醇,食品级;无水乙醇,分析纯;3-氯-2-羟丙基三甲基氯化铵(纯度69%);均为市购。
捏合机,自制;三辊式压片机,自制;万能粉粹机;PHS-25型pH计,上海仪电科学仪器科技有限公司;NDJ-5S旋转黏度计,上海昌吉地质仪器有限公司;H/T16MM台式高速离心机,湖南赫西仪器装备有限公司;FTIR- 650傅里叶变换红外光谱仪,广州科晓科学仪器有限公司;LVDV-Ⅲ Ultra型流变仪,美国Brookfield公司。
1.2 皂荚多糖的阳离子化改性路线
采用皂荚多糖的阳离子改性Williamson醚化反应,即皂荚多糖分子与阳离子醚化剂3-氯-2-羟丙基三甲基氯化铵发生双分子亲核取代反应[8-9],具体见下图。皂荚多糖在碱性环境下形成皂荚多糖氧负离子,然后作为亲核试剂进攻醚化剂环上的中心碳原子,形成阳离子皂荚多糖。

1.3 微水固相法对皂荚多糖的阳离子化改性工艺
称取皂荚种子胚乳片500 g,加入250 mL一定质量分数NaOH溶液,在35 ℃下搅拌碱化30 min,使胚乳片充分溶胀,将已完全溶胀的胚乳片进行压片处理,使用三辊式压片机将胚乳片压制成雪花片状,再加入500 mL一定质量分数的3-氯-2-羟丙基三甲基氯化铵溶液作为醚化剂,在捏合机中进行改性反应,控制反应温度和反应时间。反应结束后,即得阳离子皂荚多糖,用75%乙醇洗涤反应产物至中性,抽滤、干燥、粉碎,备用待测。
1.4 反应条件对产物黏度和取代度的影响
1.4.1NaOH质量分数 固定醚化剂溶液质量分数为69%、反应温度为60 ℃、反应时间为4 h,考察NaOH质量分数(10%、 20%、 30%、 40%、 50%)对产品黏度和取代度的影响。
1.4.2醚化剂质量分数 固定NaOH质量分数为40%、反应温度为60 ℃、反应时间为4 h,考察醚化剂质量分数(30%、 40%、 50%、 60%、 69%)对产品黏度和取代度的影响。
1.4.3反应温度 固定NaOH质量分数为40%、醚化剂质量分数为60%、反应时间为4 h,考察反应温度(40、 50、 60、 70、 80 ℃)对产品黏度和取代度的影响。
1.4.4反应时间 固定NaOH质量分数为40%、醚化剂质量分数为60%、反应温度为60 ℃,考察反应时间(1、 2、 3、 4、 5、 6 h)对产品黏度和取代度的影响。
1.5 测定方法
1.5.1含水率 按GB 5009.3—2016直接干燥法测定。
1.5.2黏度 参照SY/T 5764—2007《压裂用植物胶用技术要求》所述的方法进行测定。首先,分别配制质量分数为1.0%的阳离子皂荚多糖溶液,然后将配制好的溶液缓慢搅匀后,用旋转黏度计测量其黏度。
具体配制方法:量取500 mL的蒸馏水倒入烧杯中,低速启动搅拌器,缓慢加入3.0 g不同含水率的待测多糖(粉粹、过0.09 mm筛),搅拌至完全溶解,加盖置于25 ℃水浴锅中,恒温2 h。
1.5.3水不溶物 参照SY/T 5764—2007进行测定。按1.5.2节所述的方法配制待测溶液,配置成质量分数为0.4%的阳离子皂荚多糖溶液500 mL。在质量恒定(精确到0.1 mg)的离心管中称取配置好的溶液50.20 g,将离心管放入离心机中,在3 000 r/min的速度下离心30 min,倾倒出上层溶液;加入蒸馏水至50 mL,用玻璃棒搅拌洗涤,再离心20 min,再倾倒出上层溶液,如此洗涤3次;将离心管放入恒温干燥箱中,在105 ℃烘2 h后取出放干燥器中冷却20 min,称量,再烘干1 h,冷却,称量,直至质量恒定。
水不溶物的计算公式如下:
式中:η—水不溶物,%;m—称取的阳离子皂荚多糖样品质量,g;m2—水不溶物和称量瓶总质量,g;m1—称量瓶干质量,g;w—样品含水率,%。
1.5.4取代度 取代度是指多糖分子中每个葡萄糖单元上的羟基被取代的平均数。制备阳离子皂荚多糖所使用的阳离子试剂是3-氯-2-羟丙基三甲基氯化铵。因此,可以通过测定皂荚多糖与阳离子试剂反应后的产物分子中氮元素含量的增加值来确定皂荚多糖分子中葡萄糖苷元上的羟基被取代的量,从而计算出取代度[8]。
1.5.5红外光谱表征 将皂荚种子胚乳片、阳离子皂荚多糖(反应条件为NaOH质量分数40%、醚化剂质量分数60%、反应温度60 ℃、反应时间4 h时产物,其黏度为1 196.2 mPa·s、取代度为0.151)粉粹,过0.09 mm筛,备用。再分别精密称取1.5 mg备用样品与15.0 mg KBr混合研磨均匀,压片后在傅里叶变换红外光谱仪上进行红外光谱测试,扫描波数范围在400~4000 cm-1[10-11]。
1.5.6核磁共振氢谱表征 将一定量的阳离子化改性前后的皂荚多糖纯品分别溶于D2O中,在293 K温度下进行核磁共振仪分析(600 Hz)[12]。
1.5.7表观黏度测试 将1 g阳离子皂荚多糖样品(粉粹、过0.09 mm筛)用3 mL无水乙醇进行润湿,再迅速倒入97 mL的蒸馏水中,在60 ℃下水浴磁力搅拌,使样品达到最大程度的水合。用流变仪(LV4号转子)在20.0 ℃条件下测定溶液在不同剪切速率下的表观黏度[13]。
2 结果与讨论
2.1 反应条件对阳离子皂荚多糖黏度和取代度的影响
2.1.1NaOH质量分数 反应体系中的碱是不直接参与反应的,主要是为了活化反应基团,碱的作用有2种:一是对皂荚多糖分子上的羟基进行碱化活化;二是对阳离子醚化剂进行活化,使其产生环氧基团。碱的用量不足会导致反应基团不能充分活化,反应不能最大程度进行[14]。
NaOH质量分数对阳离子皂荚多糖黏度和取代度的影响如表1所示。随着NaOH质量分数的增加,反应产物的黏度出现明显的降低,说明碱用量对皂荚多糖的相对分子质量有显著的影响。这是因为NaOH会导致皂荚多糖的分子链断裂,随着用量的增加,皂荚多糖的分子结构被破坏得更严重,最终导致相对分子质量逐步下降,进而降低了皂荚多糖溶液黏度。为了得到较高分子质量的阳离子皂荚多糖,保留产物高分子植物多糖的基本性能。本实验中,NaOH的质量分数为40%时,产物具有较高的黏度和取代度值。
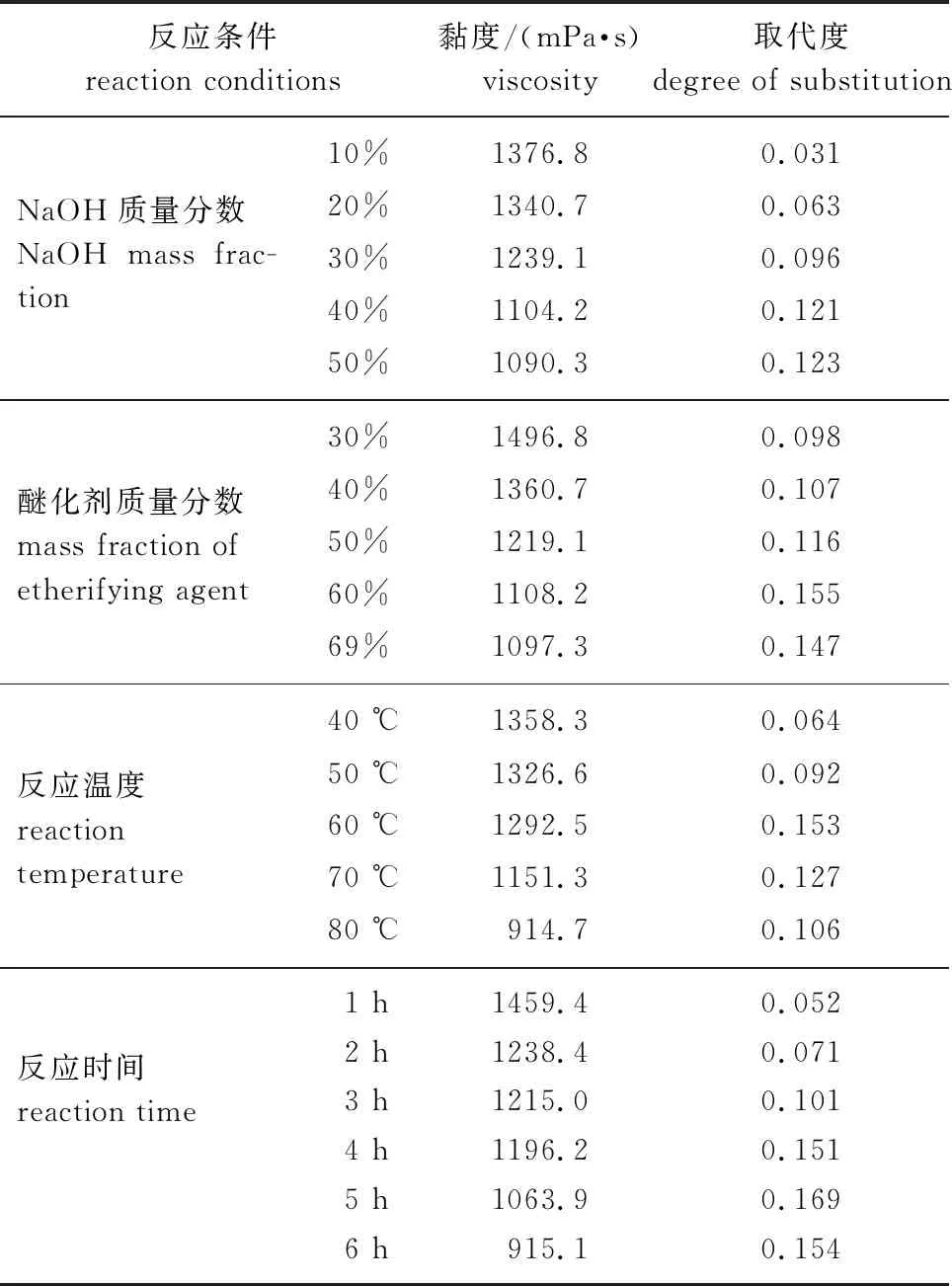
表1 反应条件对改性产物黏度和取代度的影响Table 1 Effect of reaction conditions on viscosity and substitution of modified products
2.1.2醚化剂质量分数 醚化剂质量分数对产物黏度和取代度的影响如表1所示。3-氯-2-羟丙基三甲基氯化铵是一种广泛使用的季铵盐型阳离子醚化剂。随着其用量增大,产物取代度逐渐增加;而醚化剂用量的加大,为了维持反应体系的碱性状态,NaOH的用量也是需要增加的,这会造成产物黏度逐渐降低。本实验结果表明:醚化剂质量分数60%为优,有利于在较低成本下获得较高黏度和取代度的阳离子皂荚多糖。
2.1.3反应温度 由表1可知,随着反应温度的提高,产物黏度逐渐降低;而取代度呈现先增加后降低的趋势,反应温度为60 ℃时取代度最高。这是由于提高反应温度,增加了Na+向皂荚多糖内部扩散的速率,以及皂荚多糖氧负离子与醚化剂的有效碰撞率,因此增大了醚化反应的速率,提高了产物的取代度。不过反应温度继续升高,产物分解的副反应也会更加剧烈,所以取代度又呈现下降趋势。同时,反应温度的不断升高也会引起皂荚多糖分子的降解,使产物相对分子质量降低,黏度下降,并造成醚化反应不稳定。因此,本实验最佳反应温度为60 ℃。
2.1.4反应时间 反应时间对产品黏度和取代度的影响见表1。由表1可知,反应时间越长,反应产物的黏度越低,特别是反应时间超过4 h后,产物的黏度下降更为显著,因此控制反应时间十分重要。这可能是在降解反应与醚化反应的竞争中,醚化反应时间为3~4 h对醚化取代有利,而反应时间进一步延长则对降解反应有利。另外,随着反应时间的增加,取代度增大,当反应时间超过4 h后,取代度变化则不再显著。因此确定最优反应时间为4 h。
综上所述,确定了皂荚多糖的阳离子改性条件:皂荚种子胚乳片500 g、 40% NaOH溶液250 mL、 60% 3-氯-2-羟丙基三甲基氯化铵溶液500 mL、反应温度60 ℃和反应时间4 h。该条件下制备的皂荚多糖阳离子改性产品经检测:含水不溶物2.81%,黏度为1 196.2 mPa·s(1%的水溶液,25 ℃),取代度为0.151。
2.2 红外光谱表征
皂荚多糖、阳离子皂荚多糖红外图谱如图1所示。从图中可以看出,皂荚多糖的特征吸收峰3422 cm-1处为O—H伸缩振动,2926 cm-1处为C—H伸缩振动,1652 cm-1处为C—O伸缩振动。与皂荚多糖相比,阳离子皂荚多糖还有许多新特征峰,如1489 cm-1处是季铵基团上C—H伸缩振动吸收峰,1420 cm-1处是C—N的伸缩振动,913 cm-1为C—N弯曲振动的中强吸收峰,2360 cm-1处是NH4+的振动吸收峰,这些特征峰的出现表明了阳离子醚化剂和皂荚多糖发生了反应,季铵基团成功地引入到皂荚多糖上,证实了季铵型阳离子皂荚多糖的生成[15]。
2.3 核磁共振氢谱表征
皂荚多糖、阳离子皂荚多糖以D2O为溶剂的核磁共振氢谱图见图2。

1.皂荚多糖Gleditsia polysaccharide; 2.阳离子皂荚多糖cationic Gleditsia polysaccharide

图3 不同质量分数阳离子皂荚多糖水溶液 表观黏度随剪切速率的变化Fig.3 Variation of viscosity of different mass fraction cationic Gleditsia sinensis polysaccharide aqueous solution with shear rate
由图2可知,皂荚多糖和阳离子皂荚多糖的谱图中均出现的化学位移(δ)3.9~4.5处宽而广的峰为皂荚多糖结构上氢质子峰;阳离子皂荚多糖由于季铵基团的引入,其谱图中δ3.44处出现了季铵基团上甲基的氢质子峰,由此可以证明产物实现了季铵型阳离子化反应[11]。
2.4 阳离子皂荚多糖表观黏度测试
不同质量分数阳离子皂荚多糖水溶液的表观黏度随剪切速率的变化结果见图3。由图3可知,随着剪切速率增大,阳离子皂荚多糖水溶液的表观黏度下降,表现出剪切变稀的特点,符合假塑性流体特征。当剪切速率增大到一定程度时,阳离子皂荚多糖水溶液的表观黏度趋于恒定。阳离子皂荚多糖水溶液的表观黏度随着质量分数增大而增大,当阳离子皂荚多糖质量分数增加到1.5%时,其表观黏度急剧增大。这是因为阳离子皂荚多糖水溶液的质量分数增大,其分子链之间距离减小,在水溶液中更易互相缠结形成网状结构,导致其表观黏度大幅度上升。
3 结 论
3.1以皂荚种子胚乳片为原料,以3-氯-2-羟丙基三甲基氯化铵为醚化剂,采用微水固相工艺对皂荚多糖进行阳离子化改性;通过单因素试验考察了氢氧化钠质量分数、醚化剂质量分数、反应温度及反应时间对反应产物黏度和取代度的影响,确定了最优反应条件:皂荚种子胚乳片500 g、质量分数为40%的NaOH溶液250 mL、质量分数为60%的3-氯-2-羟丙基三甲基氯化铵溶液500 mL、反应温度60 ℃和反应时间4 h。在该条件下制备的阳离子皂荚多糖产品含水不溶物2.81%、黏度1 196.2 mPa·s(1%的水溶液,25 ℃)、阳离子取代度0.151。
3.2红外光谱、核磁共振氢谱的表征结果均证明皂荚多糖实现了季铵型阳离子化反应;阳离子皂荚多糖的表观黏度测试结果符合皂荚多糖的假塑性流体特征,说明产物仍然具备皂荚多糖的大分子聚糖胶特性。
