临床药师对1例罕见的吉非替尼致肺腺癌患者肝损伤伴胆囊炎的用药分析
2020-11-30廖玉芳邹泽岳建农
廖玉芳 邹泽 岳建农
摘 要 目的:探討临床药师在吉非替尼致肺腺癌患者肝损伤伴胆囊炎治疗过程中的作用,并为类似患者的治疗提供参考。方法:临床药师参与1例吉非替尼致肺腺癌患者肝损伤伴胆囊炎的治疗过程。该患者长期口服吉非替尼片进行抗肿瘤治疗,因转氨酶异常升高入院,医师给予静脉滴注硫普罗宁钠+乙酰半胱氨酸+还原型谷胱甘肽+胞磷胆碱进行保肝治疗,效果不佳。临床药师查阅文献并结合患者病情分析后建议停用吉非替尼,采取静脉滴注异甘草酸镁注射液0.2 g+5%葡萄糖注射液250 mL,qd进行单药保肝治疗;患者出院后口服吉非替尼片,再次因转氨酶异常升高入院,并伴非感染、非结石性胆囊炎,临床药师建议继续静脉滴注异甘草酸镁注射液0.2 g+5%葡萄糖注射液250 mL,qd进行保肝治疗,同时口服胆舒胶囊0.9 g,tid进行保守治疗,并密切监护患者相关指标的变化;于出院后嘱患者停用吉非替尼,口服盐酸埃克替尼片0.125 g,tid+复方红豆杉胶囊0.6 g,tid进行抗肿瘤治疗。结果:医师采纳临床药师的意见;患者转氨酶恢复正常水平,胆囊炎性症状基本消退。结论:在治疗吉非替尼致肺腺癌患者肝损伤伴胆囊炎过程中,临床药师协助医师完善了治疗方案,保障了其用药的有效性。
关键词 吉非替尼;肺腺癌;药物性肝损伤;胆囊炎;药学监护
中图分类号 R969.3;R734.2 文献标志码 A 文章编号 1001-0408(2020)20-2546-05
DOI 10.6039/j.issn.1001-0408.2020.20.20
ABSTRACT OBJECTIVE: To investigate the role of clinical pharmacists in the therapy of gefitinib-caused liver injury complicated with cholecystitis in a patient with lung adenocarcinoma, and to provide reference for the therapy of similar type of patients. METHODS: Clinical pharmacists participated in the treatment for gefitinib-caused liver injury complicated with cholecystitis in a patient with lung adenocarcinoma. The patient took Gefitinib tablets orally for a long time for anti-tumor treatment, and was hospitalized due to abnormal increase of transaminase. The doctors gave intravenous infusion of tiopronin sodium+ acetylcysteine+reduced glutathione+citicoline to protect liver, but the effect was not good. After consulting the literature and analyzing the patients condition, clinical pharmacists suggested that gefitinib should be stopped, and Magnesium isoglycyrrhizinate injection 0.2 g+5% Glucose injection 250 mL, ivgtt, qd for liver protection treatment. After discharge, the patient took Gefitinib tablets orally and was admitted to hospital again due to abnormal increase of transaminase, and suffered from non-infectious and non-calculous cholecystitis. Clinical pharmacists suggested continuing intravenous drip of Magnesium isoglycyrrhizinate injection 0.2 g+5% Glucose injection 250 mL, qd for liver protection treatment, oral administration of Danshu capsules 0.9 g, tid for conservative treatment; at the same time, closely monitoring the changes of related indicators. After discharge, clinical pharmacists instructed patients to stop gefitinib, and take Icotinib hydrochloride tablets 0.125 g, tid+Compound Taxus capsules 0.6 g, tid for anti-tumor treatment. RESULTS: The doctors adopted the opinions of clinical pharmacists, and the transaminase levels returned to normal, and the symptoms of cholecystitis basically subsided. CONCLUSIONS: In the treatment of gefitinib-caused liver injury complicated with cholecystitis in patients with lung adenocarcinoma, clinical pharmacists assisted doctors to improve the treatment plan and ensure the effectiveness of drug use.
KEYWORDS Gefitinib; Lung adenocarcinoma; Drug- caused liver injury; Cholecystitis; Pharmaceutical care
全球每年约有200万新发肺癌患者[1],其中非小细胞肺癌(NSCLC)占肺癌患者总数的80%左右[2]。大多数NSCLC患者初期对化疗敏感,但会逐渐耐药,导致肿瘤复发和不良预后[3]。吉非替尼是表皮生长因子受体酪氨酸激酶的选择性抑制剂(EGFR-TKI)[4],2015、2018年分别被美国FDA和欧洲药品管理局(EMA)批准作为转移性EGFR突变阳性NSCLC患者的一线治疗药物,目前比较明确的不良反应可累及胃肠系统、皮肤及其附件、呼吸系统等,最常见的不良反应(发生率20%以上)表现为腹泻、皮疹、瘙痒、皮肤干燥和痤疮,一般见于服药后第1个月内,以轻度为主,无须停药且通常是可逆性的[5]。
药物性肝损伤(DILI)是指在药物治疗过程中或治疗后,由药物或其代谢产物引起的肝损伤,通常表现为不同程度的转氨酶升高,临床上分为急性肝损伤和慢性肝损伤,其中肝损伤严重者可进展为肝硬化[6]。目前并无药物性胆囊炎的明确定义,通常胆囊炎主要累及胆囊,病理表现为胆囊黏膜充血水肿,上皮细胞变性、坏死脱落,管壁内不同程度的中性粒细胞浸润,临床上以卡他性胆囊炎最常见,病变可进展为蜂窝织炎性胆囊炎[7]。有研究发现,药物毒性或代谢产物通过各种机制导致的肝细胞和胆道损伤,可引发胆红素升高等胆囊疾病[8]。国外有吉非替尼引起严重肝毒性的案例[9],但是该药导致DILI伴胆囊炎的报道却较为少见。本文报道了临床药师参与1例吉非替尼致肺腺癌患者DILI伴胆囊炎的治疗过程,从患者的病情变化、用药情况、不良反应等方面进行分析并及时给予用药建议,旨在探讨临床药师在该罕见疾病治疗过程中的作用,并为类似患者的治疗方案设计提供参考。
1 病例资料
患者,女性,52岁,身高156 cm,体质量55 kg,2019年10月8日因“肺腺癌T3N2M1(ⅣB)期,肝功能异常”于我院就诊。该患者有病毒性肝炎、结核等传染病病史。
2019年10月5日门诊肝功能检查:丙氨酸转氨酶(ALT)507 U/L↑(↑表示高于正常生理值范围),天冬氨酸转氨酶(AST)669 U/L↑,总胆红素(TBIL)23 μmol/L↑,碱性磷酸酯酶(AKP)112 U/L。入院查体:体温36.0 ℃,心率77次/min,血压107/68 mmHg(1 mmHg=0.133 kPa);神志清楚,精神欠佳;全腹无压痛、反跳痛及肌紧张等;墨菲斯征(阴性),移动性浊音(阴性);辅助检查:血常规无异常;肾功能未见异常;颅脑磁共振成像(MRI)提示右侧颞叶、顶叶异常信号,考虑脑转移;左侧胸膜增厚。
入院诊断:(1)左上肺腺癌T3N2M1(ⅣB)期;(2)脑继发性肿瘤;(3)纵膈淋巴结继发恶性肿瘤;(4)DILI。
2 治疗过程
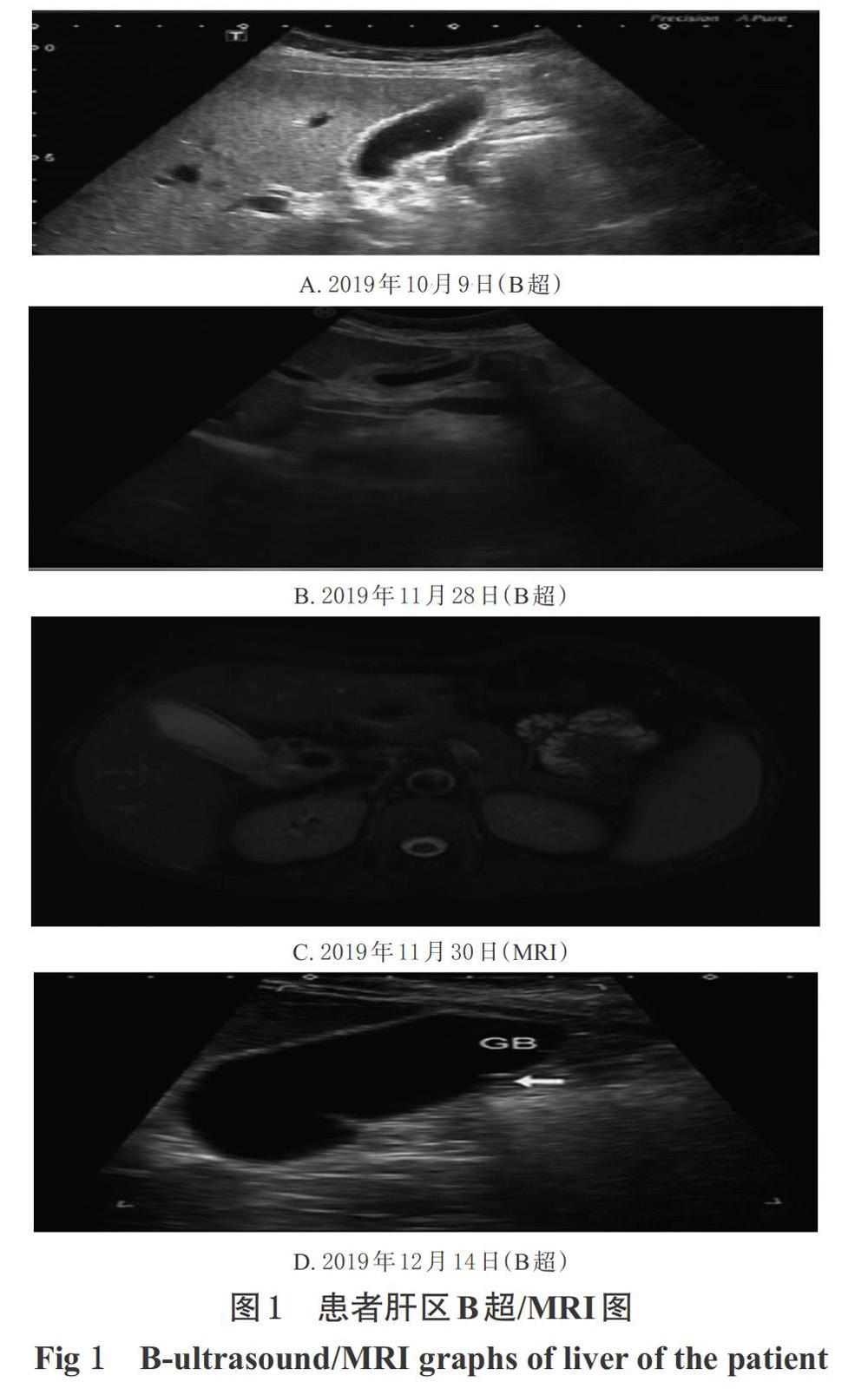
2019年10月8日,该患者入院完善相关检查示,肝功能明显异常、肾功能无异常(见前文所述);10月9日,该患者肝、胆、胰、脾B超均未见异常(以肝区为例,下同;见图1A)。医师给予保肝治疗方案:静脉滴注注射用硫普罗宁钠0.2 g+5%葡萄糖注射液(5%GS)250 mL,qd;乙酰半胱氨酸注射液8 g+10%GS 250 mL,qd;注射用还原型谷胱甘肽1.8 g+5%GS 250 mL,qd;胞磷胆碱注射液0.5 g+5%GS 250 mL,qd。10月15日,患者复查肝功能示,ALT 632 U/L↑,AST 510 U/L↑,AKP 158 U/L↑,提示该患者肝功能无明显改善。临床药师会诊时指出该患者肝损伤很可能与其长期口服化疗药物有关,建议立即停用吉非替尼片,并将保肝药物治疗方案调整为静脉滴注异甘草酸镁注射液0.2 g+5%GS 250 mL,qd。医师采纳该建议,予单药行保肝治疗8 d。10月23日,患者复查肝功能示,ALT 35 U/L、AST 34 U/L、TBIL 14 μmol/L、AKP 126 U/L,提示该患者肝功能指标完全恢复正常。患者停用保肝药物后办理出院,院外患者遵医嘱口服吉非替尼片0.25 g,qod。11月21日,该患者因“厌食、右上腹隐痛”来院复查,肝功能检查示,ALT 853 U/L↑,AST 819 U/L↑,AKP 248 U/L↑,TBIL 24 μmol/L↑,提示该患者转氨酶与TBIL明显升高。11月23日,该患者再次接受住院治疗。参照之前的治疗方案,医师立即停用吉非替尼片,并静脉滴注注射用还原型谷胱甘肽1.8 g+5%GS 250 mL,qd,异甘草酸镁注射液0.2 g+5%GS 250 mL,qd,进行保肝治疗。11月26日,患者复查体格检查显示,ALT 952 U/L↑,AST 652 U/L↑,TBIL 26 μmol/L↑,AKP 269 U/L↑,γ-谷氨酰转肽酶(GGT)306 U/L↑,5′-核苷酸酶(5′-NT)42 U/L↑,乳酸脫氢酶(LDH)257 U/L↑,血常规、尿常规、电解质、降钙素原等检查均无异常,提示该患者肝功能无明显改善。11月27日,临床药师会诊,询问该患者病情,患者主述查体时剑突下疼痛明显,墨菲斯征(阳性),考虑胆囊炎,建议保肝治疗方案仅选用异甘草酸镁注射液,并口服胆舒胶囊0.9 g,tid,同时密切监护患者相关指标的变化。医师结合患者病情完善相应影像学检查:11月28日,患者腹部B超(见图1B)示,胆囊体宽约1.8 cm,壁厚约0.9 cm,呈“双边”征,胆囊壁水肿增厚;11月30日,患者行腹部MRI(见图1C)示,胆囊饱满,腔内未见结石影,囊壁增厚,T2WI信号增高,符合胆囊炎特征;与图1A对比,患者胆囊体、胆管未见水肿及扩张等异常影像学特征,符合胆囊炎特征,因患者白细胞、中性粒细胞和降钙素均无异常,故医师诊断为非感染、非结石性胆囊炎,继续上述治疗方案进行治疗。12月14日,患者一般情况好转,复查肝功能示,ALT 71 U/L↑,AST 47 U/L↑,AKP 122 U/L,TBIL 9 μmol/L;复查腹部B超(见图1D;图中GB指胆囊)示,胆囊大小形态正常,囊壁无增厚,炎性症状基本消退。12月16日,患者准予出院。出院时,临床药师叮嘱其于院外必须严格停用吉非替尼,建议口服盐酸埃克替尼片0.125 g,tid抗肿瘤,并口服复方红豆杉胶囊0.6 g,tid(每21 d为1个疗程)辅助治疗。随访3个月,患者未再出现肝功能异常及胆囊炎症状。
3 药学监护
3.1 疾病诊断
临床药师查阅该患者病史:2018年12月确诊“左上肺腺癌T3N2M1(ⅣB)期,肺内、纵隔淋巴结及脑转移”,基因检测结果EGFR活化突变,于2019年2月起规律口服吉非替尼片0.25 g,qd,并行全脑及颅内转移灶放射治疗15次(射线剂量不详),同时2-7月期间累计完成注射用培美曲赛二钠0.8 g+注射用奈达铂140 mg化疗7个疗程(每21 d为1个疗程),过程顺利,且每月常规复查提示病情稳定,血常规、肝肾功等均无异常。10月5日,患者于门诊复查时发现转氨酶异常升高(ALT 507 U/L↑,AST 669 U/L↑);10月8日入住我院后,于8-14日静脉滴注硫普罗宁钠+乙酰半胱氨酸+还原型谷胱甘肽+胞磷胆碱进行保肝治疗;10月15日复查肝功能,发现其转氨酶异常升高未得到改善。考虑该患者转氨酶异常为吉非替尼诱导的DILI,建议立即停用吉非替尼片,并采取异甘草酸镁注射液的单药保肝治疗。10月23日,患者经单药保肝治疗后转氨酶恢复正常,准予出院。患者于院外再次口服吉非替尼片0.25 g,qod近1个月,再次出现转氨酶异常升高;同时,入院后检查发现,该患者出现非感染、非结石性胆囊炎。
临床药师查阅相关资料后发现,导致患者出现转氨酶升高的主要怀疑药品可能为吉非替尼,文献报道服用吉非替尼后约有11.1%的患者会表现出转氨酶异常[10],而这一比例在长期服药患者中可高达40%,发生转氨酶异常的中位时间为4个月[11],患者目前已连续服用吉非替尼长达近8个月,为出现转氨酶异常的高发期。通过第一阶段停用吉非替尼并行保肝治疗后,患者转氨酶基本恢复正常;但患者出院后,再次口服吉非替尼近1个月,第2轮复查肝功能再次提示转氨酶异常升高,按之前的保肝治疗方案进行治疗后,该患者转氨酶及TBIL均显著下降,结合Roussel Uclaf因果关系评估法(RUCAM)[12]及国际严重不良反应协会(iSAEC)2011年DILI生化学诊断标准[13],确认该患者血清转氨酶异常升高“极可能”为吉非替尼的“严重不良反应”。
由于目前无吉非替尼导致胆囊炎的相关报道,针对该患者出现的非感染、非结石性胆囊炎,临床药师仅能根据其他药物导致的胆囊炎特征进行推测。程树军等[14]在林可霉素(LIN)、石胆酸钠(LCA)、硫氢酸-α-萘酯(ANIT)、月桂醇红霉素酯(EE)致豚鼠胆囊炎模型的病理学及酶组化检查中发现,胆囊炎可导致胆囊壁黏膜下层和固有层水肿并伴有大量液体渗出,与本案例报道的影像学检查结果中的胆囊壁呈“双边”征增厚特征高度一致;李雅等[15]报道,吉非替尼可致患者腹痛及TBIL升高,经停药及保肝治疗后,患者胆囊炎症状明显改善。结合前文,患者前期并无胆囊炎相关症状,也未见影像学检查异常,同时亦未使用易导致胆道结石或胆囊炎的药物,再加之该患者感染指标无升高,排除细菌性胆囊炎的可能,因此按RUCAM标准[12],患者此次住院胆囊炎检查结果可判断为吉非替尼“新的、严重不良反应”。鉴于此,临床药师建议严格停用吉非替尼及可能导致肝损伤的药物,并再次选用异甘草酸镁注射液0.2 g,bid方案进行保肝治疗,但仍需严密监护患者的肝胆指标,医师采纳了临床药师的建议。
3.2 保肝方案的调整
根据《药物性肝损伤诊治指南》[16],判定该患者为肝细胞损伤型DILI,为吉非替尼的严重不良反应,联合参照《2019年欧洲肝病学会临床实践指南:药物性肝损伤》[17]中DILI的基本治疗原则,临床药师建议,及时停用引起肝损伤的吉非替尼。目前,DILI诊治指南推荐用于治疗DILI的药物包括:①治疗嚴重肝损的N-乙酰半胱氨酸(NAC);②治疗免疫机制介导的DILI或伴有自身免疫特征的自身免疫性肝炎(AIH)样DILI的糖皮质激素;③治疗ALT明显升高的急性肝细胞型或混合型DILI的异甘草酸镁;④治疗轻-中度肝细胞损伤型和混合型DILI的双环醇和甘草酸制剂(炎症较重者)、水飞蓟素(炎症较轻者)、熊去氧胆酸/腺苷蛋氨酸(胆汁淤积型DILI);⑤不推荐2种以上保肝抗炎药物联合应用,也不推荐预防性用药。该患者主要以转氨酶升高为主,按急性DILI的严重程度[17]分为1级(轻度肝损伤)。参照注射用硫普罗宁说明书,医师所选的硫普罗宁钠有诱发胆汁淤积和加重患者粒细胞、血小板减少的风险。基于上述原因,临床药师对保肝治疗方案进行了调整,采用单药异甘草酸镁进行保肝治疗。针对患者的胆囊炎,临床药师建议采取口服胆舒胶囊0.9 g,tid的保守治疗,暂不考虑手术治疗,但需密切监护其相关指标变化。
4 文献复习
临床药师查阅相关文献,总结了吉非替尼相关性肝损伤与胆囊炎的判断依据、临床特征、发病机制、治疗策略及监护要点等,以协助医师发现吉非替尼治疗过程中的风险控制点,优化治疗方案。
4.1 DILI的判断依据
对于高度疑似DILI的患者的重要参考依据是RUCAM量表,该量表具有较强的辨别能力,可有效提高诊断的准确率和可操作性,评价结果更接近一般临床判断和专家意见[18]。DILI是吉非替尼常见的不良反应之一[19],EGFR-TKI造成的肝毒性基本表现为转氨酶的升高,长期使用可导致患者肝细胞慢性坏死[20]。有研究显示,与EGFR基因突变不明的NSCLC患者相比,吉非替尼诱发DILI的发生率在疗效更显著的EGFR基因突变型NSCLC患者中更高[21],且一定程度上呈现出剂量依赖性,即高剂量组患者的转氨酶升高发生率远高于常规剂量组[22]。此外,吉非替尼致DILI的主要临床表现为不同程度的转氨酶升高[23],仅有少数患者会出现腹痛及TBIL升高等症状[15]。
4.2 胆囊炎的临床特征
本例患者在两次的住院治疗过程中均出现一定程度的TBIL升高,且第2次住院治疗过程中胆囊炎诊断明确,其腹部B超及MRI检查结果胆囊壁呈“双边”征增厚,与相关研究的病理学特征高度一致[14]。
4.3 發病机制
有学者认为,吉非替尼的肝毒性可能与其代谢中间体、自身免疫性损伤以及其直接作用相关。吉非替尼的中间代谢体(如醌亚胺)可与蛋白形成共价键,引发氧化应激反应,消耗大量的还原型谷胱甘肽,从而引起急性转氨酶升高甚至肝细胞坏死[9]。也有研究者考虑其肝毒性可能与患者自身免疫相关[24],但这一机制尚缺乏直接证据。吉非替尼直接诱导DILI的主要理论依据为该药在EGFR过表达的肝细胞中容易发生蓄积,同时吉非替尼可阻断肝细胞的细胞外信号调节激酶,减少TBIL和葡萄糖醛酸的结合,从而导致游离性胆红素的升高[6]。另一种观点认为,吉非替尼致DILI可能是由于该药及其代谢产物一定程度上抑制了代谢酶细胞色素P450(CYP)酶系中CYP2D6的活性,导致吉非替尼清除减少而体内尤其是肝细胞中的蓄积增加,从而引发肝细胞毒性[25]。此外,不同人种、地区人群CYP2D6基因多态性也可能与吉非替尼诱导的肝毒性有关[26]。现有关于药物引起胆囊炎的机制主要包括药物相关性胆道结石、胆汁淤积、药物过敏等[27],但这些理论均不足以支撑吉非替尼致胆囊炎的发生,因此笔者仍倾向于胆囊炎为吉非替尼致相对严重的肝细胞型DILI时的伴随症状,但也不排除化学性炎症磷脂酶作用于胆汁内的卵磷脂,产生溶血卵磷脂从而诱发化学炎症这一机制[26]。
4.4 治疗策略与监护要点
对于发生DILI的患者首先应根据其肝损伤程度采取积极措施,防止肝损伤的进展和迁延,同大多数DILI一样,除了预防性使用保肝药物、立即停药以及减少用量以外,并无可用的特异性治疗方案[28]。对于EGFR突变阳性的NSCLC患者,在服用吉非替尼出现DILI后,应权衡减少用量或应用其他EGFR-TKI的利弊。通常经过1~3周的停药,肝功能会逐渐好转。吉非替尼的代谢酶主要为CYP3A4,其次为CYP2D6,在有条件的情况下可以监测患者的CYP3A4与CYP2D6基因的表达情况,可考虑换用经CYP2C19、CYP3A4、CYP2E1酶代谢的埃克替尼[29],但不建议使用厄罗替尼,因其约有80%经CYP3A4酶代谢,仅少部分经CYP1A2酶及肝外同工酶CYP1A1进行代谢[30],故再次出现DILI的风险仍很高。此外,可参照DILI诊治指南[16],根据患者肝损伤程度采用适当的保肝药物治疗措施。对于出现胆囊炎表现的患者应立即停药并保守治疗,加强监护,一旦出现腹肌紧张、触及胆囊增大、白细胞计数升高等症状,应及时采取手术切除胆囊[31]。
5 结语
作为第1代EGFR-TKI的吉非替尼,具有疗效显著、耐受性好等特点,近年来广泛用于EGFR突变阳性的NSCLC患者[32]。随着临床应用的日益广泛,其一些罕见的不良反应也不断被发现。本文通过阐述临床药师参与吉非替尼致肺腺癌患者DILI伴胆囊炎的治疗过程,分析了该药致DILI伴胆囊炎的临床特征、发病机制、治疗策略及监护要点等,协助医师完善了治疗方案,保障了患者用药的有效性、安全性,可为长期服用吉非替尼患者出现DILI伴胆囊炎症状时的诊疗提供参考。建议临床实践中应严格把控使用EGFR-TKI的适应证与禁忌证,用药前可检测患者的CYP酶系亚型的表达情况,以指导不同靶向药物的选择;治疗过程中应对患者的血清生化指标及胆囊影像学进行定期检测,以避免严重肝损伤或胆囊炎的发生,确保治疗的安全、有效。
参考文献
[ 1 ] BRAY F,FERLAY J,SOERJOMATARAM I,et al. Glo- bal cancer statistics 2018:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA Cancer J Clin,2018,68(6):394-424.
[ 2 ] XIAO X,HE Z,CAO W,et al. Oridonin inhibits gefitinib- resistant lung cancer cells by suppressing EGFR/ERK/MMP-12 and CIP2A/Akt signaling pathways[J]. Int J Oncol,2016,48(6):2608-2618.
[ 3 ] LOPEZ SAMBROOKS C,BARO M,QUIJANO A,et al.Oligosaccharyl transferase inhibition overcomes therapeutic resistance to EGFR tyrosine kinase inhibitors[J]. Cancer Res,2018,78(17):5094-5106.
[ 4 ] DM ROBINSON GMK,PERRY CM. Erlotinib[J]. Am J Cancer Res,2005,12(7):870-873.
[ 5 ] 夏惠红. 82例吉非替尼不良反应的文献分析[J].中国药物警戒,2016,13(2):98-102.
[ 6 ] 葛均波、徐永健.内科学[M]. 3版.北京:人民卫生出版社,2013:416-418.
[ 7 ] 文继舫,唐建武,来茂德,等.病理学[M]. 3版.北京:人民卫生出版社,2013:209-211.
[ 8 ] 张永莉,齐晓涟.药物致胆红素升高1例分析[J].中国医院药学杂志,2010,30(9):806-808.
[ 9 ] CHEN J,GU R,WANG Q,et al. Gefitinib-induced hepatotoxicity in patients treated for non-small cell lung cancer[J]. Onkologie,2012,35(9):509-513.
[10] 王江峰.吉非替尼诱发肝损伤1例分析[J].亚太传统医药,2014,10(7):96-98.
[11] WANG J,WU Y,DONG M,et al. Observation of hepatotoxicity during long-term gefitinib administration in patients with non-small-cell lung cancer[J]. Anticancer Drugs,2016,27(3):245-250.
[12] TESCHKE R. Idiosyncratic DILI:analysis of 46 266 cases assessed for causality by rucam and published from 2014 to early 2019[J]. Front Pharmacol,2019. DOI:10.3389/fphar.2019.00730.
[13] AITHAL GP,WATKINS PB,ANDRADE RJ. Case definition and phenotype standardization in drug-induced liver injury[J]. Clin Pharmacol Ther,2011,89(6):806-815.
[14] 程树军,孔小明,董晓菊,等.药物诱发豚鼠胆囊炎的病理学及酶组化研究[J].畜牧兽医学报,1999(2):44-50.
[15] 李雅,常红莉,王哲,等.吉非替尼靶向治疗中晚期非小细胞肺癌40例[J].现代肿瘤医学,2015,23(20):2959- 2961.
[16] 于乐成,茅益民,陈成伟.药物性肝损伤诊治指南[J].实用肝脏病杂志,2017,20(2):257-274.
[17] 于乐成,赖荣陶,陈成伟. 《2019年欧洲肝病学会临床实践指南:药物性肝损伤》精粹及评析[J].临床肝胆病杂志,2019,35(6):1242-1250.
[18] 于乐成,范晔,陈成伟.药物性肝损伤的诊断和治疗[J].临床肝胆病杂志,2018,34(6):1160-1165.
[19] 于世英,姚陽.肿瘤药物相关性肝损伤防治专家共识[M].北京:中国协和医科大学出版社,2014:6.
[20] PARK K,WILLIAMS DP,NAISBITT DJ,et al. Investigation of toxic metabolites during drug development[J]. Toxicol Appl Pharm,2005,207(2 Suppl):425-434.
[21] MITSUDOMI T,MORITA S,YATABE Y,et al. Gefitinib versus cisplatin plus docetaxel in patients with non-small- cell lung cancer harbouring mutations of the epidermal growth factor receptor(WJTOG3405):an open label,randomised phase 3 trial[J]. Lancet Oncol,2010,11(2):121-128.
[22] 王晓辉,吴斌,朱珺.小分子靶向药物治疗非小细胞肺癌的不良事件研究进展[J].中国药房,2011,22(14):1329- 1331.
[23] 陈雪琴,杨邵瑜,马胜林.肺癌靶向药物肝脏毒性作用研究进展[J].中国肺癌杂志,2014,17(9):685-688.
[24] 胡洁,林丽珠,骆肖群,等. EGFR-TKI不良反应管理专家共识[J].中国肺癌杂志,2019,22(2):57-81.
[25] KIJIMA T,SHIMIZU T,NONEN S,et al. Safe and su- ccessful treatment with erlotinib after gefitinib-induced hepa-totoxicity:difference in metabolism as a possible mechanism[J]. J Clin Oncol,2011,29(19):e588-e590.
[26] 尚培中,苗建军,李晓武.急性和亚急性胆囊炎腹腔镜手术治疗的安全策略[J/CD].中华普通外科学文献:电子版,2019,13(6):426-429.
[27] 马振英.药物引起的胆囊疾病[J].国外医学:药学分册,1992,19(5):314.
[28] LIANG X,BIS,YANG W,et al. Epidemiological serosurvey of hepatitis B in China:declining HBV prevalence due to hepatitis B vaccination[J]. Vaccine,2009,27(47):6550-6557.
[29] CHEN J,ZHENG X,LIU DY,et al. Therapeutic effects and adverse drug reactions are affected by icotinib exposure and CYP2C19 and EGFR genotypes in Chinese non-small cell lung cancer patients[J]. Asian Pac J Cancer Prev,2014,15(17):7195-7200.
[30] ASAI N,OHKUNI Y,YAMAGUCHI E,et al. Successful treatment of non-small cell lung cancer with gefitinib after erlotinib-induced severe eyelid erosion:two case reports[J]. J Cancer Res Ther,2015. DOI:10.4103/0973- 1482.139392.
[31] 郭永团,朱晓黎,唐杰,等.原发性肝癌动脉化疗栓塞术少见严重并发症分析[J].医学影像学杂志,2014,24(4):537-542.
[32] 潘莹,黄思超,王霞,等. NF-κB亚单位p50/p65激活促进肺腺癌H1650细胞吉非替尼耐药[J].南方医科大学学报,2018,38(5):584-590.
(收稿日期:2020-04-29 修回日期:2020-08-29)
(编辑:邹丽娟)
