类气相ClO2脱除燃煤烟气中氮氧化物实验研究
2020-11-30孙淑君马素霞杨秉川崔荣基
孙淑君,马素霞,杨秉川,王 杰,崔荣基
(太原理工大学 电气与动力工程学院,山西 太原 030024)
燃煤火电厂发电是我国主要的发电方式,但燃煤烟气所造成的环境污染问题十分严重[1]。随着环境的日益恶化,国家对燃煤电厂烟气污染物的控制力度也逐渐增加。二氧化硫和氮氧化物是燃煤烟气中的主要污染物,也是雾霾,酸雨,光化学烟雾等环境问题产生的主要原因[2]。因此,有效脱除燃煤烟气中的氮氧化物(主要为NO)和二氧化硫成为建设“绿色”电厂的重要方面。当前,电场中主要采用湿法烟气(WFGD)脱硫[3]和选择性催化还原技术(SCR)脱硝[4]。这种分级脱硫脱硝的方法具有初始投资运行成本高,上下游设备容易互相影响,占地面积过大等问题。并且SCR技术中还存在催化剂易中毒,购买成本高,以及氨逃逸等缺点[5-6]。因此寻找更加经济有效的脱硫脱硝方法十分必要。近年来,针对NO不溶于水而NO2易溶于水的特点,采用氧化剂对烟气进行预氧化,将烟气中的NO转化为NO2,再结合脱硫装置中的碱吸收塔进行脱硫脱硝一体化处理的氧化-吸收法得到了广泛研究[7]。脱除效率高,成本低廉等优势使得该方法在未来脱硫脱硝的研究中极具竞争优势。
在氧化吸收法中,NO氧化剂的选择成为制约脱硝效率的关键因素。传统氧化剂KMnO4[8],NaClO2[9],H2O2[5,10],O3[11]等虽能有效地将NO转化为NO2,但这些氧化剂存在价格昂贵,消耗量大,适用pH范围窄等问题。因此通过结合催化剂,紫外光,微波等辅助手段促使氧化剂产生·OH等强氧化性自由基以提高氧化剂氧化能力的高级氧化法成为近年来的研究热点[12-16]。并且在这些研究中发现,一种自由基的存在往往会激发其他自由基的产生,从而进一步加强氧化作用。ClO2作为一种本身即自由基的低成本绿色氧化剂早已广泛应用于水污染处理领域[17-18],但其在烟气污染领域的研究较少,且ClO2对NO的具体脱除机理尚不明确[19-21]。由于气相ClO2需现场制备,且不易储存和运输。笔者采用液相ClO2为氧化剂进行烟气脱硝研究。锅炉尾气在经过省煤器、空气预热器和电除尘器后,烟气温度为 140 ~170 ℃,在此温度条件下,液相氧化剂ClO2会瞬间气化为类气相氧化剂[22],气化后的类气相氧化剂的比表面积和反应活性迅速增加,然后对烟气中NO进行预氧化,再结合饱和氢氧化钙溶液进行氧化产物吸收脱硝。笔者还进行了ClO2脱硝机理以及脱硝影响因素研究,为基于ClO2氧化的烟气污染物脱除的进一步研究提供参考。
1 实验系统与方法
1.1 实验系统简介
如图1所示,本文实验系统分为5部分:模拟烟气产生系统,预氧化系统,温度控制系统,氧化产物吸收系统和烟气分析系统。模拟烟气由N2,NO和SO2配置,通过转子流量计控制不同气体流量。将配置好的模拟烟气在缓冲瓶内充分混合后通向预氧化反应器(500 mL三口烧瓶)。预氧化反应器内空气温度由电加热套(ZNHW智能恒温电热套,500 mL,邦西仪器科技有限公司)控制。首先,在蠕动泵关闭的情况下,测量出初始烟气中污染物的质量浓度,待烟气质量浓度稳定后,将配置好的ClO2溶液经由蠕动泵以0.687 5 mL/min的速率缓慢滴入预氧化反应装置。进入预氧化装置的ClO2溶液瞬间变成类气相状态,并与模拟烟气充分混合反应。反应后气体随后通入饱和氢氧化钙溶液进行氧化产物吸收。吸收后气体经无水氯化钙吸收水分后进入烟气分析仪(testo350,0~5 000×10-6,精度:5%,德国德图仪器国际贸易有限公司)进行烟气组分测定。其中ClO2溶液由浓硫酸(6 mol/L)与亚氯酸钠(4 mol/L)通过反应(1)制取。
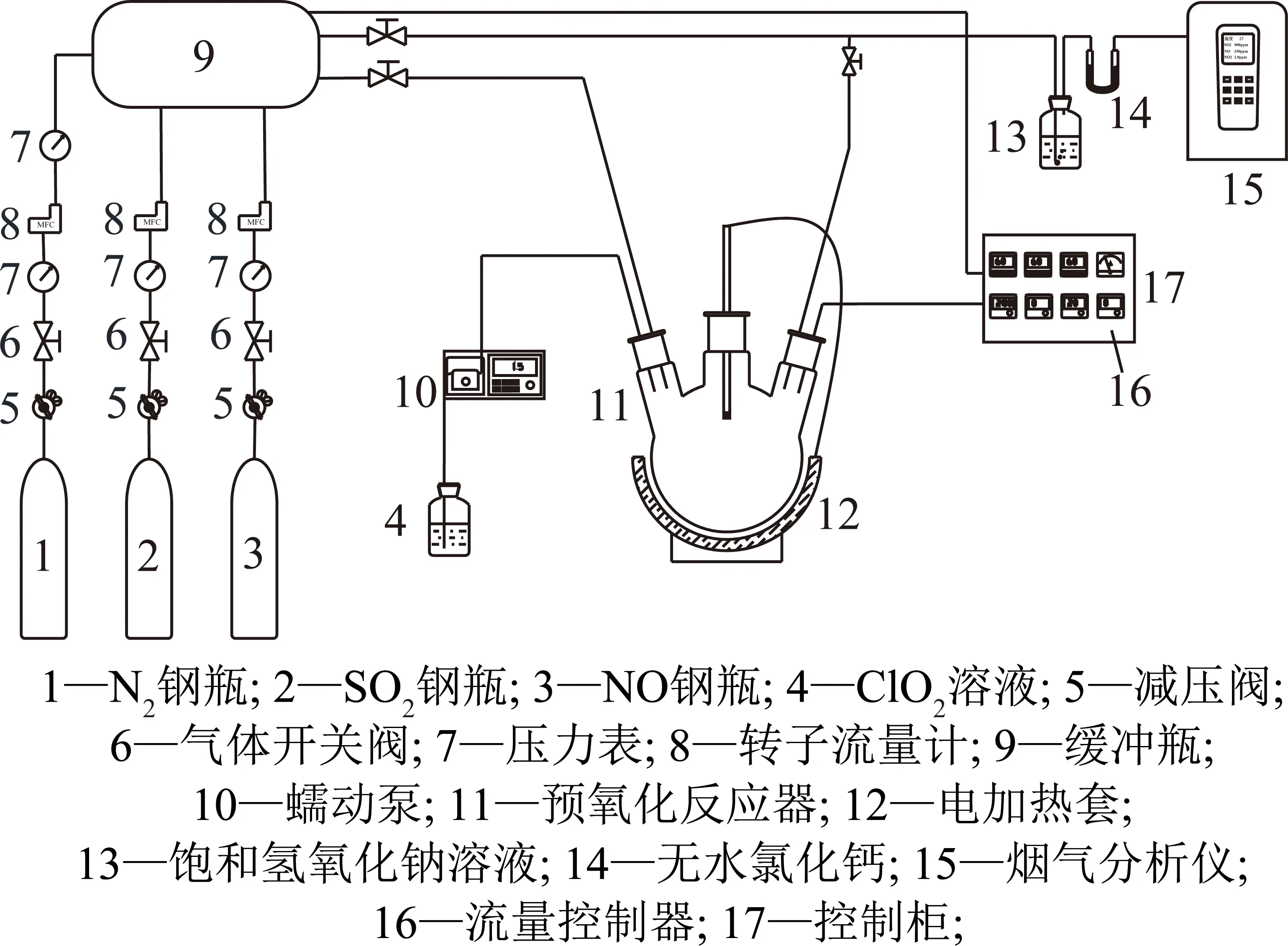
图1 实验系统装置示意Fig.1 Schematic of the experimental apparatus

(1)
制得的ClO2溶液放置于2 ℃的冰箱中避光保存备用。ClO2质量浓度测定采用碘量法[23],反复测量3次,取平均值后按比例稀释至所需质量浓度。溶液pH采用pH计(雷磁 PHS-3E)测定,并采用1 mol/L的稀硫酸和0.1 mol/L的NaOH对溶液进行pH调节。
1.2 实验计算方法
不同反应条件下,NOx的质量浓度在反应稳定5 min之后测得,并且每个条件下重复实验3次,并计算均值和误差。NOx的脱除效率的计算式为
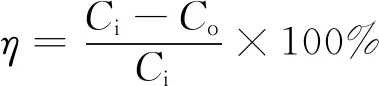
(2)
式中,η为脱除效率;Ci和Co分别为NO进出反应器的质量浓度。
1.3 实验表征方法
将反应后的预氧化反应器放置冷水中进行冷凝,收集冷凝液后采用液相离子色谱(Dionex ICS5 000,美国)进行硝酸根和亚硝酸根离子的检测。采用电子自旋共振谱仪(JEOL FA300)对ClO2氧化剂溶液在不同温度和不同质量浓度下进行电子自旋共振(ESR)中自由基检测,DMPO为自旋捕获剂。
2 实验结果与讨论
2.1 氧化剂对比
氧化剂的氧化能力在一定程度上决定了氧化剂的用量和消耗成本。图2进行了ClO2与几种常见氧化剂KMnO4,NaClO2,H2O2在相同条件下对NO的氧化能力对比。4种氧化剂的质量浓度均为470 mg/L。由图2可知,氧化能力ClO2>KMnO4> NaClO2> H2O2,当采用ClO2为氧化剂时,结合饱和氢氧化钙吸收液,烟气中NO的脱除效率可高达92.5%。远远超过其他氧化剂。ClO2在较低的质量浓度下NO表现出优异的氧化性能并且具有价格优势。纯度为99%的ClO2粉末的价格约为11.5元/kg。此外,ClO2作为一种广泛普遍消毒剂,被世界卫生组织(WHO)列为 AI 级产品,排在安全消毒方法的首位[24]。因此,以ClO2为氧化剂的氧化吸收法脱硝具有较好的应用前景。

图2 不同氧化剂对比Fig.2 Comparison of different oxidant in NO removal
2.2 物质的量比(ClO2/NO)对脱除效率的影响
物质的量比(ClO2/NO)为影响NO脱除效率的重要因素。如图3所示,在物质的量比(ClO2/NO)由0.19~0.84的变化过程中,NO的脱除效率不断增加。在这个过程中,烟气中的NO相对于氧化剂是过量的。随着氧化剂的增加,氧化效率也逐渐增加。当物质的量比(ClO2/NO)=0.84时,脱除效率可达到92.5%。继续增加物质的量比至1.0,脱除效率基本保持平稳。根据Dong-Seop Jin 等[25]提出反应方程式(3):

图3 物质的量比(ClO2/NO)对NO脱除效率的影响Fig.3 Effect of molar ratio (ClO2/NO) on NO removal efficiency

(3)
可知,ClO2/NO完全反应的理论物质的量比约为0.6。ClO2氧化反应的实际物质的量比十分接近理论物质的量比。但ClO2本身的氧化还原电位并不高,气态ClO2氧化还原电位约为0.95 eV[25]。而氧化还原电位为1.776 eV的H2O2[26]在相同条件下的氧化脱除几乎为0(图2)。
考虑到ClO2本身为一种活泼自由基,且一种自由基的存在往往激发多种自由基产生。以DMPO为电子自旋捕获剂对350 mg/L的ClO2溶液在25 ℃的条件下进行了ESR检测。图4检测结果出现了DMPO—OH的标准峰比:1∶2∶2∶1,表明ClO2溶液中出现了·OH自由基,·OH自由基作为一种氧化还原电位为2.7 eV的强氧化剂,对NO具有很强的氧化能力,可能是ClO2分子与·OH自由基的共同作用导致ClO2在低质量浓度时对NO仍具备良好的氧化脱除效果。为进一步验证·OH自由基在NO氧化过程中发挥的作用,在预氧化系统中进行了·OH自由基抑制剂添加剂实验,实验结果如图5所示,在抑制剂实验中,碳酸氢钠(SB)和异丙醇(IP)以及甲酸钠(SP)均可以湮灭·OH[27]。由实验结果可知,3种抑制剂的添加均导致了NO脱除效率的下降,但下降程度有所不同。可以判定溶液中·OH的存在。当添加质量分数10%的甲酸钠,脱除效率下降约为39.7%。不同的抑制剂由于自身特性对同一种自由基的抑制效果有所差异。因此·OH自由基在氧化过程中发挥的作用应≥39.7%。
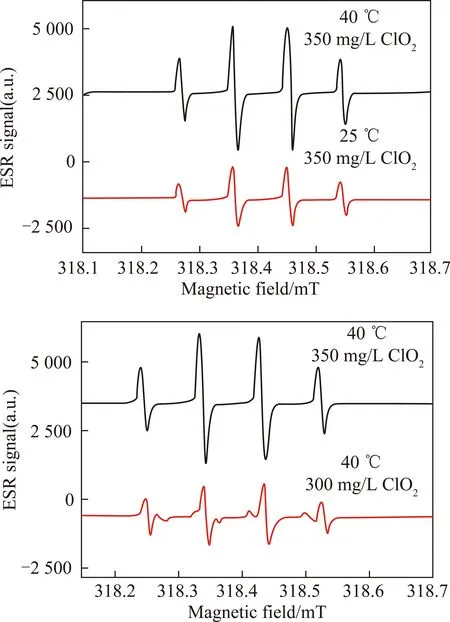
图4 ESR检测Fig.4 ESR detection of ClO2 solution
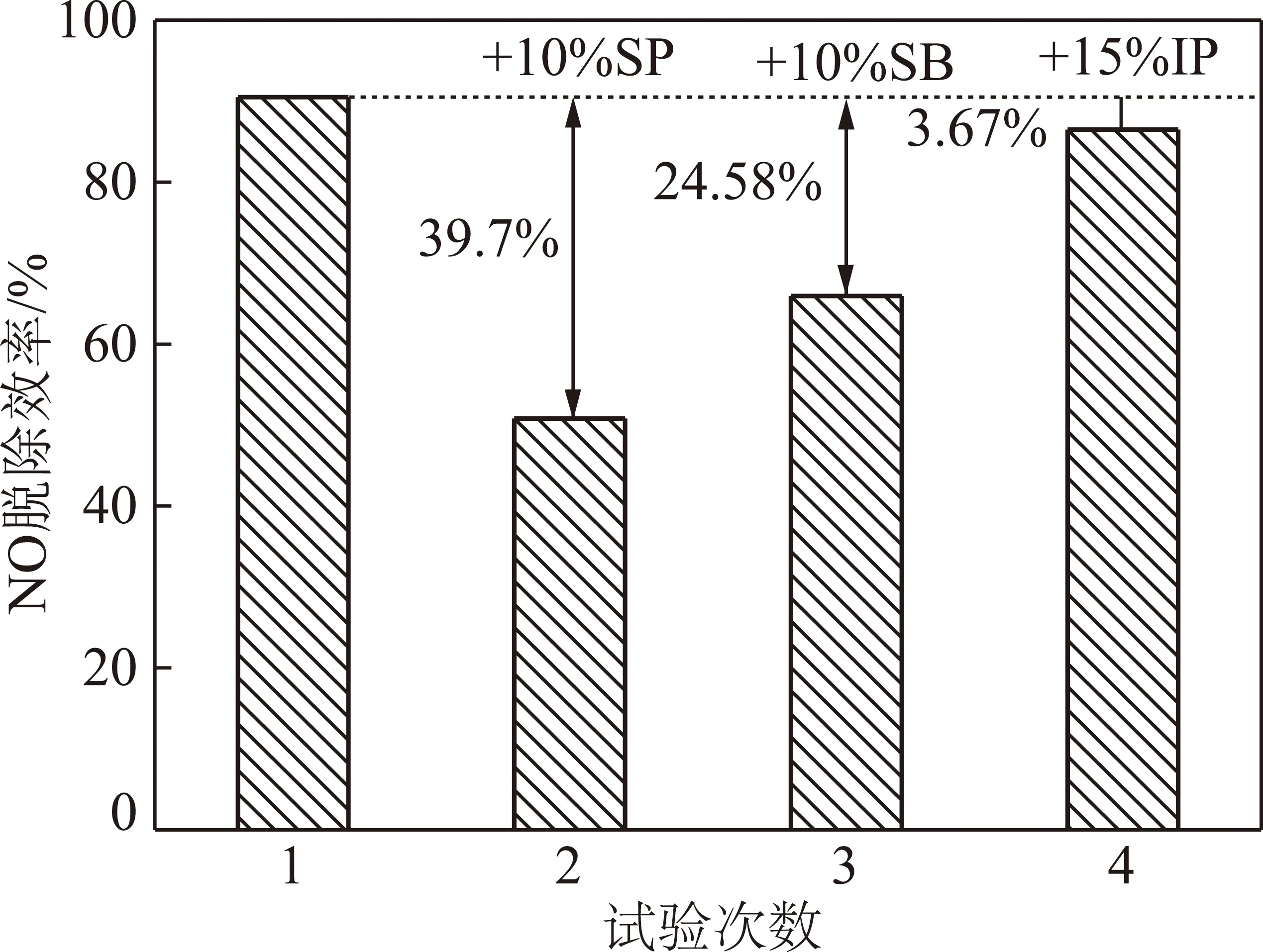
图5 抑制剂添加实验Fig.5 Inhibitor addition experiment
由于ClO2分子中并不含氢原子,因此所产生的·OH自由基中的氢原子只可能来源于水蒸汽。据相关研究,在预氧化系统中,可能发生的氧化反应[27,30]为

(4)

(5)

(6)
(7)

(8)
(9)
ClO2在水溶液中大多以溶解气体的形式存在。可能只有一小部分ClO2与H2O发生以上反应产生·OH(反应式(4))。当与烟气中NO混合时,由于·OH更易与NO结合,极大的促进了反应式(4)的正向进行,导致·OH等自由基成NO氧化的关键因素之一。除·OH外,HClO2和 ClO·(1.5~1.8 eV),O2·-(1.6 eV)[28]也均可以促进NO的氧化。但这些自由基可能由于存在的质量浓度过低而不能在ESR检测过程中捕获。因此,类气相ClO2氧化也应归属高级氧化法之一。
2.3 温度对脱除效率的影响
图6分别探究了不同物质的量比下温度对NO脱除效率的影响。由实验结果可知,在110~170 ℃,温度对类气相ClO2脱除NO的影响较小。脱除效率的变化幅度约为5%左右。一方面,温度的升高会提高参与化学反应的分子活性,促进化学反应的进行。同时也会促进溶液中·OH等相关自由基的产生,对NO的氧化增强,如图6所示。但另一方面,温度的升高也会促进ClO2的热分解,如反应(10)
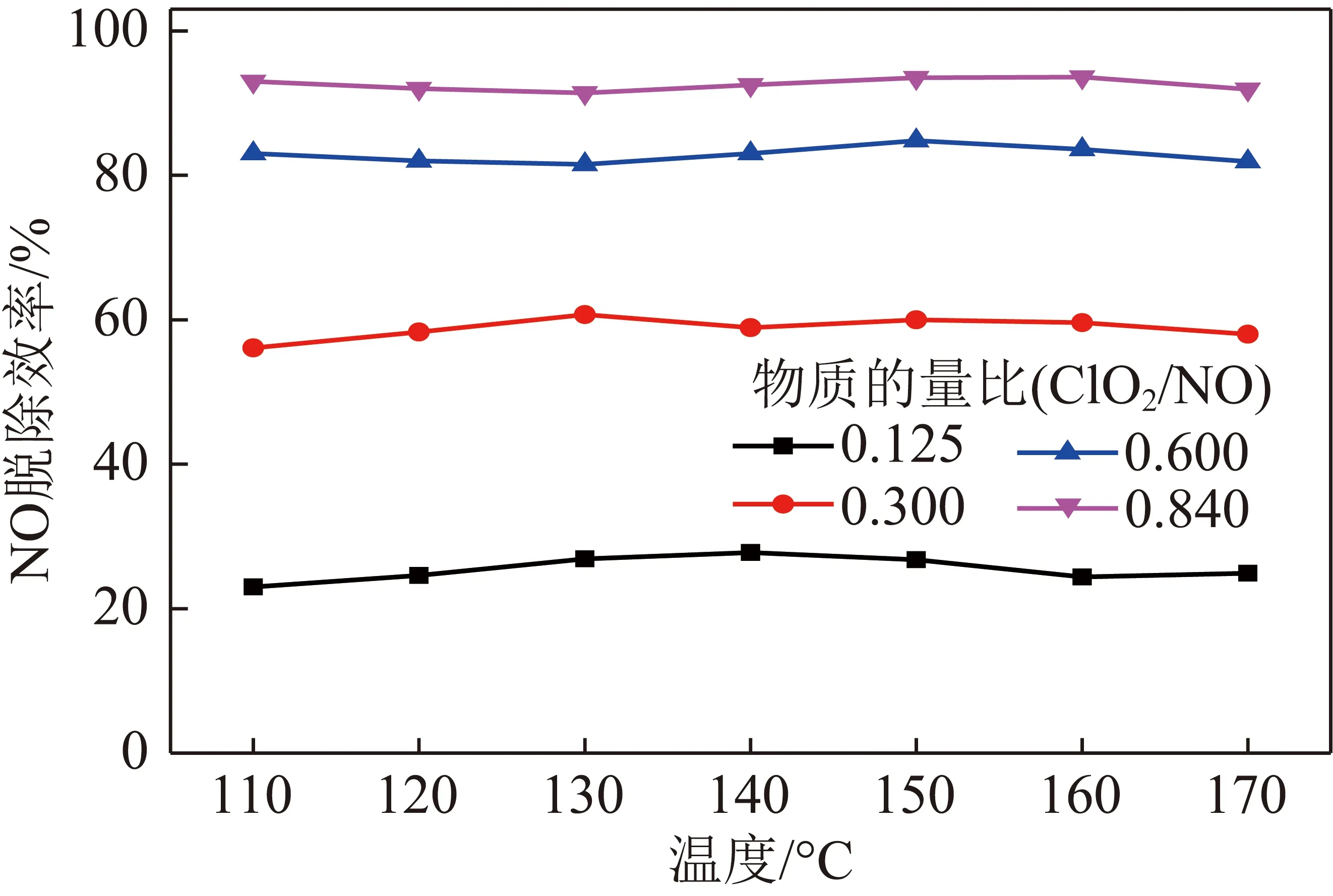
图6 温度对NO脱除效率的影响Fig.6 Effect of temperature on NO removal efficiency

(10)
Cl2和O2的氧化能力低于ClO2,致使NO的脱除效率下降。总体而言,对于经过空气预热器和电除尘器的锅炉烟气,ClO2氧化具有良好的温度适应性。
2.4 pH对脱除效率的影响
ClO2溶液本身为弱酸性,pH为3~5。在水中是纯溶解状态,不会构成二聚体或多聚体[17],所以它的氧化作用受水中pH的影响极小。由图7可知,当反应温度为140 ℃,物质的量比(ClO2/NO)=0.84时,ClO2溶液的pH变化对NO脱除效率的影响较小。总体而言,酸性条件下更加有利于NO的氧化脱除。主要原因是ClO2的氧化还原电位会随着pH的减小而增加[19]且酸性条件更加有利于溶液中·OH活性的发挥[26]。随着溶液pH的增加,ClO2溶液的氧化还原电位降低,其中一部分的ClO2会与添加的少量NaOH发生歧化反应[25],如反应(11),该反应生成的NaClO2被认为是NO氧化实验中最有效的添加剂之一[9],可与NO发生反应(12)。对NO产生了一定的氧化弥补。因此,ClO2的氧化能力并不仅限于某一pH区间,而是具有较广的pH适应性。
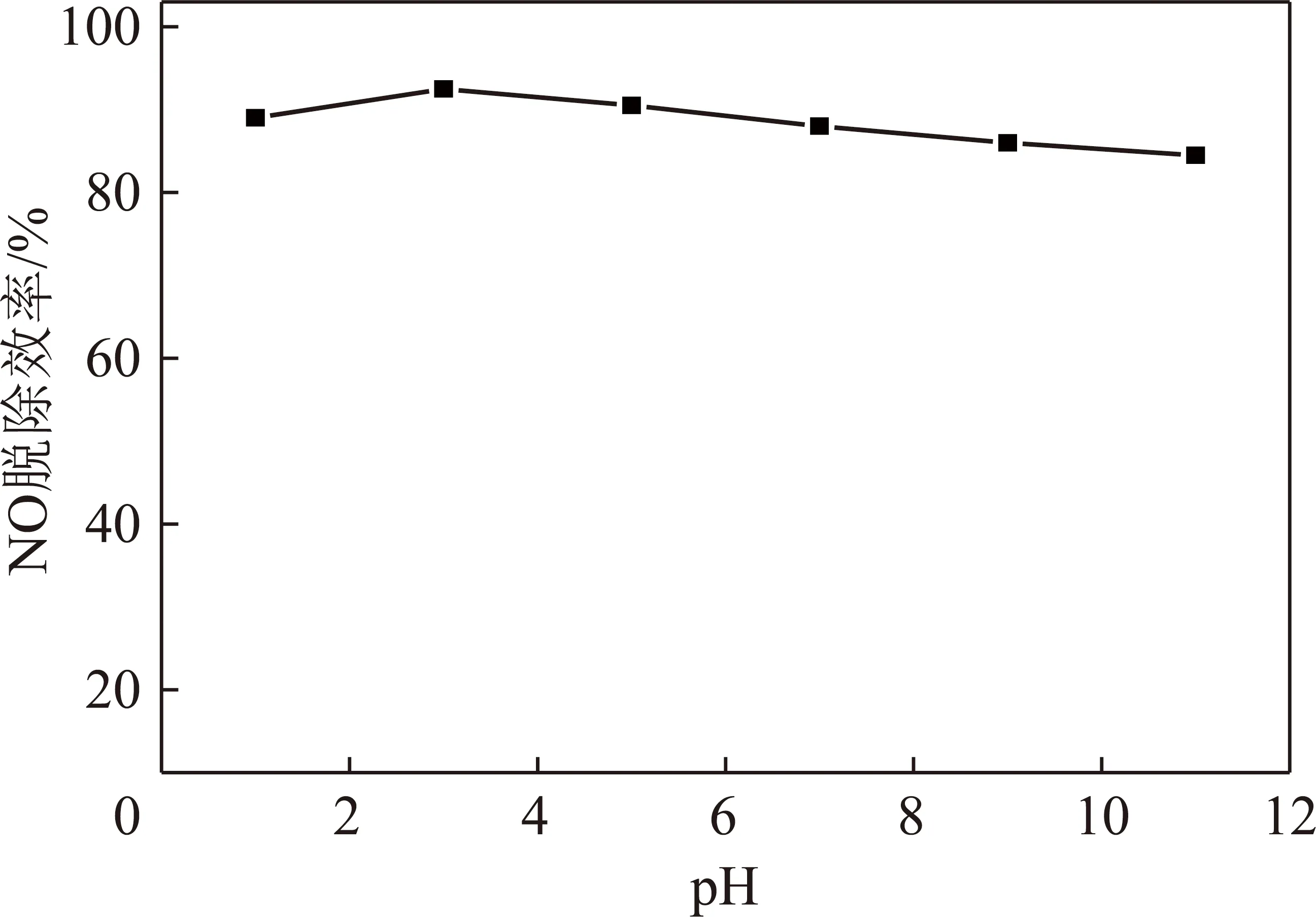
图7 ClO2溶液pH对NO脱除效率的影响Fig.7 Effect of pH on NO removal efficiency

(11)

(12)
2.5 SO2对脱除效率的影响
锅炉烟气中的主要污染物为SO2和NO,预氧化反应器中进行NO的氧化时不可避免的要受到烟气中二氧化硫的影响。对于大多数氧化剂,预氧化过程中氧化NO的同时不可避免的也会将SO2氧化成SO3,随着烟温的下降,在进入碱吸收塔之前,SO3造成的低温腐蚀严重影响了电厂锅炉相关设备的使用。图8进行了不同物质的量比(ClO2/NO)的条件下,向烟气中添加不同密度的SO2气体的脱硝实验。随着添加SO2密度的增加,NO的脱除效率出现了不同程度的下降,但随着ClO2密度的增加,NO脱除效率下降的幅度逐渐减小,可以看出当摩尔比(ClO2/NO)=0.83时,SO2质量浓度从100 mg/m3到600 mg/m3的变化过程中,SO2的添加对NO氧化脱除效率的影响约5%。根据李广培等[21]的研究,气相ClO2在NO与SO2同时存在的情况下,ClO2与NO的反应速率远高于ClO2与SO2的反应速率。因此会优先氧化NO然后氧化SO2。ClO2对NO的选择性氧化可以在一定程度上避免SO3所造成的低温腐蚀。尽管SO2的存在也会消耗一部分ClO2氧化剂,如反应式(12)。但SO2的添加也会在一定程度上促进NO的氧化吸收,如反应式(13)和(14)[31]:

图8 SO2的添加对NO脱除效率的影响Fig.8 Effect of SO2 addition on NO removal efficiency

(12)

(13)
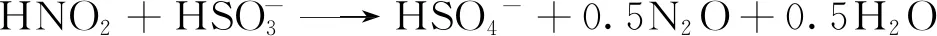
(14)
因此控制好氧化剂的添加量,可减少烟气中的SO2氧化比例,减轻潜在低温腐蚀危险。
2.6 反应机理分析
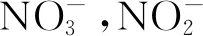
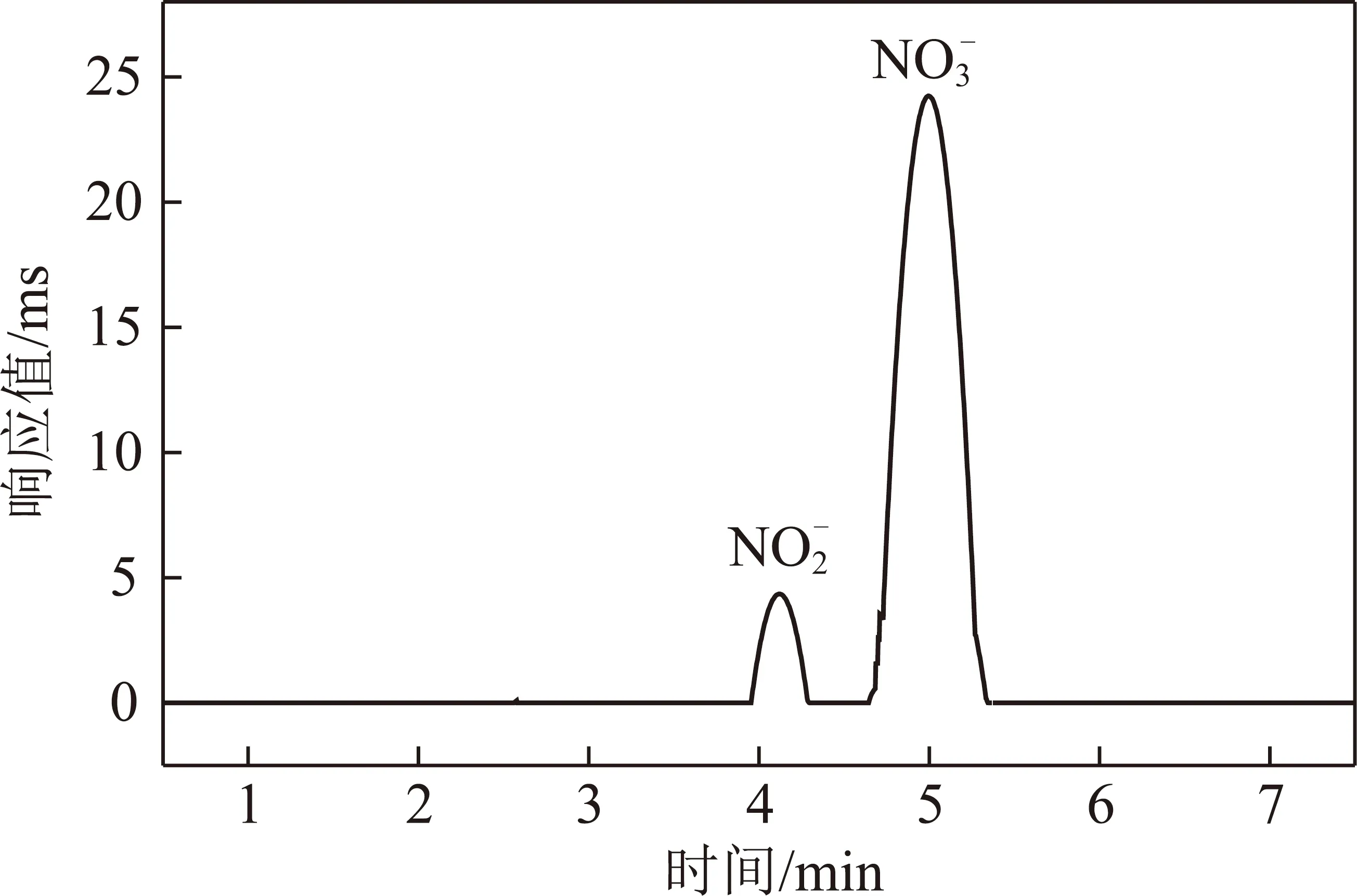
图9 冷凝液离子色谱分析Fig.9 Ion chromatography analysis of condensate

(15)

(16)
(17)
(18)

(19)
(20)

(21)

(22)
在饱和氢氧化钙吸收液中可能存在的反应[15]为

(23)

(24)

(25)
3 结 论
(1)当预氧化温度为140 ℃,ClO2溶液pH约为3,物质的量比(ClO2/NO)=0.84时,烟气中NO的氧化脱除效率可达到92.5%。类气相ClO2对NO进行氧化时具有良好的温度适应性,pH适应性。
(2)在预氧化过程中类气相ClO2中产生的·OH等自由基与ClO2分子共同作用对NO进行氧化。
(3)当烟气中SO2与NO共同存在时,类气相ClO2优先氧化烟气中的NO,可以在一定程度上减少SO3所造成的低温腐蚀。
