聚乙烯亚胺改性树脂微球的制备及铀吸附性能研究
2020-11-27黄国庆孙世操刘彦洋
黄国庆,王 力,孙世操,刘彦洋
(中国船舶集团有限公司第七一八研究所,河北 邯郸 056027)
21世纪以来,核能发展迅速,伴随着陆地铀矿开采量增加,因陆地铀矿开采逐渐困难,且将在百年内被开采殆尽[1]。而海水中约包含45亿吨铀,是陆地铀矿的1000多倍[2],可以为核能发电提供一个经济有效的供应途径。因此,海水提铀相关技术对于核能事业的发展有着十分重要的意义。
海水提铀的主要挑战有3个,首先是海水中铀浓度极低,约为3.3 ug/L,其次是铀以一种稳定的UO2(CO3)34-形式溶于海水里,再次是存在大量的竞争离子[3]。目前用于海水提铀的方法主要有离子交换法、膜透析法、生物浓缩法、浮式离心法和吸附法等[4]。吸附法因具有操作简便,成本低廉等优点,被认为是最有潜力的海水提铀方法[5]。在吸附技术中,最重要的就是开发吸附性能优异并且稳定的吸附材料。目前,国内外科研人员已进行了多种吸附材料的研究与开发,包括金属有机框架材料(MOF)、水滑石材料(LDH)、生物质材料、氧化石墨烯基材料,改性纤维和改性树脂等[6]。但其中很多材料因体积为微米级,没有良好的负载方式会使其流失,因为无法用于实海环境。
树脂已被广泛应用于从废水中除去重金属[7],其中,含氯树脂因其易于改性而被广泛应用[8]。聚乙烯亚胺(PEI)有良好的水稳定性和亲水性,且具有大量氨基和亚氨基,这些基团均具有配位能力,可以用于吸附[9]。本文所研究的PEI改性树脂微球材料是由含氯树脂和PEI经化学改性法合成制得。通过FT-IR和SEM等技术对制得的PEI改性树脂微球进行了结构分析与形貌表征。将PEI改性树脂微球浸于溶液中,采用循环震荡的方法使PEI改性树脂微球与铀溶液充分接触进行吸附,完成静态吸附实验。通过实验分析了铀溶液pH值、温度和铀浓度等因素对吸附过程的影响,并采用动力学方程、吸附等温方程等数学模型对各项吸附数据进行全面分析,探讨PEI改性树脂微球对铀的吸附类型。
结果表明,PEI改性树脂微球的饱和吸附容量为248.5 mg/g,并且对铀酰离子具有很好的选择性。上述研究表明PEI改性树脂微球材料是一种极具潜力的吸附剂材料,在海水提铀领域有着广阔的应用前景。
1 实验部分
1.1 试剂
聚乙烯亚胺(PEI)、含氯树脂、氢氧化钠、二甲苯、盐酸、酚酞指示剂、乙醇、硝酸铀酰、硝酸钠、硝酸钾、硝酸镁,均为分析纯,由市场购得后,未经进一步纯化直接使用。
1.2 PEI改性树脂微球的合成
将250mL二甲苯和5gPEI加入到500 mL三颈烧瓶中,用油浴锅加热至60 ℃,此时加入30 g含氯树脂,于搅拌回流状态下发硬4 h。反应结束,用漏斗过滤,用3×100 mL乙醇溶液洗涤反应产物,然后用去离子水将产物洗至无味。
PEI改性树脂微球胺基含量的测定:精确称取1 g功能化树脂,浸泡入100 mL 0.1 mol/L的盐酸溶液中2 h;用移液管移取上清液20 mL,加入酚酞指示剂,0.1 mol/L 氢氧化钠溶液滴定,根据公式(1)计算胺基含量:
M=(100C1-5C2V2)/m
(1)
式中:M为纤维胺基含量,单位mmol/g;C1为标准盐酸溶液浓度,单位mol/L;C2为标准氢氧化钠溶液浓度,单位mol/L;V2为消耗氢氧化钠的体积数,单位mL;m为树脂的质量,单位g。
测得PEI改性树脂微球的胺基含量为1.28 mmol/g。
1.3 测试与表征
采用美国Nicolet公司的Avater 370型傅立叶变换红外光谱仪对材料进行红外光谱测试,测试波长范围是4000-400cm-1;采用日本日立公司HitachiSU8000型扫描电子显微镜对材料的形貌特征进行观察及EDS测试;吸附实验中所涉及的溶液浓度,高浓度时,采用美国PerkinElmer公司生产的Optima-7000DV型电感耦合等离子体原子发射光谱仪(ICP-AES)进行含量测定(范围:1 mg/L-500 mg/L,浓度超过500 mg/L时稀释后再进行浓度测定);低浓度时,文采用德国Bruker公司的Bruker 820-MS型电感耦合等离子质谱仪(ICP-MS)对溶液中的铀含量进行测定(1 μg/L-500 μg/L,超过500 μg/L时稀释后测定准确浓度)。
1.4 吸附试验
本文实验所采用的吸附实验方法为封闭振荡平衡方法,通过机械震荡模拟海洋中海水冲击,震荡速度不低于150次/min。将一定质量的吸附剂与固定体积和浓度的溶液一起加入到干净并可密封的锥形瓶中,密封后在恒定温度下振荡一定时间。分析吸附后溶液中铀酰离子或其它金属离子的浓度,测得吸附前后溶液中阳离子浓度的变化。
精确称量4.220 g硝酸铀酰(UO2(NO3)2·6H2O)和1 m L浓度为1 M的硝酸溶液加入2 L的容量瓶中,用去离子水进行定容,并采用超声使溶质均匀分散。最终得到浓度为1000 mg/L的铀溶液,实验所需不同浓度的铀溶液,均使用该溶液按比例稀释配制。
将铀标准溶液按体积比例稀释到指定浓度,采用ICP测量稀释后铀的浓度。量取50ml稀释后的铀溶液,用1M的稀硝酸或者氢氧化钠溶液调节铀溶液的pH值到指定值。将20mg的吸附剂和调好pH值的铀溶液加入到100mL的锥形瓶中,并将锥形瓶放入恒温水浴振荡箱中,使吸附剂和铀溶液充分接触。水浴温度和振荡时间根据实验计划设定。
振荡结束后,进行过滤并取滤液,采用电感耦合等离子体原子发射光谱仪(ICP-AES)或电感耦合等离子质谱仪(ICP-MS)测定滤液中的铀浓度。根据测得的结果,采用公式(2)计算吸附剂的吸附容量,采用公式(3)计算吸附剂的吸附效率(η),即去除率。
Qe=(C0-Ce)V/m
(2)
η=(C0-Ce)C0×100%
(3)
2 结果与分析
2.1 红外谱图分析
利用FT-IR技术对PEI改性树脂微球进行表征,结果如图1(A)所示,在3383 cm-1和1605 cm-1位置处的吸收峰是亚氨基的伸缩振动所引起的;在2930 cm-1和2857 cm-1位置处为C-H振动吸收峰;在1170 cm-1位置处的吸收峰是C-N伸缩振动峰,这些峰的出现证明了PEI改性树脂微球合成成功。从吸附后的FT-IR曲线(B)可以看出,在900 cm-1处出现一个尖峰,此峰为铀酰离子的特征峰,证明PEI改性树脂微球成功吸附了铀酰离子。

图1 PEI改性树脂微球吸附前(A)和吸附后(B)的红外测试谱图
2.2 SEM形貌分析
图2PEI改性树脂微球吸附前(A)后(B, C)的SEM图像和吸附后EDS数据图。从图2(A)中可以看出,PEI改性树脂微球呈较为规则的球体,微球直径在400-600 μm范围内。吸附后的形貌也没有明显改变(图2 B),图2(C)为图(B)的局部放大图,对其红色框范围进行EDS测试,结果如图2(D)。数据表明,U元素的质量占比为6.75%,证明PEI改性树脂微球成功吸附了铀酰离子。

图2 PEI改性树脂微球吸附前(A)后(B,C)的SEM图像和吸附后EDS数据图(D)
2.3 吸附实验
2.3.1 溶液pH值对吸附性能的影响
铀溶液的pH值影响着铀酰离子在水溶液中的存在状态和吸附剂的表面状态,进而影响吸附剂的吸附能力。为了考察溶液的pH值对吸附过程的影响,进行了固定吸附温度(25 ℃)、溶液初始浓度(100 mg/L)、吸附时间(2h)、吸附剂质量(20 mg),以pH值为变量的吸附实验。实验结果如图3所示,溶液的pH值变化对吸附剂的吸附能力有显著的影响。在pH为2-7时,PEI改性树脂微球的铀吸附量随着pH的上升而增大,直到pH为7,达到最大吸附容量248.5 mg/g;在溶液pH在7-10的范围内,PEI改性树脂微球的铀吸附量没有明显变化,证明该材料适合在碱性条件下进行铀吸附,考虑到海水的pH约为8.3,选定pH等于8为PEI改性树脂微球的最佳吸附条件。

图3 溶液pH值对PEI改性树脂维修微球铀吸附性能的影响
2.3.2 吸附时间对吸附的影响
如图4为铀吸附量随时间变化曲线。固定吸附温度(25 ℃)、溶液初始浓度(100 mg/L)、溶液pH值(8.0)、吸附剂质量(20 mg),以吸附时间为变量的相关吸附实验。从曲线中可以看到,在吸附过程在约15 min左右时,已经达到吸附平衡,其最大吸附容量为248.5 mg/g,数据表明,PEI改性树脂微球是一种吸附速率很快的铀吸附材料。
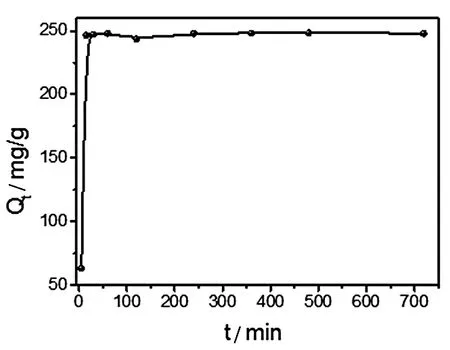
图4 吸附时间与吸附容量变化曲线
为进一步研究PEI改性树脂微球的吸附机理,确定其吸附类型,利用准一级公式(4)和准二级动力学模型公式(5)对吸附量-时间变化数据进行研究分析[10]。选用温度为25℃,溶液pH值为8条件下的吸附量-时间实验数据,进行线性拟合,拟合结果如图5所示,相关拟合参数列于表1。从表1中数据得知,利用准二级动力学方程拟合的相关性系数R2为0.999,远大于利用准一级动力学方程拟合的相关性系数,且利用准二级动力学模型计算所得到的吸附容量与实验所得数据相近,说明PEI改性树脂微球吸附剂吸附铀酰离子的过程符合准二级动力学模型,吸附过程主要是氨基、亚氨基吸附占主导的化学吸附。

图5 PEI改性树脂微球吸附剂的动力学方程拟合曲线:准一级动力学模型(A)和准二级动力学模型(B)

表1 PEI改性树脂微球吸附动力学方程拟合参数
ln(Qe-Qt)= lnQe-k1t
(4)
式中,Qe是吸附达到平衡时的平衡吸附容量,单位mg/g;Qt是吸附时间为t时吸附剂的吸附容量,单位mg/g;k1是准一级动力学常数,单位min-1。
通过公式2计算得到不同吸附时间的吸附容量,利用公式5进行准一级动力学方程拟合。
t/Qt= 1/(k2Qe2)+t/Qe
(5)
式中,Qe是吸附达到平衡时的平衡吸附容量,单位mg/g;Qt是吸附时间为t时吸附剂的吸附容量,单位mg/g;k2是准二级动力学模型速率常数,单位g/mg·min。
2.3.3 溶液的初始浓度对吸附的影响
为研究溶液的初始浓度对吸附过程的影响,固定吸附温度(25 ℃)、溶液pH值(8.0)、吸附剂质量(20 mg)和吸附时间(15 min)进行实验,实验结果如图6所示。观察两条曲线得知,随着溶液中铀酰离子初始浓度的增大,PEI改性树脂微球平衡吸附量的变化趋势是先快速上升,当溶液初始浓度为100 mg/L以后,增势放缓,逐渐趋于稳定,达到最大饱和吸附量301.75 mg/g。

图6 平衡吸附量和去除率随溶液中铀初始浓度变化曲线
吸附等温曲线是描述在恒定的温度条件下,达到吸附平衡时,溶质分子在两相中分布浓度之间关系的曲线,对液相吸附来说就是平衡吸附浓度与平衡吸附容量的关系曲线。利用Langmuir吸附等温模型公式(6)和Freundlich吸附等温模型公式(7)[11]对PEI改性树脂微球的吸附等温曲线进行拟合分析。
Ce/qe= qm/b+Ce/qm
(6)
式中,Ce是吸附平衡后溶液中的铀浓度,单位mg/L;qe是吸附平衡后的吸附容量,单位mg/g;qm是Langmuir模型的最大吸附量,即吸附剂的单层饱和吸附量,单位mg/g;b是Langmuir模型的一个常数,由交换吸附平衡常数决定,与吸附热有关,单位L/mg。
lnqe= lnKf+lnCe/n
(7)
式中,qe是达到吸附平衡后的吸附容量,单位mg/g;Kf是Freundlich模型的常数;1/n为一个系数,表示吸附点位的非均匀性。需要说明的是Freundlich模型是一个经验模型。
如图7和表2的数据可以看出,PEI改性树脂微球符合Langmuir吸附等温模型,说明吸附过程为单层吸附。

图7 吸附等温方程拟合曲线:Langmuir模型(A)和Freundlich模型(B)

表2 PEI改性树脂微球吸附等温模型拟合参数
2.3.4 竞争离子对吸附的影响
海水中所含离子情况复杂,除了浓度非常低的铀酰离子外,还共存着浓度远高于铀酰离子的其他金属离子,如Na+、K+、Mg2+、Ni2+和Ba2+等,这些共存的金属离子在实海提铀过程中,会干扰吸附剂对铀离子吸附过程,降低吸附剂性能。因此,优秀的吸附剂材料除了具有较高的吸附容量,还应该对铀酰离子具有高选择性。
为评估PEI改性树脂微球吸附剂吸附铀酰离子时的选择性和抗干扰性,本论文选取Na+,K+,Mg2+,Ni2+和Zn2+等金属离子作为竞争离子,固定吸附温度(25 ℃)、吸附剂质量(20 mg)和吸附时间(12 h),进行试验。实验结果如图8(A)所示,PEI改性树脂微球吸附剂在多种竞争离子存在时,吸附效果虽有所下降,但对铀离子的去除率仍然可以保持在较高的水平(72%)。从图8(B)可以看出,KdU远大于其它离子的Kd值,这说明PEI改性树脂微球在多离子存在的水溶液中具有很好的与铀酰离子键和的能力。所以,PEI改性树脂微球吸附剂对铀酰离子具有良好的选择性和抗干扰能力。

图8 多离子共存条件下,PEI改性树脂微球对铀酰离子和各种竞争离子的去除率(A)及Kd值(B)
2.3.5 低浓度实验
在实际的海水环境中,铀浓度仅为3.3μg/L。在此低浓度下,吸附剂是否仍具有较高的吸附效率是能否应用于海水提铀的前提。为验证PEI改性树脂微球对低浓度铀溶液的吸附能力,固定吸附温度(25 ℃)、溶液pH值(8.0)、吸附剂质量(20 mg)和吸附时间(12 h),进行了低浓度吸附实验,溶液中铀初始浓度由3.72到70.85 μg/L。结果如图9所示,在低浓度吸附实验中,PEI改性树脂微球对铀酰离子的吸附率在89%以上。这意味着PEI改性树脂微球具有海水提铀的应用前景。

图9 低浓度实验中铀的去除率
3 结论
本文以含氯树脂为原料,聚乙烯亚胺为改性剂,合成了PEI改性树脂微球吸附材料。对该材料进行了结构分析与形貌表征。通过一系列的吸附实验分析了该材料对铀的吸附性能,考察了溶液pH值、铀初始浓度等因素对吸附过程影响,并采用动力学方程和常见的吸附等温模型对吸附过程和吸附机制进行了深入分析。可得出结论如下:
1)PEI改性树脂微球铀吸附材料具有较好的吸附性能,适用于碱性溶液,如海水,其最佳吸附pH值在7.0-10.0之间。在实验室静态吸附条件下,饱和吸附容量可以达到248.5mg/g。吸附过程符合准二级动力学模型和Langmuir热力学模型,吸附剂对铀的吸附行为是单层化学吸附。
2)PEI改性树脂微球吸附铀酰离子具有良好的选择性,在多种竞争离子共存的条件下,对铀酰离子的吸附率仍能达到72%。
3)PEI改性树脂微球在低浓度实验条件下,仍对铀酰离子具有较高的吸附效率,可达89%以上。
综上所述,PEI改性树脂微球是一种优秀的铀吸附材料,在海水提铀领域有着较高的应用前景。
