甲磺酸仑伐替尼联合TACE治疗中晚期原发性肝癌的临床效果及安全性分析*
2020-11-27王洪云
王洪云
原发性肝癌在我国常见,而较多中晚期原发性肝癌患者的首选治疗方式为非手术治疗,而TACE是治疗本类患者的常见有效方式,其可有效阻断肿瘤组织的血供,对于肿瘤的控制作用值得肯定,而甲磺酸仑伐替尼作为临床近年来受肯定程度极高的一类药物,其用于中晚期原发性肝癌的效果研究较受肯定[1-2],但是其与TACE联合用于中晚期原发性肝癌的综合疗效仍有待进一步探究。本研究就甲磺酸仑伐替尼联合TACE治疗中晚期原发性肝癌的临床疗效及安全性进行研究分析,现报道如下。
1 资料与方法
1.1 一般资料 选取2017年2月-2019年1月本院收治的60例中晚期原发性肝癌患者为研究对象。纳入标准:原发性肝癌中晚期者;符合TACE治疗指征。排除标准:存在活动性出血;合并心脑肾肺等功能不全;认知异常;精神病史者。将其根据治疗方案的不同分为对照组(TACE组)30例和观察组(甲磺酸仑伐替尼联合TACE组)30例。所有患者均知情并同意本研究,且该研究已经医院伦理学委员会批准。
1.2 方法 对照组进行TACE治疗,采用赛丁格技术进行穿刺成功后,插入导管,并进行肝动脉造影,对病灶部位、血供及其他相关情况进行细致观察,将5-氟尿嘧啶(生产厂家:上海旭东海普药业有限公司,批准文号:国药准字H31020593,规格:10 mL∶0.25 g×5支/盒)1 000 mg及阿霉素(生产厂家:山西普德药业有限公司,批准文号:国药准字H14023143,规格:10 mg×10支/盒)40 mg,以明胶海绵辅助栓塞处理。观察组则采用甲磺酸仑伐替尼(生产厂家:Patheon Inc.,批准文号:注册证号H20180052,规格:4 mg×10粒×3板/盒)联合TACE进行治疗,TACE治疗与对照组相同,在此基础上以甲磺酸仑伐替尼进行服用,60 kg以下体重者的起始用量为8 mg,60 kg及以上者的起始用量为12 mg,根据患者应用情况进行剂量调整,持续用药。两组患者的其他治疗均相同。
1.3 观察指标及判定标准 比较两组的临床疗效、不良反应发生率、治疗前后的肿瘤标志物及浸润转移相关指标。(1)临床疗效:根据实体瘤疗效评价标准进行治疗效果的评估,本标准以病灶消失,且维持4周以上为完全缓解;病灶缩小50%以上,且维持4周以上为部分缓解;病灶缩小不足50%或增加不足25%为稳定;病灶增大25%以上为进展[3]。总有效=完全缓解+部分缓解+稳定。(2)不良反应:统计高血压、疲乏、腹泻、关节痛及腹痛情况,根据WHO相关标准分别为0~Ⅳ级[4]。(3)于治疗前及治疗2、4周后采集两组的空腹静脉血,将血标本离心(半径15 cm、时间5 min,转速3 000 r/min)后取血清进行检测,检测指标为肿瘤标志物及浸润转移相关指标,前者包括AFP、CA199及CA125,后者则包括GPC-3、VEGF及GP73,上述指标均以酶联免疫法试剂盒进行定量检测,由经验丰富者进行操作检测。
1.4 统计学处理 采用SPSS 22.0软件对所得数据进行统计分析,计量资料用(±s)表示,比较采用t检验;计数资料以率(%)表示,比较采用χ2检验。以P<0.05为差异有统计学意义。
2 结果
2.1 两组一般资料比较 对照组中男25例,女5例;年龄57~75岁,平均(65.3±5.9)岁;病灶直径4.1~8.1 cm,平均(5.7±0.5)cm;BCLC分期:B期20例,C期10例。观察组中男23例,女7例;年龄56~75岁,平均(65.6±5.5)岁;病灶直径4.1~8.3 cm,平均(5.6±0.7)cm;BCLC分期:B期21例,C期9例。两组患者的上述一般资料比较,差异均无统计学意义(P>0.05),具有可比性。
2.2 两组的临床疗效比较 观察组的临床总有效率为53.33%,显著优于对照组的23.33%,差异有统计学意义(χ2=5.711,P=0.016),见表1。

表1 两组的临床疗效比较 例(%)
2.3 两组的不良反应发生情况比较 两组的高血压、疲乏、腹泻、关节痛、腹痛发生率比较,差异均无统计学意义(χ2=0.082、0.077、0.089、0.111、0.111,P=0.774、0.781、0.765、0.739、0.739),见表2。
2.4 两组治疗前后的肿瘤标志物比较 治疗前,两组的肿瘤标志物比较,差异均无统计学意义(P>0.05);治疗2、4周后,观察组的肿瘤标志物水平均显著低于对照组,差异均有统计学意义(P<0.05)。见表3。
2.5 两组治疗前后的浸润转移相关指标比较 治疗前,两组的浸润转移相关指标比较,差异均无统计学意义(P>0.05);治疗2、4周后,观察组的浸润转移相关指标均显著低于对照组,差异均有统计学意义(P<0.05)。见表4。
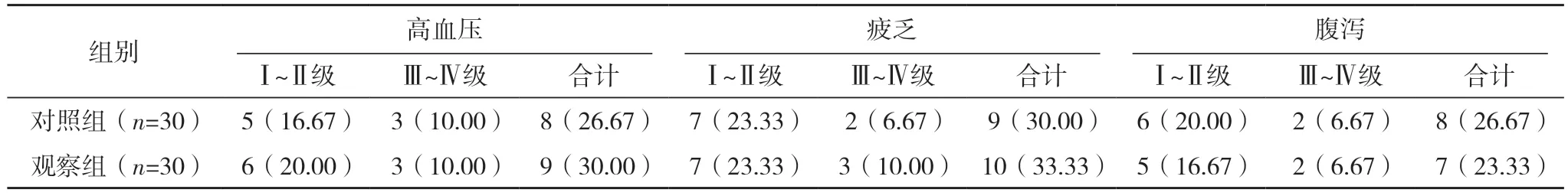
表2 两组的不良反应发生情况比较 例(%)

表2 (续)
表3 两组治疗前后的肿瘤标志物比较(±s)

表3 两组治疗前后的肿瘤标志物比较(±s)
注:t1、P1值为两组治疗前比较;t2、P2值为两组治疗2周后比较;t3、P3值为两组治疗4周后比较。
表4 两组治疗前后的浸润转移相关指标比较(±s)

表4 两组治疗前后的浸润转移相关指标比较(±s)
注:t1、P1值为两组治疗前比较,t2、P2值为两组治疗2周后比较,t3、P3值为两组治疗4周后比较。
3 讨论
中晚期原发性肝癌的临床治疗方式中,TACE是效果受肯定程度较高的一类治疗方式[5-8]。本类治疗方式主要为通过阻断病灶的血供来达到控制疾病的目的,但是其效果仍有待进一步提升,在新生血管控制方面的作用欠佳等情况提示了对其进行联合治疗的必要性[9-10]。甲磺酸仑伐替尼是用于肝癌治疗的新一线药物,其作为靶向治疗药物,在肝癌中的作用主要为对血管内皮生长因子受体进行抑制,因此对于肿瘤病灶的新生血管生成具有积极的控制作用,并且对血管及肿瘤生成相关的通路具有控制作用,因此在肝癌患者中的效果值得肯定[11-13]。临床中关于本药与TACE联合应用的效果研究可见,但是其细致全面的作用仍有待深入探究。除直观地对病灶的控制作用外,药物应用的安全性及对疾病相关指标表达的控制作用研究也有待针对性的探究[11-12]。
本研究就甲磺酸仑伐替尼联合TACE治疗中晚期原发性肝癌的临床疗效及安全性进行探究,结果显示观察组的临床总有效率为53.33%,显著优于对照组的23.33%,差异有统计学意义(P<0.05)。两组的高血压、疲乏、腹泻、关节痛、腹痛发生率比较,差异均无统计学意义(P>0.05)。且患者治疗2、4周后的肿瘤标志物及浸润转移相关指标表达也得到有效控制,因此肯定了甲磺酸仑伐替尼联合TACE治疗中晚期原发性肝癌的临床应用价值。分析原因,TACE治疗在有效阻断病灶血流的基础上,加用甲磺酸仑伐替尼可有效控制新生血管的生成,对于病灶侧支循环的控制作用显著[14-16],因此对病灶的治疗作用得以提升。而肿瘤标志物,尤其是浸润转移相关指标的表达显著降低,两者联合应用对病灶的血供切断作用更为彻底有效,因此在临床应用中优势更为突出[17-20]。
综上所述,笔者认为甲磺酸仑伐替尼联合TACE治疗中晚期原发性肝癌的临床疗效较好,且安全性值得肯定,在中晚期原发性肝癌中的应用价值较高。
