全降解镁合金组织工程支架孔隙特征与性能关系研究
2020-11-27熊美萍贾高智袁广银
熊美萍,贾高智,袁广银
我国每年因外伤、感染、肿瘤和先天性等原因导致的颌骨缺损的发生率约为0.24%[1]。颌骨缺损不仅影响容貌及颌面部的正常生理功能,还会带来心理问题,严重影响患者的生活质量。近年来,骨组织工程学的发展,使颌骨缺损尤其是大段骨缺损的功能性重建修复变成可能,并成为当前研究热点[2-3]。其中,支架材料在组织工程中起关键作用。理想的支架材料应满足如下条件[4-5]。①生物相容性良好:支架作为细胞生长和繁殖的场所,要求支架材料及其降解产物无毒、无炎症反应。为便于细胞的粘附、增殖及生长,支架材料还应具有骨传导与骨诱导性能。②具备体内降解性能:支架材料在完成其作用后应能够逐渐降解至消失,随着新生骨组织的长入,最终达到自体骨修复的目的。支架降解的速率需要和新骨的形成速率相匹配。③三维联通的多孔结构:适合的孔隙尺寸以适应新生骨组织的生长,便于新的血管和神经的长入,还要便于体系内外营养物质的交换和代谢产物的运输。④适宜的力学强度和可塑性:其力学性能应与骨组织相匹配(人体松质骨弹性模量为0.1~0.5 GPa,抗压强度为4~12 MPa[6])。此外还需良好的加工工艺性能,以便能加工成所需形状。
和陶瓷及高分子材料相比,镁合金作为一种可降解医用金属生物材料具有更好的综合性能,包括更高的强韧性以及更好的加工工艺性,并且镁合金材料在人体环境中会发生腐蚀降解,可望实现植入物在体内逐渐降解并最终消失。作者以及他人的研究均表明,镁合金降解过程中释放出的镁离子能够促进成骨细胞的粘附、增殖以及类骨质的生长,具有显著的成骨诱导作用[7-9]。此外,还有研究表明镁离子能促进血管内皮生长因子VEGF的表达,有望在引导血管生成的同时促进成骨、破骨细胞的分化[10]。由此可见,镁合金具有成为理想的骨组织工程支架材料的潜质。
本文研究了组织工程支架用镁合金多孔结构的制备工艺调控,研究了不同孔隙特征参数(圆形孔、不规则孔以及孔径大小等)对力学性能、细胞行为和降解行为的影响规律,以期为进一步开展镁合金骨组织工程支架在口腔缺损修复领域的临床应用奠定实验和科学基础。
1 材料与方法
1.1 实验材料与设备
球形和不规则多面体形氯化钠颗粒,颗粒尺寸约800 μm,如图1所示。高纯镁(纯度≥99.98%)、镁合金(Mg-Nd-Zn-Zr,简称JDBM)、场发射扫描电子显微镜SEM(JSM 7600F,日本)、微机断层扫描(micro CT,Bruker Skyscan 1176,美国)、室温压缩力学性能测试机(Zwick AG-100KN,德国)、细胞培养液DMEM(Gibco,美国)、细胞培养箱(Thermo,美国)和荧光显微镜(Olympus IX71,日本)。

图1 NaCl颗粒微观形貌Fig.1 Micrograph of NaCl particles
1.2 支架制备方法
采用模板复制法制备开孔多孔镁基支架,将松散态NaCl颗粒利用热压烧结工艺制成开孔多孔预制体,烧结压强7.5 kPa,烧结温度为720 ℃,烧结时间为24 h;使用80 t液压机进行渗流铸造,将预制体和镁锭放入模具后由电磁感应设备加热镁料至720 ℃熔化,熔化过程在96%(体积分数)CO2+4%(体积分数) SF6气氛中进行,随后冲头以3 mm/min速度进行压力铸造,冷却后即得预制体和镁的复合材料。通过线切割将复合材料加工为φ=10 mm、d=2 mm的圆片和φ=10 mm、d=15 mm的圆棒。复合材料中的NaCl预制体经水溶解滤除,并用1%(体积分数)硝酸乙醇超声清洗多孔支架30 s。
1.3 微结构及力学测试
表面微观形貌观察使用扫描电子显微镜SEM观测,利用微机断层扫描检测多孔支架的内部及横截面形貌,空间分辨率为9 μm。通过Mimics软件对micro CT数据重构分析,计算出表面积。对1.2中制备的圆棒进行室温压缩力学性能测试,压缩速率为1 mm/min,取应变量为0.2%平行于弹性区的截线与压缩曲线的交点为压缩屈服强度,模量为弹性区的斜率。
1.4 降解性能测试
在Hank’s模拟体液中进行浸泡析氢实验,记录产生氢气体积。在湿度95%、37 ℃、5%(体积分数)CO2细胞培养条件下进行浸泡降解形貌测试,12孔板内将1.2中制备的圆片状样品(1件/孔)浸泡于3 mL细胞培养基中,培养基为DMEM(Gibco,美国)+10%(体积分数)胎牛血清(FBS,Gibco,美国)+1%(体积分数)双抗(青/链霉素,Gibco,美国),定期更换新鲜培养液。
1.5 支架与细胞共培养观察
采用小鼠颅顶前成骨细胞株(MC3T3-E1),实验采用第3~8代细胞。将降解7 d的纯镁多孔支架在超声条件下浸泡在75%(体积分数)无水乙醇消毒20 min 后,在细胞超净台内经2 h 吹干待用。将MC3T3-E1细胞悬液稀释为2×106个/mL,在12孔板内每孔逐滴加入50 μL细胞悬液置于小圆片样品表面,随后加入3 mL细胞培养基,培养12 h。细胞在支架表面粘附形貌采用Live/Dead活死细胞染色法观察。
2 结 果
2.1 球形孔和不规则多面体形孔的微结构检测
micro CT检测支架横截面及内部的微观结构如图2所示,结果显示两组支架的孔隙形貌与NaCl颗粒的几何形状保持一致,且支架内部未见NaCl颗粒残留。对两组支架的三维结构分析发现球形孔支架的孔隙率为75%,表面积与宏观体积比为(3.43±0.15)/mm;不规则多面体形孔支架的孔隙率为68%,表面积与宏观体积比为(7.37±0.51)/mm。SEM观察球形孔支架和不规则多面体形孔支架的微观结构如图3所示,结果显示两组支架不仅复制了NaCl颗粒的外形及尺寸,更重要的是孔与孔之间的联通孔构成了三维联通的开孔多级孔尺寸结构。球形孔支架的微观结构在三维空间具有均匀重复的孔隙结构,而不规则多面体孔支架由于主孔在三维空间随机的取向以及不同的形貌和尺寸使其三维孔隙结构没有重复性。此外,球形孔支架的联通孔尺寸主要为200~350 μm,而不规则形多面体孔支架的联通孔尺寸主要为50~300 μm。

图2 多孔镁支架的micro CT横截面形貌 Fig.2 Cross-sectional images of the scaffolds from micro CT results
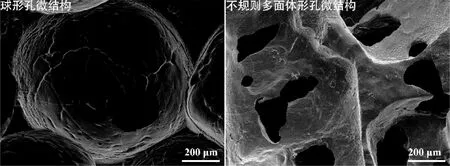
图3 多孔镁支架的SEM微观形貌Fig.3 SEM images of the microstructures of spherical pore structure
2.2 多孔镁合金支架的压缩力学测试
对铸态镁合金JDBM支架和540 ℃、8 h固溶处理后的JDBM球形孔结构支架进行压缩力学性能测试和微观组织观察,结果如图4~5所示。压缩力学曲线显示铸态JDBM镁合金支架具有更高的屈服强度和弹性模量,分别为11.50 MPa和1.01 GPa,但是铸态支架在最大抗压强度(12.43 MPa)后曲线局部出现锯齿状波动,在45%应变后应力明显开始下降。固溶处理后的多孔JDBM镁合金支架应力随应变增加平稳升高,呈现典型的松质骨压缩力学曲线特征,但压缩屈服强度和弹性模量分别降低至4.33 MPa和0.44 GPa。图5中固溶处理前在支架孔壁表面可清晰观察到网络状分布的强化相Mg12Nd,可以显著提高支架的力学性能。然而,Mg12Nd金属间化合物在孔壁变形中由于自身的脆性会产生裂纹,表现为变形曲线中应力的降低。固溶处理后该强化相消失,固溶强化效果弱于第二相强化效果,造成了压缩屈服强度的降低,但多孔支架在变形中的结构完整性提高。

图4 JDBM镁合金球形孔支架压缩力学曲线Fig.4 Compressive stress-strain curves of JDBM scaffolds

图5 固溶处理前后JDBM镁合金微观形貌Fig.5 Typical microstructure of pore wall before and after solution treatment
2.3 降解性能测试
图6是球形孔结构和不规则多面体孔结构的纯镁支架在Hank’s模拟体液中的析氢量测试结果,两种支架都呈现在初期快速释放氢气,10 d后氢气释放量趋于平稳。不同的是,在整个析氢实验中不规则多面体形孔支架的氢气释放量都显著多于球形孔结构支架。在第14天后不规则多面体形孔支架的析氢量约是球形孔结构支架的2倍。两种支架不同的析氢速率和析氢总量与自身的微结构特征直接相关,在相同的宏观体积下,不规则多面体形孔支架的总表面积约是球形孔结构支架总表面积的1.15倍,与Hank’s溶液具有更多的接触反应面积。因此,在相同时间内不规则多面体形孔支架会产生更多的析氢量;同时由于不规则形孔支架较低的孔隙率使支架具有比球形孔结构支架更多的基体质量,在后期稳定降解过程中会产生更多的析氢总量。图7是多孔镁支架在细胞培养条件下浸泡14 d后的宏观形貌,到第14天时降解产物完全覆盖了支架表面,孔隙结构已几乎不可识别。

图6 纯镁支架析氢实验结果Fig.6 Hydrogen evolution results of the two Mg scaffolds

图7 纯镁支架浸泡降解前后宏观形貌Fig.7 Macrographs of Mg scaffolds before and after immersion tests
2.4 细胞与支架共培养观察
选择静态浸泡7 d后的多孔纯镁支架进行成骨细胞直接培养,该时间点的支架降解环境较为稳定而且孔隙结构仍保留完好。从图8中的染色结果可以看出接种MC3T3-E1成骨细胞12 h后两组支架表面均粘附有大量活细胞。但是,不规则多面体结构的支架存在较多死细胞,孔隙中发现大量气泡,细胞在孔壁夹角有明显聚集倾向。

图8 两组纯镁支架上MC3T3-E1成骨细胞Live/Dead染色结果Fig.8 Live/Dead staining result of MC3T3-E1 osteoblasts on Mg scaffolds
3 讨 论
模板复制法是较为广泛的多孔结构制备方法,需先设计预制体模板或造孔粒子,作为被复制对象,通过机械混合或压力渗流等技术将目标支架材料填充到预制体模板或造孔粒子的空隙进而形成二者的复合材料,随后通过溶解滤除或热分解去除预制体模板或造孔粒子,将预制体模板或造孔粒子的结构形状和尺寸复制为支架的孔结构和孔尺寸[11]。常用的造孔介质有盐粒(NaCl)[12-13]、石蜡(paraffin)[14]和聚氨酯泡沫(polyurethane foam)等。模板法因实施方便、支架的孔形和孔尺寸精确可控的特征,广泛应用于金属、陶瓷和聚合物的多孔结构制备[15]。
NaCl的熔点为801 ℃,在25 ℃水中的溶解度为36 g/L,其高熔点和在水溶液中快速溶解的特性使其成为模板复制法制备多孔材料中被使用最多的造孔粒子。本研究中使用了尺寸相近的NaCl颗粒,模板滤除后都呈现完全开孔的空间结构,但不同的孔形结构对支架的联通性产生了显著差异。球形孔结构支架内的联通孔为大尺寸(200~350 μm)且集中分布,不规则多面体孔结构支架中联通孔为小尺寸(50~250 μm)且各尺寸联通孔相对数量相近;同时两种支架的微观结构表明,球形孔结构支架内的联通孔在孔壁均匀分布,不规则多面体孔结构支架内的联通孔在孔壁分布及取向都呈随机化。据此可以判断球形孔结构支架比不规则多面体孔结构支架具有更高的联通性能。
金属镁化学性质活泼,在溶液中与水通过氧化还原反应形成氢氧化镁并释放氢气,这也是镁在体内降解的基本原理,但是在生理环境中存在的Cl-会破坏氢氧化镁膜层,加速基体腐蚀[16]。多孔结构赋予镁支架更大的比表面积,而且联通的孔隙特征为腐蚀介质的进入提供了便利,这样镁的腐蚀过程将被进一步加快。目前对多孔镁支架降解规律的研究存在共同的认识,即孔隙率越高支架降解速率越快[17]。本研究中两组多孔镁支架虽然微结构存在差异,但降解相同时间后表面多孔结构均被降解沉积物填充,基本丧失了多孔结构的联通性。不同的是孔隙率较低,比表面积较高的不规则多面体形孔支架呈现更高的析氢速率,氢气的快速释放可能会抑制支架微结构内细胞的代谢和组织的长入。
本研究测试了微结构中金属间化合物对多孔支架力学性能的影响。Mg12Nd是JDBM合金的主要强化相,该合金具有优越的力学性能、耐腐蚀性能和良好的生物相容性[18],其在孔壁的网络状分布有效提高了支架的抗压屈服强度,但是该金属间化合物较硬的物理特征导致在变形中微结构局部断裂和应力下降。对多孔镁合金支架的固溶处理虽然导致了力学强度的下降,但是变形过程中应力无下降现象,与松质骨的变形特征更为一致[19]。
细胞是材料在植入后首先与其发生作用的生命单元,了解细胞与材料的相互作用是生物医用材料的研究重点,镁及镁的浸提液对细胞行为的影响已有大量报道[20-21]。多孔镁支架的三维孔隙结构是给细胞在空间范围进行迁移、增殖及分化和最终矿化和成骨提供场所,通过在多孔镁支架上进行体外细胞直接培养可以初步研究孔隙特征与细胞活性及粘附的关系。在相同表观体积条件下不规则多面体形孔支架的总表面积更大,细胞接种时落在支架上的细胞数量可能多于球形孔结构支架,然而大的比表面积可能会造成孔结构内微环境中离子浓度、pH值和渗透压等的明显改变,严重影响细胞的正常代谢行为。
综上所述,多孔镁基支架的微结构对联通性和降解性能有直接影响,微结构中第二相金属间化合物可显著提高支架的力学强度,但是多孔结构过快的降解速率不利于成骨细胞在支架孔隙内部的粘附铺展和增殖。在后续研究中,需要对多孔镁及镁合金支架开展功能化涂层修饰,提高支架的耐腐蚀性能和生物相容性,进一步探索微结构与生理组织的适配机制。
