颈后路脊柱内镜治疗神经根型颈椎病1 年随访研究*
2020-11-27陈志瑞吴彬彬杨明浩胡屹鹭衡冰冰占恭豪饶高峰
陈志瑞 吴彬彬 杨明浩,3 胡屹鹭,3 衡冰冰,4 刘 佳 占恭豪 饶高峰
(1 温岭市第一人民医院康复科,台州317500;温州医科大学附属第二医院2 疼痛科;4 麻醉科,温州,325027; 3 温州医科大学第二临床医学院麻醉学系,温州325000;5 台州市中心医院康复科,台州318000)
神经根型颈椎病 (cervical spondylotic radiculopathy, CSR) 是临床上最常见的颈椎病类型,占颈椎病发病率的50%~60%,是临床上导致颈肩部和上肢疼痛的最常见病因之一,CSR 的治疗逐渐成为社会关注的热点之一。CSR 主要因颈椎间盘髓核突出、钩椎关节骨刺形成、关节移位等原因导致单侧或双侧脊神经根受刺激或压迫,临床表现为与脊神经根分布区一致颈肩痛、上肢放射性疼痛、上肢肌力下降和/或手指疼痛、麻木等,多发于中老年人,严重影响病人生活质量[1]。大部分病人症状可经保守治疗缓解,经保守治疗无效或疗效不理想则需手术治疗。
既往对于单一或多个节段的CSR 病人通常采用开放性手术治疗,如颈椎间盘切除术伴或不伴融合内固定、单间隙减压植骨融合、颈椎次全切除减压术、人工椎间盘置换术等[2]。尽管手术方式不同,最终目的都是彻底解除神经压迫,重建颈椎稳定性并尽量减少并发症。随着微创技术的发展,近几年颈后路脊柱内镜逐渐应用于临床,因其创伤小、出血少、术后恢复快等优点在临床上迅速推广。有研究显示颈后路脊柱内镜是治疗CSR 安全、有效的手术方式[3,4],但目前国内外仍缺乏大样本颈后路脊柱内镜治疗CSR 术后长期临床疗效随访研究。因此,针对以上问题,本研究共纳入诊断为“神经根型颈椎病 (CSR) ”并在我科接受颈后路脊柱内镜治疗的病人68 例,术后对其进行1 年临床随访和评估,为颈后路脊柱内镜治疗CSR 的安全性和临床疗效提供重要参考依据。
方 法
1. 一般资料
本研究经温州医科大学附属第二医院伦理委员会审批,共纳入诊断为“神经根型颈椎病 (CSR)”并于2017 年1 月至2018 年10 月在疼痛科接受颈后路脊柱内镜手术治疗病人68 例,男性36 例、女性32 例,病人年龄36~82 岁(平均55.4±11.2 岁),术前疼痛平均持续时间为114.5±23.5 月。手术节段为C3-44 例、C4-515 例、C5-636 例、C6-712 例、C5-6和C6-71 例。手术所需时间平均78.1±9.6 min。平均住院天数为4.3±1.6 天,所有病人完成术后1 年随访。
纳入标准:①病变椎间盘位于C3-4至C6-7之间,并为初次接受颈椎手术;②临床症状、体征与影像学检查包括颈椎X 片、CT 和MRI 等的结果相符,CSR 诊断明确(典型病例见图1);③经保守治疗疗效不理想,并同意接受颈后路脊柱内镜手术。
排除标准:①神经根型以外的其他类型颈椎病或混合型颈椎病;②无法耐受或不愿接受颈后路脊柱内镜手术;③存在全身感染、凝血功能异常等疾病;④精神异常无法配合手术;⑤不愿接受随访者。
2. 手术过程
本研究中的所有手术主要由两位经验丰富的手术医师采用Joimax 脊柱内镜系统(卡尔斯鲁厄,德国)完成。病人俯卧位,采用C 臂机X 光引导下定位责任椎间盘和椎板位置,画定位点。旁开中线约2 cm 处进针,穿刺点皮下注射2 ml 0.5%利多卡因局部麻醉后插入穿刺针,并在C 臂机X 光引导下插入至椎板位置(见图2)。经筋膜层及椎板位置时分别退出针芯,注入8~10 ml 0.5%利多卡因进一步麻醉。插入导引钢丝、退出穿刺针,沿导引钢丝制造一个直径0.6~0.8 cm 的切口,逐级插入扩张管和工作导管。退出导引钢丝和扩张管,插入导棒,沿工作导棒方向先后插入工作套管和脊柱内镜,分离椎板位置骨膜暴露骨面,应用磨钻及咬骨钳等工具切除椎板骨质,制造一个直径0.6~0.8 cm 骨窗,镜下摘除突出髓核或增生骨质,并对脊髓背侧进行充分减压,解除神经根压迫(见图3)。手术完毕后,对术野进行灌洗和充分止血,最后退出内镜,缝合切口。

图1 C4-5 髓核突出、诊断为“神经根型颈椎病”病人的术前MRI(外院)和CT 图像Fig. 1 Preoperative MRI (Examined in another hospital) and CT images of patients with C4-5 nucleus pulposus protrusion and diagnosed as "cervical spondylotic radiculopathy"
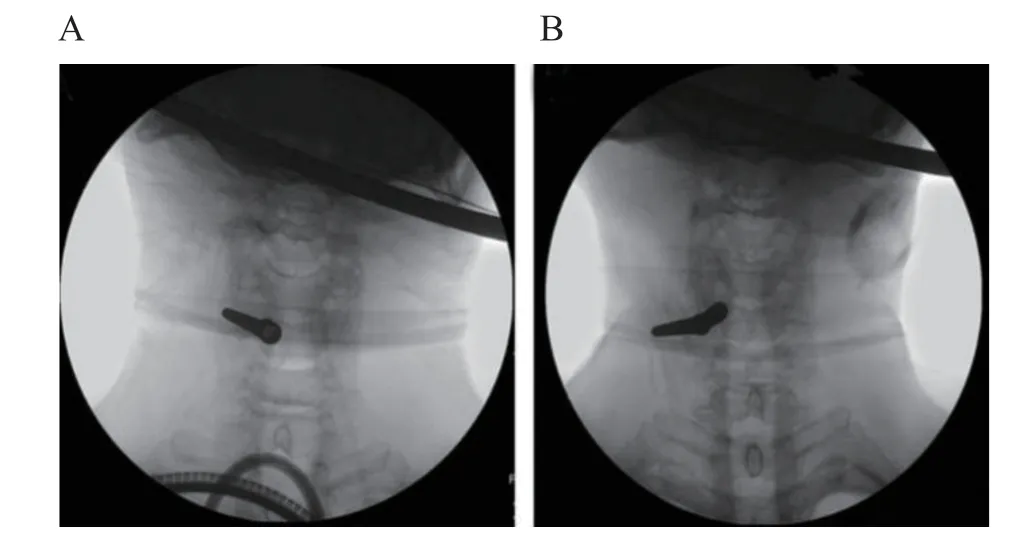
图2 术中放置工作通道到达C5 节段椎板上缘DSA 透视图Fig. 2 DSA fluoroscopic images of the upper edge of C5 lamina after placing the working channel during the operation.
3. 指标记录和术后复查
所有病人术后复查颈椎MRI 和三维CT(见图4)。在术前、术后1 天、7 天、1 月、3 月、6 月和1 年等时间点对纳入病人进行随访,采用疼痛数字评分法 (numeric rating scales, NRS) 评估疼痛(0~10 分),Oswestry 功能障碍指数(Oswestry disability index, ODI) 评估生活质量(0~100 分),日本骨科协会评分量表(Japanese orthopaedic association, JOA)(0~17 分)评估术后恢复。在术后1年随访中采用改良Macnab标准评估病人临床预后。改良Macnab 评估标准:“优”为症状完全消失,恢复原来的工作和生活;“良”为有轻微症状,活动轻度受限,对工作生活无异常;“可”为症状减轻,活动受限,影响正常工作和生活;“差”为治疗前后无差别,甚至加重。
4. 统计学分析
所有数据采用SPSS 25.0 软件统计分析,计量资料采用均数±标准差(±SD)表示,计数资料采用百分比(%)表示。对计量资料进行正态分布分析,本研究中各时间点NRS、ODI 和JOA 数据非正态分布,采用相关样本秩和检验分析。改良Macnab评估结果采用X2检验。P< 0.05 认为差异有统计学意义。
结 果
1. 手术前后NRS、ODI 指数和JOA 评估比较
68 例病人术前颈肩部NRS 评分为5.1 ± 2.6,术后1 天降至0.9±1.5 (P< 0.01),术后7 天、1 月、3 月、6 月和1 年的颈肩部NRS 评分均显著低于术前(P< 0.01)。上肢痛术前NRS 评分为4.7±3.1,术后1 天为1.2±1.7 (P< 0.01),术后其余各时间点NRS评分均较术前显著降低(P< 0.01)。术前ODI 指数为41.8±4.3,术后1 天降至31.3±3.8 (P< 0.05),术后其余各时间点ODI 均显著低于术前(P< 0.01)。术前JOA 评分为6.9±0.3,术后1 天升至12.1±0.4 (P< 0.01),术后其余各时间点JOA 评分均较术前显著增高(P< 0.01,见表1)。
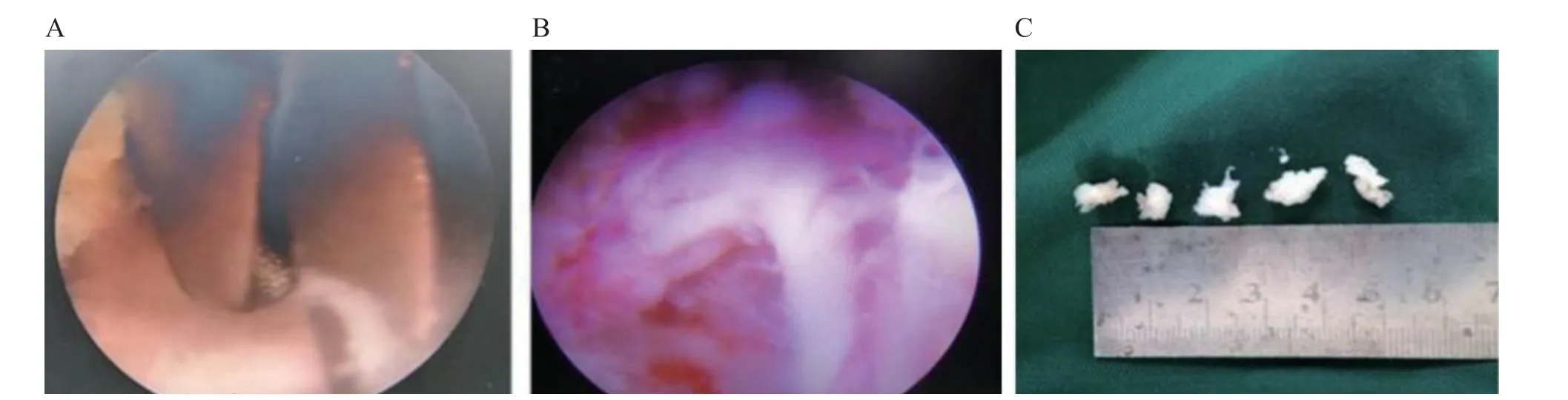
图3 (A)脊柱内镜下钳夹突出髓核图像;(B)突出髓核完全摘除后,神经根完全减压后的图像;(C)术中钳夹的突出髓核的图像Fig. 3 (A) The image of protruding nucleus pulposus under spinal endoscopy; (B) Image after the completely removal of the herniated nucleus pulposus and adequate decompression of the nerve roots; (C) The image of protruding nucleus pulposus that is resected during operation.

图4 (A) 术后MRI 矢状位图像;(B) 术后MRI 轴位图像;(C) 术后CT 三维重建图像;(D)术后CT 轴位图像 显示颈后路脊柱内镜完全摘除C4-5 突出髓核,硬膜囊膨胀良好。Fig. 4 (A) The sagittal MRI image at postoperation; (B) The postoperative axial MRI image; (C) 3-dimensional reconstructive image after operation; (D) The postoperative axial CT image. It shows that C4-5 herniated nucleus pulposus is completely removed under posterior cervical spinal endoscopy, and the dural sac is well expanded.
2. 术后Macnab 疗效评估结果和并发症统计
在最后1 次随访中对68 例病人采用改良Macnab 方法进行评估,其中有38 例为“优”、20 例“良”、9 例“可”、1 例“差”(见表2),“优良率”达85.3%。68 例病人术中均无发生神经根损伤、硬膜囊撕裂或感染等并发症,且无病人在随访时间内因症状复发需要接受二次微创或开放手术治疗。
讨 论
既往临床中对CSR 治疗主要包括保守治疗、微创手术和开放手术治疗三大类。其中保守治疗主要包括牵引、理疗、口服非甾体类消炎镇痛药物、硬膜外注射糖皮质激素等[5],但存在治疗时间长、症状易反复等缺点。经保守治疗疗效不理想者可采用手术治疗。既往开放性手术是治疗CSR 的主要方式,术中切除突出的髓核或增生骨赘有效减压,对椎体进行内固定并尽可能维持椎间高度[6]。尽管研究报道开放性手术具有较好临床疗效[7~9],但存在加速上下节段椎间盘退变、椎体曲度变直等缺点,因而在临床上的应用受到限制[10]。近年来随着脊柱微创手术方式和手术器械的发展,颈后路脊柱内镜已逐渐广泛应用于临床[11]。其与传统开放性术式相比主要具有以下优点:①可在局部麻醉下开展,老年病人可耐受,术中病人保持清醒,实时与手术医师保持沟通,有助于避免神经根损伤等并发症;②对颈部手术结构组织破坏少,极大程度降低颈椎节段性不稳的发生率;③术后恢复快,住院时间和所需费用较小;④不存在内固定植入后的相关并发症,因此易于被病人接受。然而,颈后路脊柱内镜也存在不足,如仍存在发生神经根损伤、硬膜囊撕裂、感染和出血等并发症的风险;减压范围不及开放手术,对于某些病例无法从后路完全摘除突出髓核或钙化韧带等压迫组织,而是采取部分摘除加开骨窗间接减压的处理方式,由此可能造成减压不彻底等[12]。尽管已有研究报道颈后路脊柱内镜下髓核摘除术与颈前路椎间盘切除内固定术均为治疗CSR 的有效、安全的手术方式,但前者创伤更小,术中出血量更少[3,4]。前期探索颈后路脊柱内镜治疗CSR 的研究均为小样本研究或未进行术后长期随访,因此颈后路脊柱内镜对CSR 病人术后长期临床疗效未阐明。
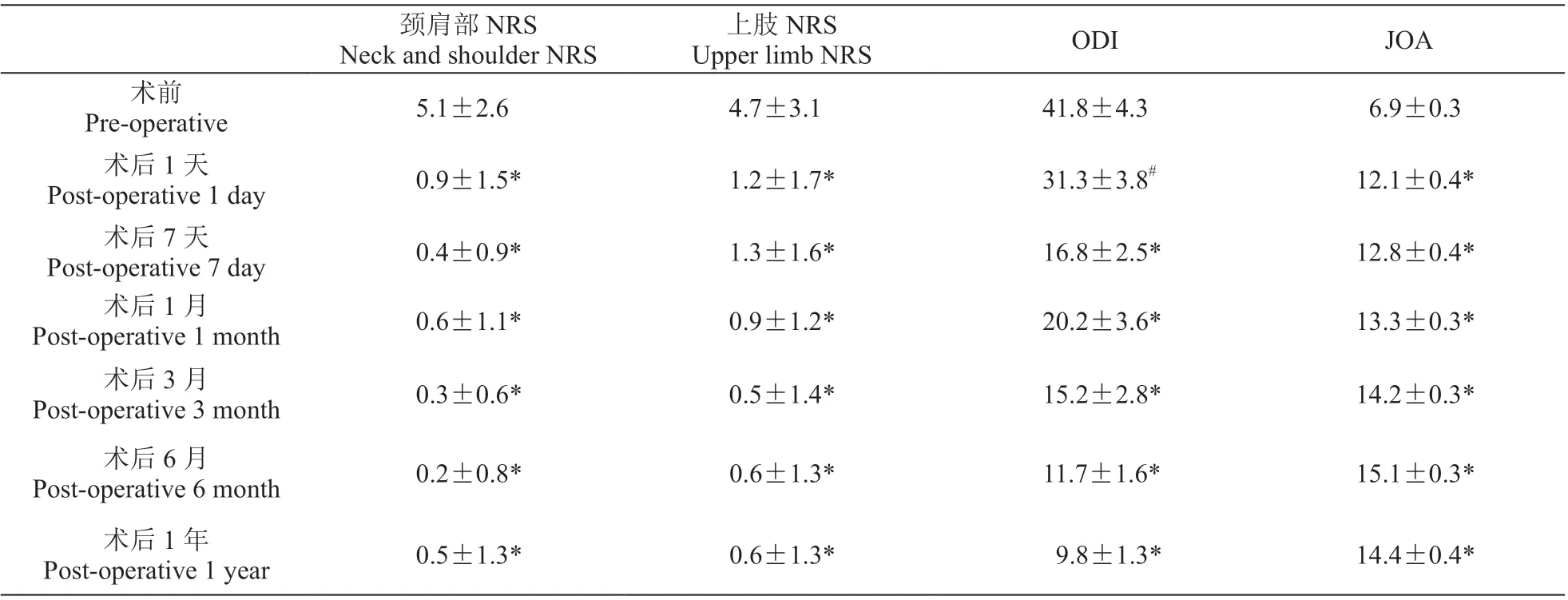
表1 CSR 病人各随访时间点NRS、ODI 和JOA 评估比较Table 1 Comparison of NRS, ODI, and JOA score of CSR patients at the follow-up time points

表2 CSR 病人1 年随访改良Macnab 评估Table 2 CSR patients with modified Macnab 1 year follow-up evaluation
本研究中共纳入CSR 病人68 例,所有病人完成术后1 年随访,完成术前、术后1 天、7 天、1月、3 月、6 月和1 年的颈肩部和上肢NRS 评分、ODI 和JOA 评估,并在术后1 年随访中采用改良Macnab 评估临床预后。结果发现颈后路脊柱内镜术后各时间点较术前的颈肩部和上肢NRS 评分、以及ODI 指数均显著低于术前,JOA 评分较术前显著增高,术中无病人发生神经根损伤、硬膜囊损伤、感染等并发症,随访时间内没有病人因症状复发需二次微创或开放手术治疗,改良Macnab 评估结果“优良率”达85.3%,其中有1 例病人因术后上肢疼痛缓解不明显而评估为“差”,推测可能与术中摘除突出髓核时对附近神经根刺激有关,术后该例病人继续接受保守治疗,未接受二次手术治疗。此外,因颈后路脊柱内镜术中出血量少,且术中术野为在灌注状态下进行,因此未能对术中出血量进行精确统计。
虽然本研究结果提示颈后路脊柱内镜为治疗CSR安全且有效的治疗方式,但本研究设计存在以下不足:①未能纳入其他治疗方式组别作为对照组;②未对术后椎间盘高度进行测量;③随访指标中仅统计NRS 评分、ODI 和JOA 等指标,未能记录病人疼痛相关的情绪量表指标,进一步探索与疼痛相关指标。针对以上不足,将在未来的研究中改进和完善。
综上所述,颈后路脊柱内镜为治疗CSR 的一种有效且安全的手术方式,可有效改善症状和病人生活质量,针对本研究存在的局限性,将在未来研究中进一步证实。
