深度学习在医学影像学领域应用研究进展*
2020-11-25龚尚瑾渠鸿竹方向东
龚尚瑾 渠鸿竹 方向东
(1中国科学院北京基因组研究所 中国科学院基因组科学与信息重点实验室 北京100101 2中国科学院大学 北京100049)
1 引言
医学影像技术是疾病诊断和预防的手段之一,是治疗疾病及提高患者健康管理的关键环节。随着技术发展,医学影像设备以更快速度和更强分辨率产生数据,这些数据大多需要进一步分析。传统医学影像分析通常基于临床经验,计算机医学图像分析则根据预先定义的计算公式提取某一特征,但由于临床上很多影像特征都是定性的,因此很容易导致漏诊和误诊[1]。利用深度学习数据分析方法可解决这一问题。深度学习是机器学习范围的重要分支。近年来在语音与音频识别[2]、计算机视觉[3]、自然语言处理以及生物信息学等领域取得突破性进展[4],被称为2013年以来10大技术突破之一。在医学影像方面,深度学习通过对图像的分类、检出、分割和配准,实现对2D和3D医学影像数据的分析和诊断,在减轻医生工作负担的同时有效提高工作效率和准确率[5]。本文简要概述了深度学习的原理和主要模型结构,以脑部疾病和乳腺癌为例,对国内深度学习方法在医学影像学中应用进行了分析并对其局限性进行讨论。
2 深度学习方法原理及模型结构
2.1 方法原理
深度学习是一种多层次表示学习方法,通过将所需复杂映射分解为一系列嵌套的简单映射(每个由模型的不同层描述)来解决问题,分为可见层、隐藏层和输出3部分[6],见图1。从底层向高层逐步学习提取特征,构建相应网络模型,最终得到训练对象的相关特征。例如一张以像素值数组形式存在的图片,可见层为输入像素,第1隐藏层表示的学习特征是识别图像中特定位置和方向的边缘;第2隐藏层根据第1层描述的边缘,鉴定可识别为角和扩展轮廓的边集合;第3隐藏层根据轮廓和角的特定组合检测特定对象;最后输出对象识别结果[7]。值得注意的是深度学习的优点在于其表示层并非手动定义,而是从大数据中学习得到的,可取代由人工提取数据特征的传统方法,实现自主学习[8]。同时由于深度学习的网络模型具有深层次、高运算量等特征,较适用于图像、语言等直观意义不明显的大数据处理分析[5]。
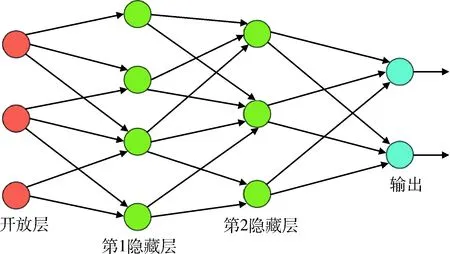
图1 深度学习模型示意图
2.2 主要模型结构
深度学习部分模型结构已应用于医学影像学图像大数据分析领域。常见模型包括:卷积神经网络、栈式自编码器、稀疏编码网络、受限玻尔兹曼机、深度信念网络等。
3 深度学习在医学影像学中的应用
3.1 概述
深度学习在医学影像学领域的研究主要涉及以下3方面:一是利用深度学习算法对影像学图像进行分类;二是基于影像学大数据,利用深度学习算法对特定疾病实现早期诊断筛查;三是通过可穿戴设备对病人健康指数进行管理,见图2。下文以脑部疾病和乳腺癌为例,对深度学习在国内医学影像学中的应用进行分析。
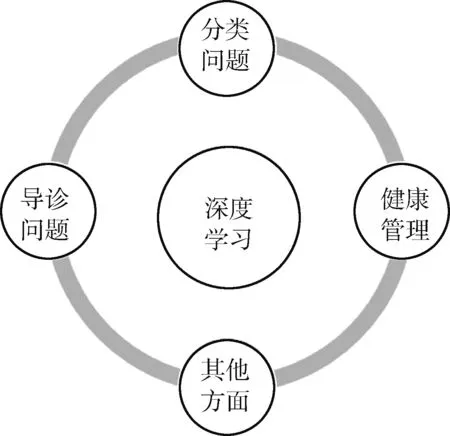
图2 深度学习在医学影像领域中的应用
3.2 脑部疾病应用
神经退行性疾病是由神经元或其髓鞘丧失所导致的疾病状态。临床上主要包括阿尔茨海默症、肌萎缩性脊髓侧索硬化症、亨廷顿氏舞蹈症、帕金森病(Parkinson′s Disease,PD)等。目前我国基于深度学习方法已经开展了很多关于神经退行性疾病的相关研究,主要涉及阿尔茨海默症和帕金森病。张巧丽[8]等针对帕金森病症的病例特点,在原有AlexNet网络基础上进行了算法优化,利用18 204例原始核磁共振图像数据(13 571例训练集、2 396例验证集和2 237例测试集)实现了帕金森病症早诊以及区分帕金森病和多系统萎缩,且其分类效果优于传统AlexNet网络算法。王金甲[9]等采用卷积神经网络算法(Convolutional Neural Networks,CNN),通过对DAPHNet数据集[10](由Tel AvivSourasky医疗中心神经科的步态与神经动力学实验室采集的有关10位帕金森患者的步态冻结(Freezing of Gait, FOG)数据)分析,识别帕金森患者中常见的步态障碍-FOG。与阈值法及其他传统机器学习方法所得结果相比,深度学习方法将平均正确率提高到91.43%,灵敏性提高到85.58%,特异性提高到93.63%。李自臣[11]等利用深度信念网络(Deep Belief Networks,DBN)和稀疏自编码(Spase Auto Encoder,SAE)算法对PINKs(PD致病基因)基因的活性结构数据进行分析,构建PINKs活性预测深度模型,实现对PINKs基因活性预测。实验结果表明DBN算法平均预测精度较传统机器学习算法,即支持向量机算法(Support Vector Machine,SVM)和近似最近邻分类算法(Approximate Nearest Neighbor,ANN)分别提高28.04%和18.84%;SAE算法平均预测精度较传统机器学习算法(SVM和ANN)分别提高23.51%和14.31%。吕鸿蒙[12]等根据阿尔茨海默症特点对原始AlexNet模型进行改进,利用公共数据库阿尔茨海默症神经影像学计划(Alzheimer′s Disease Neuroimaging Initiative,ADNI)中的核磁共振(Magnetic Resonance Imaging,MRI)数据和首都医科大学附属北京天坛医院临床数据,对阿尔茨海默症、轻度认知障碍和健康人群进行诊断。最终通过绘制受试者工作特征(Receiver Operating Characteristic,ROC)曲线,计算敏感度、特异度、精确度,比较传统AlexNet模型和增强AlexNet模型,得出改进的AlexNet网络模型展示出较好分类效果。
3.3 乳腺癌应用
乳腺癌在女性人群中发病率和死亡率较高,已引起世界卫生组织和相关科研机构高度重视。郑群花[13]等采用以AlexNet 为架构的卷积神经网络模型,成功根据病理图像将乳腺癌分为乳腺导管原位癌、乳腺浸润性导管癌、乳腺纤维腺瘤和乳腺增生4类。同时采用迁移学习和数据增强方法解决因标记样本过少导致过拟合问题。实验结果表明该模型准确率可达99.74%。李静[14]等通过用3种深度学习方法对143例患者影像数据进行分析,实现对乳腺良恶性分类。针对小样本数据集存在的过拟合问题,采用迁移学习思想将在大数据集上训练完成的模型迁移至小样本数据集,根据自己的数据集对模型参数进行优化,能够得到比重新训练模型更好的分类结果。
4 深度学习在医学影像学领域应用局限性
4.1 图像获取难度高
医学影像学图像与一般自然图像具有本质区别。医学影像学图像在内容上表达的是医学概念实体,是通过特定医学影像成像设备及原理人工合成的图像;由于涉及伦理、隐私以及经济等方面问题,医学影像学数据无法大规模获取[6]。
4.2 数据缺乏完整性
对于有监督的深度学习算法而言,为了提高模型拟合度,需要大量已标注过的训练集样本。医学影像学属于医工交叉学科,只有专业人士才能对医学影像学图像进行标注,但目前我国尚缺乏此类人才。同时我国绝大部分医院未建立完善的影像学图像数据库,导致薄层图像甚至历史数据均未储存[15]。
4.3 数据采集标准化不足
影像学数据来源于计算机断层扫描(Computed Tomography,CT)、磁共振成像、超声图像等,需要特定机器以及算法获得,但不同厂商的机器在图像获取、重建算法和参数设置上存在较大差异,缺乏统一标准[16]。而同种疾病常涉及多种类型影像学图像,处理时受图像分辨率、视野和切片厚度等因素影响,无法对不同影像图像进行精确比较。有研究表明影像组学特征及筛选受到机器平台、重建算法、扫面序列和成像参数等多种因素影响[17]。
4.4 图像自身限制
近年来随着光学相机技术发展,一般自然图像可达到较高分辨率。而由于成像原理以及伦理限制,绝大多数医学影像学图像在大小、像素上远不如一般自然图像。因此与目前计算机视觉和图像领域应用图像相比,医学影像学图像像素较低。
5 结语
除在脑部疾病和乳腺癌中应用外,深度学习在肺癌[18-20]、肝癌[21-23]等应用中展现了较好效果。此外深度学习也广泛应用于生物信息学领域,如利用深度学习方法预测非编码脱氧核糖核酸(Deoxyribo Nucleic Acid,DNA)突变对基因表达和疾病的影响[4]以及预测潜在药物分子活性,研究结果表明深度学习方法较其他机器学习方法准确率要更高。值得注意的是目前深度学习尚处于发展阶段,其在医学影像学中的应用也存在一定局限性,需进一步探讨改进措施。
