CYP2C19中间代谢型冠心病患者PCI术后发生氯吡格雷抵抗的危险因素分析
2020-11-17王尚毛云郑璐徐亚威袁伟腾唐涵杨海波
王尚,毛云,郑璐,徐亚威,袁伟腾,唐涵,杨海波
(郑州大学第一附属医院 心血管内科,河南 郑州 450000)
经皮冠状动脉介入术(percutaneous coronary intervention,PCI)是临床上解决冠状动脉粥样硬化性心脏病(冠心病)的重要方法[1],阿司匹林联合氯吡格雷双重抗血小板治疗是目前PCI术后患者抗血栓治疗的首选方案。然而临床发现,部分患者服用氯吡格雷仍无法有效抑制血小板的聚集与活化,导致缺血事件的发生[2],此现象即氯吡格雷抵抗(clopidogrel resistance,CR)。研究发现,CR是PCI术后再发血栓的重要原因,其不良心血管事件(major adverse cardiovascular events,MACE)发生率也高于非抵抗患者[3]。CYP2C19基因多态性造成CR是目前研究的热点,其与氯吡格雷生物活性受损、血小板抑制作用降低等有关,然而临床上对于CYP2C19中间代谢型患者在治疗中出现CR的研究较少且存在争议。本研究旨在通过对CYP2C19中间代谢型患者PCI术后血小板功能的检测,从而探讨对于此类患者在PCI术后常规服用阿司匹林联合氯吡格雷双重抗血小板治疗时CR发生的危险因素,为后续临床治疗提供参考及指导意见。
1 资料与方法
1.1 材料来源选取2018年10月至2019年9月于郑州大学第一附属医院因冠心病住院的患者192例,入院均采用“荧光标记、自动荧光原位杂交法”行CYP2C19基因多态性检测,确诊为中间代谢型(CYP2C19*1/*2、CYP2C19*1/*3)并接受PCI治疗。同时,考虑到普通肝素、糖蛋白Ⅱb/Ⅲa受体拮抗剂等药物的代谢规律,所有患者于PCI术后36 h空腹或餐后2 h以上,采集3 mL外周静脉血,应用江苏英诺华PL-16多参数血小板功能分析仪,按照仪器说明书添加二磷酸腺苷(adenosine diphosphate,ADP),以ADP诱导剂引起的血小板最大聚集率(maximum aggregation rate,MAR)作为氯吡格雷抗血小板疗效的评价指标,其中MAR≥55%称为CR。最终将192例患者分为抵抗组(55例)和有效组(137例)。本研究经郑州大学第一附属医院医学伦理委员会批准,患者或家属签署知情同意书。
1.2 纳入及排除标准(1)纳入标准:①符合中国经皮冠状动脉介入治疗指南(2009版)[4]中PCI指征的诊断标准;②CYP2C19基因多态性检测为CYP2C19*1/*2或CYP2C19*1/*3。(2)排除标准:①存在阿司匹林、氯吡格雷禁忌;②合并严重肝脏疾病及凝血功能障碍;③胃十二指肠炎症或溃疡等;④临床资料不完整。详细记录入选者的年龄、性别、高血压病史、脑梗史、吸烟史、饮酒史、主要合并用药等一般情况。
1.3 治疗方法所有患者入院后完善血常规、肾功能、C反应蛋白(C-reactive protein,CRP)、降钙素原(procalcitonin,PCT)、D-二聚体(D-Dimer)、空腹血糖(fasting plasma glucose,FPG)、糖化血红蛋白(hemoglobin a1c,HbA1c)、血浆总胆固醇(total cholesterol,TC)、甘油三酯(triglyceride,TG)、高密度脂蛋白胆固醇(high density liptein cholesterol,HDLC)、低密度脂蛋白胆固醇(low density liptein cholesterol,LDLC)、脂蛋白a[Lipoprotein(a),LP(a)]等生化检查,且接受双联抗血小板治疗,氯吡格雷[赛诺菲(杭州)制药有限公司,国药准字 J20180029]每日75 mg,阿司匹林(拜耳医药保健有限公司,国药准字 J20171021)每日100 mg,连续服用6 d以上,或PCI术前至少6 h口服阿司匹林300 mg和氯吡格雷450 mg的负荷剂量。术后继续口服阿司匹林每日100 mg,氯吡格雷每日75 mg。
2 结果
2.1 一般资料两组患者性别、年龄、高血压病史、脑梗史、吸烟史、饮酒史、主要合并用药等情况比较,差异无统计学意义(P>0.05)。见表1。
2.2 生化指标抵抗组肾功能、血常规、PCT、CRP、D-Dimer、HbA1c、TC、HDLC、LDLC、LP(a)与有效组比较,差异无统计学意义(P>0.05)。抵抗组FPG、TG水平高于氯吡格雷有效组,差异有统计学意义(P<0.05)。见表2。
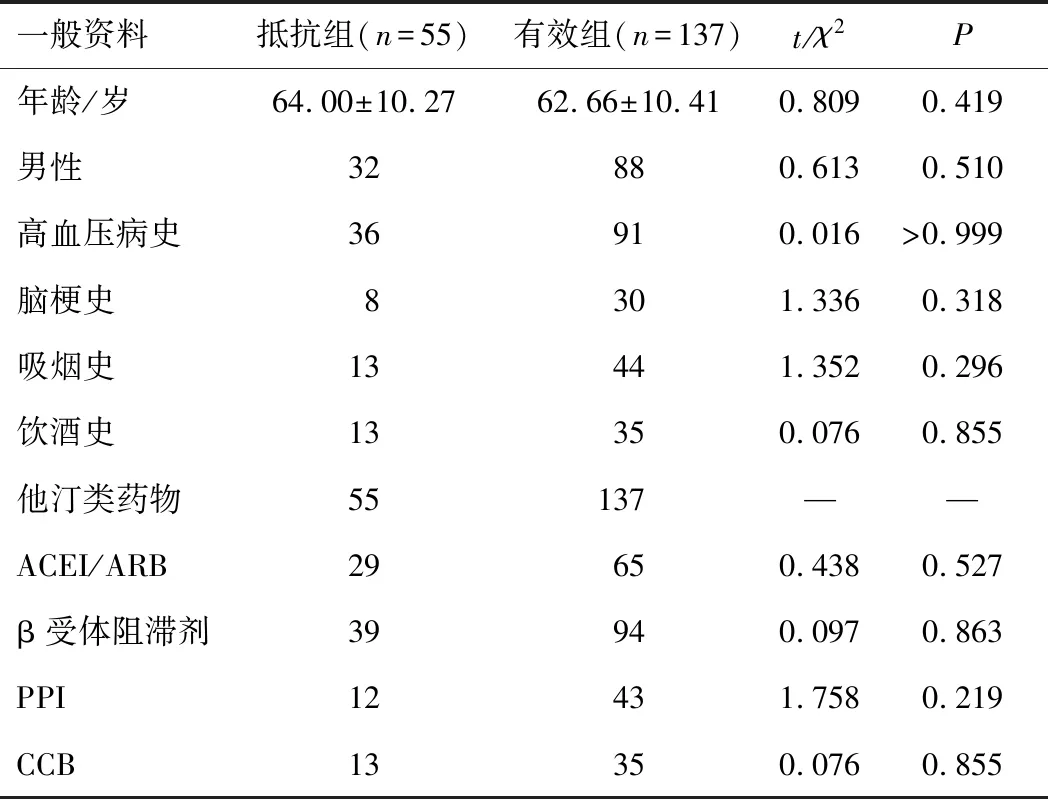
表1 两组患者一般资料的比较

表2 两组患者生化指标的比较
2.3 氯吡格雷抵抗的多因素分析通过利用Binary logistic回归分析发现,FPG及TG升高是CYP2C19中间代谢型冠心病患者PCI术后氯吡格雷抵抗的独立危险因素(P<0.05)。见表3。

表3 氯吡格雷抵抗的多因素回归分析
3 讨论
随着氯吡格雷在临床的广泛应用,研究发现,氯吡格雷抗血小板作用在个体上存在较大差异,部分PCI术后患者在常规服用氯吡格雷后出现CR,最终发生PCI术后血栓再形成的MACE[5]。故及早甄别CR,合理调整治疗方案有助于改善PCI术后患者预后。CR的发生主要与基因、伴随疾病、服用药物等多种因素有关[6-7]。其中,CYP2C19基因多态性造成患者对氯吡格雷抵抗的个体差异近年备受关注[8],尤其对于CYP2C19中间代谢型患者,此类患者情况复杂,在治疗上选择维持原有剂量或者增加剂量,或者选用其他抗血小板药物尚未达成统一共识[9-10],仍需进一步的研究获得科学依据。
本研究首先对氯吡格雷抵抗组和有效组一般资料差异进行分析,结果表明两组间患者性别、年龄、既往史、主要合并用药等一般资料差异无统计学意义,这可能提示对于CYP2C19中间代谢型的冠心病患者,氯吡格雷抵抗的发生与其他合并疾病或当前主要药物治疗方案无关,导致氯吡格雷反应性降低的原因可能来自于冠心病病理生理过程或者患者先天遗传因素。
在对两组一般血生化指标的分析中发现,FPG升高是CYP2C19中间代谢型冠心病患者PCI术后CR的一个独立危险因素。FPG而非HbA1c水平的高低影响血小板聚集率,这与符少华、许强等[11-12]结果一致。研究人员推测这与短期内血糖不稳定或控制不佳有关,而与长期血糖控制关系不大。分析其可能机制,较高血糖水平可促进血小板的黏附与聚集,同时也导致血小板表面膜蛋白的糖基化,增强血小板的活性,影响抗血小板药物的效果。此外,血糖代谢产物甲基乙二醛水平升高可影响多个血小板激动剂的信号传导通路,这对血小板活性的发挥起到重要作用[13],但是也不能排除是否由于患者体内血管炎症反应加重,引起应激性血糖升高,导致血小板激活的同时,造成了两组间FPG水平的差异,这仍需要更多的研究加以考证。
此外,TG水平升高也是CYP2C19中间代谢型冠心病患者PCI术后发生CR的独立危险因素,这可能与TG通过特定途径单独引起血小板活性变化有关。研究证实,TG主要存在于富含甘油三酯脂蛋白(triglyceride-rich lipoprotein,TRLs)中[14-15],而TRLs可能通过增加纤维蛋白原水平或上调纤溶酶原激活物抑制剂的水平,诱导促凝状态,增强血小板聚集及血栓形成[16]。此外,也可能与表达在血小板表面的CD40L(或称T细胞-B 细胞活化分子)有关。血小板CD40L表达阳性率与TG水平呈一定程度的正相关,这使得血小板免疫活化增加[17],从而启动后续炎症、免疫和凝血反应。
综上所述,对于CYP2C19中间代谢型冠心病患者,PCI术后服用双抗治疗时,FPG和TG升高是造成CR的独立危险因素,提示医生在控制好此类患者血糖、血脂水平的同时,根据此类患者FPG与TG水平调整氯吡格雷剂量或选用其他类型抗血小板药物,可在一定程度上减少MACE的发生,帮助指导临床制定个体化、精确化的治疗方案。研究的不足之处在于本研究为回顾性研究,在病例的选择上可能存在偏倚,其次,本研究为单中心研究,某些结果可能与样本量较小有关,无法体现统计学意义,对于此类患者发生CR更加准确的分析,需要更大规模的临床试验进一步研究。
