安罗替尼三线治疗广泛期小细胞肺癌的效果
2020-11-16赵文文肖超冯青青阮岱玮赵文飞魏红梅
赵文文 肖超 冯青青 阮岱玮 赵文飞 魏红梅
[摘要] 目的 探讨安罗替尼三线治疗广泛期小细胞肺癌(E-SCLC)的效果及安全性。方法 选取15例E-SCLC三线及以上治疗病人,口服安罗替尼12 mg/d,服药2周停药1周为1个治疗周期,每治疗2个周期后进行1次疗效评估。结果 15例病人均完成安罗替尼单药2~8周期治疗,随访1.9~7.4个月,疗效为部分缓解2例、疾病稳定9例、疾病进展4例,疾病控制率为73.3%。中位无进展生存期(PFS)为4.3个月,ECOG评分0~1分组中位PFS明显长于ECOG评分2分组,差异有显著性(P=0.004)。不良反应有高血压(3例)、疲乏(4例)、手足综合征(2例)等,主要为1~2级,未发生4级及以上的不良反应。结论 安罗替尼治疗E-SCLC效果显著,不良反应较轻。ECOG评分良好的病人具有更好的临床获益。
[关键词] 小细胞肺癌;安罗替尼;血管生成抑制剂;药物疗法;治疗结果
[中图分类号] R739.9 [文献标志码] A [文章编号] 2096-5532(2020)06-0727-03
doi:10.11712/jms.2096-5532.2020.56.179 [开放科学(资源服务)标识码(OSID)]
[网络出版] https://kns.cnki.net/kcms/detail/37.1517.R.20201016.1125.006.html;
[ABSTRACT] Objective To investigate the clinical effect and safety of anlotinib as the third-line treatment of extensive-stage small cell lung cancer (E-SCLC). Methods A total of 15 patients with E-SCLC who underwent third-line treatment or above were enrolled and were given oral anlotinib 12 mg/d. Each treatment cycle was 2 weeks of administration followed by 1 week of drug withdrawal, and clinical outcome was evaluated every two treatment cycles. Results All 15 patients completed 2-8 cycles of monotherapy with anlotinib and were followed up for 1.9-7.4 months. Among the 15 patients, 2 achieved partial remission, 9 achieved stable disease, and 4 experienced disease progression; the disease control rate was 73.3%. The median progression-free survival (PFS) time of the 15 patients was 4.3 months, and the patients with an ECOG score of 0-1 had a significantly longer median PFS time than those with an ECOG score of 2 (P=0.004). Major adverse reactions included hypertension (3 patients), fatigue (4 patients), and hand-foot syndrome (2 patients), which were mainly grade 1-2 reactions, and no grade 4 adverse events or above were observed in this study. Conclusion Anlotinib has a marked clinical effect in the treatment of E-SCLC, with relatively mild adverse reactions, and the patients with a lower ECOG score tend to gain better clinical benefits.
[KEY WORDS] small cell lung carcinoma; anlotinib; angiogenesis inhibitors; drug therapy; treatment outcome
肺癌是最常見的恶性肿瘤之一。统计显示,2018年肺癌病人占全球癌症新发和死亡病例的首位[1]。肺癌分为非小细胞肺癌(NSCLC)和小细胞肺癌 (SCLC),其中SCLC病人占肺癌总数15%~20%[2-4],而且60%~70%病人在确诊时即为广泛期。SCLC较NSCLC侵袭性更强,虽然其对放化疗敏感,但易复发并快速进展。二线治疗进展后广泛期SCLC(E-SCLC)再化疗的有效率非常低,病人很难获益[5]。有研究显示,多靶点抗血管生成的小分子酪氨酸激酶抑制剂(TKI)用于SCLC三线治疗可使病人临床获益[6-7]。安罗替尼是我国自主研发的一种多靶点小分子TKI药物[8-10]。目前有关安罗替尼胶囊三线治疗E-SCLC报道较少。本文探讨安罗替尼胶囊治疗E-SCLC的临床效果及安全性。
1 资料与方法
1.1 一般资料
2018年6月—2019 年12月,我院应用安罗替尼治疗E-SCLC病人15例,男12例,女3例;年龄 41~75岁,平均(57.14±4.21)岁。其中ECOG评分 0分3例,1分5例,2分7例;有吸烟史10例,脑转移6例,放射治疗史8例。病人纳入标准:①年龄18~75岁,ECOG评分0~2分;②经病理学检查确诊、复治的E-SCLC病人,具有可测量病灶;③既往至少接受过两种系统性化疗方案治疗后疾病进展(PD)的E-SCLC病人。排除标准:①预计生存期<3 个月;②既往使用过其他抗血管生成靶向药物、免疫抑制剂的病人;③过敏体质病人;④有神经、精神病史及痴呆病人;⑤伴其他恶性肿瘤病人。
1.2 治疗方法
病人每日空腹服用盐酸安罗替尼胶囊(正大天晴药业集团股份有限公司)1粒(12 mg),连续口服2周停药1周,即3周为1个治疗周期,直至PD或不能耐受。期间根据不良反应程度调整盐酸安罗替尼剂量为10 mg或8 mg,如剂量为8 mg仍无法耐受,则永久停药。
1.3 疗效评价
所有病人在完成第2个治疗周期后进行疗效评估,此后每2个治疗周期后进行1次评估。根据实体瘤疗效评价标准(RECIST)1.1版,近期疗效分为完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)和PD[11]。疾病控制率(DCR)指CR、PR和SD且维持4周以上的病例数占可评价疗效病人的比例。无进展生存期(PFS)定义为自入组至PD、病人死亡或末次随访时间。随访截止时间为2020年4月10日,无失访病人。
1.4 安全性评价
药物不良反应根据美国国立癌症研究所常见不良事件评价标准(NCI CTCAE)5.0版进行评估。
1.5 统计学处理
采用SPSS 19.0软件进行统计学分析。计数资料用例数或百分比表示,采用Kaplan-Meier法绘制生存曲线,生存时间比较采用Log Rank检验。以P<0.05为差异有统计学意义。
2 结 果
2.1 治疗效果
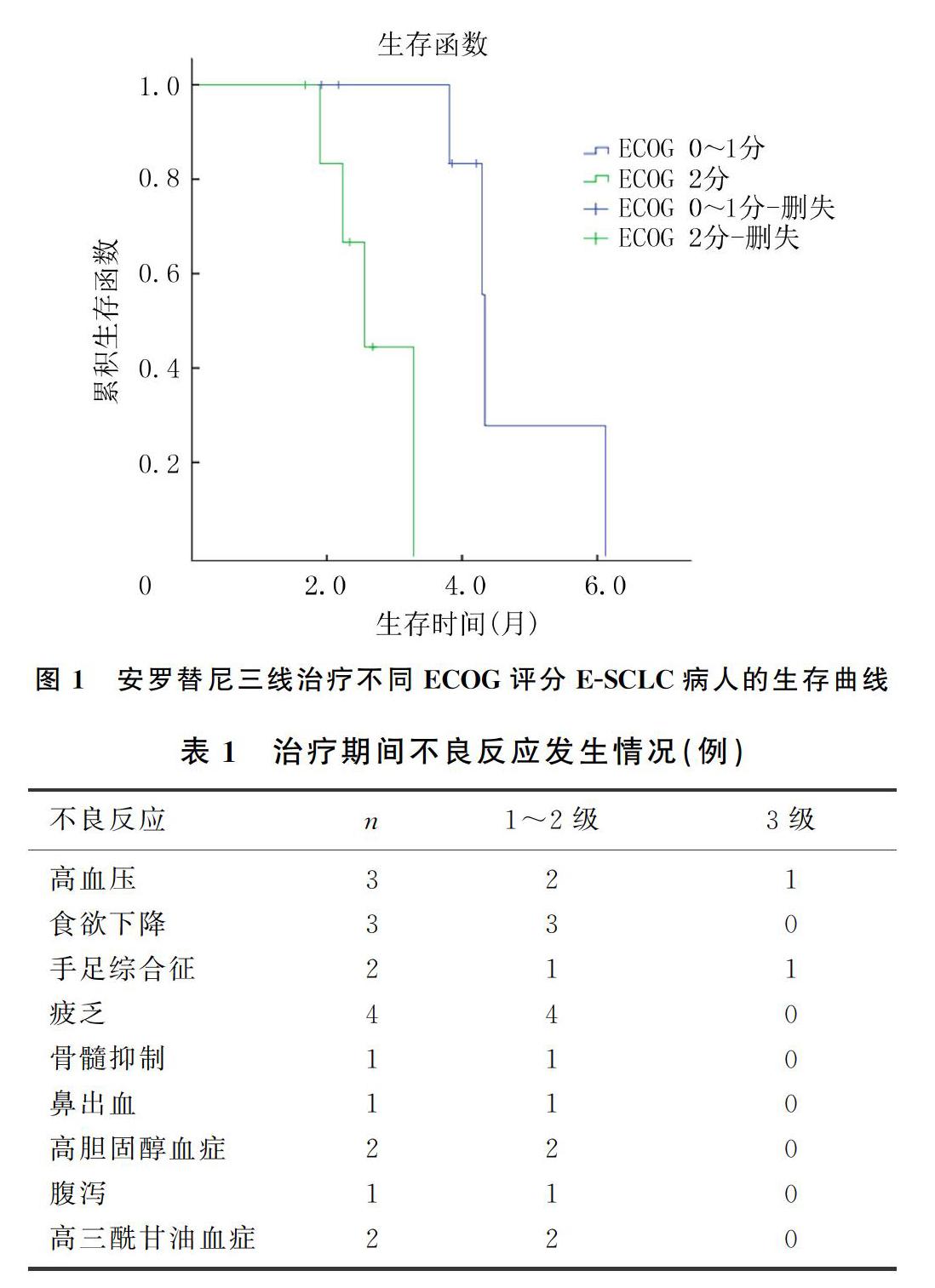
本文15例病人完成2~8周期治疗,其中PR者2例,SD者9例,PD者4例,DCR为73.3%。随访1.9~7.4个月,15例病人中位PFS为4.3个月(95% CI=3.1~5.5个月),ECOG评分0~1分组中位PFS为4.8个月(95% CI=4.2~5.4个月),ECOG评分2分组中位PFS为2.7个月(95%CI=1.9~3.2个月),两组中位PFS比较差异有显著性(P=0.004)。见图1。
2.2 药物不良反应
治疗期间病人出现的不良反应主要有高血压、食欲下降、疲乏等,主要为1~2级,未发生4级及以上的不良反应。此外,有2例病人出现2种及2种以上的不良反应。见表1。1例病人因出现鼻出血将药物减量至10 mg,1例出现3级手足综合征将药物减量至8 mg。无治疗相关死亡。
3 讨 论
近年来,分子靶向治疗在NSCLC治疗方面不断取得突破性进展。E-SCLC为一种难治性肿瘤,三线治疗病人的客观反应率(ORR)不足30%,中位生存期仅为4.0~5.0个月。安罗替尼是目前国内唯一批准用于SCLC三线治疗的抗血管生成的多靶点小分子TKI药物。有研究显示,难治、多线复发的SCLC病人应用安罗替尼治疗的PFS较安慰剂组提高了3.4个月,疾病进展风险降低了81%[12]。安罗替尼可显著延长放化疗失败、对靶向治疗药物耐药或无法耐受放化疗的SCLC病人生存时间。
抗血管生成是晚期肺癌重要的治疗手段之一,血管内皮生长因子(VEGF)/血管内皮细胞生长因子受体(VEGFR)在肿瘤血管形成的过程中发挥重要作用,其可通过增加微血管通透性、刺激血管内皮细胞增殖以及促进血管内皮细胞迁移等作用促进肿瘤异常血管的生成[13]。安罗替尼为TKI,可通过抑制血管生成相关的信号通路,强效抑制VEGFR、血小板衍生生长因子(PDGF)受体、成纤维细胞生长因子受体(FGFR)和C-Kit等多个靶点,达到抗肿瘤血管生成和抑制肿瘤生长的双重作用[14]。
本研究15例E-SCLC病人均完成了2~8个疗程治疗,其中PR者2例,SD者9例,PD者4例,DCR为73.3%;随访1.9~7.4个月,病人的中位PFS长达4.3个月,与相关研究结果一致[15]。由于本文病例有限,且观察时间较短,未对安罗替尼治疗病人总生存期进行统计分析。本文结果还显示,ECOG评分0~1分组中位PFS明显长于2分组,差异有统计学意义,提示安罗替尼治疗对ECOG评分良好的病人具有更好的临床获益。安罗替尼常见的药物相关不良反应为高血压、蛋白尿、疲乏和手足综合征等,本文病人的不良反应多为1~2级,仅2例发生3级不良反应,表现为高血压和手足综合征。本研究中出现高血压病人给予降压药物治疗后,血压均降至正常范围内。对于发生手足综合征的病人可酌情局部使用润肤霜、尿素霜、糖皮质激素软膏等药物治疗。安罗替尼抑制VEGF信号传导通路可破坏血管内皮细胞完整性引起凝血功能障碍,从而降低伤口愈合能力,增加出血风险。本研究中1例病人出现2级鼻出血,安罗替尼减量至10 mg后出血消失。本研究中安罗替尼治疗病人出现的不良反应,通过对症治疗和安罗替尼减量后均得到控制,无因不良反应而停药者。此外,安罗替尼是口服药物,临床应用中病人接受程度高。
综上所述,对于二线化疗失败的E-SCLC病人,应用安罗替尼三线治疗效果较好,ECOG评分良好的病人临床获益更多。并且该药物安全性及耐受性良好。但由于本研究样本量小,且未进行随机对照研究,结果存在一定的偏倚。因此,安罗替尼三线治疗E-SCLC价值有待进一步研究。
[參考文献]
[1] BRAY F, FERLAY J, SOERJOMATARAM I, et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries[J]. CA: a Cancer Journal for Clinicians, 2018,68(6):394-424.
[2] JEMAL A, SIEGEL R, XU J Q, et al. Cancer statistics, 2010[J]. CA: A Cancer Journal for Clinicians, 2010,60(5):277-300.
[3] SIEGEL R L, MILLER K D, JEMAL A. Cancer statistics[J]. CA-Cancer J Clin, 2015,64(1):5-29.
[4] 孙可欣,郑荣寿,曾红梅,等. 2014年中国肺癌发病和死亡分析[J]. 中华肿瘤杂志, 2018,40(11):805-811.
[5] HOWINGTON J A, BLUM M G, CHANG A C, et al. Treatment of stage Ⅰ and Ⅱ non-small cell lung cancer: diagnosis and management of lung cancer, 3rd Ed: American College of Chest Physicians evidence-based clinical practice guidelines[J]. Chest, 2013,143(5 Suppl):e278S-e313S.
[6] SHAO L, WANG W X, SONG Z B, et al. The efficacy and safety of anlotinib treatment for advanced lung cancer[J]. OncoTargets and Therapy, 2019,12:6549-6554.
[7] FAN Y, HUANG Z, LI W, et al. P1.12-01 A single-arm multi-center phase Ⅱ study of apatinib in patients with ES-SCLC after second/third-line chemotherapy[J]. Journal of Thoracic Oncology, 2018,13(10):S573.
[8] 金振兴,杜秀平. 盐酸安罗替尼治疗晚期非小细胞肺癌的临床观察[J]. 临床与病理杂志, 2020,40(4):905-912.
[9] 王俊,冉凤鸣,金兵. 安罗替尼治疗恶性肿瘤的临床研究进展[J]. 中国肿瘤, 2019,28(5):359-366.
[10] 斯晓燕,王汉萍,张晓彤,等. 安罗替尼治疗晚期非小细胞肺癌16例临床分析[J]. 中华内科杂志, 2018,57(11):830-834.
[11] EISENHAUER E A, THERASSE P, BOGAERTS J, et al. New response evaluation criteria in solid tumours: revised RECIST guideline (version 1.1)[J]. European Journal of Can-cer (Oxford, England: 1990), 2009,45(2):228-247.
[12] CHENG Y, WANG Q, LI K, et al. OA13.03 anlotinib as third-line or further-line treatment in relapsed SCLC: a multicentre, randomized, double-blind phase 2 trial[J]. Journal of Thoracic Oncology, 2018,13(10):S351-S352.
[13] JAYSON G C, KERBEL R, ELLIS L M, et al. Antiangioge-nic therapy in oncology: current status and future directions[J]. Lancet (London, England), 2016,388(10043):518-529.
[14] LIN B Y, SONG X M, YANG D W, et al. Anlotinib inhibits angiogenesis via suppressing the activation of VEGFR2, PDGFRβ and FGFR1[J]. Gene, 2018,654:77-86.
[15] CHENG Y, WANG Q, LI K, et al. Anlotinib as third-line or further-line treatment in relapsed SCLC: a multicentre, randomized, double-blind phase 2 trial[J]. Journal of Thoracic Oncology, 2018,13(10):S351-S352.
(本文編辑 黄建乡)
