水泥生料基固硫剂密实态和分散态的反应特性研究
2020-11-09酒少武杨爱武陈延信
酒少武,杨爱武 ,陈延信
(1.西安建筑科技大学 材料科学与工程学院,陕西 西安 710055;2.西安博研仪器分析应用科技有限公司,陕西 西安 710061)
水泥生产采用的原料和燃料中含有一定量的硫元素,会产生SO2的排放而形成环境污染[1-4]。近年来,随着水泥回转窑协同处置危废和固废技术的应用发展,更多的硫元素进入水泥生产系统,导致SO2排放愈加突出[5-7]。水泥生料的主要成分为石灰石,会分解成高活性的CaO,因此水泥生料具有固硫作用[8-9],在水泥生产中硫元素以SO2气体形式被释放,一部分被系统中CaO捕集再逐步转化为硫酸盐形式的稳定矿物相被固化下来,其余则进入尾气被排放[9]。深入研究水泥生料基固硫剂在煅烧过程中的反应机理,有助于充分发掘水泥生产系统的固硫潜力,对水泥工业固硫减排技术开发具有重要的意义。
在水泥生产过程中,水泥原料在悬浮预热预分解系统中以分散态存在,在分解炉内形成大量的活性分散态CaO与SO2气体充分接触,有助于SO2的捕集和固化[9];但在回转窑内、大颗粒流化床,以及其他采用粒状生料煅烧技术的反应器中,水泥生料以密实态(即紧密堆积态)存在,一方面形成的活性CaO与SO2接触面积减小而导致密实态钙基固硫效率降低,但另一方面密实结构抑制生成的硫酸盐固硫相的分解而提高了固硫相稳定性利于SO2的固化。关于水泥生料在固硫效率、固硫机理、固硫特性以及固硫影响因素等方面研究较少且不够深入,尤其是不同堆积态水泥生料固硫研究鲜有记载。
本文以密实态和分散态水泥生料基固硫剂为研究对象,采用热分析和红外联用的试验方法,对两种堆积态试样分别模拟预热预分解系统和回转窑系统内水泥生料基固硫剂的煅烧反应过程。采用TG、DTG、DSC、FTIR和红外定量等分析方法,对两种堆积态下水泥生料基固硫剂的反应特征、反应种类、气体产物及流量特征进行研究,以活性CaO生成和CaSO4的分解特征来表征评价体系对SO2的吸收和固硫效果,探讨该体系的固硫机理,为水泥生料固硫研究和技术开发提供参考。
1 实验部分
1.1 材料与仪器
水泥生料,取自某水泥厂生产线;纯石膏(CaSO4·2H2O),分析纯,二水石膏的含量>99.0%。
NETZSCH STA409PC 同步热分析仪与BRUKER VERTEX70 红外光谱仪联用系统。
1.2 实验原理
对水泥生料基固硫剂,最重要的固硫特性主要体现在活性CaO的生成和固硫后物相的高温稳定性两方面[10-11]。采用的热分析-红外联用实验方法,是将样品经过STA同步热分析加热,释放的气体产物通过在传输管线进入红外光谱气体池。由于不同结构、不同含量的分子在红外光谱中吸收峰位和吸光度特征不同,通过解析红外可以确定分子结构和进行定量,再结合热分析获取的质量和热流变化信息,就能对样品的反应过程和特征进行准确的表征。在本研究中,通过红外解析出的气体产物和流量,结合热分析的信息,可以对水泥生料基固硫剂在两种状态下的反应历程、活性CaO的生成反应特性和固硫相的热稳定性进行准确的表征和评价。
1.3 实验方法
实验采用水泥生料和石膏配制水泥生料基固硫剂,其化学成分见表1。
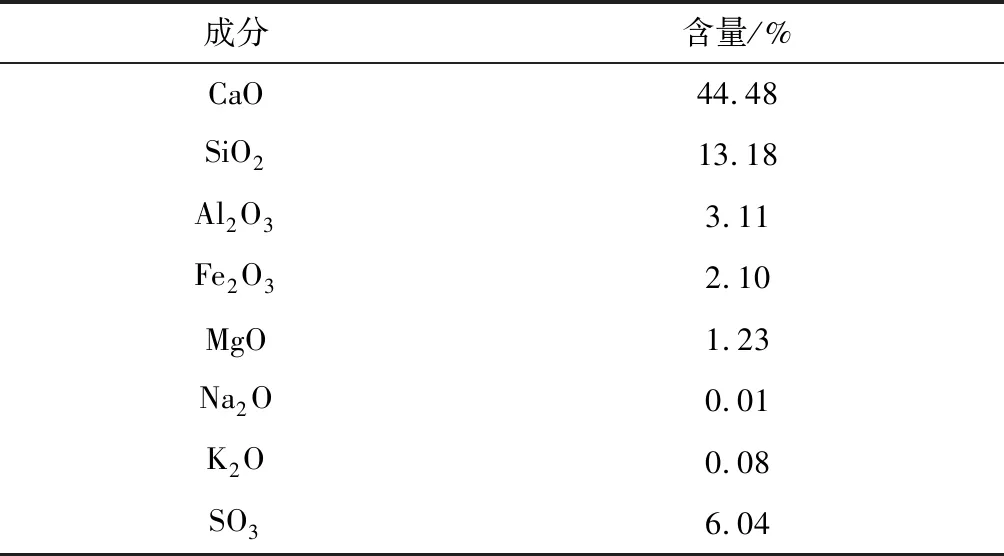
表1 水泥生料基固硫剂化学成分Table 1 Chemical composition of cement raw materials based sulfur fixation agent
对原料进行研磨,用100目标准筛进行筛分,筛余物继续研磨直至全部通过。将物料均匀混合后分成两部分:一部分经过20 MPa压制成Φ13 mm的块状试样,作为密实态实验的原料,编号为A;另一部分作为分散态实验的原料,编号为B。
对密实态A和分散态B两个样品分别进行热分析-红外联用实验。称取相同质量试样于氧化铝坩埚中,放入STA同步热分析仪检测器上进行STA-FTIR联用实验。升温速率为25 K/min,温度范围为40~1 400 ℃,反应气氛为空气,吹扫气体流量为100 mL/min,红外光谱采集波数范围4 000~700 cm-1,MCT检测器。
2 结果与讨论
2.1 分析结果
2.1.1 STA-IR热红联用结果 对密实态(A)和分散态(B)试样进行热分析-红外联用测试,由热分析得到的TG-DTG-DSC图谱见图1,由红外分析得到的气体产物红外光谱吸收三维图谱见图2。
由图1和图2可知,试样A和B反应过程类似,但在细节特征方面存在明显差异。水泥生料基固硫剂在加热过程中共有4个阶段的反应:第1反应阶段,样品A和B的温度范围分别为123.54~150.81 ℃和125.83~154.48 ℃,反应为吸热过程,失重量分别为 1.73%和1.74%。样品A在该阶段的失重速率最大点对应的温度为135.93 ℃,而样品B在该点的温度为140.39 ℃,滞后于A。DSC曲线上吸热峰的峰值温度,样品A为148.45 ℃,样品B为149.91 ℃。样品A和样品B在该阶段释放的气体产物的红外吸收光谱中(见图2)在3 600 cm-1和1 600 cm-1附近均存在宽吸收峰。
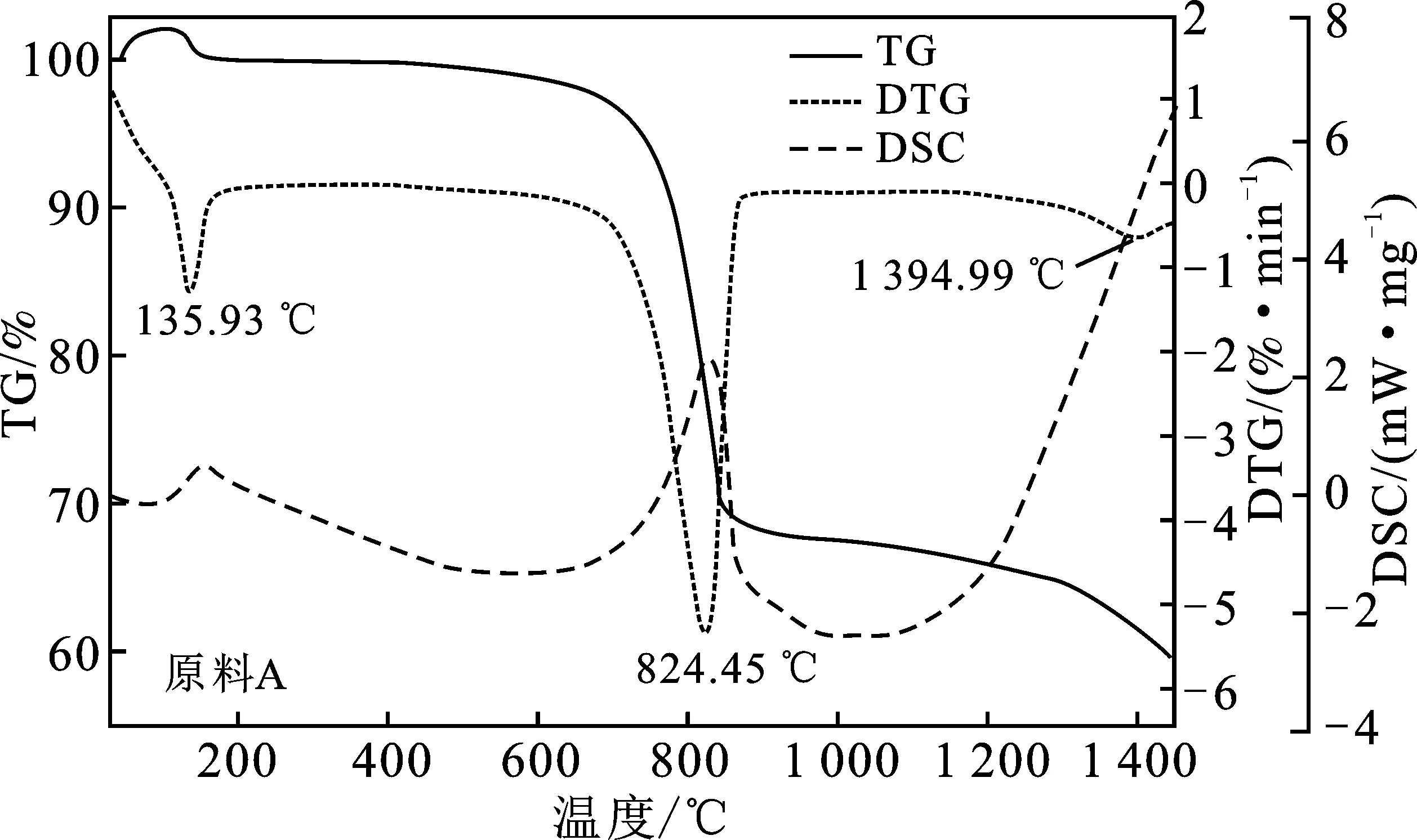
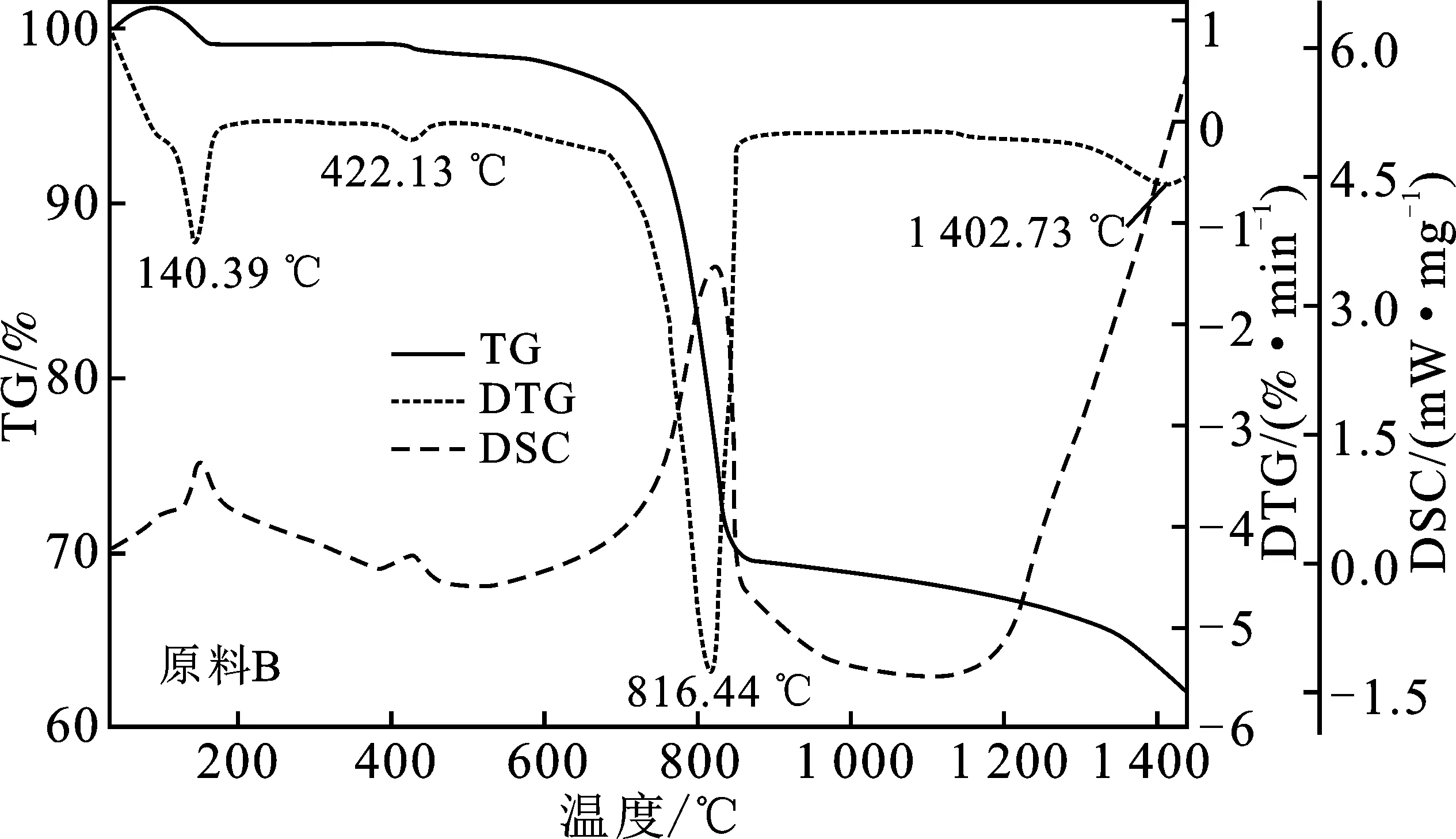
图1 密实态(A)和分散态(B)样品的TG-DTG-DSC图谱Fig.1 TG-DTG-DSC spectrum of dense state sample(A) and dispersed state sample(B)
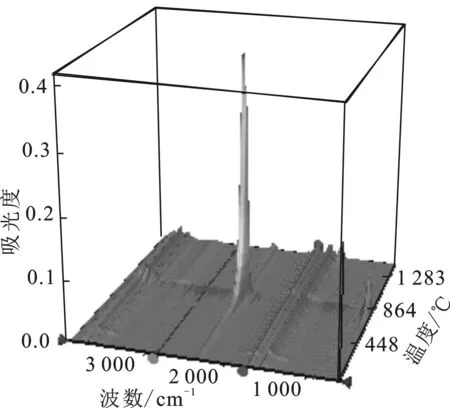
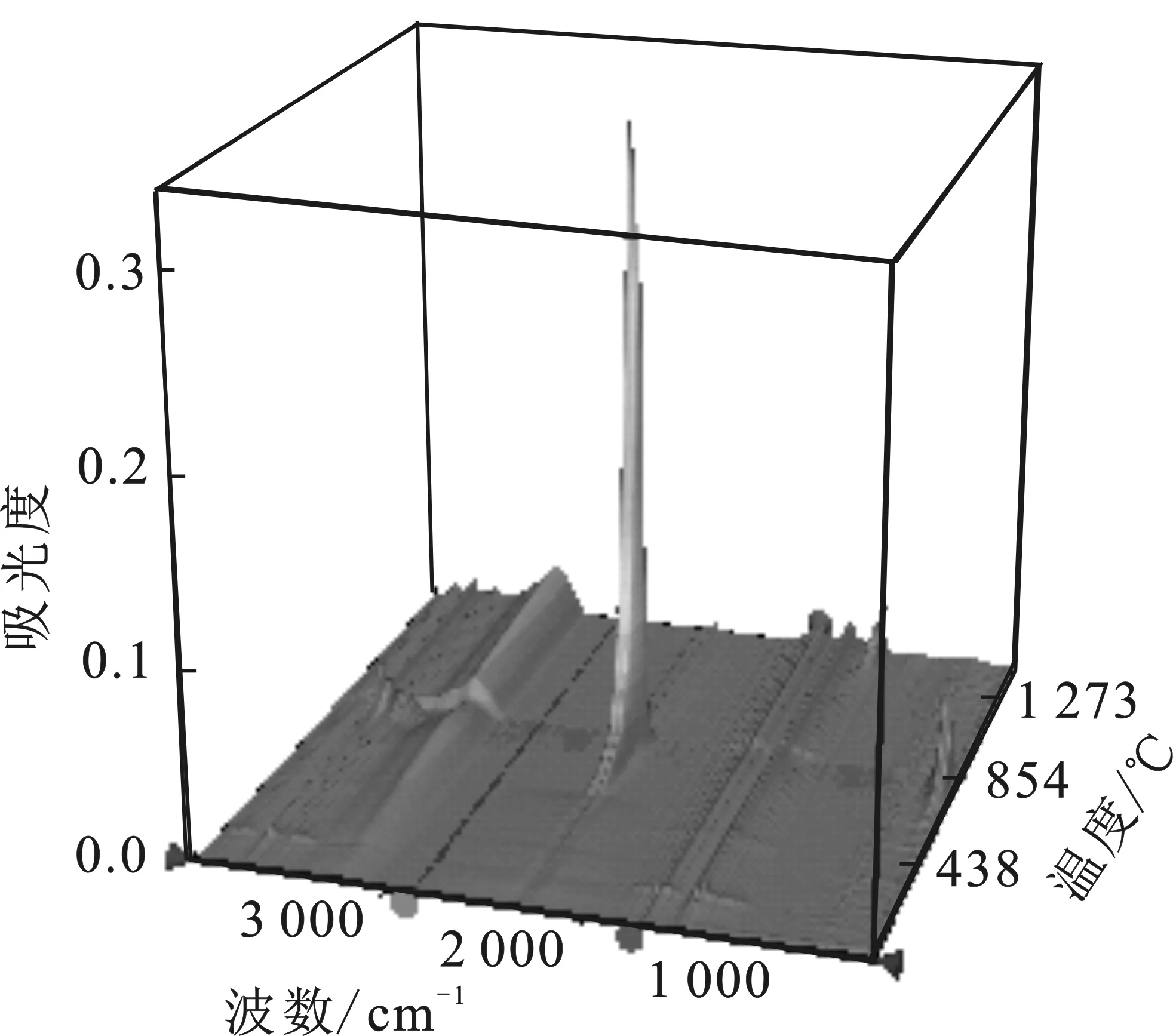
图2 密实态(A)和分散态(B)样品的气体产物3D红外吸收光谱图Fig.2 3D gas products infrared absorption spectra of dense state sample(A) and dispersed state sample(B)
第2反应阶段,分散态B在401.18~435.12 ℃出现失重峰,失重为0.45%,在422.13 ℃失重变化率达到最大,反应中伴随吸热现象,DSC曲线吸热峰的峰值为427.40 ℃,释放气体的3D红外光谱中在3 600,1 600 cm-1存在微弱宽吸收峰。但密实态A在这一阶段中反应特征并不明显,TG曲线只有轻微的失重,但DSC曲线无明显吸热峰,在3D红外吸收光谱中也未出现明显的吸收特征。
第3反应阶段,样品A和B均出现剧烈吸热反应。样品A在该阶段反应的温度范围为764.35~847.03 ℃,失重量A为28.34%,失重变化率达到最大的温度点为824.45 ℃,DSC曲线吸热峰的峰值为826.67 ℃。样品B在该阶段反应的温度范围为760.89~836.91 ℃,失重量A为25.73%,失重变化率达到最大的温度点为816.44 ℃,DSC曲线吸热峰的峰值为818.63 ℃。样品A和样品B在该阶段发生反应释放的气体产物红外吸收相近,在3D红外吸收图谱中2 300 cm-1出现超强的吸收峰。
第4反应阶段,样品A和样品B在1 200 ℃后均发生缓慢的失重,同时DSC曲线开始有吸热趋势。样品A在1 330.23 ℃之后失重反应明显加快,在1 394.99 ℃失重变化率达到最大。样品B对应的起始温度为1 302.22 ℃,在1 402.73 ℃失重速率达到最大。在该阶段,DSC热流曲线向吸热方向偏移,样品A和样品B从起始点到失重速率最大点的失重分别为2.31%,2.89%。样品A和样品B释放气体在3D红外吸收光谱中的3 600 cm-1和1 500~1 100 cm-1均出现吸收峰。
2.1.2 气体产物红外光谱解析及流量分析 从密实态(A)和分散态(B)试样释放气体产物的3D红外吸收光谱(见图2)中,解出4个反应阶段红外吸收最大时的红外吸收光谱进行产物类型解析,4个反应阶段分别编号为:第1反应阶段(a),第2反应阶段(b),第3反应阶段(c),第4反应阶段(d),解出4步反应阶段红外光谱见图3。

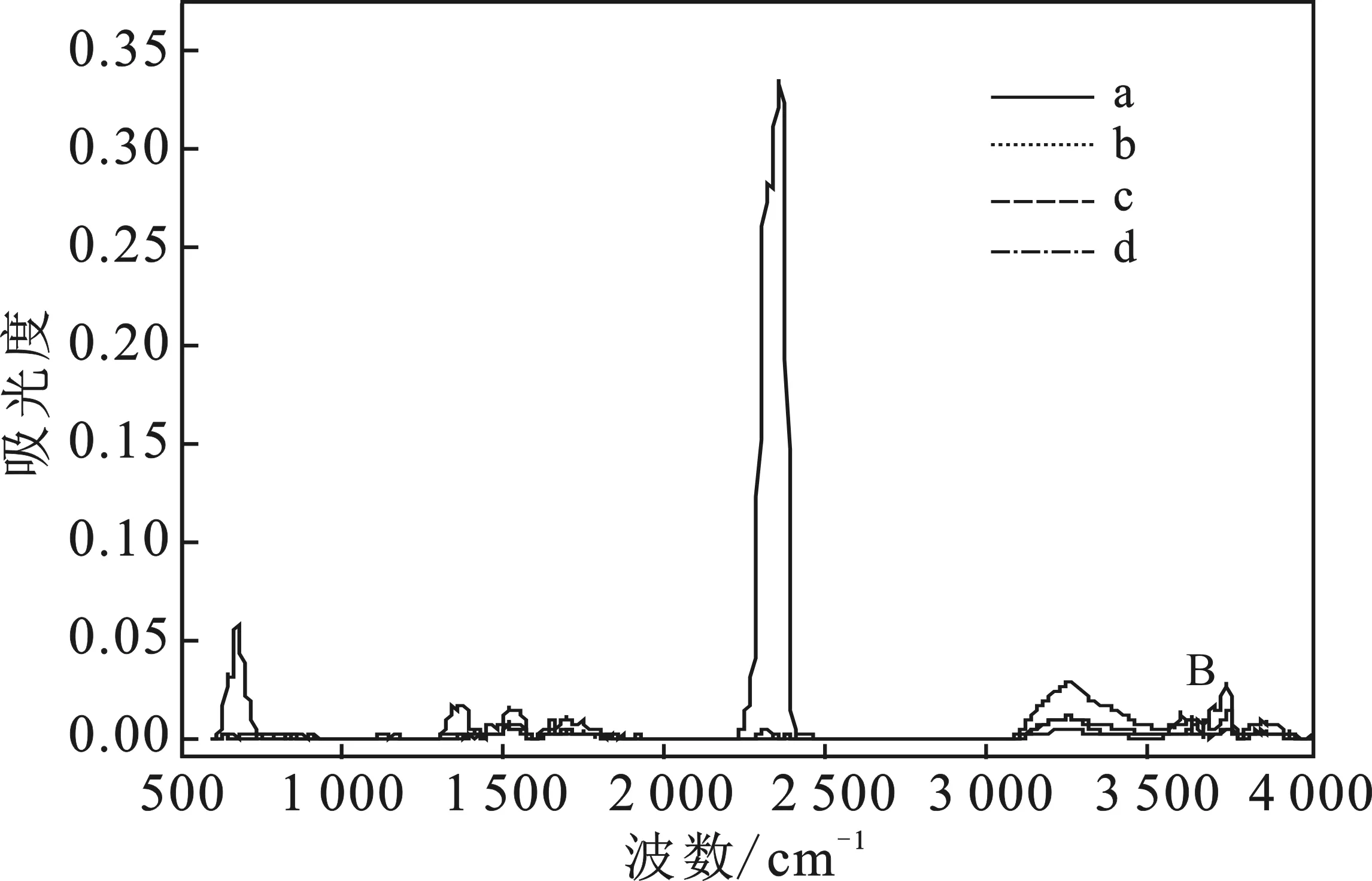
图3 密实态(A)和分散态(B)样品在四反应阶段(a,b,c,d)反应释放气体的红外光谱图Fig.3 FTIR spectra of dense state sample(A) and dispersed state sample(B) gases released from reaction process at four reaction stages(a,b,c,d)
由图3可知,在第1反应阶段,样品A和样品B释放的气体产物红外吸收特征相同,即3 900~3 500 cm-1和1 800~1 400 cm-1吸收峰,表明气态产物主要是水蒸气;结合试样的化学成分,可以确定该阶段的反应是石膏成分的脱水。在第2反应阶段,样品A的气体产物没有明显的红外吸收特征,样品B的释放气体产物在3 900~3 500 cm-1以及1 800~1 400 cm-1的吸收峰,表明样品B在该阶段的气体产物是水蒸气[12]。由图2可知,当样品B在第2反应阶段反应速率最大时对应的温度是422.13 ℃。该温度条件与水泥生料黏土质组分中的高岭石矿物的脱水温度条件相吻合[13],因此样品B在第2阶段发生的反应是高岭石的脱水。在第3反应阶段,样品A和样品B释放气体在2 400~2 230 cm-1出现超强吸收峰,是典型的CO2气体的伸缩振动,表明样品A和样品B在第3反应阶段的气态产物是CO2[12-14]。根据试样成分可知,该阶段的反应主要是石灰石分解形成活性CaO。在第4反应阶段,样品A和样品B在1 410~1 280 cm-1及1 200~1 100 cm-1出现吸收峰,这是典型的SO2气体的伸缩振动,证明生成大量SO2[12]。由此可知,该阶段发生的反应主要是CaSO4的分解。
2.1.3 气体定量流量 根据4个反应阶段的气体产物类型解析结果,对3D红外吸收光谱(见图2)数据进行建模计算,得到H2O、CO2、SO2三种气体产物在反应过程中的释放流量曲线,见图4。
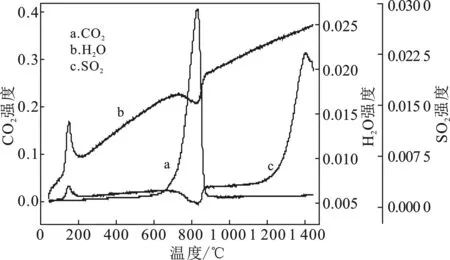
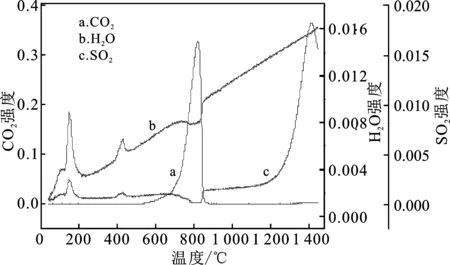
图4 密实态(A)和分散态(B)样品的气体产物释放流量曲线图Fig.4 Flow curves gas products from reaction process of dense state sample(A) and dispersed state sample(B)
由图4可知,H2O(水蒸气)的释放主要有两个阶段,在200 ℃之前是由于石膏的脱水产生的,而在401.18~435.12 ℃之间主要是由于黏土中的高岭石脱水产生的;对比图4(A)和图4(B)水蒸气的释放特征可知,在分散态B中可以看到高岭石的脱水特征,而在密实态A中则看不到。CO2气体的释放出现在第3反应阶段,是碳酸钙大量分解形成活性CaO的过程;密实态(A)的温度范围为 764.35~847.03 ℃,分散态(B)的温度范围为760.89~836.91 ℃,分散态下CaO的形成温度较低,温度区间更小。SO2气体的释放主要出现在第4反应阶段,是由CaSO4的分解产生的,可以从其释放特征表述固硫相矿物的热稳定性;密实态(A)在1 186.5 ℃时CaSO4逐渐出现分解,分解速率最大点的温度为1 394.99 ℃,分散态(B)在1 195.8 ℃时CaSO4逐渐出现分解,分解速率最大点的温度为1 402.73 ℃,可知分散态下,CaSO4的分解温度高,热稳定性更好。
综上所述,水泥生料基固硫剂的反应过程为:首先发生石膏脱水反应;随后黏土中高岭石相脱除羟基(—OH)转变为水蒸气;然后大约760 ℃石灰石开始分解,大量产生活性CaO,并释放CO2,活性CaO开始吸附SO2,并逐步转化为CaSO4稳定固硫相;最后大约1 186.5 ℃之后,CaSO4开始分解释放SO3,进一步高温分解为SO2,分解反应在大约1 300 ℃之后明显加速,此步反应会降低固硫效应。
根据上述分析并结合文献[8,14],水泥生料基固硫剂的反应方程式如下:


Al2O3+2SiO2+2H2O↑


2.2 结果与讨论
在工业生产中,粉状和块状的固硫剂都有广泛的应用。将水泥生料基固硫剂在密实态和分散态的反应特性进行对比分析,可以为水泥生产和其他钙基固硫剂的应用提供参考。将密实态(A)和分散态(B)的数据进行分类比较,得到TG-DTG对比图见图5,其中(a)、(c)代表密实态(A)的TG、DTG曲线,(b)、(d)分散态(B) 的TG、DTG曲线。密实态(A)和分散态(B)样品的DSC对比见图6。
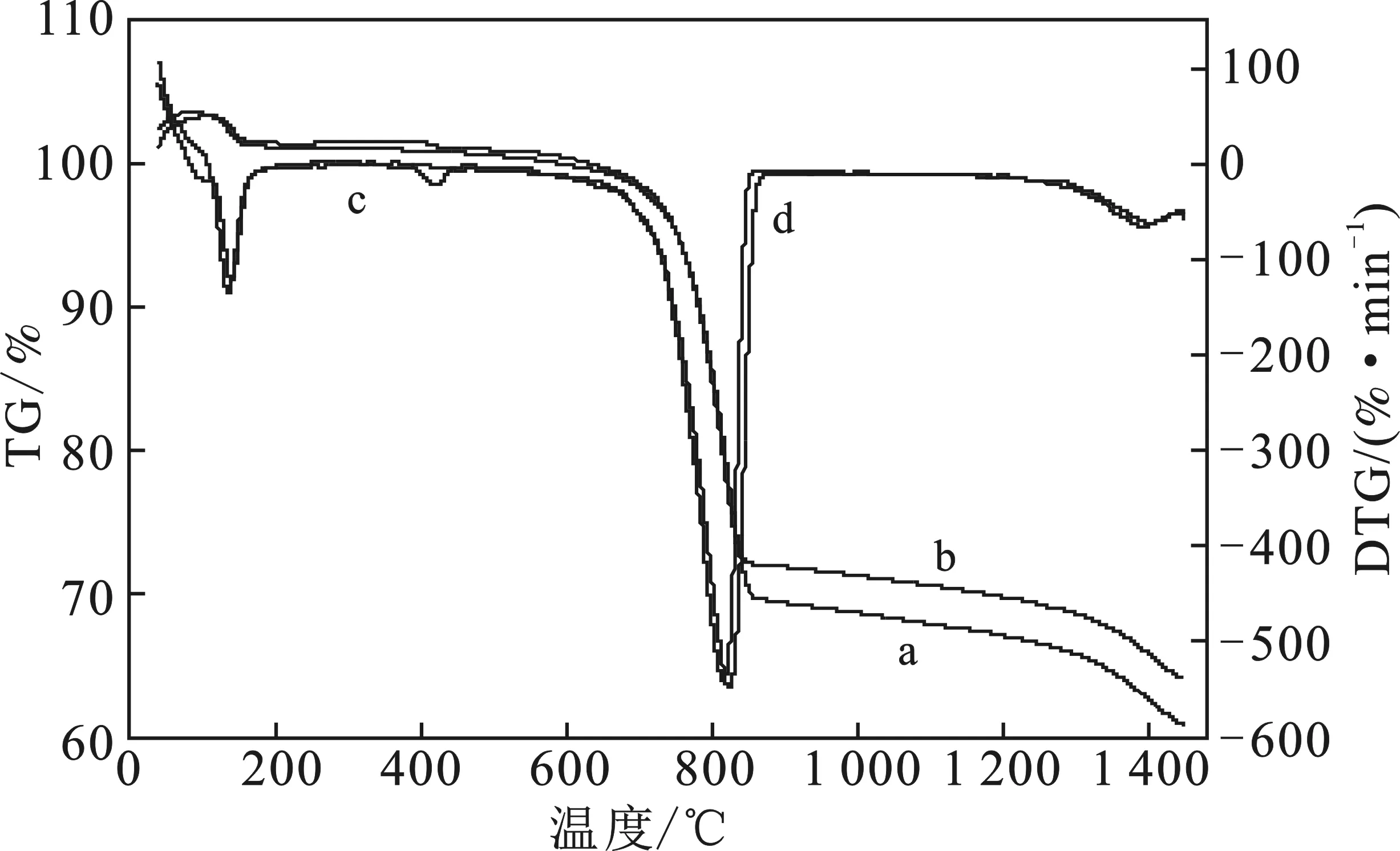
图5 密实态(A)和分散态(B)样品的TG-DTG对比图Fig.5 TG-DTG curves of dense state sample(A) and dispersed state sample(B)

图6 密实态(A)和分散态(B)样品的DSC对比图Fig.6 DSC comparison of dense state sample(A) and dispersed state sample(B)
密实态(A)和分散态(B)样品在4个反应阶段(第1反应阶段a,第2反应阶段b,第3反应阶段c,第4反应阶段d)释放气体产物的红外光谱对比见图7。
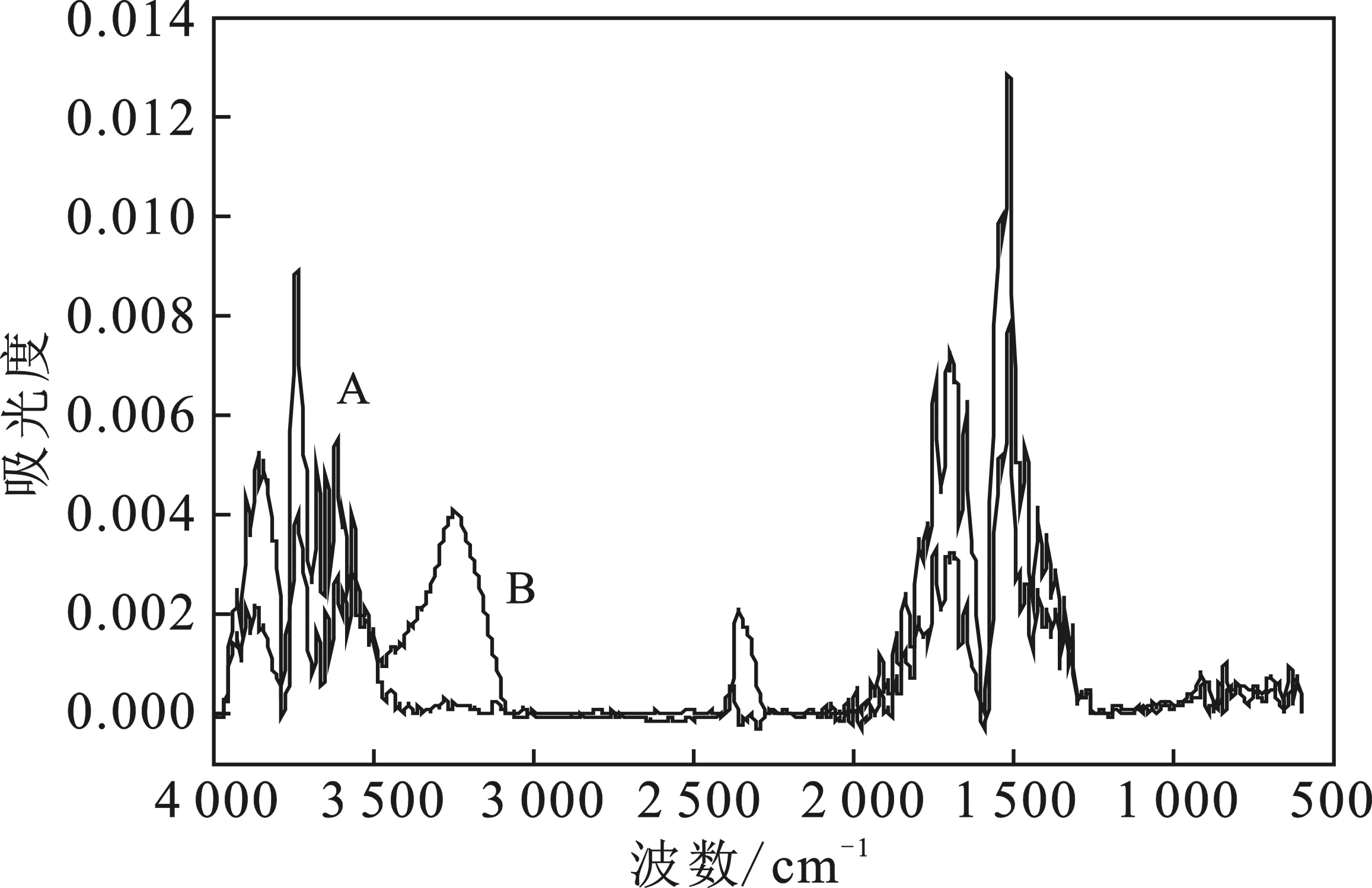
a.第1反应阶段
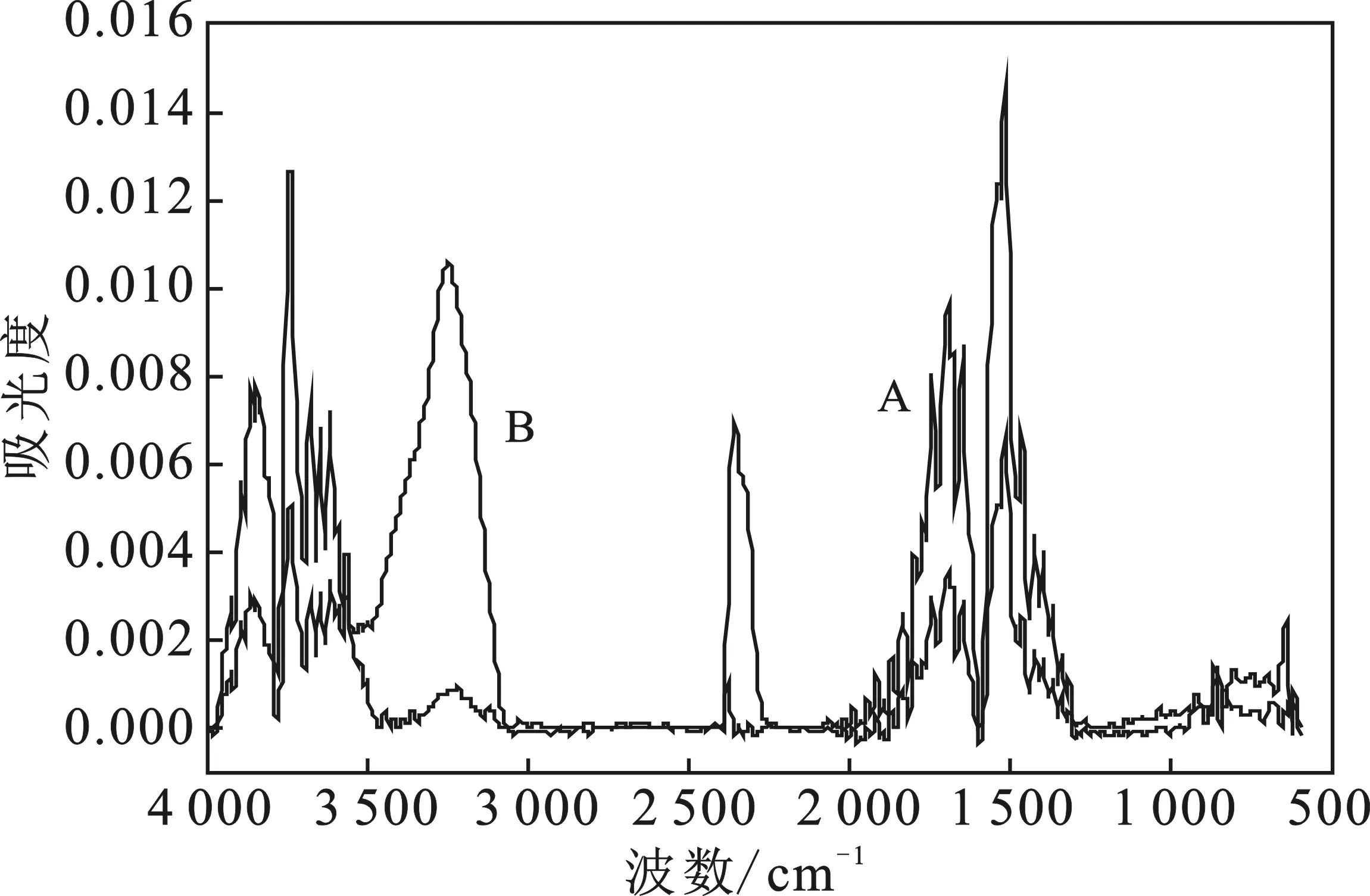
b.第2反应阶段
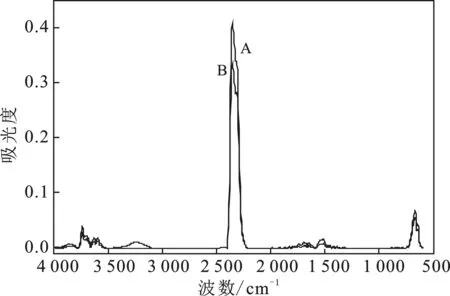
c.第3反应阶段

d.第4反应阶段图7 密实态(A)和分散态(B)样品在4阶段反应(a,b,c,d)的气体产物红外光谱的对比图Fig.7 Comparison of IR spectra of dense state sample(A) and dispersed state sample(B) gases products in four reaction states(a,b,c,d)
密实态(A)和分散态(B)样品释放的CO2、H2O、SO2气体流量对比见图8。



图8 密实态(A)和分散态(B)样品释放的CO2、H2O、SO2气体流量对比图Fig.8 CO2,H2O and SO2 flow comparison of dense state sample(A) and dispersed state sample(B)
由图5~图8可知,密实态A和分散态B在反应历程方面大致相似,但细节方面存在一定的差异。在第1反应阶段主要是石膏中结晶水的脱除,两个样品的失重相近,但样品B更容易发生脱水,这是因为分散态的传热条件更好。在第2反应阶段,主要是黏土中高岭石矿物的脱水,该过程只有在分散态B中出现,这是因为分散态下,有利于热量传递和气态产物的扩散,而在密实态下少量的水蒸气扩散阻力较大[15],不能扩散到料块的表面,所以分散态B检测不到明显的反应特征。在第3反应阶段,石灰石大量分解形成活性CaO,这是固硫剂关键的反应步骤,TG-DSC比较可见,密实态A相较于分散态B的反应温度高,温度区间大;红外光谱分析比较可见,密实态A相较于分散态B的CO2峰较大;流量图比较可见,密实态A相较于分散态B的CO2流量较大,而样品B的CO2流量较小。说明分散态B更容易发生反应生成活性CaO,有利于SO2的吸收。在第4反应阶段,固硫稳定相CaSO4开始分解,但密实态的样品A的分解温度比分散态的样品B低,半峰宽大。这说明分散态B较密实态A而言CaSO4分解更困难,分解量也小,固硫的效果较好。综上分析,在固硫效率和固硫效果方面,分散态比密实态更加适合。
3 结论
水泥生料基固硫剂内的反应共分为4个阶段:第1阶段的反应是石膏的脱水,分散态下脱水反应容易发生;第2阶段的反应是粘土中矿物质结晶水的脱除,气态产物为水蒸气,只能在分散态下观察到反应现象;第3阶段的反应是活性CaO的形成,气态产物是CO2,分散态下反应温度低、反应区间温度跨度小,反应效率高,生成的CaO活性更好;第4阶段的反应是CaSO4的分解,气体产物是SO2,同等条件下,分散态的分解温度高、分解量小,固硫相的热稳定性更好。就水泥生料基固硫剂的固硫反应特征和效果而言,分散态的比密实态更适合用于含硫尾气的处理。
