利伐沙班原料药中重金属镍残留量的检测方法与评价
2020-10-31
江苏省淮安市食品药品检验所,淮安223001
利伐沙班 (Rivaroxaban) 化学名为5-氯-N-(((5S)-2-氧代-3-(4-(3-氧代-4-吗啉基) 苯基)-1,3-恶唑烷-5-基)甲基)-2-噻吩甲酰胺[1],分子式为C19H18ClN3O5S,是一种口服的抗凝血药物,它通过高选择性直接抑制Xa 因子达到抑制凝血酶产生和血栓形成的作用,与传统抗凝血药物相比,具有服用方便、起效迅速、安全性高等特点[2]。
在利伐沙班合成中,用到雷尼镍作为催化剂[3],镍及其盐类的毒性较低,但由于它本身具有生物化学活性,故能激活或抑制一系列的酶(精氨酸酶、羧化酶、酸性磷酸酶和脱羧酶)而发挥其毒性。长期接触(如冶炼镍、镀镍等)、吸入或注射镍化物,均有致癌作用。欧洲药物评审组织(EMEA)将金属催化剂按风险级别分类管理,镍作为第1 类金属,规定注射用原料药中不得超过1 μg·g-1[4]。
药物中镍含量的测定方法主要有火焰原子吸收法、石墨炉原子吸收法、电感耦合等离子体质谱法等。本研究采用微波消解法进行样品前处理,建立了石墨炉原子吸收法、电感耦合等离子体质谱法两种方法测定利伐沙班中残留的镍,并作比较分析,为药物中痕量镍的测定提供参考。
1 石墨炉原子吸收分光光度法测定利伐沙班原料药中镍残留
1.1 仪器与药品、试剂
1.1.1 仪器 安东帕微波消解仪(奥地利安东帕公司);Aglient 240AAS 原子吸收分光光度计、Aglient PSD120 可编程进样器、镍空心阴极灯(均美国安捷伦公司);BP211 电子分析天平(德国赛多利斯公司)。
1.1.2 药品与试剂 利伐沙班(某药厂提供)批号为20151001、20151002、20151003、20151004、150401、150402;镍标准溶液(100 μg·mL-1,中国计量研究院,批号:16041);硝酸;超纯水。
1.2 方法与结果
1.2.1 仪器工作条件 检测波长:232.0 nm,狭缝:0.2 nm;灯电流:4.0 mA;背景校正:塞曼;石墨炉原子吸收光谱仪进样体积为20.0 μL,重复测定次数:3次。石墨炉升温参数见表1。
1.2.2 对照品溶液制备 取镍标准溶液 [C (Ni)=100 μg·mL-1]1 mL 置50 mL 量瓶中,加2%稀硝酸制成含镍2 μg·mL-1的溶液,作为对照品储备液;取储备液5 mL 置100 mL 量瓶中,加2%稀硝酸溶液制成含镍100 μg·L-1的溶液,作为对照品溶液。
1.2.3 供试品溶液的制备 取样品约0.2 g,精密称定,置消解罐中,加硝酸10 mL,放置过夜,按表2 升温程序进行微波消解,待消解结束后,取出消解罐并加热,挥去大部分酸液(残液约1 mL),将消解罐中的残液转移至25 mL 量瓶中,用超纯水稀释至刻度,得供试品溶液。同法制备空白溶液。
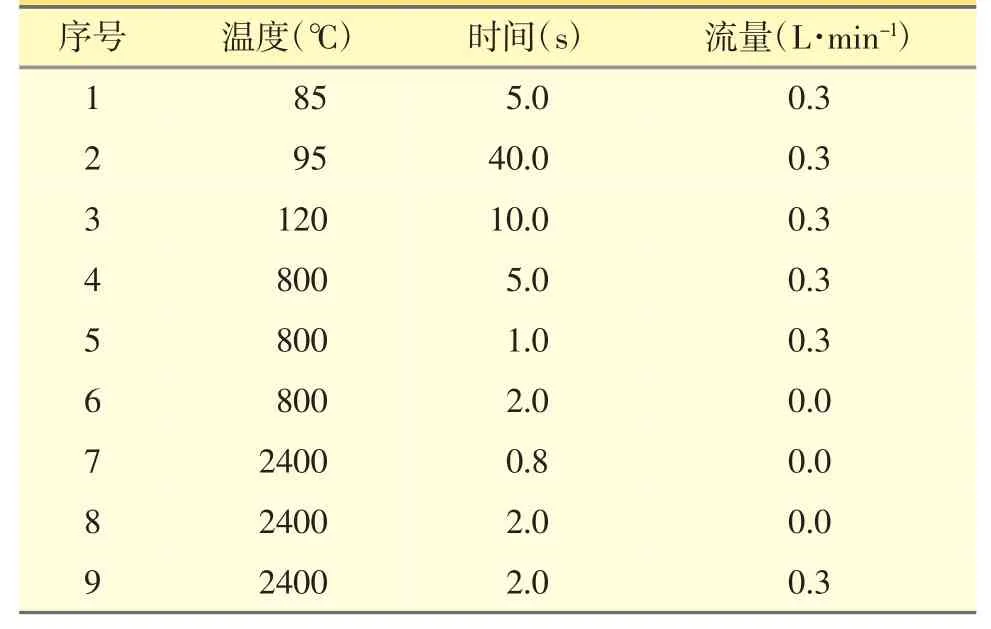
表1 石墨炉升温程序
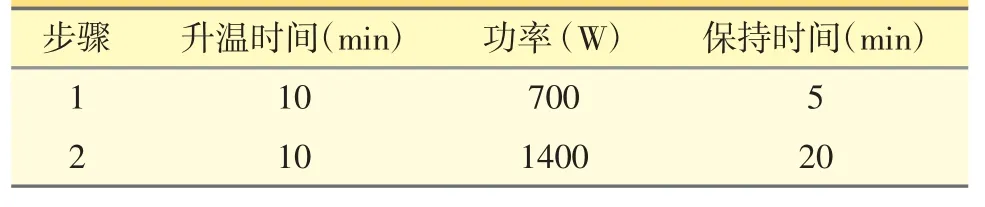
表2 微波消解条件
1.2.4 线性与范围 镍贮备液的配制以“1.2.2”项下对照品溶液为母液,采用自动配标方式,按“1.2.1”项下的条件以0、10、30、50、80、100 μg·L-1标准溶液进样,以浓度对吸光度绘制标准曲线,得回归方程:Y=5.81×10-3X+2.707×10-2、r=0.999 6,结果表明,利伐沙班中镍元素含量的线性范围:0~100 μg·L-1。
1.2.5 回收率 精密称取每份约0.2 g 利伐沙班(批号为20151001) 共9 份,分别加入含镍量为0.8、1.0、1.2 μg 的硝酸10 mL,每个浓度3 份,按“1.2.3”项下样品处理方法进行前处理,并按“1.2.1”项下的条件进行测定,计算平均回收率为112.0%,RSD 为4.7%。
1.2.6 精密度试验 取“1.2.2”项下对照品储备液1 mL 置50 mL 量瓶中,加2%稀硝酸溶液制成含镍40 μg·L-1的溶液,按“1.2.1”项下的条件,平行测定6次,平均值为40.66 μg·L-1,RSD 为1.6%(n=6)。
1.2.7 检测限与定量限 分别按公式LOD=3.3σ/S、LOQ=10σ/S,确立检测限与定量限。
其中σ 为对空白溶液连续进行11 次测定的响应值的标准偏差,S 为标准曲线的斜率(参照《中国药典》2015 年版四部9101)。计算最低检测浓度为1.9 μg·L-1,分析方法的检测限为0.2 μg·g-1;最低定量浓度为5.9 μg·L-1,分析方法的定量限为0.7 μg·g-1。
1.2.8 样品测定 取利伐沙班6 个批号样品,按“1.2.3”项下方法进行样品前处理,并按“1.2.1”项下的条件进行测定,结果见表3。
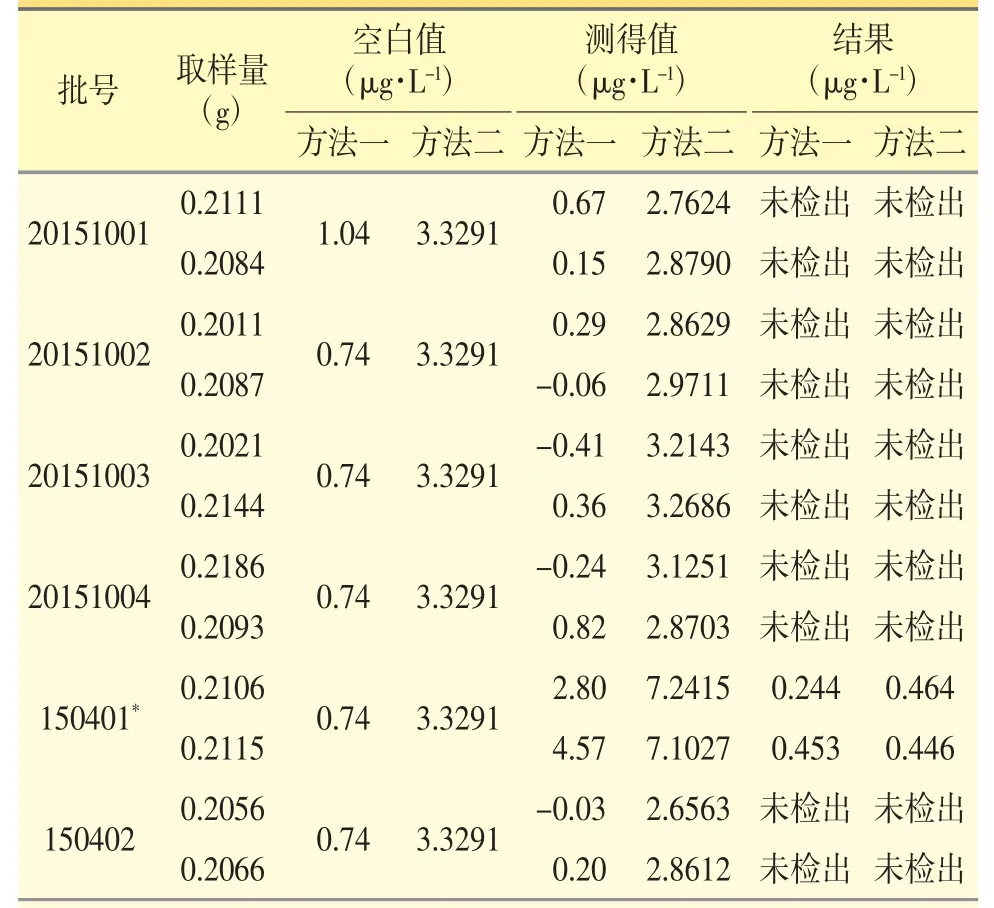
表3 样品测定结果汇总表
2 电感耦合等离子体质谱法测定利伐沙班原料药中镍残留
2.1 仪器与药品、试剂
2.1.1 仪器 安东帕微波消解仪(Multiwave3000奥地利安东帕公司);NexION 300 电感耦合等离子体质谱仪;BP211 电子分析天平(德国赛多利斯公司)。
2.1.2 药品与试剂 利伐沙班由同一厂家提供,批号同“1.1.2”;镍标准溶液(100μg·mL-1,中国计量研究院,批号:16041);锗标准溶液(10μg·mL-1,PE 公司,批号:CL12-143YPY1);调谐液(PE 公司);硝酸;超纯水。
2.2 方法与结果
2.2.1 微波消解程序 消解条件同表2。
2.2.2 ICP-MS 测试条件 发射功率:1.1kW;采样锥:镍锥;雾化器:旋流雾室雾化器;雾化气流速:0.9 L·min-1;等离子体气(氩气):15.0 L·min-1;辅助气(氩气):1.2 L·min-1;碰撞气(氩气):3.0 L·min-1;扫描方式:跳峰;测量点/峰:3 点。扫描质量数:待测元素镍60,内标元素Ge 为74。进样方式:手动进样,内标元素Ge 通过T 型三通管在线引入等离子体。
2.2.3 对照品溶液的制备 取镍标准溶液[C(Ni)=100 μg·mL-1]适量,加2%稀硝酸溶液制成含镍1 μg·mL-1的溶液,作为对照品储备液;取对照品储备液适量,用2%稀硝酸溶液稀释制成0.5、1、5、10、20 ng·mL-1的系列浓度对照品溶液。
2.2.4 供试品溶液的制备 同“1.2.3”。
2.2.5 内标溶液的制备 精密量取锗标准溶液,用2%稀硝酸溶液稀释制成50 ng·mL-1的内标溶液。
2.3 线性与范围
取“2.2.3”项下系列浓度对照品溶液,按“2.2.2”项下的条件进样测定,以镍元素每秒计数(CPS)与内标锗元素的每秒计数(CPS)的比值为纵坐标,每个对照品溶液对应的浓度为横坐标,进行线性回归,得回归方程:Y=0.289X-7.1×10-2(r=0.999 7)。
结果表明,利伐沙班镍元素含量的线性范围:0.5~20 μg·L-1。
2.4 回收率试验
精密称取利伐沙班(批号20151001)约0.2 g,计9 份,分别加入含镍量为0.125、0.25、0.375 μg 的硝酸溶液10 mL,每个浓度3 份,按“1.2.3”项下方法进行样品前处理,并按“2.2.2”项下的条件测定,计算平均回收率为97.90%、RSD 为1.8%。
2.5 精密度试验
取“2.2.3” 项下10 μg·L-1的镍对照品溶液,按“2.2.2”项下的条件平行测定6 次,平均值为10.10μg·L-1、RSD=0.5%(n=6)。
2.6 检测限设定
仪器自动最低检测浓度为0.056 μg·L-1,分析方法的检测限为0.007 μg·g-1。
2.7 样品测定
取利伐沙班6 批,按“1.2.3”项下方法进行样品前处理,并按“2.2.2”项下的方法进行测定,结果见表3。
3 讨论
本实验建立了石墨炉原子吸收法、电感耦合等离子体质谱法两种方法,分别测定利伐沙班中残留的镍。在方法建立初期研究取样量时,参考了一般药品取样量,结果发现取样0.5 g 时,消解完溶液呈深黄色,略不透明,因此判断需要调整取样量或是消解程序,分别试验了取样0.1、0.2、0.3、0.4 g 以及调整微波消解的功率和保持时间。功率过小则需延长保持时间,功率加大虽然可以缩短保持时间,但消解样品时容易压力过高;减少取样量虽然可以消解完全,但是过少则没有代表性,经试验取样0.1~0.3 g 时,用“2.2.1”的消解程序完全消解且溶液澄清透明。
根据6 批样品的检验结果表明,两种方法对结果的测量无明显差异;但电感耦合等离子体质谱法由于具有分析速度快、检测限更低、灵敏度高以及可多种元素同时测定等优点,在重金属痕量分析检测方面更具优势。
