3-氨基-4-亚硝基呋咱的热分解动力学
2020-10-28张明燕陈利平吴文倩王顺尧陈网桦
张明燕,陈利平,吴文倩,王顺尧,陈网桦
(1.南京理工大学 化工学院,江苏 南京210094; 2.金陵科技学院,江苏 南京211169)
引 言
高能量密度材料(HEDM)是含能材料领域研究的热点[1]。呋咱环本身就是一个爆炸性基团,单呋咱化合物可作为含能材料,最简单的取代呋咱也会因呋咱环的存在而使分子能量增加[2]。因呋咱类化合物具有氮含量高、能量密度高[3],分解产物具有高的生成焓和氧平衡等优点,不仅可作为含能材料助剂和火箭推进剂,亦可作为气体发生剂及烟火药[4],近年来备受关注。呋咱并[3,4-e]-4,6-二氧化-1,2,3,4-四嗪(FTDO)是目前应用前景最佳的高能量密度材料[5]。3-氨基-4-亚硝基-呋咱(ANSF)是合成FTDO的中间体之一,也是合成3,4-二氰基呋咱的重要原料。3,4-二氰基呋咱不仅可作为火箭推进剂,也是重要的有机合成中间体[6]。
近年来,呋咱类含能材料的热分解特征成为国内外学者的研究重点[7]。Kohsari等[8]研究了合成呋咱的原料二氨基乙二肟(DAG)和3,4-二氨基呋咱(DAF)在不同升温速率下的热稳定性,用Ozawa法计算出DAF的分解反应活化能为156.5kJ/mol,DAG的分解反应活化能为108.7kJ/mol;李战雄[9]、张君启等[10]研究了呋咱类含能化合物3,3′-二氨基-4,4′-偶氮呋咱(DAAF)和3,3′-二氨基-4,4′-偶氮氧化呋咱(DAOAF)的爆炸性能及稳定性;WILLIAMS等[11]研究了呋咱衍生物的快速热分解特性,研究结果表明多数呋咱类衍生物的分解反应产生CO2、CO、NO、H2O、HCN、N2O等产物,分解过程十分复杂;Zhao Feng-qi等[12]用Kissinger法研究了3,4-二硝基呋咱基氧化呋咱(DNTF)的热分解反应动力学参数;Wei-Peng Lai等[13]研究了FTDO的热稳定性,结果表明FTDO稳定性极差,需在特定条件下使用。但至今未见ANSF的热稳定性及其分解机理研究。ANSF结构中含有亚硝基,与其他取代基相比该基团更不稳定。因此,对ANSF的热稳定性和分解反应动力学研究十分必要。
本实验利用差示扫描量热法(DSC)研究了ANSF的热稳定性,并利用等转化率法(即无模型法)和基于模型的动力学方法对其分解反应动力学参数进行了计算,为进一步研究ANSF的热危险性提供参考。
1 实 验
1.1 样 品
ANSF,熔点76~78℃,土黄色片状固体,实验室自制,纯度97%。合成工艺参见文献[14-15]。
1.2 测试条件
采用瑞士梅特勒托利多公司生产的DSC1型差示扫描量热仪测试热分解特性。实验在30μL的高压密闭不锈钢坩埚中进行,测试过程中以50mL/min速率进行N2吹扫,保持测试环境稳定可重复。测试样品ANSF质量(m)为(0.5±0.1)mg,升温速率(β)为2、4、6、10K/min。
2 结果与讨论
2.1 ANSF的动态热分解特性
在30~450℃,以不同升温速率对ANSF进行DSC动态测试。测试结果显示,200℃以后已无放热峰出现。不同升温速率下ANSF的DSC动态曲线及热分解特征参数见图1及表1。
由图1及表1可知,ANSF在其熔点附近出现相变吸热峰;在100℃以后出现分解放热峰。不同升温速率下,ANSF分解反应的平均比放热量(ΔHd)为2945J/g。升温速率越快,ANSF分解反应的最大放热速率越高。同时,ANSF起始分解温度(Tonset)、放热峰对应的峰值温度(TP)均增大。
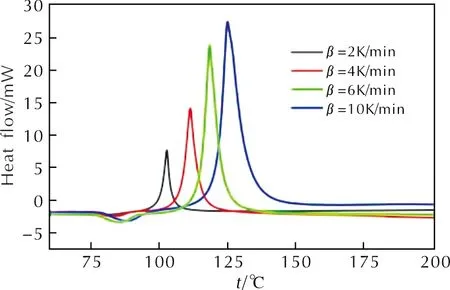
图1 ANSF动态DSC测试曲线Fig.1 Dynamic DSC curves of ANSF

表1 ANSF的热分解参数
由此可知,ANSF热稳定性较差,放热速率快,放热量大。出现此现象的原因是由于其结构中不仅含有“潜硝基”—N—O—N—键[16],同时含有亚硝基,两者均是含能官能团,且亚硝基更不稳定。
2.2 ANSF自催化特征判定
由DSC动态测试结果可知,ANSF热分解放热峰尖锐且狭窄,表现出自催化的分解特征,有必要进一步研究其是否具有自催化特性。对该物质进行等温DSC实验。若等温实验中出现钟形峰,则该物质分解反应具有自催化特性[17]。
在动态DSC实验中,该物质先熔融后分解,因此为确定其液态和固态分解是否都存在自催化特性,分别选取高于其熔点的温度和熔点以下的温度进行等温测试。0.64mg ANSF在89℃下的等温DSC测试结果见图2(a),1.36mg ANSF在65℃下的等温DSC测试结果见图2(b)。
由图2(a)可知,89℃等温条件下,该物质立即开始分解,10min后分解反应速率达最大值,30min后放热结束,其比放热量约2700J/g。整个放热过程放热速率先增加后减小,呈现具有自催化特性的钟形峰。
由图2(b)可知,约75min后ANSF开始分解,约150min时放热速率达到最大值1.9mW,其比放热量约2300J/g。同液态下分解放热曲线类似,放热速率先增加后减小,曲线为钟形峰,进一步表明该物质具有热不稳定性,且固相分解亦具有自催化特性。65℃等温实验中分解反应比放热量小于动态测试结果,是由于此时物质为固相分解且温度较低,故分解反应并不完全,或分解完全需要更长的时间。

图2 不同质量ANSF在不同温度下的等温DSC曲线Fig.2 Isothermal DSC curve of ANSF with different mass at different temperatures
2.3 ANSF分解反应动力学参数
2.3.1 等转化率法
利用不同升温速率下ANSF的动态DSC曲线进行其热分解反应的动力学计算。首先,应用等转化率微分法(Friedman法)进行分解反应动力学参数的初步计算,Friedman法基于以下方程[18]:
(1)
式中:α为反应进程,即反应转化率;Ea为活化能;A为指前因子;f(α)为机理函数。对不同升温速率下的数据进行非线性拟合,得到分解反应进程及反应速率与温度关系曲线,拟合曲线与实验曲线比较见图3。
由图3可知,拟合曲线与测试曲线一致性较好;利用等转化率法计算得到E(α)、ln[Af(α)]与α的关系见图4。由图4可知,在α为0.1~0.9范围内,活化能随α的变化明显,在48~101kJ/mol之间,ln[Af(α)]在6~25之间变化,这说明ANSF分解反应过程复杂,不能用单步反应进行描述[19]。
根据等温DSC测试结果,该物质分解反应具有自催化特征。在反应分解起始阶段即α较小时,由于体系中没有催化性质的分解产物存在,故分解反应活化能较大;随着反应进行,体系中的分解产物对反应的催化作用使活化能减小[20],与图5中的E(α)—α曲线变化趋势一致。
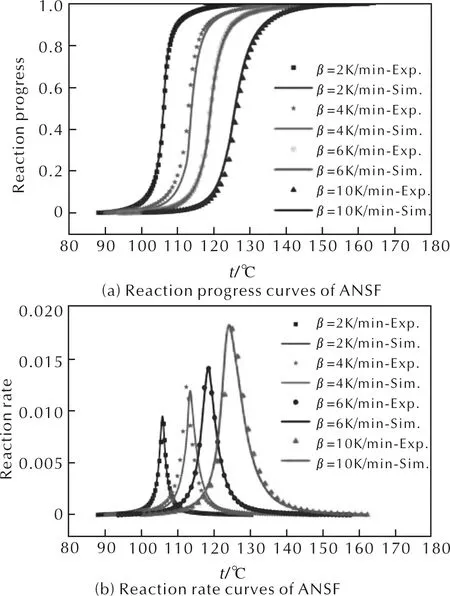
图3 ANSF分解反应进程及反应速率拟合曲线与 实验曲线的比较Fig.3 Comparison between simulated curves and experimental curves of reaction progress and reaction rate for ANSF

图4 E(α)、ln[Af(α)]及相关系数与α的关系Fig.4 The relationship of E(α),ln[Af(α)] and correlation coefficient with α
2.3.2 模型拟合法
利用等转化率法得到ANSF分解反应E(α)随α变化明显,说明该反应过程是复杂反应,ANSF的热分解具有自催化特征,故对该物质分解反应建立自催化反应模型。选取简化后带有引发阶段的Benito-Perez模型(B.P.模型)对ANSF的分解过程进行描述。其反应过程可表示为[21]:
引发反应阶段:
(2)
自催化反应阶段:
(3)
则两步反应总的速率方程为:
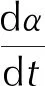
(4)
令
EZ=E1-E2
若
E2=EA2=A
代入式(4)即得到基于简化B.P.模型的反应速率表达式:
ri=Ae-E/RT(1-α)n1(z0e-EZ/RT+αn2)
(5)
式中:A为指前因子;Z为自催化因子;Ez为引发反应与自催化反应两步活化能之差;n1、n2为反应级数。
利用俄罗斯CISP公司研发的热分析软件TSS(Thermal safety Software)中Formal Kinetics模块,根据上述反应过程进行动力学建模,通过非线性拟合方法计算出不同升温速率下的分解反应放热量(Q)及放热速率(dQ/dt)随时间变化曲线,拟合值与测试值比较分别见图5(a)和图5(b)。
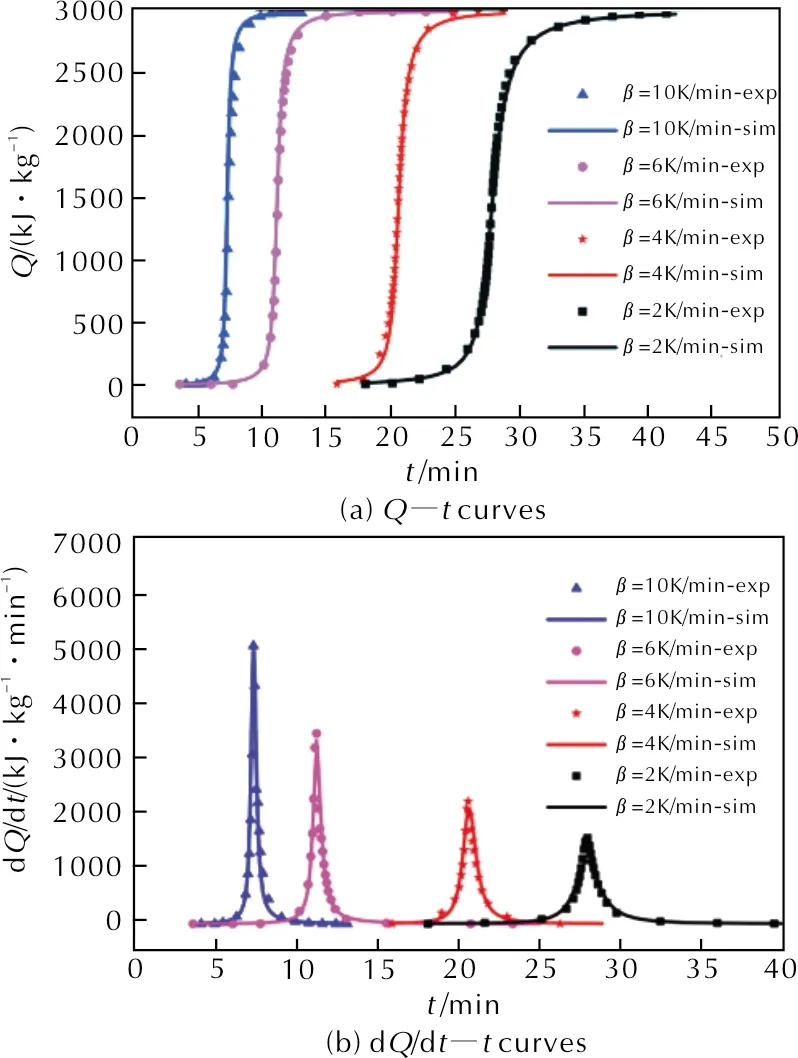
图5 基于模型的分解反应比放热量及放热速 速率拟合曲线与实验曲线对比Fig.5 Comparison between experiments and simulations of Q and dQ/dt based on reaction model
从图5(a)可知,拟合放热量曲线与实验曲线具有较好的一致性。从图5(b)可知,升温速率高时放热速率曲线拟合值与实验值一致性较好,升温速率2K/min时放热速率拟合曲线与实验曲线的峰值相比偏小。
由模型拟合方法直接计算得到ANSF分解反应比放热量为2977.77kJ/kg,与DSC测试结果相近;分解过程中自催化阶段指前因子为8.55×1013s-1,表观活化能为109.02kJ/mol,反应级数1.60;引发阶段和自催化阶段两步活化能之差为5.73kJ/mol,即引发阶段活化能为114.75kJ/mol;引发阶段的反应级数为2.14。
3 结 论
(1)DSC测试结果表明,ANSF大约从100℃开始分解,不同升温速率下平均比放热量可达2945J/g。该物质热稳定性较差,其起始分解温度较低、比放热量较大。
(2)ANSF热分解反应具有自催化性质,通过等转化率法计算得到该反应活化能随转化率的变化明显,表明反应过程复杂,不能用单步反应动力学进行描述。
(3)根据简化的B.P.模型,利用模型拟合方法计算得到具体动力学参数。ANSF分解反应引发阶段表观活化能为114.75kJ/mol,自催化阶段表观活化能约109.02kJ/mol。该动力学模型及参数为进一步研究该物质的热危险性提供了参考依据。
