钛基多孔羟基磷灰石/氧化镁复合涂层制备及其生物活性研究
2020-10-27张岚
张 岚
(厦门医学院药学系,福建厦门361023)
羟基磷灰石[Ca10(PO4)6(OH)2](HA)代表约70%的天然人类骨骼,已广泛应用于整形外科[1]。 但是有研究表明钛底材上HA涂层的机械强度差,为了解决HA生物陶瓷涂层的问题,该问题的一种解决方案是采用电泳沉积的方法在钛植入物上沉积HA复合涂层[2]。有研究表明致密的HA涂层不利于与机体之间的生物相容,植入材料的多孔结构以及空隙表面在成骨环境中会更有利于蛋白的沉积,骨细胞的附着和增殖[3]。MgO作为骨科植入材料在模拟体液测试中可诱导磷灰石层的形成,表现出良好的生物活性[4]。采用电泳沉积的方法在钛基体表面沉积HA/MgO/壳聚糖CS涂层,经过高温烧结后,CS分解致孔,MgO作为中间颗粒可以缓冲HA与钛基体之间的应力差,能够提高复合涂层与基体之间的粘结力[5-6]。
1 实验部分
1.1 实验材料和仪器
无水氯化钙(CaCl2)、磷酸氢二铵(NH4H2PO4) 、尿素(H2NCONH2)、十二烷基硫酸钠(SDS):AR,西陇科学有限公司;脱乙酰度约为96.4%的壳聚糖(CS),青岛金湖有限公司;纯钛(西北有色金属研究院);其余药品均购自国药股份有限公司;离子水。
采用Hitachi FlexSEM1000扫描电子显微镜观察产物的表面微观形貌;Bruker ALPHA型红外光谱仪表征产物的组成;采用Hitachi FT7700 Exalens高分辨透射电镜表征产物的微观结构;LLOYD LR5K型万能材料实验机测试涂层与钛基体的结合强度。
1.2 实验步骤
1.2.1 纳米羟基磷灰石制备
称取0.78g的CaCl2和0.55g的NH4H2PO 加入到烧杯中(Ca/P=1.67),然后加入约35mL的去离子水搅拌溶解,加入0.2gSDS和1.5g的尿素继续搅拌10min,转移到100mL水热反应釜中,条件设置为120℃水热合成12h,自然冷却至室温,取出用离心机分离,粉体分别用水洗、乙醇洗,最后在烘干机中60℃烘干5h,放入干燥器备用。
1.2.2 电泳沉积复合涂层
纯钛片裁剪成1mm×10mm×100mm,经砂纸磨光,在5%氢氟酸和5 mol/L硝酸中蚀刻1min后放入盛有丙酮的烧杯中在超声仪中超声洗涤30min,取出用去离子水清洗自然晾干后备用。称取0.268g HA纳米粉体、0.268g CS微粒(球磨后过筛,<38.5μm)和0.268g MgO(球磨后过筛,<38.5μm)于烧杯中,加入40mL的正丁醇作为分散剂,加入0.5mL的三乙醇胺,超声分散1h后陈化24h。电泳沉积采用DYY-2C型稳压稳流电泳仪(北京六一仪器厂),设置电压为35V,铂片为阳极,处理后钛片为阴极,电极间距为0.7cm,沉积面积为10 mm×10mm,电泳沉积时间为60s,电泳沉积后取出钛片自然晾干备用。
1.3 生物活性评价
将烧结后的涂层浸泡在1.5倍离子浓度的人体模拟体液如表1中,保持温度在37℃,分别浸泡9天、10天和12天后取出自然晾干,SEM观察涂层表面的微观形貌,FTIR分析涂层的组成。
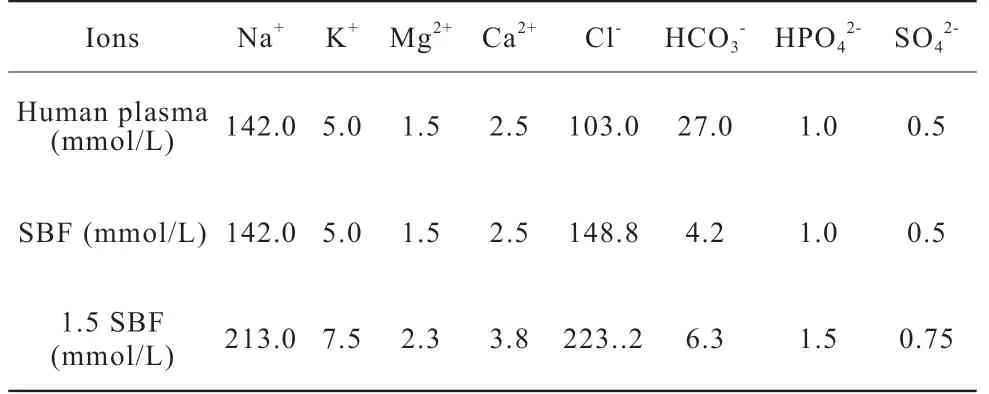
表1 1.5 倍离子浓度的人体模拟体液Table 1 The ion concentration of 1.5SBF
2 结果与讨论
2.1 羟基磷灰石粉体表征

图1 HA粉体透射电镜图Fig.1 TEM image of the HA nanoparticles
图1 是水热制备的羟基磷灰石(HA)粉体的透射电镜图,从图中可以看出,在120℃条件下的水热合成12h后制备的羟基磷灰石呈纳米棒状,长度在200nm~400nm之间, 直径约为20nm,形成纳米棒状结构可能是添加的表面活性剂SDS诱导HA晶体的生长方向[7]。
2.2 电泳沉积涂层组成表征
电泳沉积后的涂层用刀片刮下粉末的红外谱图如图2所示,从图中可以看出,在569cm-1、603cm-1、962cm-1以及1035cm-1~1094cm-1处出现PO43-强吸收峰,在3571cm-1也有OH-特征吸收峰[8];在1638cm-1和1598cm-1处吸收峰分别为CS的酰胺Ⅰ谱带特征吸收峰和-NH2的弯曲振动吸收峰,1385cm-1是官能团-CH2-OH中C-O伸缩振动吸收峰[9],说明电泳沉积能够使HA颗粒与CS颗粒共沉积在钛表面。

图2 电泳沉积涂层的红外谱图Fig.2 FT-IR spectra of composite coating
2.3 烧结和浸泡后涂层表面形貌图
电泳沉积复合涂层经过700℃保温2h后的SEM图如图3所示,可以看出,烧结后涂层中的CS颗粒高温分解形成孔隙,孔隙大约在10μm~15μm如图3(a)所示,孔隙较深,孔状的结构有利于成骨离子浓度的增加,同时也可以使成骨溶液与涂层之间的接触角减少,有助于晶核的形成[10];HA颗粒相互粘结使涂层致密致密,表面有少许裂纹;同时可以看出有球形颗粒镶嵌在涂层表面和涂层中间如图3(b)所示,说明MgO颗粒与HA共沉积在钛表面,可以有效缓和HA涂层与基体之间的应力不匹配(Ti: 8.7×10-6K-1;HA: 13.6×10-6K-1)[11],增强HA涂层与基体之间的结合能力,经过拉力测试多孔涂层基体之间的结合力可达30.2MPa。

图3 烧结后复合涂层的SEM图Fig.3 SEM images of composite coatings after sintering
2.4 浸泡后涂层的组成和微观形貌
相比于未浸泡涂层的FTIR谱图(图4b),从多孔HA/MgO涂层在1.5SBF中浸泡12天后的FTIR谱图(图4a)可以看出,在1400cm-1~1552cm-1和870cm-1处出碳酸根的吸收峰,说明随着浸泡时间的延长,涂层表面的多孔结构能够不断的诱导模拟体液中的Ca2+、OH-离子形成碳酸羟基磷灰石晶体,形成的机理如下:

多孔HA/MgO涂层在1.5SBF中浸泡6天后碳酸羟基磷灰石晶体基本覆盖涂层表面如图5(a)所示,而在浸泡9天[图5(b)和12天图5(c)]后已经完全覆盖涂层,从浸泡12天后的涂层表面局部放大[图5(d)]可以看见蠕虫状的小孔布满碳磷灰石表面,这可能是碳酸羟基磷灰石与体液中的离子交换导致[12],有研究表明作为人体植入材料在人体模拟体液中浸泡后能否形成碳酸羟基磷灰石晶体层是衡量该材料是否具有良好的生物活性的一个重要指标[13],综上所述,制备的多孔HA/MgO涂层具有较好的生物活性。

图4 多孔 HA/MgO复合涂层于1.5SBF中浸泡12d前后的FT-IR图Fig.4 FT-IR spectra of porous HA/MgO composite coatings before and after immersion in 1.5SBF for 12 d

图5 多孔HA/MgO复合涂层于1.5SBF中浸泡后的SEM图Fig.5 SEM images of porous HA/MgO composite coatings after immersion in 1.5SBF
3 结论
采用水热合成的方法制备了长度在200nm~400nm,直径约为20nm的羟基磷灰石纳米棒;以正丁醇为分散剂,三乙醇胺为添加剂,配制HA/MgO/CS质量比为1/1/1的稳定悬浮液,通过电泳沉积的方法在金属钛表面沉积HA/MgO/CS复合涂层,经过700℃烧结保温2 h后,CS高温分解后致孔,得到孔隙在10μm~15μm的钛基多孔HA/MgO复合涂层,涂层与基体之间的结合力可达30.2MPa;涂层在1.5SBF中浸泡12天后表面完全覆盖了碳酸羟基磷灰石层,说明涂层具有良好的生物活性。
