负载钌的氮掺杂石墨烯催化剂的制备及应用
2020-10-27李路刘灵惠徐金铭黄延强张涛
李路,刘灵惠,徐金铭,黄延强,张涛
(1 中国科学院大连化学物理研究所,辽宁大连116023; 2 烟台大学化学与化工学院,山东烟台264005;3 重庆大学化学与化工学院,重庆400044)
引 言
二维层状材料是一类应用前景极其广阔的新兴材料,通常层状材料的层内原子间以较强的共价键或者离子键结合,层与层之间则是依靠较弱的范德华力堆叠在一起[1]。由于其结构具有特殊性,以层状材料作为基础,构筑新型纳米复合材料,引起了各学科的广泛关注。常见的层状材料根据层板带电性不同可以大致分为三类:层板带正电性的层状化合物,例如层状双羟基金属氧化物(LDHs)和稀土金属氧化物[2−6];层板带负电性氧化物,例如层状钛酸及其盐、层状铌酸及其盐和层状氧化锰等[7−10];除此之外还有层板为电中性的石墨烯、氮化碳和硫化钼等层状材料[11−12]。2004 年,Geim 小组[13]首次用机械剥离法获得了单层或薄层的新型二维原子晶体——石墨烯,自此开创了石墨烯研究的新潮时代。石墨烯(graphene)是一种由碳原子以sp²杂化轨道组成六角形呈蜂巢晶格的二维纳米材料,由于石墨烯具有高的表面积、特殊的光电性能、优异的面内导电性和机械耐久性[14−16],使其成为复合材料开发的理想载体,石墨烯纳米复合材料不但能继承石墨烯的优良特性,而且对担载的活性组分有电子改性的作用,可产生新的协同效应,使得这类纳米复合材料成为近年最具潜力的新兴材料之一。此外,石墨烯材料改性的研究对石墨烯基材料的催化应用有着十分重要的意义,除了形貌调控,杂原子掺杂是目前采用的最为广泛调节石墨烯性能的方法,它能实现石墨烯骨架电子结构的调变,从而使其表现出独特的催化功能并发挥潜在用途[17−21]。石墨烯及复合材料有如此优异的性能,所以除对石墨烯进行修饰改性外,制备石墨烯及复合材料的新方法的研究方兴未艾。
基于此,设计新型硬模板法成功一步制备出负载钌纳米粒子的层状二维含氮石墨烯催化剂(Ru−NG)。该方法以蒙脱石(MMT)为模板,将钌−邻菲罗啉络合物插层入蒙脱石层间,惰性气氛下高温炭化后用酸刻蚀除去蒙脱石得到Ru−NG 催化剂。在二氧化碳加氢制甲酸反应中,相比于常规浸渍−还原法制备的活性炭负载的Ru/AC 催化剂,Ru−NG表现出超高的活性。
1 实验材料和方法
1.1 材料
氯化钌,购于天津市风船化学试剂科技有限公司;盐酸,氢氟酸和乙醇,均为分析纯,购于天津市大茂化学试剂厂;邻菲罗啉,分析纯,购于天津市科密欧化学试剂有限公司;氟化钠,四水乙酸镁,异丙醇铝,无水乙酸钠和气相二氧化硅(15 nm),均为分析纯,购于上海阿拉丁生化科技股份有限公司。
1.2 分析仪器
X 射线衍射仪(PANAnalytical X’Pert−Pro);扫描电子显微镜JSM−7800F;透射电子显微镜(JEOL JEM−2100F);X 射 线 光 电 子 能 谱 仪(Thermo ESCALAB 250Xi);电感耦合等离子体发射光谱仪(PerkinElmer Optima 7300DV);拉 曼 光 谱 仪(LabRAM HR800);液相色谱(Agilent 1100 series)。
1.3 催化剂制备
1.3.1 Ru−NG制备
(1)蒙脱石的制备。参考并改进Reinholdt 等[22]的工作在实验室中合成制备蒙脱石。在75℃水浴内,将异丙醇粉末加入去离子水中,搅拌0.5 h 后升温至95℃蒸发异丙醇1.0 h,重新加入蒸发失去的去离子水得到氢氧化铝悬浊液。在塑料烧杯中,机械搅拌下加入去离子水、氟化钠、无水乙酸钠和四水乙酸镁。加入上述制得的氢氧化铝悬浊液,加入二氧化硅,搅拌均匀。将混合物放入装有聚四氟乙烯内衬不锈钢反应釜中,在220℃自生压力下水热反应72 h 后将水热釜空气中冷却到室温。过滤,去离子水洗涤,空气中干燥2 d,再放入75℃烘箱中干燥。
(2)邻菲罗啉插层蒙脱石材料(PMIM)的制备。将40 g自制蒙脱石加入500 ml去离子水和500 ml乙醇混合溶剂中,加入20 g邻菲罗啉于以上悬液中,常温下搅拌24 h,过滤,得白色产物,常温下自然通风干燥。
(3)取3.6 g PMIM 加入200 ml去离子水搅拌,待分散均匀后,加入适量质量分数为9.5%的RuCl3·3H2O 溶液于悬液中,室温条件下搅拌24 h,使得邻菲罗啉与金属钌前体充分发生配位反应。所得的浅灰绿色钌配位的邻菲罗啉插入蒙脱石层间化合物(Ru−PMIM),在管式炉中氮气气氛下进行800℃炭化3 h,炭化后所得黑色固体用过量的HF 酸洗24 h,再用过量HCl 酸洗24 h,酸洗去除模板后得到Ru−NG 催化剂。四种不同钌负载量的催化剂制备过程中原料的加入量与负载量的关系如表1所示。
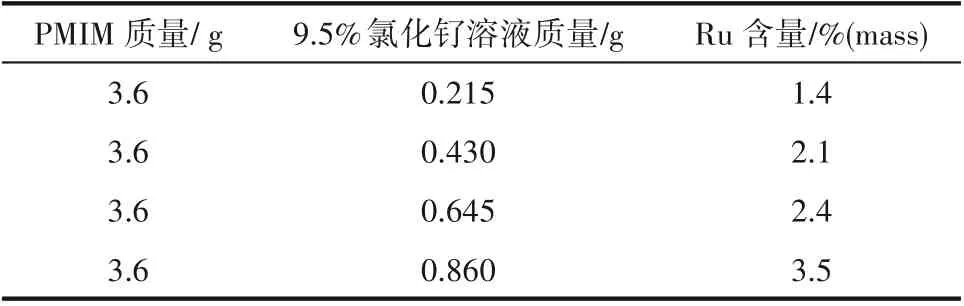
表1 不同钌负载量催化剂的制备参数Table 1 Synthesis conditions of Ru-NG catalysts with different Ruthenium loadings
1.3.2 Ru/AC制备 采用传统常规的浸渍法制备负载量为2.5%的Ru/AC 催化剂进行对比实验。取1.5 g 活性炭于25 ml 烧杯中,0.44 g 9.5%RuCl3·3H2O 溶液加入烧杯中,混合均匀,放置6 h,80℃干燥6 h,300℃焙烧3 h 后在氢气气氛下250℃还原2 h 得到Ru/AC催化剂。
1.4 催化反应测试
催化剂活性评价探针反应选择二氧化碳加氢生成甲酸的反应,反应在高压釜(美国Parr 公司)中进行,水为溶剂,加入1,8−二氮杂二环十一碳−7−烯(DBU)作为碱,催化剂用量为5 mg。反应产物通过液相色谱检测分析:流动相为0.05 mol/L 的稀硫酸,柱压为45 bar(1 bar=0.1 MPa),柱箱温度为45℃,流量为0.5 ml/min。
2 实验结果与讨论
2.1 催化剂表征
2.1.1 Ru−NG 表征 邻菲罗啉分子及钌−邻菲罗啉配位络合物均能吸附在蒙脱石层间形成插层复合物。由于邻菲罗啉分子中的芳环较多,在惰性气氛下高温热解的过程中,热解残炭率较高,且易形成大片层类石墨烯的共轭结构,所以选择邻菲罗啉为石墨烯前体。蒙脱石为含水硅铝酸盐构成的层状矿物,天然的蒙脱石矿物中含有较多的杂质,即使经过化学提纯后,在蒙脱石的晶格中也会含有相当数量的Fe3+、Ti4+和Mn2+等杂质离子,为减少这些杂质的影响,采用人工合成的方法制备较为纯净的蒙脱石为模板。
为了考察所制备蒙脱石模板剂及催化剂的结构,将所制备材料进行了XRD 表征。图1(a)中MMT为自制蒙脱石的XRD 谱图,与JCPDS 标准卡片及文献[23−24]对比,结果吻合较好,无其他晶相杂峰的出现,这说明实验室自制蒙脱石较为纯净,是制备层状石墨烯材料的理想模板剂。图1(a)中PMIM 为邻菲罗啉与蒙脱石插层结构的XRD 谱图,通过与蒙脱石XRD 谱图比对,发现插入邻菲罗啉后,蒙脱石层状结构没有遭到破坏,并且第一个衍射峰向低角度偏移,层间距增加,这是由于邻菲罗啉进入蒙脱石的片层间,对蒙脱石片层起到了插层与柱撑的作用,说明邻菲罗啉与蒙脱石的形成插层复合材料。图1(b)为脱除蒙脱石后,不同Ru负载量Ru−NG催化剂的XRD 谱图。从图中可以看出,随着Ru 含量的增加,所有催化剂谱图几乎完全一致,且均未发现Ru的特征峰,即使在3.5%Ru−NG 也未观察到,其可能原因为Ru 粒子的尺寸较小,而不是Ru 的含量较低造成。Ru−NG 催化剂的XRD 谱图中,2θ 在26.6°和44.2°出现较宽的衍射峰,分别对应着石墨的(002)和(101)晶面衍射峰,是因为在除去硬模板后,石墨烯少部分片层发生重叠,形成了类似石墨的结构,但这也说明所制备的催化剂具有石墨烯的层状结构。
Ru−NG 的扫描电子显微镜(SEM)图见图1(c)和图1(d)。从SEM 图中可以清晰地看出Ru−NG 催化剂的层状结构,且有较多褶皱,这说明硬模板法制备的Ru−NG 催化剂石墨烯片层面积较大,并且非常薄,其自身强度不足以支撑平面结构,因而形成褶皱状。这种褶皱状的结构,使得脱除蒙脱石模板后,石墨烯不易完全有序堆叠形成完美石墨结构,利于充分暴露催化剂的金属活性位点。
图2 为Ru−NG 催化剂的拉曼光谱,表2 为相应的峰位置、半峰宽及ID/IG值。石墨烯拉曼光谱三个主要的特征峰分别为D 峰、G 峰和2D 峰,峰位置分别在1350、1580、2700 cm−1左右,D 峰(结构无序峰)代表石墨结构的晶格缺陷,低对称结构的增加。G峰对应于布里渊中心的E2g声子,是sp2杂化碳结构的特征峰。2D 峰(D 峰倍频峰)与结构缺陷或sp3杂化的碳原子有关。R(ID/IG)为D 峰强度与G 峰强度的比值,R 值的大小对应着催化剂偏离石墨晶体的结构缺陷大小[25−27]。从表2看到,四个不同负载量的Ru−NG 催化剂拉曼特征峰的出峰位置没有明显的变化,但是D峰和G峰的相对强度略有变化,表明不同Ru 负载量催化剂的晶格缺陷略有不同,其中2.1%Ru−NG 的R 值最大,说明这个催化剂具有最多结构缺陷,石墨烯的缺陷主要由N掺杂引起,与后面XPS 分 析 中2.4%Ru−NG 表 面N 含 量 最 高 的 结 果一致。
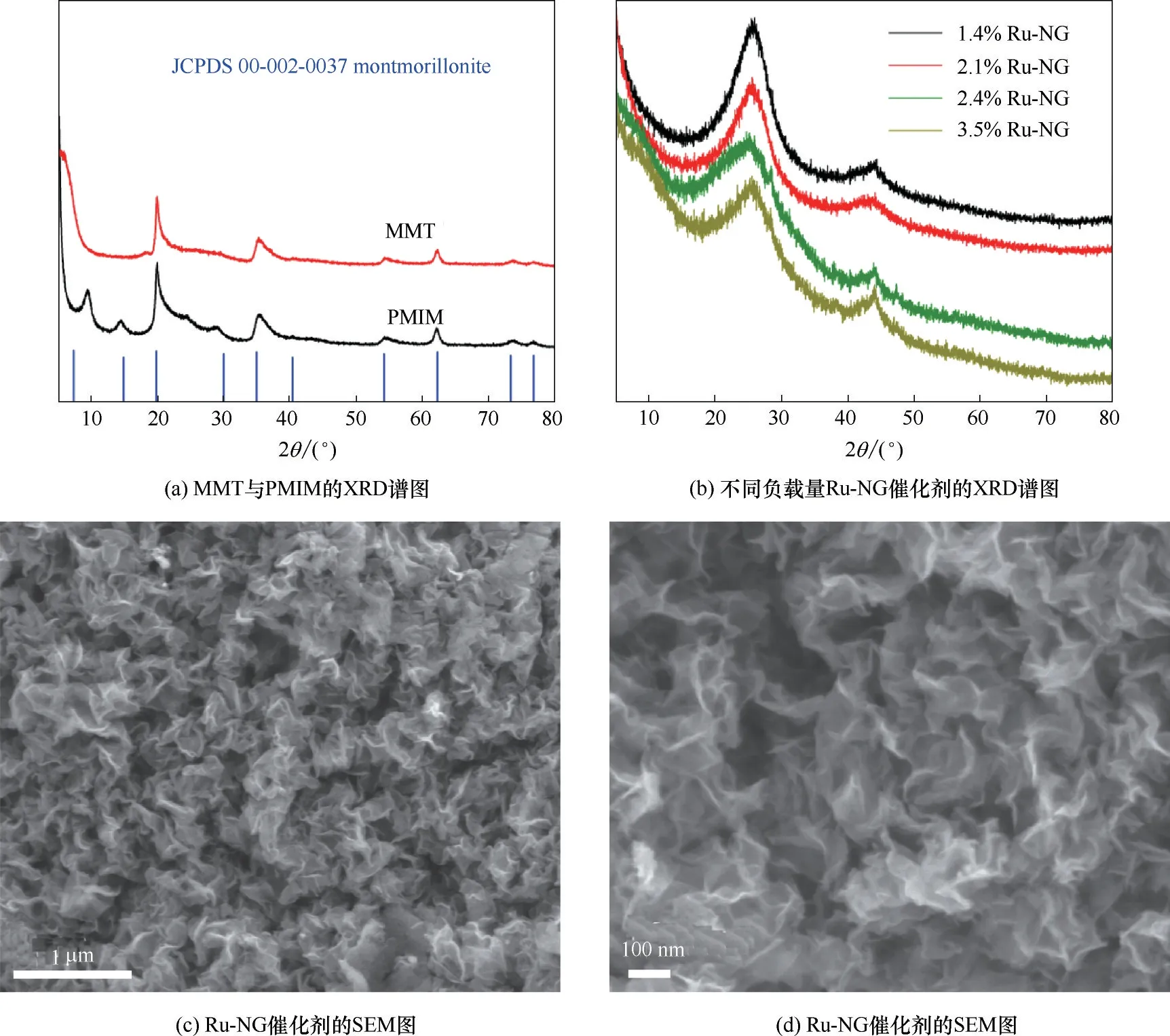
图1 催化剂的XRD谱图与SEM图Fig.1 XRD patterns and SEM images of Ru−NG catalysts
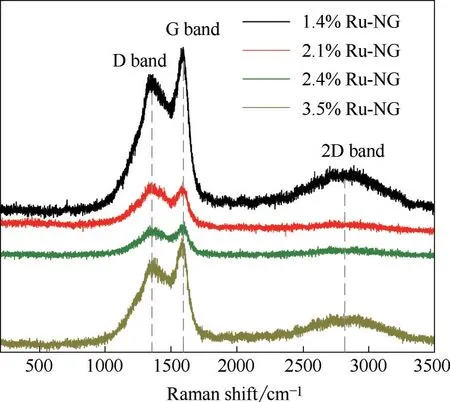
图2 Ru−NG 催化剂的拉曼图谱Fig.2 Raman spectra of Ru−NG catalysts

表2 Ru-NG 催化剂的拉曼特征峰参数Table 2 Raman spectral parameters of Ru-NG catalysts
图3(a)为不同负载量Ru−NG催化剂的扫描透射电镜图(STEM),从电镜图中发现Ru 纳米粒子高度分散在石墨烯载体上,且粒径较均一。通过粒径统计分析,四种不同负载量的Ru−NG 平均粒径在1.2~1.4 nm 之间,随着Ru 含量的增加,粒子尺寸没有明显的改变。这说明在所考察的范围内,含N 石墨烯载体上,负载量对Ru 粒子尺寸影响不大,其可能的原因如下:(1)模板剂蒙脱石片层的物理限域作用,限制了Ru 粒子的长大;(2)Ru 离子与邻菲罗啉间存在着较强的配位作用,且在热解过程中钌物种与有机含氮物种始终保持着这种相互作用,抑制了Ru 纳米粒子迁移和聚集。通过对1.4%Ru−NG催化剂的主要元素进行元素分布分析发现,C、N、O 及Ru元素在催化剂中分布均匀,见图3(b)。
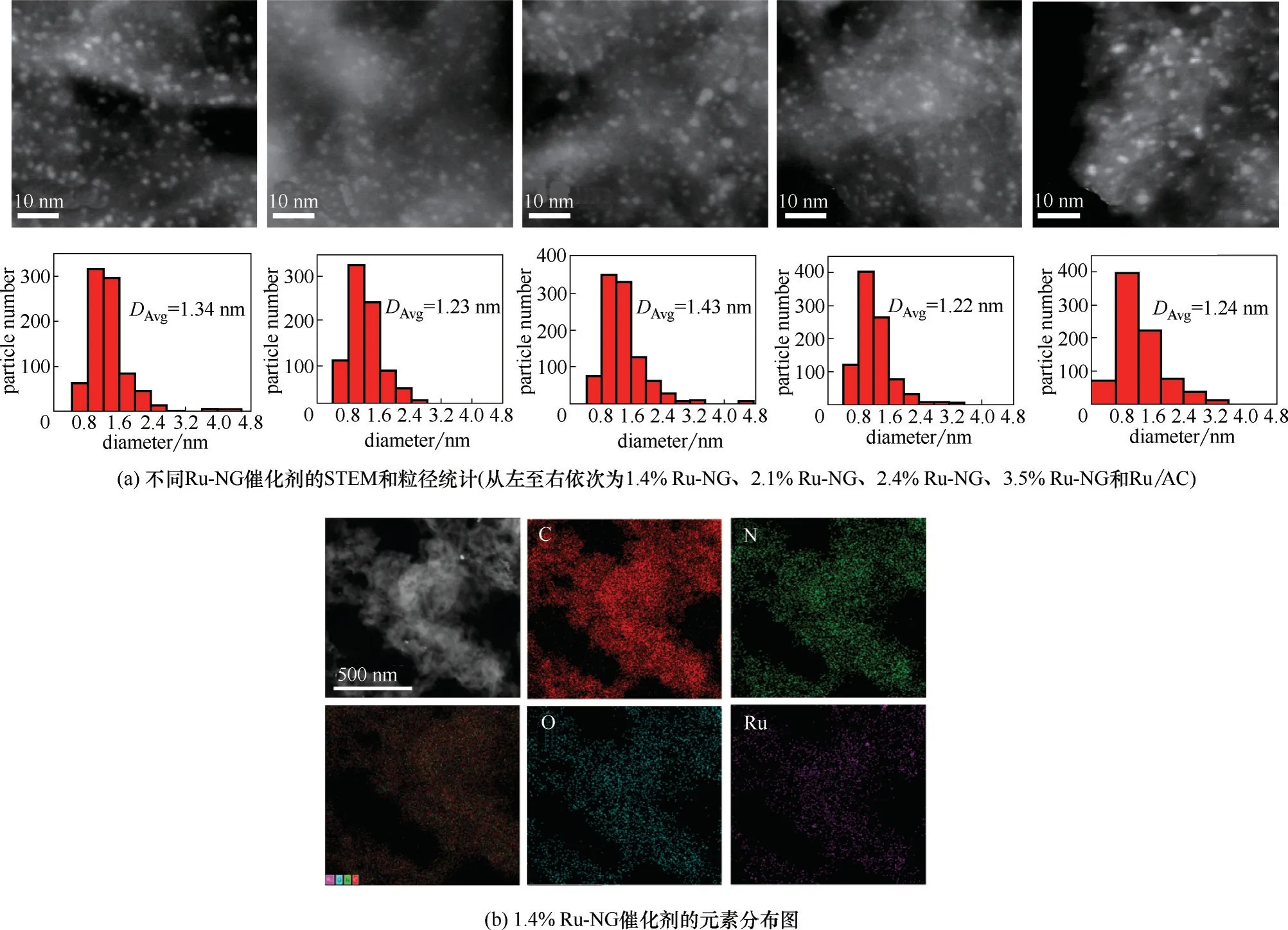
图3 Ru−NG催化剂的扫描透射电镜与元素分布图Fig.3 STEM and EDX maps of Ru−NG catlysts
XPS 不仅能够给出材料表面的化学组成及含量,而且可以分析出化学价态等信息。催化剂的XPS全谱扫描如图4(a)所示。Ru−NG 催化剂主要包含碳、氮、氧、钌元素,这与图3(b)元素分布图相吻合。图4(b)中,N1s 谱经拟合可得到石墨氮(401.5 eV)、吡咯氮(400.1 eV)和吡啶氮(398.5 eV)。随着Ru 含量的增加,Ru−NG 催化剂中石墨氮的含量逐渐减少,说明sp2杂化的吡咯氮和吡啶氮的含量有所增加,这是因为Ru 和此类氮物种有强相互作用,这与文献[28−30]报道中sp2杂化氮官能团有更多电子,容易与金属阳离子发生配位相符合。
对于Ru−NG 催化剂的氮气物理吸附的结果列于表3,其中1.4% Ru−NG 催化剂比表面积高达416.9 m2/g,孔容为0.26 cm3/g。Ru−NG 催化剂表面积和孔容随着催化剂钌金属含量的增加而略有减小,其原因可能为催化剂在炭化过程中,Ru 与邻菲罗啉配位作用较强,对邻菲罗啉热解交联形成含氮石墨烯的结构有所影响,从而导致催化剂比表面积有所降低。
2.1.2 Ru/AC 表征 为与本文报道的方法制备的Ru−NG 催化剂作对比,用传统浸渍−还原法制备了活性炭负载钌的催化剂Ru/AC。ICP 测试得到Ru/AC 催化剂中Ru 含量为2.5%(质量分数)。如图3(a)中最右侧Ru/AC 催化剂的STEM 图和粒径统计所示,传统浸渍−还原法制备的Ru 催化剂粒子分布在0.6~2.1 nm 之间,粒子平均粒径1.24 nm 与硬模板法制备的Ru−NG 相差不大,但粒径分布的均一性远差于Ru−NG。
与传统浸渍−还原法相比,硬模板法对金属粒子有限域作用,抑制Ru 粒子发生团聚,使所制备的Ru 纳米粒子高度分散,粒径均一;同时,800℃炭化后,氮物种与Ru 金属配位稳定,使得催化剂较传统制备方法合成的负载型金属纳米粒子催化剂具有更好的耐温性和稳定性。
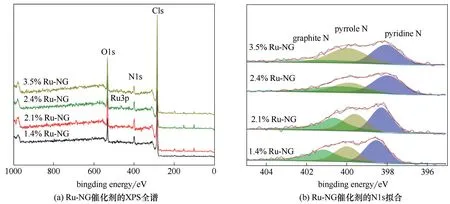
图4 Ru−NG催化剂的XPS全谱和N1s拟合谱图Fig.4 XPS survey spectra(a)and XPS spectra of N1s peaks(b)of Ru−NG catalysts
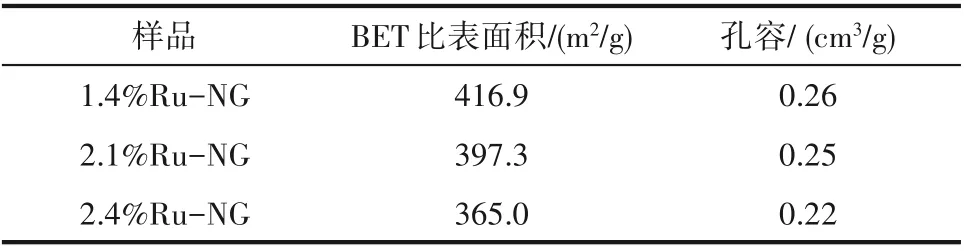
表3 Ru-NG催化剂的比表面积和孔容Table 3 Specific surface area and pore volume of Ru-NG catalysts
2.2 催化反应测试
目前我国的能源结构仍以煤炭、石油和天然气等化石燃料为主,CO2排放总量巨大。将CO2转化成具有更高价值的化学品是缓解碳排放压力的有效途径之一[31],CO2加氢合成甲酸为原子经济性反应,生成的甲酸不仅是一种用途非常广泛的基本化工原料,同时也是一种理想的液态储氢材料[32−33]。因此,开发用于CO2加氢生成甲酸的催化剂有着十分重要的研究意义。
CO2加氢合成甲酸的反应体系中,均相催化剂具有活性高、选择性好和金属利用率高等优点,但存在产物不易分离和催化剂循环利用困难等不利因素;相较之下,非均相催化剂具有易分离和连续操作的工业应用优势,并可以通过暴露与增加单位催化活性位点来提高催化活性和选择性[34−35]。因此,制备负载型催化剂在非均相体系中催化反应CO2加氢合成甲酸。
CO2加氢合成甲酸的反应中,1,8−二氮杂双环[5.4.0]十一碳−7−烯(DBU)作为Lewis 碱,可以作为氢键受体,激活底物,有效促进反应进行[36]。因此,反应中加入10 ml 1 mol/L DBU,反应温度为140℃,原料气压力PCO2= 4 MPa,PH2= 4 MPa,反应时间为24 h。催化剂活性如表4 所示,所有Ru−NG 催化剂反应活性都优于传统浸渍法制备的Ru/AC 催化剂。相同Ru 负载量时,2.4% Ru−NG 与2.5% Ru/AC 的TON 比值为19.1,说明此硬模板法制备的Ru−NG 催化剂在该反应中性能优异。
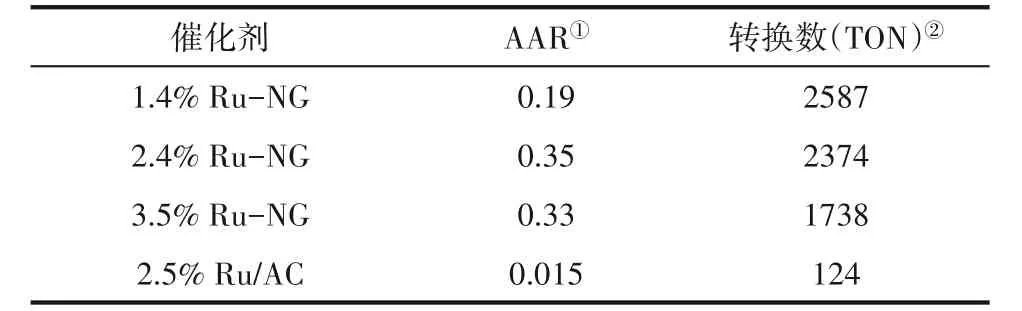
表4 Ru-NG催化剂的二氧化碳加氢制甲酸反应活性Table 4 Hydrogenation of carbon dioxide to formate with Ru-NG catalysts
为进一步研究CO2加氢合成甲酸的反应温度和原料气压力对活性的影响,选取催化剂2.4%Ru−NG为研究对象。当固定CO2压力为4 MPa,氢气压力为4 MPa,反应时间为24 h,CO2加氢制甲酸反应转换数(TON)与温度的关系如图5(a)所示。随着反应温度的升高,Ru−NG 催化剂的催化活性增加,原因是升高温度有利于反应产物形成活化分子,从而使得活化分子数增多,有利于二氧化碳的转化;且升高温度,反应速率加快,有利于反应的进行。当固定CO2压力为4 MPa,反应温度为140℃,反应时间为24 h,CO2加氢制甲酸反应的TON 随氢气压力的变化见图5(b)。催化剂的活性随着氢气压力的增加而成倍增加,这是因为二氧化碳加氢生成甲酸的反应是压力减小的反应,升高反应压力有利于反应正方向进行;另升高压力反应物浓度增加,进而反应速率加快。
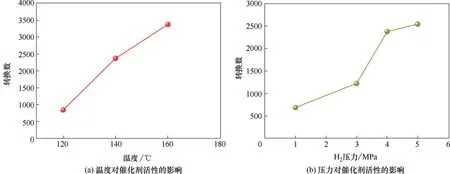
图5 温度与压力对CO2转换数(TON)的影响Fig.5 Effects of temperature and pressure on the TON of CO2over 2.4%Ru−NG
3 结 论
以邻菲罗啉−钌络合物插层的蒙脱石作前体,采用硬模板法成功制备出负载钌纳米粒子的氮掺杂石墨烯基催化剂(Ru−NG)。Ru−NG 催化剂具有蒙脱石类似的层状结构,C、N、O 及Ru 元素在催化剂中分布均匀。由于受蒙脱石片层的物理限域作用及钌物种与有机含氮物种强配位作用,金属钌纳米粒子尺寸分布较窄,平均粒径在1.2~1.4 nm,并高度分散于氮掺杂石墨烯载体上。该催化剂在CO2加氢制备甲酸的反应中表现出优异的催化活性,其中,2.4%Ru−NG 应用于CO2加氢制备甲酸的反应中TON 值为传统浸渍−还原法制备2.5%Ru/AC 的19.1倍。
