神经免疫之峰的攀登者——郝峻巍教授
2020-10-27刘海杰郝峻巍
王 菲 刘海杰 杨 佳 刘 峥 郝峻巍
(首都医科大学宣武医院,北京 100053)
1 个人简介
郝峻巍教授(图1),1977年生,南开大学和美国Barrow神经病学研究所联合培养博士,主任医师、教授、博士生导师,专注于神经免疫性疾病和脑血管病的诊断与治疗。现任首都医科大学宣武医院副院长,神经内科高级卒中单元和神经免疫疾病病区主任。

图1 郝峻巍教授
2008至2011年,郝峻巍教授赴美国Barrow神经病学研究所开展博士及博士后课题研究,开启了神经免疫学的探索之路。2011年人才引进至天津医科大学总医院神经内科,先后任主治医师和三级主任医师,培养神经病学硕士生、博士生60余人。郝峻巍教授精通神经免疫疾病先进诊疗技术,并持续开展基础与临床转化研究,凭借对神经免疫疾病丰富的临床经验及深刻的认识,将神经炎症的研究拓展到了脑血管病,并取得了一系列创新性成果。2011年,郝峻巍教授入选教育部“新世纪优秀人才支持计划”,2013年获得国家自然科学基金优秀青年科学基金,2015年入选国家“万人计划”青年拔尖人才,2016年获得首批中国医师协会“中国杰出神经内科医师(青年医师奖)”,2018年获得国家杰出青年科学基金。
天津医科大学总医院神经内科与首都医科大学宣武医院有着深厚的历史渊源,严谨求实、开拓创新的精神一脉相承。郝峻巍教授于2019年加入首都医科大学宣武医院,依托作为国家重点学科和临床重点专科的神经内科,致力于以临床转化为目的的科学研究,思考与追寻疾病新的致病机制与诊疗思路,在神经免疫领域不断攀登新的高峰。
郝峻巍教授作为一名出色的神经病学专家,以神经系统自身免疫性疾病和急性脑血管病为切入点,取得了一系列丰硕的成果(图2):共获得国家自然科学基金(5项)、国家973课题等12项课题资助,在PNAS、JExpMed、AnnNeurol、JAMANeurol、CellRep、EMBOMolMed、Stroke、JImmunol等杂志上发表SCI文章68篇,以第一发明人申请专利9项,其中授权专利5项。

图2 临床实践与基础研究相结合,在神经免疫领域不断取得新的成绩
同时,郝峻巍教授积极参与学会建设与发展,任中国神经科学学会第七届理事会理事、中华医学会神经病学分会神经免疫学组委员,并作为主任委员筹建中国神经科学会神经免疫学分会。
2 主要学术贡献
中枢神经系统(central nervous system,CNS)内的免疫与炎症反应具有独特的发生发展机制,不但可以直接参与多种CNS自身免疫性疾病,如多发性硬化(multiple sclerosis,MS)、视神经脊髓炎疾病谱、自身免疫性脑炎等,在急性脑血管病、颅脑外伤、阿尔茨海默病、帕金森病等其他类型神经系统疾病的病程中也起着重要作用。郝峻巍教授以经典的神经系统自身免疫性疾病和脑血管病为着力点,探索免疫炎症干预的新策略。
2.1 在神经系统自身免疫性疾病中,揭示了NK细胞及分泌乙酰胆碱的NK细胞亚群在脑内区域免疫学的抗炎特征,阐述了关键炎症反应信号通路在该类疾病中的作用及靶向干预策略
在神经系统自身免疫性疾病中,免疫系统异常激活,免疫细胞浸润中枢、分泌炎症因子,识别并攻击髓鞘及神经元,导致脑损伤。自然杀伤细胞(natural killer cell,NK细胞)是人体内排在T和B淋巴细胞之后的第三大淋巴细胞,通过免疫调节及杀伤功能在神经系统自身免疫性疾病中发挥调控作用。而这种具有调控作用的NK细胞具有独特的脑内区域免疫学特性。针对神经系统自身免疫性疾病中NK细胞的区域免疫学特点,郝峻巍教授课题组取得了一系列重要发现:1)早期研究[1]发现,脑内固有NK细胞具有独特的区域免疫学功能,通过抑制Th17细胞活化,可以减轻中枢神经系统炎症反应损伤;2)在此基础上,利用IL-2/抗IL-2单抗复合物可有效扩增CNS内NK细胞,从而减轻脑内炎症反应、髓鞘脱失、免疫细胞浸润,缓解临床症状[2];3)为了进一步揭示脑内NK细胞的区域免疫学特点以及探索新的NK细胞亚群,课题组首次发现,NK细胞具备完整的胆碱能合成代谢系统。乙酰胆碱转移酶作为合成乙酰胆碱的关键酶,在部分NK细胞亚群中表达,尤其在浸润中枢的NK细胞中表达增加。分泌乙酰胆碱的NK细胞亚群具有独特的免疫表型,通过与CCR2+Ly6Chi促炎单核巨噬细胞形成免疫突触,抑制促炎免疫细胞[3]。以上研究成果揭示了CNS器官特异性NK细胞在神经免疫疾病中的保护作用。
郝峻巍教授关于NK细胞在CNS的器官免疫学特性的研究取得了一系列重大突破,提出了“外周浸润脑内的NK细胞具有免疫调节作用”的假说。国外后续在MS患者上应用IL-2Rα单克隆抗体Daclizumab开展的一系列临床研究显示,通过扩增NK细胞能有效减少MS患者的新发病灶,直接验证了该科学假说。美国食品药品监督管理局(Food and Drug Administration,FDA)已于2016年5月批准Daclizumab用于治疗MS。郝峻巍教授受邀在Neuroscience&BiobehavioralReviews杂志撰写内源性胆碱能抗炎通路作为神经系统疾病新型治疗策略的专题综述[4]。
在此基础上,课题组进一步利用临床标本和动物模型验证神经系统自身免疫性疾病中关键炎症反应信号通路的作用及靶向干预治疗策略,发现程序性死亡受体配体1(programmed cell death-Ligand 1,PD-L1)、DNA损伤诱导转录因子4(DNA damage inducible transcript 4,DDIT4)、过氧化物酶体增殖物激活受体γ辅助活化因子1(PPARγ co-activator-1α,PGC-1α)等信号通路在自身免疫性疾病中的重要作用,并应用micro/lincRNA、小分子靶向药物及基因条件敲除等手段干预,通过调控T细胞和小胶质细胞/巨噬细胞的表型功能,减轻免疫反应,缓解临床症状[5-9]。目前,课题组还在开展MS患者免疫修正药物治疗试验,利用PET-MRI技术标记脑内过表达的转运蛋白(translocator protein,TSPO)监测神经炎症变化规律(图3),为中枢神经系统自身免疫疾病的治疗效果和预后评估提供重要依据。
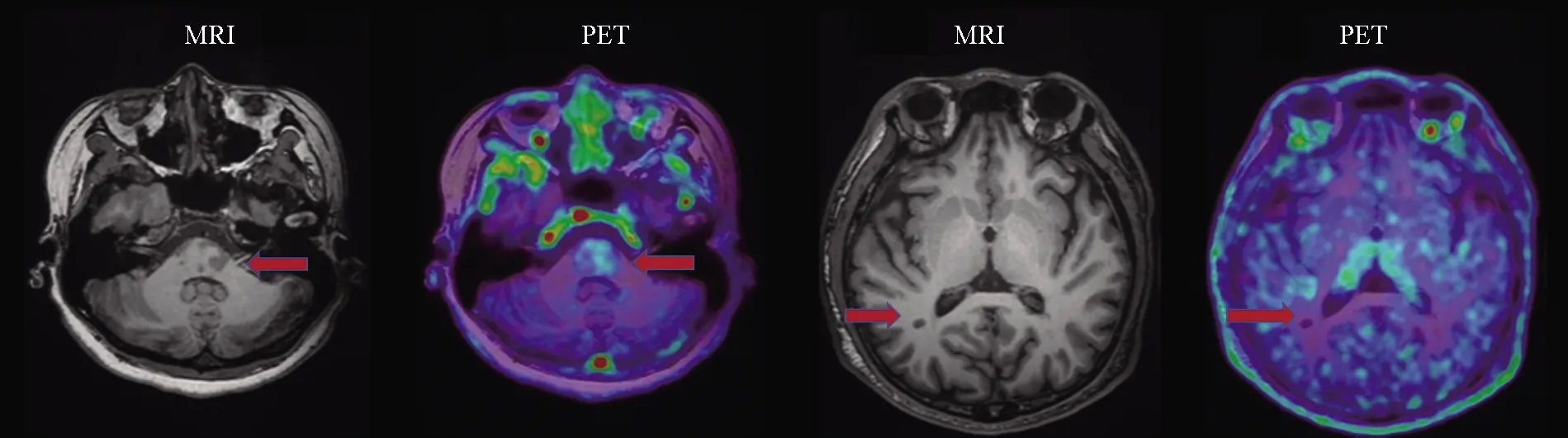
图3 TSPO摄取范围大于MRI上显示的病灶范围,表明常规MRI正常区域亦存在炎症反应,证实MS存在弥漫性脑损伤
郝峻巍教授近年来在神经免疫领域学术研究的丰硕成果,获得国际同行的高度认可,被Nature、Lancet、PNAS等相关领域综述及论文引用。
2.2 在急性脑血管病中,阐述了免疫和炎症反应促进神经损伤的分子机制,开展了免疫干预转化研究策略的探索
在急性缺血性脑血管病中,坏死的神经组织及细胞释放损伤相关因子,启动并激活炎症反应信号通路,促进炎性因子释放的同时趋化外周免疫细胞向中枢浸润,加重中枢神经损伤。当前研究显示,免疫炎症反应是介导脑卒中后水肿及继发损伤的关键因素。卒中发生后,脑内固有免疫细胞与外周浸润的以NK细胞为代表的免疫细胞存在相互作用,课题组对此开展研究,探索细胞相互作用的分子机制,率先发现缺血性卒中后白细胞介素-15(interleukin-15,IL-15)表达升高,并主要来自星形胶质细胞。进一步研究表明,在脑卒中患者的脑病理样本中,同样存在星形胶质细胞IL-15表达增加。通过构建星形胶质细胞IL-15过表达的转基因小鼠,建立缺血性损伤模型,发现NK细胞及CD8+T细胞浸润增加;利用单抗删除NK及CD8+T细胞可减轻IL-15过表达造成的神经损伤。该项研究阐明了星形胶质细胞来源的IL-15在缺血性脑卒中急性期损伤中起到关键致病作用,为拓展以IL-15为靶点的免疫治疗提供了依据,相关研究成果发表于PNAS[10]。该项研究在同期杂志获得专题评述 “Astrocytes fuel the fire of lymphocyte toxicity after stroke”,作者为德克萨斯大学休斯顿医学中心神经内科主任、卒中研究中心主任、美国NIH课题评审顾问Louise D.McCullough教授,明确指出这一新的研究证据对理解脑卒中后胶质细胞与淋巴细胞的相互作用具有重要意义[11]。
立足于上述研究基础,聚焦缺血性脑卒中急性期神经损伤,课题组对胶质细胞活化的分子机制及可能的干预靶点开展了进一步筛选。研究[12]显示,在脑卒中后激活的炎症反应信号通路中,利用单克隆抗体特异性干预PD-L1通路可促使小胶质细胞向抗炎小胶质细胞表型分化,从而对缺血性脑卒中发挥保护作用。通过抑制小胶质细胞转化生长因子-β1的转录,可以减少星形胶质细胞CXC趋化因子配体1[chemokine(C-X-C motif)ligand 1,CXCL1]的分泌,抑制中性粒细胞向中枢浸润,从而减轻脑损伤[13](图4)。卒中后活化的促炎小胶质细胞通过与神经元相互作用,引起神经元凋亡,导致卒中后神经组织损伤及功能障碍。通过上调神经元PGC-1α,可改善神经元线粒体能量代谢,抑制活性氧产生,缓解神经元损伤,减轻缺血后认知功能障碍[14]。通过以上对脑卒中后胶质细胞活化、外周免疫细胞浸润以及神经元损伤的相互作用和机制的研究,为探索脑卒中免疫干预治疗提供了新的线索和依据。
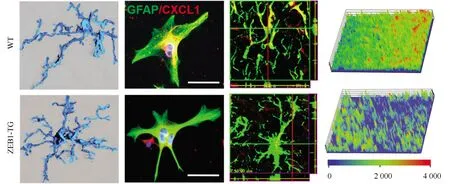
图4 ZEB1是小胶质细胞卒中后免疫反应的重要转录因子,改变小胶质细胞形态可减少CXCL1分泌[13]
3 科学意义与展望
科学的飞速进步促使我们对各类疾病的认识不断加深,新药物、新技术和新疗法不断涌现,然而神经疾病领域的药物研发进展缓慢,神经系统疾病依然是人类健康的重大威胁:在全球范围内,神经系统疾病依然是首位致残因素和第二大死亡原因[15]。近年来,随着免疫学的发展,免疫疗法作为新的探索方向,在肿瘤等领域取得了巨大的进步,为神经系统疾病的诊疗带来新的思路,神经-免疫相互作用也得到越来越多的认知及探索。神经免疫疾病及其他神经系统疾病的免疫机制的研究,对筛选治疗靶点和拓宽治疗思路,具有十分重要的科学意义。首都医科大学宣武医院具备丰富的临床资源和成熟的科研转化体系,这为进一步开展临床试验、提高我国神经系统疾病诊疗和研究水平奠定了坚实基础。目前,郝峻巍教授课题组正在进行一系列临床转化研究,包括对进入我国的免疫修饰药物在神经免疫疾病中的应用,神经系统自身免疫抗体的检测以及小分子药物在神经免疫疾病和血管病的免疫治疗等。
秉持“扶伤济世、敬德修业”的校训,一代代首医人诚勤严精、勇攀高峰,必将续写更加华丽的篇章。
