磁性纳米颗粒催化NaClO 降解有机废水研究
2020-10-22姚佳伟杨庆峰陆盛森刘阳桥
姚佳伟,杨庆峰,陆盛森,刘阳桥
(1. 中国科学院上海高等研究院绿色化学工程技术研究中心,上海201210;2. 中国科学院大学,北京100049; 3. 中国科学院上海硅酸盐研究所,上海200050)
在当前对污水排放要求越来越严格的形势下,如何使浓度高、 毒性大且又稳定的有机废水如染料废水达标排放受到广泛关注。 对于这类废水一般采用高级氧化工艺(AOPs)进行处理〔1〕。 但是传统的AOPs 工艺复杂且成本高,为此研究人员开发了基于HClO/NaClO 的AOPs,其基本原理见反应式(1)〔2〕或式(2)〔3〕。其中,作为氧化剂的HClO/NaClO 的价格远比双氧水低,可使处理成本大大降低。 J. Behin 等〔4〕利用NaClO/Fe2+工艺处理高浓度试验废水,处理成本从Fenton 法的96.5 美元/t 降到48.4 美元/t,几乎减少了1 倍;同时反应可以扩展至碱性条件下进行,提升了工艺适用范围。但是在NaClO/Fe2+工艺中,存在需要额外紫外光和催化剂Fe2+损失等问题。 研究表明,对于传统的AOPs 利用Fe3O4、纳米零价铁(NZVI)和α-Fe2O3等作为非均相催化剂, 可使得操作简化和成本降低。 对此,本研究以共沉淀法制备了Fe3O4磁性纳米颗粒(Fe3O4MNPs),将其作为非均相催化剂,探究了其催化NaClO 降解有机废水的性能。另外,研究中发现镍氧化物也能提高NaClO 的氧化能 力〔5-6〕, 因 此 以 水 热 合 成 法 制 备 了NiFe2O4磁 性纳米颗粒(NiFe2O4MNPs),将其与Fe3O4MNPs 进行了对比。
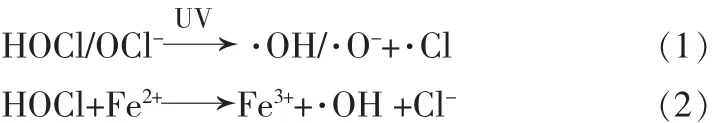
1 材料和方法
1.1 实验药品
六水合氯化铁、对苯醌、异丙醇、亚甲基蓝(MB),购于上海泰坦科技股份有限公司;六水合硫酸镍、六水合硫酸亚铁、次氯酸钠、氢氧化钠、硫酸,购于国药集团化学试剂有限公司。以上药品均为分析纯。实验中使用的水为蒸馏水。 通过碘量法得到所用NaClO的活性氯为5.2%。
1.2 催化剂的制备及表征方法
Fe3O4MNPs 的制备。 将0.2 mol 的六水合硫酸亚铁和0.2 mol 的六水合氯化铁溶于100 mL 蒸馏水中并搅拌,完全溶解后,将溶液转移到烧瓶中,密闭。然后在90 ℃水浴锅中边搅拌边加热, 待温度稳定后,将40 mL 5 mol/L 的NaOH 溶液快速加入到烧瓶中并剧烈搅拌,溶液迅速生成黑色沉淀。快速搅拌1 h,制得具有磁性的Fe3O4纳米颗粒〔7〕。
NiFe2O4MNPs 的制备。 将0.1 mol 的六水合硫酸镍和0.2 mol 的六水合氯化铁溶于100 mL 蒸馏水中,边搅拌边向溶液中缓慢滴加5 mol/L 的NaOH 溶液,至溶液pH 为12,然后置于90 ℃水浴锅中搅拌蒸发1 h。浓缩后将悬浮液置于聚四氟乙烯内衬的水热合成反应釜中,然后在200 ℃的烘箱中放置20 h,制得具有磁性的NiFe2O4纳米颗粒〔8〕。
通过X 射线衍射仪(XRD,Ultima ⅥX,Rigaku)判断制备的纳米催化剂的晶型; 纳米催化剂的形貌和粒度通过场发射扫描电子显微镜(FESEM,S400,Hitachi)进行观察;使用X 射线电子能谱(XPS,KAlpha+,Thermo Fisher Scientific)确定纳米催化剂表面元素的价态;通过振动样品磁强计(VSM,MPMS XL-7,Quantum Design)评估催化剂的磁性能。
1.3 评价和分析催化剂活性方法
选择危害性大且性质稳定的有机染料亚甲基蓝作为模拟有机污染物。 采用UV/vis 分光光度计(DR3900,Hach)在波长664 nm 处测定MB 浓度。 实验中MB 初始质量浓度为20 mg/L。 其他实验条件:通过加入NaClO 使得活性氯投加量为150 mg/L,初始反应pH 为9,催化剂投加量为5 g/L,反应温度为(20±1) ℃。 加入NaClO 前将催化剂在MB 溶液中搅拌(400 r/min)反应30 min,以消除催化剂的吸附影响。结果表明,吸附对催化降解结果的影响可合理地忽略。 采用MB 降解率评价催化剂的催化性能,使用伪一级动力学方程对实验数据进行拟合。
2 结果和讨论
2.1 催化剂表征结果
图1 为制备的催化剂样品的XRD 表征结果。
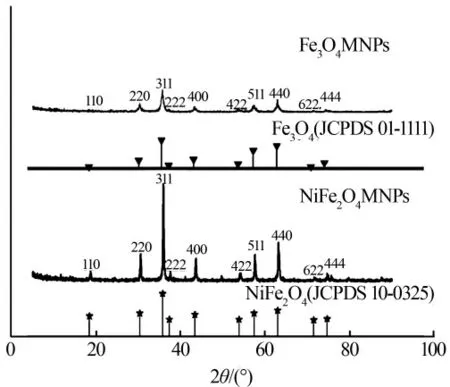
图1 催化剂的XRD 图
由图1 可以看出,Fe3O4和NiFe2O4的衍射峰分别与其标准卡片Fe3O4(JCPDS 01-1111)和NiFe2O4(JCPDS 10-0325)中特征峰的位置和高度比例相吻合,证明成功合成了Fe3O4和NiFe2O4晶体颗粒〔9-10〕。
制备的催化剂样品的表面形貌和纳米结构如图2 所示。

图2 催化剂的FESEM 图
由图2 可知,Fe3O4颗粒为椭球状,直径为20~30 nm;NiFe2O4颗粒大小为70~90 nm,具有明显的尖晶石八面体形貌。
XPS 表征结果表明,对于Fe3O4,其Fe 2p3/2特征峰由Fe(Ⅱ) 2p3/2和Fe(Ⅲ) 2p3/2构成,证明在Fe3O4样品表面存在Fe(Ⅱ)〔11〕。对于NiFe2O4,Ni 2p 峰位置为872.23 eV 和854.64 eV,分别属于Ni(Ⅱ) 2p1/2和Ni(Ⅱ) 2p3/2特征峰,证明在NiFe2O4样品表面存在Ni(Ⅱ)〔12〕。 通过分析2 种样品的VSM 磁滞回线可知,制备的Fe3O4和NiFe2O4的饱和磁化强度分别为48.4 emu/g 和42.7 emu/g,磁滞回线没有滞后且剩余磁化强度和矫顽力接近0, 表明Fe3O4和NiFe2O4均为超顺磁性物质。通过以上一系列表征,证明成功合成了Fe3O4磁性纳米颗粒和NiFe2O4磁性纳米颗粒。
2.2 催化剂的催化性能
催化剂催化NaClO 降解MB 的性能如图3 所示。
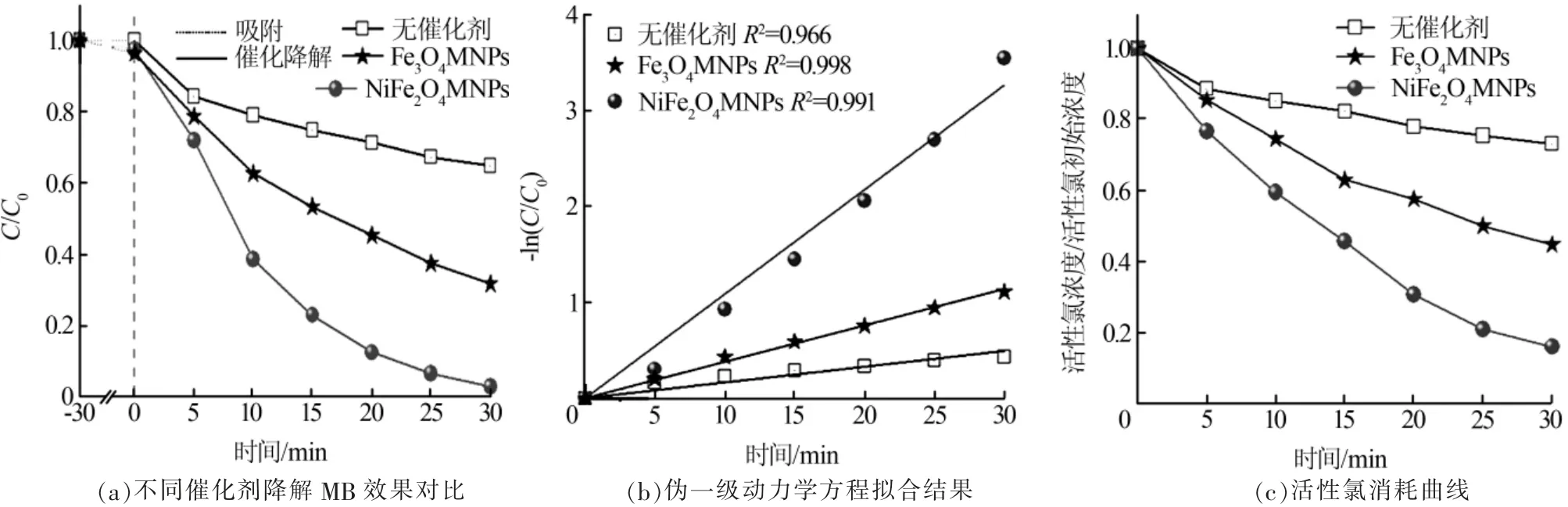
图3 催化剂催化NaClO 降解MB 性能
由图3 可以看出,加入NaClO 搅拌反应30 min后 ,Fe3O4MNPs 体 系 和NiFe2O4MNPs 体 系 对MB 的降解率分别为68.3%和97.2%, 而仅使用NaClO 对MB 的降解率为35.3%。拟合结果表明,NaClO 对MB的降解过程符合伪一级反应动力学,其中不添加催化剂体系、Fe3O4MNPs 体系和NiFe2O4MNPs 体系降解MB 的速率常数分别为0.016 4、0.037 9、0.108 6 min-1。不同体系中活性氯浓度的变化即为次氯酸钠的消耗。 可以看出,不添加催化剂体系、Fe3O4MNPs 体系和NiFe2O4MNPs 体系在反应30 min 时的次氯酸钠消耗量分别为26.7%、55.5%和84.7%。 实验结果表明,Fe3O4MNPs、NiFe2O4MNPs 均能催化NaClO 降解MB, 而且NiFe2O4MNPs 的催化效果更好, 速率约为Fe3O4MNPs 的2~3 倍。
2.3 初始pH 和反应温度对催化降解效果的影响
研究表明,NaClO 在酸性溶液中容易引发如下反应〔13〕:
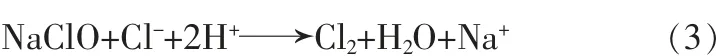
该反应在造成NaClO 大量损失的同时,还会产生剧毒气体Cl2,因此该催化体系适宜在中性和碱性条件下进行。 pH 对催化降解效果的影响如图4 所示。
由图4 可知,在pH=8,反应15min 时,Fe3O4MNPs、NiFe2O4MNPs 体系的MB 降解率分别为65.7% 和90.7%;与pH=9,反应30 min 时的降解效果几乎相同。 pH=8,反应30 min 后,NiFe2O4MNPs 体系的MB降解率为99.7%,几乎完全降解, NaClO 的消耗量达到89.3%;Fe3O4MNPs 体系的MB 降解率也达到了96.6%,NaClO 的消耗量为76.4%。 实验表明,碱性条件下降低反应pH 能明显提升反应速率。
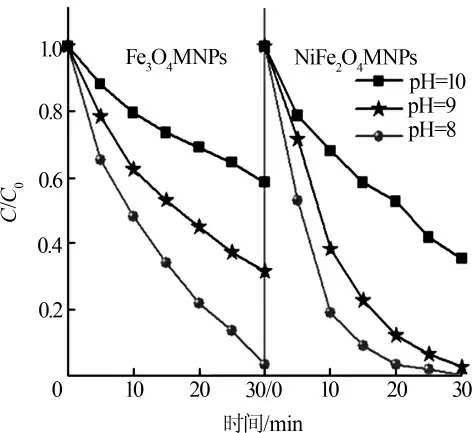
图4 初始pH 对催化降解效果的影响
温度对催化降解效果的影响如图5 所示。
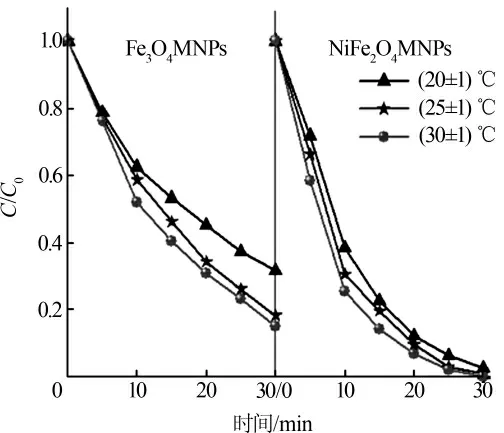
图5 反应温度对催化降解效果的影响
由图5 可以看出,提高反应温度,Fe3O4MNPs 和NiFe2O4MNPs 催化体系均能加快降解MB 的速率,符合一般实验规律。因此在实际应用中,可以利用部分工厂如热电厂产生的余热, 来提高Fe3O4MNPs 和NiFe2O4MNPs 催化体系反应温度, 使之短时间内就能降解废水,进而可减小废水停留时间,加快处理效率,降低成本。
2.4 Fe3O4 和NiFe2O4 磁性纳米颗粒催化作用机理
向系统中分别添加·OH 清除剂异丙醇(1 g/L)和·OOH 清除剂对苯醌(10-4mol/L)〔14〕,考察自由基清除剂对催化降解效果的影响,结果如图6 所示。
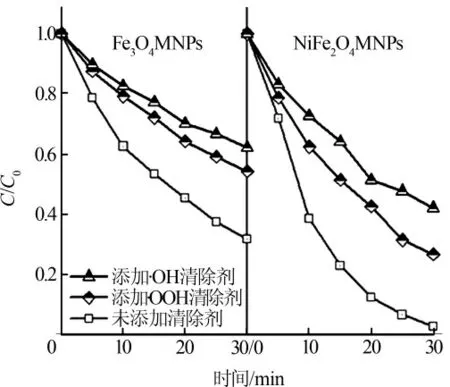
图6 添加自由基清除剂对催化降解效果的影响
由图6 可以看出,清除·OH 后,Fe3O4MNPs 体系和NiFe2O4MNPs 体系对MB 的降解率分别降低了39.3%和30.4%;清除·OOH 后,Fe3O4MNPs 体系和NiFe2O4MNsPs 体系对MB 的降解率分别降低了23.9%和22.6%。 实验表明,Fe3O4MNPs 和NiFe2O4MNPs 能催化NaClO 产生·OH 和·OOH 降解MB, 其中·OH发挥的作用大于·OOH。 由于是在碱性条件下,金属离子浸出极少,催化作用主要发生在催化剂表面。≡Fe 和≡Ni 代表在催化剂表面的Fe 和Ni,催化反应可总结如下:
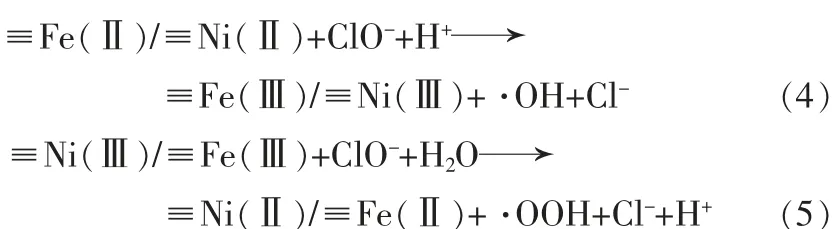
2.5 重复利用实验
将使用后的磁性纳米催化剂颗粒通过钕磁铁从溶液中分离出来,并用蒸馏水多次清洗后,再次应用于降解实验。结果表明,循环使用5 次后,Fe3O4MNPs体系和NiFe2O4MNPs 体系对MB 的降解率分别由初次使用的68.3%、97.2%降至66.1%、94.9%, 表明制备的纳米催化剂性质稳定,重复利用效果好。 同时,Fe3O4MNPs 和NiFe2O4MNPs 均为非均相催化剂,具有超顺磁性且饱和磁化强度较大, 能够在外部磁场作用下与液体快速分离, 撤掉磁场后又能快速在液体中分散,不会有污泥等危废的产生。 在实际应用中,Fe3O4MNPs 和NiFe2O4MNPs 通过搅拌分散在水中后,可通过磁分离机迅速聚集从水中分离,进而回收和重复使用,这将有效降低基于HClO/NaClO 的AOPs工艺的操作难度,具有广阔的工业化应用前景。
3 结论
(1)表征结果表明,通过共沉淀法和水热合成法分别成功地合成了Fe3O4MNPs 和NiFe2O4MNPs。2 种非均相催化剂都能有效地催化NaClO 降解模拟有机污染物亚甲基蓝。
(2)当pH=8,反应30 min 时,NiFe2O4MNPs 体系的MB 降解率达到99.7%,几乎完全降解; Fe3O4MNPs体系的MB 降解率也达到了96.6%。 碱性条件下,降低pH 和适当提升反应温度可以提高催化效率。 自由基清除实验表明,Fe3O4MNPs 和NiFe2O4MNPs能催化NaClO 产生·OH 和·OOH 降解有机污染物。
(3)Fe3O4MNPs 和NiFe2O4MNPs 在 循 环 使 用 后能保持良好的催化活性, 且具有高的饱和磁化强度和超顺磁性, 使用后将有效降低基于HClO/NaClO的AOPs 的操作难度,且没有污泥的产生,具有工业化应用前景。
