急性缺血性卒中大血管闭塞性质的判断与取栓方式和材料的选择
2020-10-21朱其义韩红星王贤军王浩
朱其义,韩红星,王贤军,王浩
2015年一系列血管内治疗随机对照研究阳性结果的发表,促进了中美率先颁布急性缺血性卒中(acute ischemic stroke,AIS)早期血管内治疗指南,给予机械取栓治疗前循环大血管闭塞性AIS最高级别的推荐[1-2]。之后随着研究的进一步深入,血管内治疗时间窗从6 h拓宽到24 h[3-4],促进相关指南不断更新。同时医学工程学、材料学的长足发展,球囊导引导管、Navien为代表的中间导管和具有抽吸功能的ACE导管等相继问世,为取栓治疗提供了良好的技术支撑和新的手段;闭塞靶血管取栓扩展到大脑中动脉M2/M3段、大脑前动脉A2段和后循环。在血管开通治疗中,直接决定治疗获益并影响患者预后的关键在于能否尽早开通闭塞血管,挽救缺血半暗带[5]。因此,提高手术质量,快速、安全地完成手术,需要术者正确判断闭塞病变的性质,并选择适合的取栓方式和手术材料。
1 大血管闭塞病变性质的判断
AIS大血管常见闭塞病变性质有3种:动脉粥样硬化狭窄性闭塞、栓塞性闭塞、动脉夹层性闭塞。可通过病史、起病形式和脑血管造影征象鉴别,个别病例需在术中进一步甄别。
1.1 病变性质初步判断
1.1.1 动脉粥样硬化狭窄性闭塞 动脉粥样硬化性狭窄是导致缺血性卒中的重要原因之一,亚裔人群颅内动脉粥样硬化比例更高(30%~50%)[6-7]。常见支持狭窄性闭塞的证据:①既往有该处动脉狭窄病史(TCD、CTA、MRA或DSA证据);②术前CT或MRI上责任血管供血区有分水岭梗死征象;③首过效应,即微导丝携带微导管通过闭塞段后,回撤微导管造影可见闭塞局部纤细的造影剂通过;④可显影支架有明显的“束腰征”者,动脉粥样硬化性狭窄性闭塞可能大。
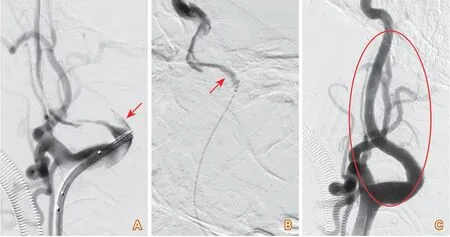
图1 动脉夹层性闭塞病例
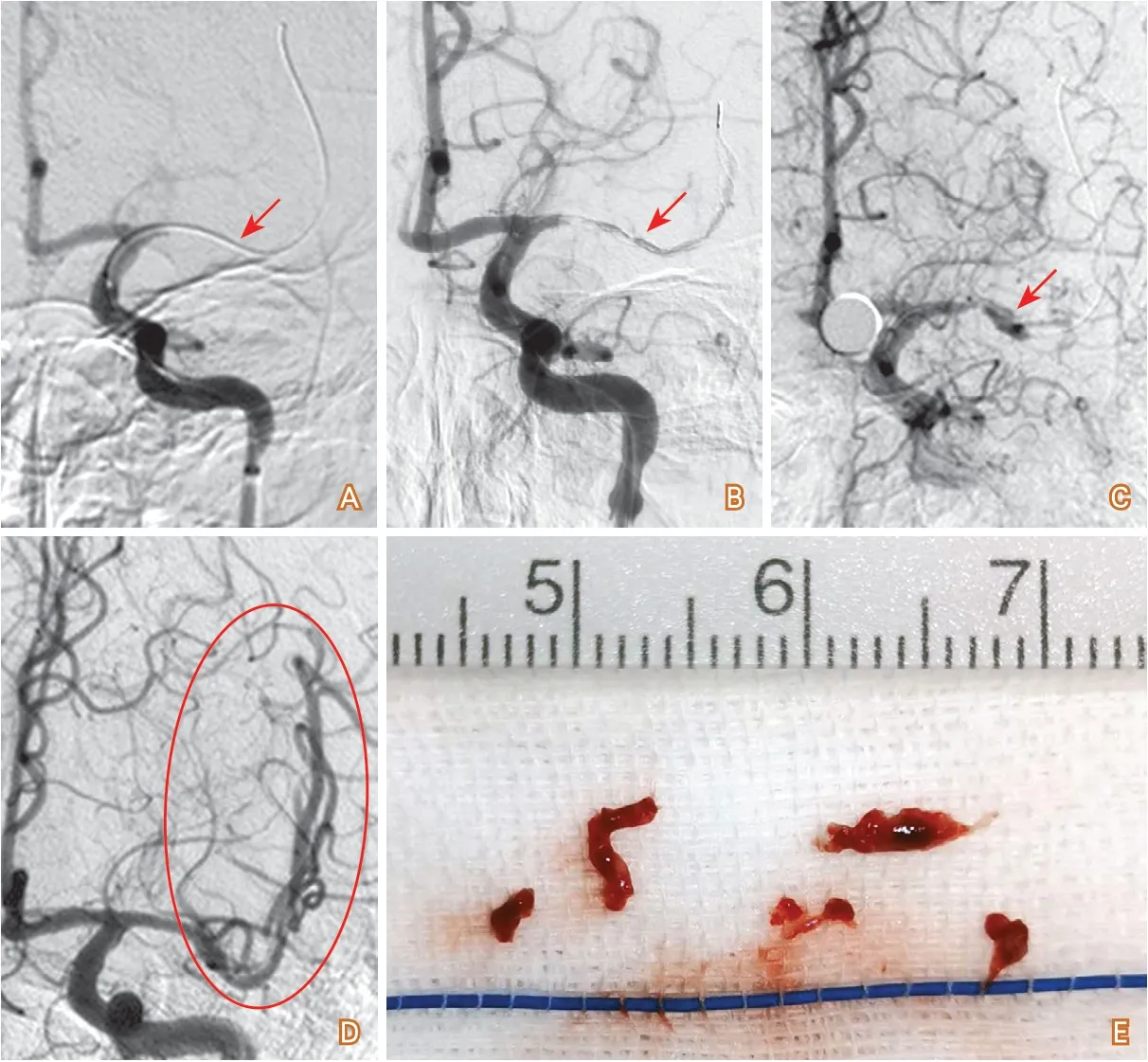
图2 血栓呈橡皮样栓子的栓塞性病例
1.1.2 栓塞性闭塞 脑栓塞栓子主要来源于心脏、大动脉和静脉反常栓塞,以心源性栓塞为主占全部缺血性卒中的14%~30%[8-9]。急骤起病是该类闭塞的临床特点,伴有以下情况支持栓塞性闭塞:①有心脏病史、骨科外伤史、美容脂肪填塞史等易脱落栓子的疾病史;②术中造影发现闭塞血管近端有重度血管狭窄;③造影见闭塞部位高密度血栓影;④球囊扩张后造影,没有造影剂通过,或纤细造影剂通过但维持时间较短。
1.1.3 动脉夹层性闭塞 脑动脉夹层导致的卒中发病率低,仅占所有缺血性卒中的2%。颈部外伤史、按摩和颈椎复位是动脉夹层的常见诱因;脑动脉夹层多见于颈内动脉C1段、椎动脉V3段。脑血管造影可见动脉血管串珠样狭窄或闭塞、血管平滑或不规则变细、内膜悬垂,“双腔征”是其最有力的确诊依据[10-12](图1)。
1.1.4 复合闭塞 常见于近端狭窄性闭塞或夹层闭塞,局部形成的血栓脱落到远端引起栓塞,如颈内动脉、椎动脉起始部闭塞,继发血栓脱落到颅内;或多个心源性栓子同时栓塞多条血管。
1.2 术中病变性质再判断 对于部分患者造影后仍不能判定病变性质或证据不充分者,首先使用取栓支架,根据取栓情况及造影特征,来判断血管闭塞的性质。具体可见以下几种情况:①颅内闭塞释放取栓支架后,造影见闭塞血管血流充盈良好,但回收取栓支架未能取出血栓,即刻造影血管完全闭塞,动脉夹层可能性大;②取栓支架释放后无复流或少量血流通过,未能取出血栓,造影见局部血流通过并能维持一定时间者,支持狭窄性闭塞;③取出质地较硬的紫黑色团块状尤其是韧性较高的类橡皮样或胶冻样血栓者,支持栓塞性闭塞(图2~图3)。
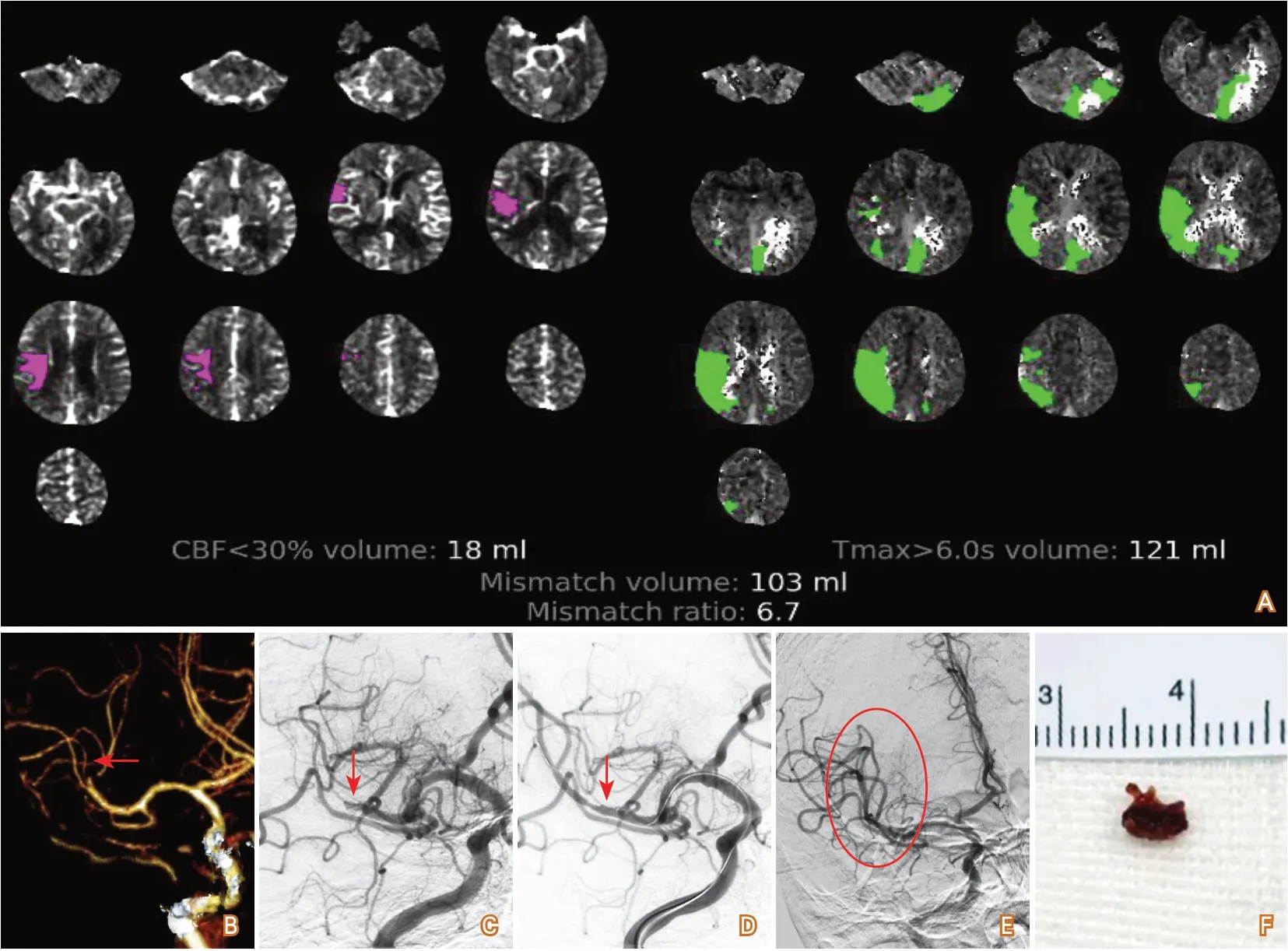
图3 心源性栓塞病例
2 大血管闭塞性血管内治疗手术方式
AIS大血管闭塞病变性质是选择手术方式和取栓材料的基础,同时应参考手术路径,亦应追求用最小的经济成本完成手术。目前常用的取栓方式有支架取栓、抽吸导管取栓、球囊/支架成形术及动脉溶栓,根据不同病情选择其中一种或几种方式联合取栓。
2.1 支架取栓 取栓支架最早用于机械取栓,是已被证实具有显著疗效的取栓材料,也作为拥有最多循证医学证据的取栓方式被多国指南优先推荐[13-15]。支架取栓可用于大多数机械取栓手术。
对于栓塞性闭塞,多数病例优先使用支架取栓,如Trevo取栓系统、Solitaire FR取栓系统、Revive取栓系统等均可使用,但应注意病变血管内径,以选择尺寸相当的支架。一般来说,大脑中动脉M1段闭塞使用直径4 mm取栓支架,颈内动脉末端栓塞可使用6 mm取栓支架,大脑中动脉M2、M3和大脑前动脉栓塞应考虑减轻血管内膜损伤,可使用4 mm直径支架不全释放或使用直径更小的取栓支架取栓,后循环闭塞视血管粗细选择支架大小,也有研究显示支架越长取栓效果越好[16]。闭塞性质不明者可试用支架取栓,颅内的动脉夹层性闭塞使用Solitaire取栓支架可能是较好的选择,必要时解脱取栓支架覆盖夹层(图4)。
2.2 抽吸导管取栓 抽吸导管抽吸血栓其优点是手术时间较短和血管内膜损伤较小,亦被多个随机对照研究证实具有较支架取栓非劣性结果[17-18]。和支架取栓类同,更适用于路径好的大脑中动脉和基底动脉栓塞性闭塞,尤其基底动脉尖栓塞,也可用于大脑前动脉A2、A3段和大脑中动脉M2、M3段较细血管的闭塞(图5)。
2.3 球囊/支架成形术 适用于颅内外狭窄性病变,球囊扩张不能维持有效血流时进行支架置入[19-20],或支架置入作为机械取栓术的补救措施[21]。颈内动脉和椎动脉狭窄性闭塞常常在其远端有大量血栓,造影可见高密度血栓影,应使用保护伞或近端保护装置阻断血流,避免血栓逃逸;大脑中动脉、大脑前动脉、基底动脉和大脑后动脉狭窄性闭塞,据笔者团队多年的临床经验在这些血管远端未见大量血栓形成,故无须使用保护措施,推测与穿支血管较多,有一定的吻合支血流有关,闭塞局部可见少量新鲜血栓,随着微导丝和微导管通过闭塞段脱落到远端或因抗栓药物使用以及血流冲击而溶解。
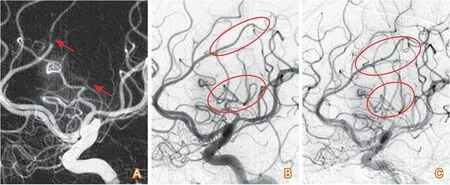
图5 大脑前动脉A3和大脑中动脉M3段栓塞ACE导管取栓
支架成形术对于动脉夹层可能更适合,不仅可以封闭夹层开口,还能挤压假腔,恢复真腔血流,避免动脉夹层复发。
无论是否桥接静脉溶栓药物,在拟实施球囊/支架成形术前都应给予有效的抗血小板药物,避免球囊/支架损伤血管壁诱发急性血栓形成。口服抗血小板药物起效慢,在术中宜使用替罗非班静脉给药,维持12~24 h,然后在影像排除颅内出血后桥接口服双联抗血小板治疗。颅内支架患者双联抗血小板治疗维持6个月,颅外支架置入者维持1个月。双联抗血小板治疗结束后,服用单一抗血小板药物。
2.4 微导管超选择动脉溶栓 经动脉溶栓治疗所起的作用有限,可作为机械取栓的补充治疗手段,但必须是在尝试机械取栓效果不佳时使用而不是作为主要治疗手段[22]。对于发病<4.5 h、路径较迂曲、内径<2 mm的血管,也可考虑微导管超选动脉溶栓。
3 手术材料的选择与组合
取栓过程中,常用的辅助材料包括:导引材料(如导引导管、球囊导引导管和长鞘)、中间导管(如Navien、Dac)等,其选择取决于取栓方式。以下简单介绍目前较常用的辅助材料及组合:
(1)8F/9F球囊导引导管+取栓支架,适合大多数栓塞性闭塞,尤其血栓负荷量较大时。研究证实BGC配合支架取栓或联合中间导管/抽吸导管抽吸,可显著减少血栓碎片逃逸,降低远端栓塞事件,并可显著缩短取栓时间,提高血管再通率[23](图6)。
(2)8F/9F球囊导引导管或6F/7F长鞘+中间导管+取栓支架,使用颅内支撑导管辅助Solitaire FR支架取栓+抽吸技术(Solitaire FR With Intracranial support catheter for Mechanical thrombectomy,SWIM)等,适用于各种栓塞性闭塞取栓。
(3)8F/9F球囊导引导管或6F/7F长鞘+抽吸导管,在直接抽吸取栓技术(A Direct Aspiration First Pass Technique,ADAPT)中使用,适用于各种栓塞性病变的取栓。
(4)明确的单纯颅内动脉狭窄性闭塞,不合并明显血栓者,可使用6F导引导管+球囊/支架。
(5)路径较迂曲的特殊病例,可使用长鞘+抽吸导管+取栓支架,抽吸导管比中间导管有更好的通过性和更大的内腔,更宜于取栓(图7)。
(6)术中材料的匹配:术前应熟练掌握所用材料内外径以及长度,避免材料不匹配延误手术时间。颈内动脉起始部狭窄或夹层,需内径较大的导引导管如8F导引导管或9F球囊导引导管,以便必要时释放颈动脉支架。目前国内已上市的8F球囊导引导管不能通过外径6F的中间导管、5MAX ACE和多数颈动脉支架。
血管内治疗是大血管闭塞性AIS标准的治疗方法,术者应结合病史、发病形式、影像学检查以及脑血管造影等综合判断病变性质,并参考手术路径,选择适宜的手术方式和合适的材料,迅速安全地完成手术。尽管大血管闭塞性AIS血管内治疗已取得显著疗效,但仍存在闭塞血管完全开通率不高、再闭塞和出血等并发症。未来研究的方向仍是致力于使用更有效的方法快速开通闭塞血管,及时恢复缺血区再灌注,降低围手术期并发症,改善患者预后。相信随着取栓材料和技术的不断进步,这些都将会进一步得到改进。
