蒙药地梢瓜的质量标准研究
2020-10-20吴依静喜杰钟国跃苏日娜李辉虎罗维早
吴依静 喜杰 钟国跃 苏日娜 李辉虎 罗维早


摘 要 目的:建立蒙药地梢瓜的质量标准。方法:采用薄层色谱法(TLC)鉴别地梢瓜药材;按2015年版《中国药典》(四部)方法检测药材中的水分、总灰分、醇溶性浸出物含量;采用高效液相色谱法(HPLC)测定药材中地梢瓜苷的含量。结果:TLC图斑点清晰,供试品(地梢瓜药材)与对照品(地梢瓜苷)在相应位置上均显示相同的黄绿色荧光斑点。22批地梢瓜药材的水分含量为6.18%~12.97%,总灰分含量为4.64%~7.95%,醇溶性浸出物含量为12.46%~32.70%。地梢瓜苷检测进样量的线性范围为0.048~3.050 μg(R 2=0.999 9);精密度、稳定性、重复性、耐用性试验的RSD均小于1%;加样回收率为104.03%~106.36%(RSD=0.96%,n=6);22批地梢瓜药材中地梢瓜苷的含量为0.006 2%~0.130 5%。结论:初步拟定地梢瓜中水分不得超过11.50%,总灰分不得超过7.50%,醇溶性浸出物不得少于17.00%,地梢瓜苷含量不得少于0.05%。所建质量标准可用于蒙药地梢瓜药材的质量控制。
关键词 蒙药;地梢瓜;地梢瓜苷;薄层色谱法;高效液相色谱法;含量测定;质量标准
中图分类号 R282;R917 文献标志码 A 文章编号 1001-0408(2020)18-2230-05
DOI 10.6039/j.issn.1001-0408.2020.18.10
ABSTRACT OBJECTIVE: To establish the quality standards of Mongolian medicine Cynanchum thesioides. METHODS: TLC was used for the qualitative identification of C. thesioides. According to 2015 edition of Chinese Pharmacopeia (part Ⅳ), the moisture, total ash and ethanol-soluble extract were determined. HPLC method was used to determine the content of thesioideoside in C. thesioides. RESULTS: TLC spots were clear, there were same yellow green fluorescent spots on the corresponding position of the sample (C. thesioides) and control (thesioideoside). In 22 batches of samples, contents of moisture were 6.18%-12.97%, total ash were 4.64%-7.95%, ethanol-soluble extract were 12.46%-32.70%. The linear range of thesioideoside were 0.048-3.050 μg(R 2=0.999 9). RSDs of precision, stability, repeatability and durability tests were all less than 1%. The recoveries were 104.03%-106.36% (RSD=0.96%, n=6). The contents of thesioideoside in 22 batches of C. thesioides were 0.006 2%-0.130 5%. CONCLUSIONS: It is suggested that the moisture and total ash should not exceed 11.50% and 7.50%, respectively; the contents of ethanol-soluble extract and the sioideoside are no less than 17.00% and 0.05%, respectively. The established quality standards can be used for quality control of Mongolian medicine C. thesioides.
KEYWORDS Mongolian medicine; Cynanchum thesioides; Thesioideoside; TLC; HPLC; Content determination; Quality standards
蒙藥“特莫-呼呼/特莫恩-胡乎(音译)”,又称地梢瓜,为萝藦科植物地梢瓜[Cynanchum thesioides(Freyn)K. Schum.]的干燥果实,味苦,性钝、燥、糙、凉,具有清“协日”、止泻的功效[1]。在临床上,地梢瓜常被蒙医用于治疗黄疸、腑“协日”热、肠刺痛、菌痢、热泻等症,同时该药也是治疗肠热痢疾、腹泻的经典方剂“茵达日-4汤”的君药[1]。目前,地梢瓜药材尚无国家标准,仅在《卫生部药品标准(蒙药分册)》[2]和《内蒙古蒙药材标准》[3]中以“特莫-呼呼/地梢瓜”之名收载,以种子入药且这两种标准中仅有地梢瓜种子性状和显微鉴别,无其余药用部位水分、总灰分检查和浸出物含量测定,也未有其主要成分的薄层色谱鉴别(TLC)和含量测定。此外,据市场和使用现状调查结果显示,市售及临床均以地梢瓜果实入药。因此,有必要对其质量标准进行完善,以全面有效地控制药材质量。有文献发现,地梢瓜主要含有三萜类、甾体类、黄酮类、酚酸类等化学成分[4-7],具有抗衰老、抗氧化、止泻等药理作用[8-11];其黄酮类主要成分地梢瓜苷对神经细胞脂质过氧化反应、DNA损伤及人脐静脉内皮细胞均有抑制或保护作用[12-13]。基于此,本研究采用TLC法对地梢瓜药材进行鉴别,同时按2015年版《中国药典》(四部)方法对其水分、灰分、醇溶性浸出物等进行考察;采用高效液相色谱法(HPLC)对其主要成分地梢瓜苷进行定量分析,旨在为完善其质量标准提供参考。
1 材料
1.1 仪器
LC-20A型HPLC仪,包括LC-20 AT型输液泵、SPD-M20A型二极管阵列检测器、SIL-20A型自动进样器、CTO-20A型柱温箱、CBM-20A型系统控制器、Lab LC solutions工作站(日本Shimadzu公司);2100型紫外-可见分光光度仪(北京瑞利分析仪器有限公司);BT 124S型十万分之一电子天平[赛多利斯(上海)贸易有限公司];KQ-5200 DB型超声波清洗机(昆山市超声波仪器公司);DE-100g型万能粉碎机(浙江红景天工贸有限公司);SX-2.5-10型箱式电阻炉控制箱(天津市泰斯特仪器有限公司);HH-W420型数显恒温水浴锅(深圳市欧莱博科技有限公司);DHG-Ⅲ型电热鼓风干燥箱(上海新苗医疗器械制造有限公司)。
1.2 药品与试剂
22批地梢瓜药材(编号:S1~S22),经江西中医药大学药学院钟国跃研究员鉴定为萝藦科植物地梢瓜[C. thesioides(Freyn)K. Schum.]的干燥果实,其信息来源详见表1。所有药材样品均于60 ℃干燥48 h后粉碎,过二号筛,备用。硅胶G薄层板(青岛谱科分离材料有限公司);地梢瓜苷对照品(本课题组自制,纯度:>98%);乙腈、甲酸为色谱纯,其余试剂均为分析纯,水为超纯水。
2 方法与结果
2.1 TLC鉴别
取22批地梢瓜药材(编号:S1~S22)粉末5 g,加入50%乙醇100 mL,超声(功率:500 W,频率:40 kHz,下同)处理30 min,滤过,滤液蒸发至无醇味后,以等体积乙酸乙酯萃取3次,再以等体积正丁醇萃取2次,合并正丁醇萃取液,挥干,残渣加入甲醇1 mL使溶解,作为供试品溶液(Ⅰ)。精密称取地梢瓜苷对照品适量,加入甲醇制成每l mL含1 mg的溶液,作为对照品溶液(Ⅰ)。按照2015版《中国药典》(四部)通则“薄层色谱法”[14]操作,吸取上述供试品溶液、对照品溶液各5 μL,分别点于硅胶G薄层板上,以正己烷-乙酸乙酯-无水乙醇-水-甲酸(2.5 ∶ 2.5 ∶ 4 ∶ 0.5 ∶ 0.5,V/V/V/V/V)为展开剂,展距8 cm,饱和20 min后,展开,取出,烘干,喷以3%三氯化铝溶液显色,于105 ℃加热至斑点清晰,置于紫外灯(365 nm)下检视。结果,在供试品TLC中,于对照品TLC相应位置上显相同的黄绿色荧光斑点,详见图1。
2.2 水分
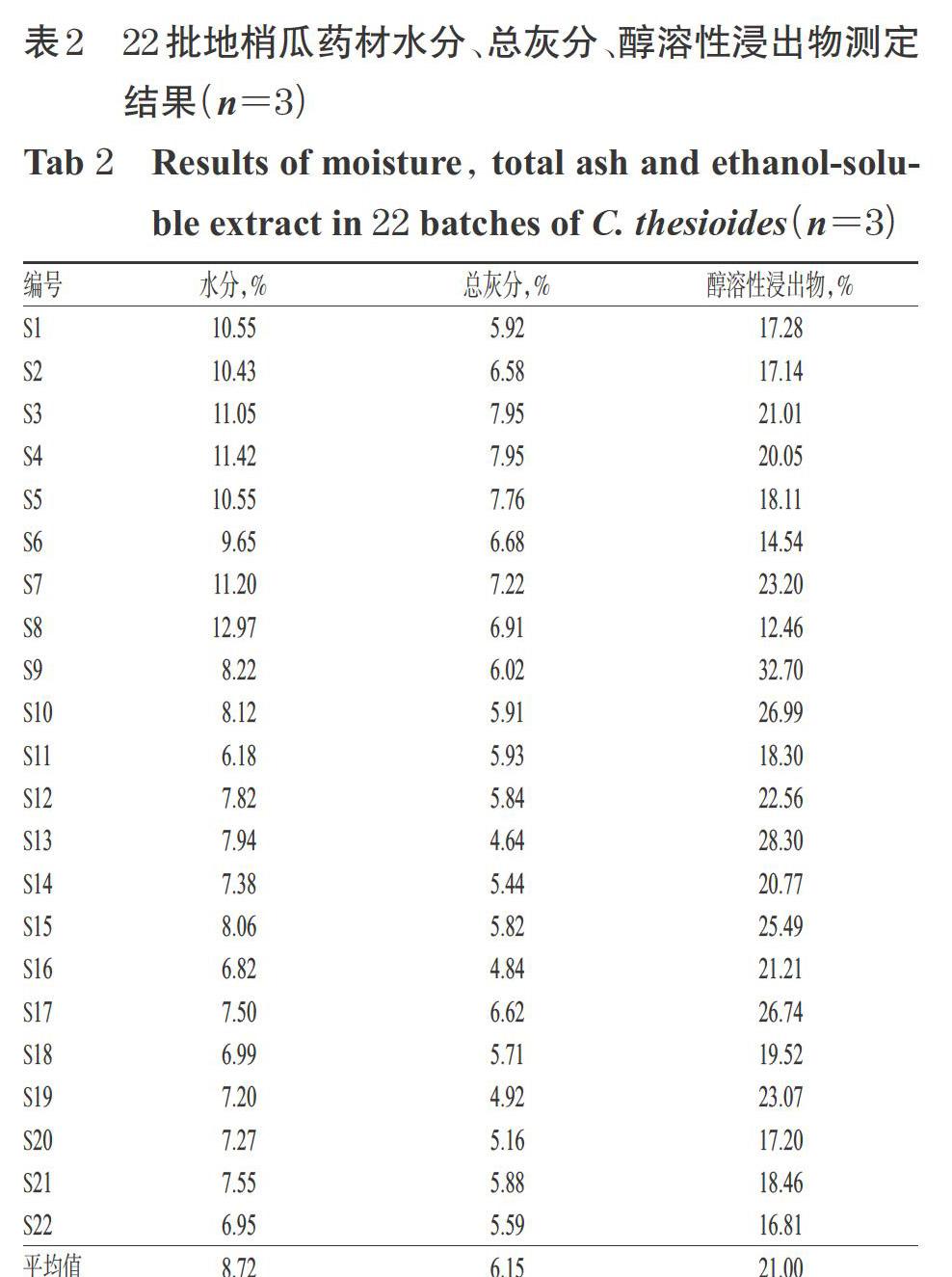
取22批地梢瓜药材(编号:S1~S22)粉末适量,精密称定,按2015年版《中国药典》(四部)通则“水分测定法”项下“烘干法”[14]测定水分,每批平行3次。结果,22批地梢瓜药材水分含量为6.18%~12.97%,平均值为8.72%,详见表2。将22批地梢瓜药材水分含量均值上浮30%[15],作为水分限度标准,即药材水分含量不得超过11.50%。
2.3 总灰分检查
取22批地梢瓜药材(编号:S1~S22)粉末适量,精密称定,按2015年版《中国药典》(四部)通则“灰分测定法”项下“总灰分测定法”[14]测定总灰分,每批平行3次。结果,22批地梢瓜药材总灰分为4.64%~7.95%,平均值为6.15%,详见表2。将22批地梢瓜药材总灰分均值上浮20%[15],作为总灰分限度标准,即药材总灰分不得超过7.50%。
2.4 醇溶性浸出物检查
取22批地梢瓜药材(编号:S1~S22)粉末适量,精密称定,按2015年版《中国药典》(四部)通则“浸出物测定法”项下“醇溶性浸出物测定法(热浸法)”[14]以50%乙醇热浸测定醇溶性浸出物含量,每批平行3次。结果,22批地梢瓜药材醇溶性浸出物含量为12.46%~32.70%,平均值为21.00%,详见表2。将22批地梢瓜药材醇溶性浸出物含量均值下浮20%[15],作为醇溶性浸出物限度标准,即药材醇溶性浸出物不得少于17.00%。
2.5 含量测定
2.5.1 对照品溶液(Ⅱ)的制备 精密称取地梢瓜苷对照品适量,加入50%乙醇,制成每1 mL含305 μg的对照品溶液(Ⅱ)。
2.5.2 供试品溶液(Ⅱ)的制备 取地梢瓜药材粉末约1.0 g,精密称定,置于具塞锥形瓶中,精密加入50%乙醇25 mL,称定质量,超声处理30 min,放冷,再次称定质量,用50%乙醇补足减失的质量,摇匀,滤过,取续滤液,即得。
2.5.3 检测波长的确定 取“2.5.1”项下对照品溶液(Ⅱ)适量,加入50%乙醇稀释,制成质量浓度为0.76 μg/mL的检测溶液,使用紫外-可见分光光度仪于190~900 mn全波长范围内进行扫描。结果,检测溶液在254 nm波长处有最大吸收,故选择该波长为检测波长,详见图2。
2.5.4 色谱条件 色谱柱:Inertsustain C18(250 mm×4.6 mm,5 ?m);流动相:乙腈(A)-0.4%甲酸水溶液(B),梯度洗脱(0~10 min,15%A→28%A;10~12 min,28%A→29%A;12~15 min,29%A→30%A;15~17 min,30%A→95%A);流速:1.0 mL/min;柱温:30 ℃;检测波长:254 nm;进样量:20 μL。
2.5.5 系统适用性试验 取上述对照品溶液(Ⅱ)、供试品溶液(Ⅱ)、空白溶液(50%乙醇溶液)适量,按“2.5.4”项下色谱条件进样测定,记录色谱图。结果,地梢瓜苷的保留时间约为13 min,其与相邻峰的分离度均大于1.5,理论板数按地梢瓜苷计应不低于3 000,空白溶液对测定无干扰,详见图3。
2.5.6 线性关系考察 取“2.5.1”项下对照品溶液(Ⅱ)适量,加入50%乙醇稀释,制成质量浓度分别为152.5、76.25、38.13、19.06、9.53、4.76、2.38 μg/mL的系列线性溶液,分别精密吸取20 μL,按“2.5.4”項下色谱条件进样测定,记录色谱图。以地梢瓜苷进样量(X,μg)为横坐标、峰面积(Y)为纵坐标进行线性回归。结果,地梢瓜的回归方程为Y=2 023 470.17X-12 998.29(R 2=0.999 9),表明地梢瓜苷进样量在0.048~3.050 μg范围内与峰面积的线性关系良好。
2.5.7 定量限与检测限考察 取“2.5.6”项下质量浓度为4.76 μg/mL的线性溶液适量,用50%乙醇倍比稀释,按“2.5.4”项下色谱条件进样测定,以信噪比10 ∶ 1、3 ∶ 1分别计算定量限、检测限。结果,地梢瓜苷的定量限为1.19 μg/mL,检测限为0.53 μg/mL。
2.5.8 精密度试验 取“2.5.6”项下质量浓度为9.53 μg/mL的线性溶液适量,按“2.5.4”项下色谱条件连续进样测定6次,记录峰面积。结果,地梢瓜峰面积的RSD为0.02%(n=6),表明仪器精密度很好。
2.5.9 穩定性试验 取“2.5.2”项下供试品溶液(Ⅱ)(编号:S1)适量,分别于室温下放置0、6、10、16、18、24 h时,按“2.5.4”项下色谱条件进样测定,记录峰面积。结果,地梢瓜苷峰面积的RSD为0.66%(n=6),表明供试品溶液于室温下放置24 h内稳定性良好。
2.5.10 重复性试验 取地梢瓜药材(编号:S1)粉末约1.0 g,精密称定,共6份,按“2.5.2”项下方法制备供试品溶液(Ⅱ),再按“2.5.4”项下色谱条件进样测定,记录峰面积并按外标法计算地梢瓜苷含量。结果,地梢瓜苷的平均含量为0.074 4%(RSD=0.80%,n=6),表明方法重复性好。
2.5.11 加样回收率试验 取地梢瓜药材(编号:S1)粉末约0.41 g,精密称定,共6份,加入“2.5.1”项下对照品溶液(Ⅱ)1 mL,按“2.5.2”项下方法制备供试品溶液,再按“2.5.4”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表3。
2.5.12 耐用性试验 取地梢瓜药材(编号:S1)粉末适量,按“2.5.2”项下方法制备供试品溶液(Ⅱ),再按“2.5.4”项下色谱条件以不同进样量、流速、柱温、色谱柱进样测定,记录峰面积并按外标法计算地梢瓜苷含量。结果,地梢瓜苷含量的RSD均小于0.80%(n=3),表明方法耐用性良好,详见表4。
2.5.13 样品含量测定 分别取22批地梢瓜药材(编号:S1~S22)粉末适量,按“2.5.2”项下方法制备供试品溶液(Ⅱ),再按“2.5.4”项下色谱条件进样测定,平行测定3次,记录峰面积并按外标法计算地梢瓜苷含量。结果,22批地梢瓜药材中地梢瓜苷含量为0.006 2%~0.130 5%,平均含量为0.069 7%(n=3)[(该平均值为将所有数据采用G检验和D检验[16],排除异常值(本试验中S9样品所测结果异常)后所得],详见表5。将22批地梢瓜药材地梢瓜苷平均含量下浮25%[15],作为含量限度标准,即地梢瓜苷含量不得少于0.05%。
3 讨论
3.1 药用部位的选择
藏、蒙医药经典《医药月帝》[17](藏文本汉译名为《月王药诊》,约8世纪)中记载,药材“度格模农”(药材藏文名
3.2 TLC条件筛选
本研究前期对不同展开系统[三氯甲烷-甲醇-甲酸(6 ∶ 3 ∶ 1,V/V/V)、环己烷-乙酸乙酯-丙酮-冰醋酸(2.5 ∶ 3.5 ∶ 1,V/V/V)、正己烷-乙酸乙酯-无水乙醇-水-甲酸(2.5 ∶ 2.5 ∶ 4 ∶ 0.5 ∶ 0.5,V/V/V/V/V)]进行了考察。结果,以正己烷-乙酸乙酯-无水乙醇-水-甲酸(2.5 ∶ 2.5 ∶ 4 ∶ 0.5 ∶ 0.5,V/V/V/V/V)为展开剂时,供试品与对照品色谱在相应位置上显示相同的黄绿色荧光斑点。同时,本研究还考察了在不同相对湿度(18%、88%)及温度(4、35 ℃)条件下TLC法的耐用性。结果在上述条件下,TLC图斑点均清晰,且分离度良好,表明本TLC法耐用性良好。
3.3 浸出物测定方法考察
本研究前期考察了不同浸出溶液(水、25%乙醇、50%乙醇、75%乙醇)、浸出方法(冷浸、热浸)对醇溶性浸出物测定结果的影响。结果,以50%乙醇热浸所得浸出物含量较高,故选择50%乙醇热浸法为浸出物测定方法。
3.4 供试品溶液(Ⅱ)制备方法考察
本研究前期对不同提取溶剂(100%甲醇、70%甲醇、50%甲醇、30%甲醇、95%乙醇、70%乙醇、50%乙醇、30%乙醇)、提取方式(超声、回流)、提取溶剂用量(25、50、100 mL)、提取时间(15、30、60 min)等因素进行了考察,最终确定采用“2.5.2”项下供试品溶液(Ⅱ)的制备方法。此外,在药材粉碎过程中笔者发现,由于地梢瓜果皮和种毛纤维性强,难以粉碎且易起绒,不易过筛,使得取样不均匀,从而导致所测地梢瓜苷含量偏差较大,故将地梢瓜药材样品于60 ℃干燥48 h后再行粉碎。
3.5 限度规定
本研究参照2015年版《中国药典》(四部)[14]对地梢瓜药材的水分、总灰分、浸出物进行了测定,并对地梢瓜苷的含量进行了定量分析;同时,参考相关文献[15],初步拟定地梢瓜水分含量不得超过11.50%,总灰分不得超过7.50%,醇溶性浸出物不得少于17.00%,地梢瓜苷含量不得少于0.05%。
综上所述,本研究所建含量测定HPLC法稳定性、重复性良好,可用于蒙药地梢瓜中地梢瓜苷的含量测定;质量标准可用于蒙药地梢瓜药材的质量控制。
参考文献
[ 1 ] 国家中医药管理局中华本草编委会.中华本草:蒙药卷[M].上海:上海科学技术出版社,2004:151.
[ 2 ] 卫生部药典委员会.中华人民共和国卫生部药品标准:蒙药分册[S].北京:人民卫生出版社,1998:13.
[ 3 ] 内蒙古自治区卫生厅.内蒙古蒙药材标准[S].赤峰:内蒙古科学技术出版社,1987:401.
[ 4 ] 苑辉卿,左春旭.地梢瓜化学成分的研究[J].中国中药杂志,1992,17(12):739-741、763.
[ 5 ] 苑辉卿,左春旭.地梢瓜化学成分的研究[J].药学学报,1992,27(8):589-594.
[ 6 ] 王玎.地梢瓜果实化学成分及三七中皂苷类成分的研究[D].沈阳:沈阳药科大学,2007.
[ 7 ] 李熠,张力,包玉敏,等.地梢瓜叶中总黄酮提取及含量测定[J].化学工程与装备,2012,41(4):32-34.
[ 8 ] 龚谨.药食两用回药地梢瓜对D-半乳糖致衰小鼠模型的抗衰老作用研究[J].中外健康文摘,2013,8(34):74-75.
[ 9 ] 常日辉.内蒙古100种药用植物抗氧化活性的比较研究[D].呼和浩特:内蒙古师范大学,2013.
[10] 喜杰,奥·乌力吉,钟国跃,等.茵达日-4汤中“度格模农”不同基原药材对腹泻大鼠血清电解质及cAMP、ATP-ase的影响[J].中药材,2018,41(4):978-981.
[11] 喜杰,李辉虎,钟国跃,等.蒙药“度格模农”不同基原药材止泻作用及对血清DAO、TNF-α的影响:以蒙药传统经典方剂茵达日-4汤为研究对象[J].中药材,2017,40(9):2202-2205.
[12] 商战平,王德兴,商朝,等.地梢瓜苷对神经细胞脂质过氧化反应和DNA损伤的保护作用实验研究[J].哲里木畜牧学院学报,2000,10(4):8-10、15.
[13] 司艳红,商朝,祝云平,等.地梢瓜苷对人脐静脉内皮细胞的保护作用及机制[J].中成药,2016,38(7):1611-1614.
[14] 国家药典委员会.中华人民共和国药典:四部[S]. 2015版.北京:中国医药科技出版社,2015:57、103、202、204、374、377.
[15] 喜杰,周華蓉,乌查日拉图,等.常用蒙药“度格模农”(止泻木子)的本草考证[J].中国中药杂志,2016,41(20):4267-4273.
[16] 国家质量监督检验检疫总局,国家标准化管理委员会.数据的统计处理和解释正态样本离群值的判断和处理:GB/T 4883-2008[S].2008-07-06.
[17] 哲里木盟蒙医研究所.医药月帝[M].赤峰:内蒙古科学技术出版社,1985:314.
[18] 关布扎布.必用药剂诸品[M].赤峰:内蒙古科学技术出版社,2014:105.
(收稿日期:2020-05-13 修回日期:2020-07-03)
(编辑:陈 宏)
