碳化法去除硫酸锰浸出液中钴、镍的研究
2020-10-09陈晓亮王海峰王家伟赵平源
陈晓亮, 王海峰*,3, 王家伟,3, 赵平源,3
1.贵州大学 材料与冶金学院,贵州 贵阳 550025;
2.贵州省冶金工程与过程节能重点实验室,贵州 贵阳 550025;
3.贵州省电池用锰材料工程技术研究中心,贵州 铜仁 554300
硫酸锰为锰系锂电池正极中最基础、最重要的锰源材料[1]。若硫酸锰材料中钴、镍重金属杂质的含量过高,将直接降低电池的比容量以及充放电次数等关键性能[2],因此在获取高纯硫酸锰溶液时,除杂是其中的重要工艺。
基于我国锰矿贫矿多、富矿多,矿石中的杂质含量高等特点,在净化硫酸锰溶液时普遍存在钴、镍等重金属杂质含量过高、除杂工艺复杂、溶液很难达标等问题。目前除Co、Ni的方法主要有共沉淀法、物理吸附法、硫化物沉淀法等[3,4],共沉淀法是利用Fe(OH)3或Al(OH)3胶体的吸附性能实现对Co、Ni的去除,但此方法在生产过程中存在,Fe、Al离子超标的风险;物理吸附法利用活性炭吸附能力虽强,但存在价格高、用量大等问题,因此只能用作辅助手段除杂[5];硫化物沉淀法[6]可以利用溶度积的差异实现Ni、Co等重金属与Mn的分离,但此方法存在投量大、废渣产率大、锰损失高等缺点,且会引入S杂质及产生H2S等有毒气体。因此,需寻求一种简单、经济、高效的方法去除硫酸锰体系中钴、镍的方法。
本文以纯度为99.995%的CO2为碳化剂,采用碳化沉锰,反溶净化溶液的方法去除钴、镍杂质,此方法较传统的共沉淀法、物理吸附法、硫化物沉淀法等相比,不会引入新的杂质,除杂更彻底,且安全无污染。
1 实验
1.1 实验原料
实验原料为贵州铜仁某电解锰企业经初级净化除杂后的硫酸锰溶液,利用ICP-MS测定溶液成分,结果见表1。
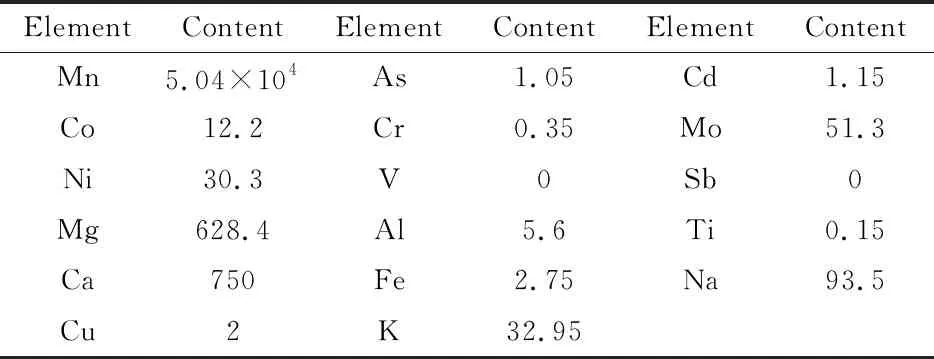
表1 样品元素分析结果/(mg·L-1)
表1结果表明,溶液主要成分为硫酸锰,其中Co、Ni等重金属含量较高,分别为12.2 mg/L、30.3 mg/L。
粗除杂后的硫酸锰结晶产品,经ICP分析结果如表2所示。

表2 硫酸锰结晶杂质ICP成分分析
由表2结果表明,此硫酸锰溶液在一次结晶之后的产品中,Co、Ni、Ca、Mg、Na含量较高,分别为342.9 mg/kg、935 mg/kg、1 263 mg/kg、7 379 mg/kg、1 021 mg/kg,其中Co、Ni含量分别为0.034 2%和0.093 5%。
1.2 实验原理
碳化过程中Mn2+、Co2+、Ni2+存在的行为:
Mn2++CO32-=MnCO3↓
(1)
Co2++CO32-=CoCO3
(2)
Ni2++CO32-=NiCO3
(3)
MnCO3、CoCO3、NiCO3在硫酸锰溶液中25 ℃时的理论沉淀pH如表3所示[7-8]。

表3 25 ℃理论沉淀pH
由式(1)、(2)、(3)可知,在碳化反应的过程中,Mn2+、CO2+、Ni2+会生成MnCO3、CoCO3、NiCO3。经查阅文献[9]可知,CoCO3、NiCO3在酸性条件下具有较好的可溶解性。由表3可知,开始生成碳酸钴和碳酸镍沉淀是的pH在7.6以上,而碳酸锰在pH为6.9时就会完全沉淀。因此在碳化沉锰的过程中,通过合理控制pH,使CoCO3、NiCO3继续留在溶液中,仅使碳酸锰从原溶液中沉淀出来,再将沉淀产品进行反溶,从而达到除杂的目的。
1.3 实验方法
CO2碳化实验装置主要包括CO2气瓶、恒温水浴锅、释放器、温度计和pH计。实验过程:取定量的样品注入反应器中,打开高纯CO2气瓶阀门,向其中通入一定流量的CO2气体,由于气流具有搅拌的作用,故只通过恒温水浴锅控制温度。同时为控制pH保持恒定,向反应器中缓慢滴加pH调节剂A。搅拌反应一段时间后,停止加入调节剂A并停止通入CO2,随后继续搅拌一段时间。反应后的溶液经过滤和多次洗涤后,将获得的碳酸锰沉淀用硫酸返溶得到硫酸锰溶液。实验装置如图1所示。

图1 CO2碳化硫酸锰溶液实验装置:1—CO2 gas cylinder;2—Constant temperature water bath;3—Gas release part;4—thermometer;5—pH meter
1.4 分析方法
本次实验的实验原料和产物中Mn、Co、Ni的含量均采用ICP -MS质谱仪进行测定,ICP -MS质谱仪可以针对无机元素进行定性分析、无机元素定量、半定量分析并具有智能摄谱功能,能较好地实现对实验原料和产物中Mn、Co、Ni含量的测定;碳化产物的物相组成采用XRD分析。
检测仪器如表4所示。

表4 检测仪器
2 结果和讨论
2.1 CO2流量的影响
常温下取锰含量为50 g/L的硫酸锰溶液1 L,控制反应温度35 ℃,反应时间35 min,pH=7.0不变,研究CO2流量对MnSO4中钴、镍净化效果及锰沉淀率的影响如图2所示。
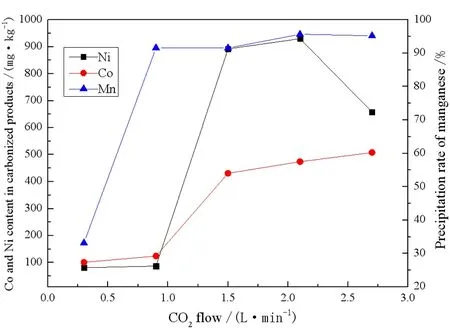
图2 CO2流量对去除效果及锰沉淀率的影响
由图3可知,随着二氧化碳流量的增加,锰的沉淀率一直升高,CO2流量为2.7 L/min时锰的沉淀率达到最高为95.21%。碳化产物中钴、镍杂质的含量随着二氧化碳流量的增加而增加,在CO2流量为0.9 L/min之后钴含量迅速增加,镍含量也增加较快,继续增加CO2流量,杂质含量会增多。综合锰的沉淀率和碳化产物中钴、镍杂质的含量考虑,取最适宜的CO2流量为0.9 L/min。
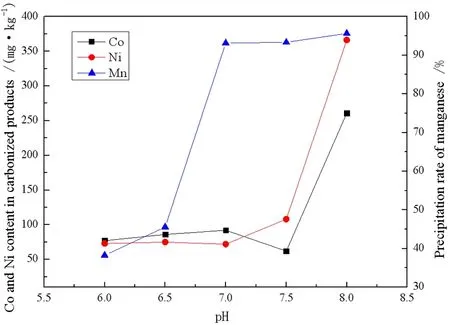
图3 pH对去除效果及锰沉淀率的影响
热力学角度分析可知,增加二氧化碳流量,溶液中碳酸根离子浓度高,则溶液中碳酸根离子的过饱和度越高,愈有利于碳化反应晶核的生成[10],随着CO2流量的增加,碳酸根的浓度增高,碳酸锰沉淀过快,将Co、Ni离子包裹进沉淀中,使沉淀中的Co、Ni杂质含量升高。
2.2 pH值的影响
常温下取锰含量为50 g/L的硫酸锰溶液1 L,控制反应温度25 ℃,反应时间35 min,CO2流量0.9 L/min不变,研究pH值对MnSO4中钴、镍净化效果及锰沉淀率的影响如图3所示。
由图3可知,随着pH值的不断提升,锰的沉淀率先迅速升高,在pH达到6.9时,锰的沉淀率趋于平缓。碳化产物中钴、镍杂质的含量在pH6~7.5之间变化平缓,在pH达到7.5之后,钴、镍杂质在碳化产物中的含量迅速上升。
由表3可知,碳酸锰在pH为6.9时达到沉淀平衡,继续增大pH,锰的沉淀率几乎不再变化,因此锰的沉淀率在pH为7左右时才达到最佳值附近。当溶液的pH升高到7.6、7.7时,溶液碱性增强,CoCO3、NiCO3分别开始生成沉淀,随着pH的升高,CoCO3、NiCO3进入沉淀的量增多,因此杂质含量会迅速升高。
综合锰的沉淀率和碳化产物中钴、镍杂质的含量考虑,取最适宜的pH为7.5。
2.3 反应温度的影响
常温下取锰含量为50 g/L的硫酸锰溶液1 L,控制反应pH=7.5,反应时间35 min,CO2流量0.9 L/min不变,研究反应温度对MnSO4中钴、镍净化效果及锰沉淀率的影响如图4所示。

图4 反应温度对净化效果的影响
由图4可知,随着反应温度的升高,锰的回收率增加,当温度为45 ℃时,锰的沉淀率最高达到97.79%。钴、镍杂质在碳化产物中的含量呈上升趋势。
从动力学角度分析,随着温度的升高,液体黏度减小,粒子布朗运动加快[11],接触碰撞动能增加,晶体合并凝聚长大的趋势上升[12],MnCO3、CoCO3、NiCO3的沉淀量均会增加,因此锰的沉淀率及沉淀中杂质的含量均会增加。在温度为25 ℃时杂质的含量最低,综合考虑选择最适宜反应温度为25 ℃。
2.4 反应时间的影响
常温下取锰含量为50 g/L的硫酸锰溶液1 L,控制反应pH=7.5,反应温度为25 ℃,CO2流量0.9 L/min不变,研究反应时间对MnSO4中钴、镍净化效果及锰沉淀率的影响如图5所示。

图5 反应时间对去除效果及锰沉淀率的影响
由图5所知,随着反应时间的增加,锰的沉淀率升高,但在反应时间在60 min之后略微下降。碳化产物中钴、镍杂质的含量随着反应时间的增加呈现先下降的趋势,在45 min之后含量趋于平缓。且60 min时锰的沉淀率最高,故选择60 min为最适宜反应时间。
综合以上实验的最佳条件为应温度25 ℃,溶液pH为7.5,二氧化碳流量0.9 L/min,反应时间60 min,此条件下锰的回收率为99.36%,碳化产物中Co、Ni的含量分别为26 mg/kg和46 mg/kg。
3 碳化产物分析
在最适宜工艺条件下获得的碳化产物的XRD图如图6所示。
如图6所示,图中MnCO3表现为强峰,说明产物中的Mn主要以MnCO3的形式存在[13],结晶度较好。还存在少量的Ca、Mg等杂质,且杂质主要以碳酸盐和硅酸铁钙的形式存在。
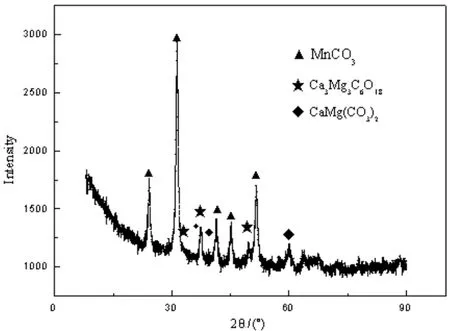
图6 碳化产物XRD图
将碳化产物中的Co、Ni、Ca、Mg元素含量经ICP测定结果如表5所示。

表5 产物元素含量
国家高纯碳酸锰GB10503-89I型标准中钴、镍含量的要求如表6所示。

表6 高纯碳酸锰质量指标
由表5、表6可知,在最适宜的工艺条件下所得的碳化产品中,Co、Ni含量仅为0.003%和0.005%,比硫酸锰一次结晶产物分别降低了0.031 29%和 0.088 5%,符合高纯硫酸锰GB10503-89 I型品的标准。
4 结论
(1)实验确定了碳化法去除硫酸锰浸出液中Co、Ni的最适宜工艺条件为:反应温度25 ℃,溶液pH为7.5,二氧化碳流量0.9 L/min,反应时间60 min。
(2)碳酸锰完全沉淀时的理论pH值为6.9,而Co、Ni杂质在pH大与7.5时会迅速增加,因此合理控制溶液反应的最终pH是此方法的关键。
(3)在最适宜的工艺条件下获得的产品中主要成分为碳酸锰,其中Co、Ni含量分别为0.003%和0.005%,符合碳酸锰GB10503-89 I型品的标准,后续可将碳酸锰产品反溶成硫酸锰。较共沉淀法、物理吸附法、硫化物沉淀法等比,此方法获得的碳酸锰产品中不会引入新的杂质,除杂更彻底、锰的沉淀率高且安全无污染。
