腹腔镜微波消融术联合肝动脉化疗栓塞治疗中晚期肝癌的疗效分析
2020-09-27尤孙武林祥胡逸人潘江华童晓春徐智锋郑志强
尤孙武,林祥,胡逸人,潘江华,童晓春,徐智锋,郑志强
(1.温州医科大学附属第二医院 胃肠外科,浙江 温州 325027;温州市人民医院,浙江 温州 325000,2.普外科,3.中医科)
肝癌是最常见的恶性肿瘤之一,其发病率和死亡率分别居全球第7位和第3位,且逐年提高[1]。手术切除是肝癌治疗的首选[2]。由于肝癌发病早期无特异症状,大多数患者发现时即为中晚期,或由于心肺肝功能障碍,常常无法进行手术治疗[3]。肝动脉化疗栓塞(transarterial chemoembolization,TACE)是治疗不能手术切除肝癌的常用方法,TACE通过肿瘤的供血血管给予化疗药物杀死肿瘤细胞,并用碘化油等栓塞剂封闭血管阻断肿瘤血供以达到治疗目的[4]。超声引导下经皮微波消融术(percutaneous microwave coagulation therapy,PMCT)近年来在临床上应用广泛[5]。相较于传统手术切除,PMCT有升温快、热效高、热场分布均匀、凝固区组织坏死彻底、形态规则和边界清楚的优点,且可以反复操作。但肿瘤靠近肝门、膈顶、胆囊窝等经皮超声盲区时,PMCT便难以操作。而腹腔镜微波消融(laparoscopic microwave ablation,LMWA)可以解决上述困难。LMWA在腹腔镜超声探头引导下插入肿瘤中心,减少正常肝组织受损的范围[6]。本研究回顾性分析2014年1月至2018年12月温州市人民医院LWMA联合TACE及单纯TACE治疗的90例中晚期肝癌病例临床资料,以评估TACE+LWMA联合治疗的安全性和疗效。
1 资料和方法
1.1 一般资料
本组共90例,其中接受LMWA联合TACE治疗46例(研究组),单纯TACE治疗44例(对照组)。两组患者在性别、年龄、一般病情等方面均无统计学差异(P>0.05),具有可比性(详见表1)。本研究经温州市人民医院伦理委员会同意,所有患者均已签署知情同意书。

表1 两组基本资料
1.2 诊断、纳入及排除标准
1.2.1 诊断标准:根据原发性肝癌诊疗规范[7],所有患者均经影像学(增强CT、磁共振或超声造影)、血清肿瘤标志物(AFP)或穿刺活检确诊为肝癌。
1.2.2 纳入标准:(1)经彩超及增强CT等影像学检查明确确诊为肝癌;(2)巴塞罗那肝癌分期(BCLC)B期(中期)、C期(晚期);(3)血小板(PLT)≥50×109/L;(4)凝血酶原时间(PT)延长不超过4 s;(5)未发生其他重要脏器肿瘤转移;(6)未发现肝静脉主干或门静脉癌栓,无淋巴结转移;(7)肿瘤距离肝总管、左右肝的距离≥5 mm;(8)无手术麻醉禁忌证。
1.2.3 排除标准:(1)合并其他严重系统性疾病,无法耐受手术治疗;(2)肝外肿瘤广泛转移;(3)肝功能Child-pugh分级C级。
1.3 治疗仪器
(1)超声设备:丹麦BK公司UltraView Pro Focus 2202;(2)腹腔镜超声探头:丹麦BK公司四向腹腔镜探头8666-RF(末端可屈曲软质探头);(3)微波治疗仪:南京庆海微波电子研究所,MTC-3C型微波凝固治疗仪,微波频率(2 450±50)Hz,功率0~100 W。(4)DSA设备:荷兰Philips公司Allura Xper FD20血管造影系统。
1.4 治疗方法
TACE:(1)以Seldinger技术行股动脉穿刺;(2)透视下插管至腹主动脉、肝固有动脉并造影,确定治疗方案;(3)超选肿瘤相应供血动脉并插管;(4)注入奥沙利铂100~200 mg、表柔比星4 mg灌注化疗;注入表柔比星50 mg与碘油和明胶海绵混合剂进行栓塞;(5)再次行肝动脉造影了解栓塞效果。术前术后改变见图1~2。
LWMA:(1)患者取仰卧位,全身麻醉,脐上缘穿刺,建立压力12~15 mmHg的CO2气腹;(2)在剑突下、左肋缘下或右肋缘下切口分别置入一个12 mm Trocar及两个5 mm Trocar,粘连在肝表面的网膜或其他组织用超声刀或电钩剥离,充分暴露肝脏;(3)根据腹腔镜超声扫描结果决定治疗方案。肿瘤贴近胆囊或已侵犯胆囊,可先行胆囊切除;(4)在超声引导下,微波消融针经皮直接穿入肿瘤中心,设置时间4~10 min、功率80~100 W进行治疗;(5)治疗结束后,退出微波针并行针道消融;(6)消融结束后,再次以超声探头扫查肝脏,必要时可行超声造影。观察术区有无胆漏或出血,必要时放置腹腔引流管。术前术后改变见图3~4。
1.5 观察指标及临床疗效观察标准
患者离院后通过定期门诊和电话随访,跟踪记录病情变化。疗效评价:(1)有效性:首次治疗结束后1个月以改良的实体瘤疗效评价标准(Modified response evaluation criteria in solid tumors,mRECIST)评价近期疗效:①完全缓解(CR):所有治疗病灶动脉期增强均不显影;②部分缓解(PR):治疗病灶的直径总和缩小比率≥30%;③疾病稳定(SD):病灶新增未达PD或缩小未到PR;④疾病进展(PD):出现新发病灶或治疗病灶直径总和新增≥20%。(2)安全性:记录首次治疗结束后发生的不良反应,并用不良反应事件评价标准5.0版(common terminology criteria for adverse events,CTCAE v5.0)进行评价。计算公式:客观有效率=(完全缓解例数+部分缓解例数)/总例数,疾病控制率=(完全缓解例数+部分缓解例数+疾病稳定例数)/总例数。
1.6 统计学分析
2 结果
2.1 近期疗效
与对照组比,研究组的客观有效率(37.0%vs13.6%,P<0.05)和疾病控制率(80.4%vs61.4%,P<0.05),首次治疗效果有优势,详见表2。
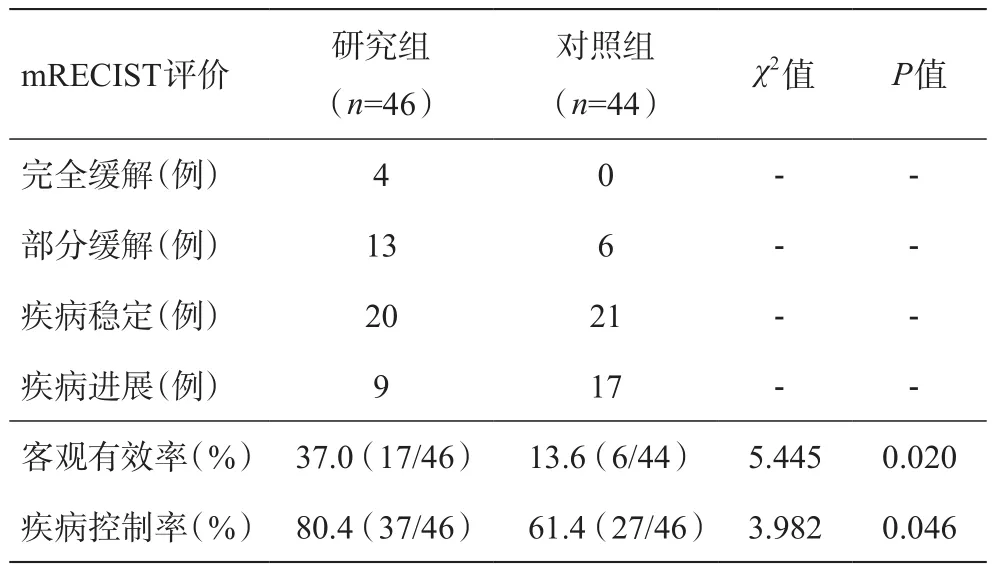
表2 首次治疗mRECIST评价
2.2 远期疗效
截至2018年12月31日,随访率100%。随访时间10~59个月,中位随访时间为20.9个月。死亡76例,存活14例。研究组与对照组的中位生存期21(95%CI10.0~32.0)个月vs12(95%CI5.2~18.8)个月,1年生存率69.6%vs43.5%(P=0.012),2年生存率39.1%vs27.8%(P=0.027),有统计学差异(P<0.05)。
2.3 预后影响因素
单因素分析:BCLC分期、AFP是否大于400 ng/mL、PIVKA是否大于40 μg/L、肿瘤是否多发、治疗方案、首次治疗效果是预后影响因素,见表3和图5~10。多因素分析:AFP大于400 ng/mL、PIVKA大于40 μg/L、肿瘤多发、治疗方案的选择、首次治疗效果是影响预后的独立危险因素,见表4。
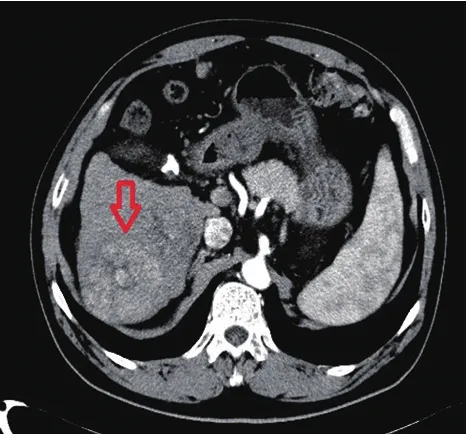
图1 术前CT图像

图2 TACE术后CT图像

图3 TACE术前MRI图像
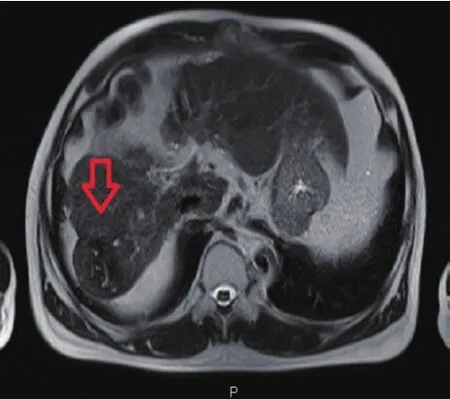
图4 联合治疗后MRI图像

表3 中晚期肝癌患者影响预后的单因素分析
2.4 不良反应
两组病例首次治疗发生的不良反应全部属于CTCAE1、2级,未发现严重不良反应及围术期死亡。对照组未发生主要不良反应,研究组发生2例肝出血,5例胸腔积液,经保守治疗后好转。次要不良反应包括恶心呕吐、腹痛、腹胀及发热,7 d之内可自行好转。两组不良反应发生率比较差异无统计学意义(P>0.05)。见表5。
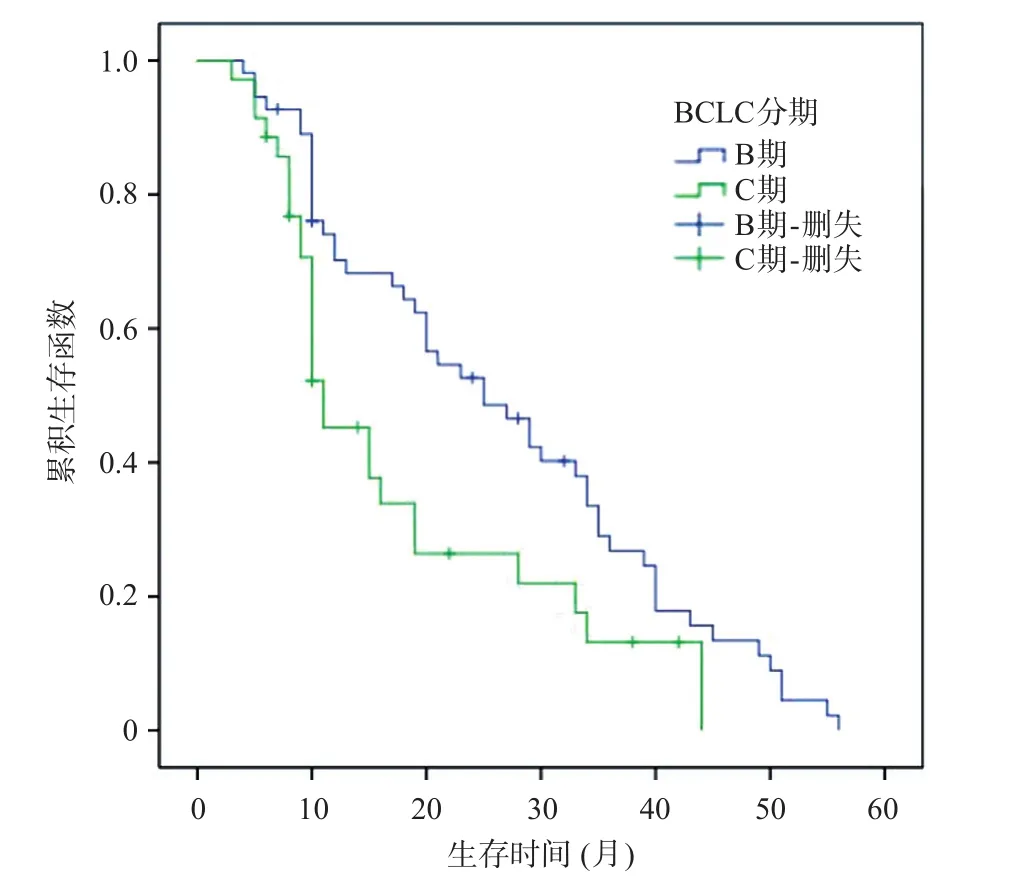
图5 BCLC分期B期、C期的生存曲线

表4 影响预后的COX多因素分析
3 讨论
我国肝癌发病率和病死率均占全世界的50%以上,其在肿瘤病死率中居第2位,仅次于肺癌[8]。大部分患者由于临床分期较晚、身体不耐受等原因不能接受手术。对于此类患者来说,TACE是一种较为理想的治疗方法。但单纯TACE存在肝功能损伤大、栓塞不完全、侧支循环易建立等局限性,治疗效果仍不理想。消融技术已广泛应用于肝癌治疗[9]。消融技术包含射频消融(radiofrequency ablation,RFA)、微波消融(microwave ablation,WMA)、冷冻消融(cryoa-blation,CRA)等。射频消融是利用高频率的电流(375~500 kHz)交替激发引起电极周围组织内的离子高频振动产生高温,致使蛋白质不可逆的凝固性坏死,达到杀死肿瘤细胞的目的。射频消融的治疗效果与组织内的电导率有相关性[10]。人体组织发生凝固性坏死的最佳温度为60~65 ℃,温度高于100 ℃时,人体组织会迅速发生脱水和碳化,导致组织的阻抗增加,从而阻止能量的进一步地沉积[11]。射频消融存在一定的缺陷,如电流的加热过程有其自限性,组织内的液体气化、组织脱水和碳化可逐渐增加组织的电阻抗,进而降低电流通过电场所产生的温度。活体组织的热传导性随着血流灌注进一步降低。WMA避免了射频消融的上述缺点。PMCT应用广泛,但对于特殊部位(胆囊旁、膈顶、肝门)肝癌患者的疗效并不理想。LMWA就避免了PMCT的劣势。LWMA术中同一个点能反复进行穿刺,同时可以避免经皮肝穿刺过程中热效应损伤腹壁,以及肿瘤经过腹壁针道发生转移播散[12]。

图6 AFP≥400 ng/mL和<400 ng/mL的生存曲线
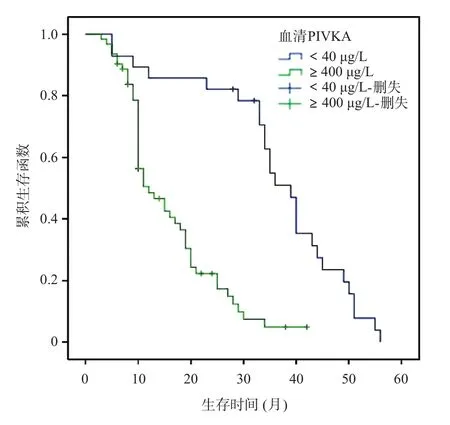
图7 PIVKA≥40 μg/L和<40 μg/L的生存曲线

图8 肿瘤单发和多发的生存曲线

图9 首次治疗是否有效的生存曲线

图10 研究组和对照组的生存曲线
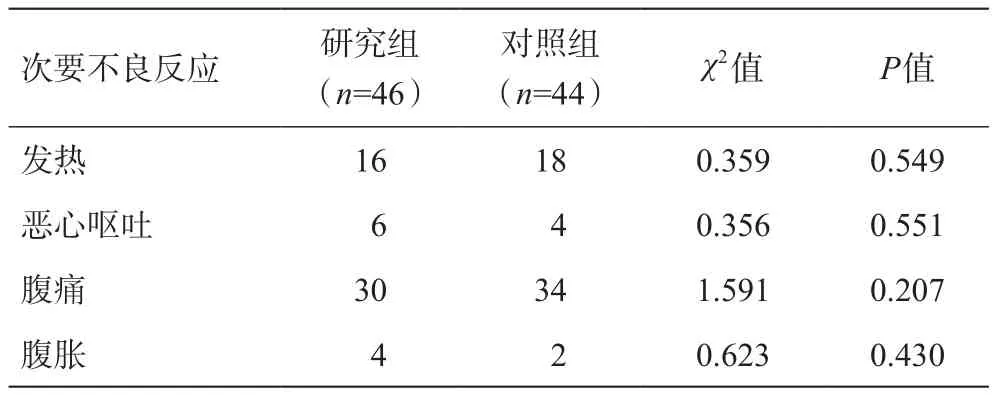
表5 次要不良反应发生情况
TACE联合RFA治疗肝癌已被证实近期疗效良好[13]。TACE和消融互为补充、相互增效,一方面,栓塞剂的沉积有利于定位消融靶灶,另一方面,TACE阻断了供应肿瘤组织的动脉,既可以减少消融术中热量散失,又可以显著减少血道转移的可能性[14]。最后,消融术后肿瘤组织的细胞膜通透性增强有利于发挥化疗药物的作用。TACE联合LWMA治疗肝癌近期疗效好于单纯TACE治疗,远期亦可获得较长生存期[15]。在本研究中,研究组首次治疗的疾病控制率、客观有效率均高于对照组,中位生存时间(21个月)明显长于对照组(12个月),故我们认为联合治疗的近期疗效较好,生存时间长。
异常凝血酶原(protein induced by vitamin k antagonist-II,PIVKA-II)在肝癌患者接受治疗后下降幅度显著大于AFP[16]。在本研究中,我们引入了该指标进行生存分析,提示PIVKA-II≥40 μg/L是影响生存的独立因素,这与纪文斌等[17]所报道的结论一致。本研究证实,AFP≥400 ng/mL与肿瘤个数是影响预后的独立危险因素,故我们认为该指标可以用来评价疗效及进行预后预测。中晚期肝癌难以根治,短时间内快速减少肿瘤负荷能给患者带来生存获益。本研究中,首次治疗是否有效对患者的中位生存期影响显而易见(40个月vs12个月),所以首次治疗方案对疗效影响极大。本次研究中,BCLC分期在单因素分析中提示对预后有影响,而在多因素分析中未被认为是独立的影响因素,这可能和本次研究样本数较少,不能排除选择偏倚有关。
在不良反应事件评价标准(CTCAE 5.0)体系中,主要不良反应是指危及生命、延长住院时间,其余为次要不良反应[18]。TACE因化疗药物注射、碘油栓塞而容易导致次要不良反应。本研究中,未发生主要不良反应,发生的次要不良反应为恶心呕吐、腹胀、腹痛及发热,均可自行好转,故可认为联合治疗是一种安全的治疗手段。
综上所述,腹腔镜微波消融术联合肝动脉化疗栓塞治疗中晚期肝癌近期疗效好,生存期长,严重不良反应发生率低,是一种安全、有效的治疗方案。