凝固漂浮有机液滴-分散液液微萃取结合高效液相色谱法同时测定地表水中多环芳烃和酞酸酯
2020-09-23袁继委王金成徐威力徐方曦卢宪波
袁继委, 王金成, 徐威力, 徐方曦, 卢宪波
(1. 台州市环境监测中心站, 浙江 台州 318000; 2. 中国科学院大连化学物理研究所, 辽宁 大连 116023)
多环芳烃(PAHs)是指含有两个或两个以上苯环的稠环型化合物,主要通过含碳有机物如燃油、木材、煤等在高温情况下的不完全燃烧[1,2]以及肉类烧烤或烹饪过程中形成,是世界公认的持久性难降解半挥发性有机污染物。多环芳烃通过石油污染、空气污染物沉降、工业废水及城市污水处理厂排放的废水而进入江河湖海中。多环芳烃具有致癌、致畸、致突变及生物累积等危害[3],其中16种组分已被欧盟和美国环保署列为优控污染物。
酞酸酯(PAEs)是一类日常生活及工业生产中大量使用的化学品[4]。酞酸酯分为两类:一类是低分子量酞酸酯(酯侧链为1~4个碳),主要用于个人护理品、洗涤剂、香味剂;另一类是高分子量酞酸酯(酯侧链为5个碳以上),主要作为增塑剂添加到塑料制品中。酞酸酯在塑料中与高分子聚合物以较弱的范德华力结合,因此使用过程中易从塑料制品中逸出而进入环境或食品中。研究表明,酞酸酯能够导致人类生殖、内分泌及呼吸系统疾病[5],欧盟、美国环保署及相关国际组织已经将酞酸酯列为优先危险污染物。
为了避免多环芳烃和酞酸酯对环境的污染以及它们对人类健康的危害,准确快速地测定水中多环芳烃和酞酸酯非常重要。但是这些污染物在地表水中的浓度很低,测定前常需要富集浓缩。目前测定水中多环芳烃的方法有液液萃取-气相色谱-质谱法(LLE-GC-MS)[6]、SPE-GC-MS[7]、SPE-HPLC[8-10]、分散液液微萃取(DLLEM)-HPLC[11]、DLLEM-GC[12]等。测定水中酞酸酯的方法有SPE-GC-MS[13]、固相微萃取(SPME)-GC[14]、DLLEM-HPLC[15]、DLLEM-HPLC[16]、DLLEM-GC-MS[17]等。LLE、SPE费时费力,且需要消耗较多的有机溶剂;SPME虽然环境友好,但成本太高;DLLEM简便、快速,成本低廉,但所用的溶剂氯代烃为有毒溶剂。目前,对水中这两类污染物同时测定的方法鲜有报道。凝固漂浮有机液滴-分散液液微萃取(DLLME-SFO)是对DLLEM的改进,它保留了DLLEM简便、快速、成本低廉的优点,但使用低毒的十一醇、十二醇为萃取溶剂,因此更加环境友好。本研究团队前期曾经采用DLLME-SFO-HPLC测定了水中氯代多环芳[18];吴翠琴等[19]采用DLLME-SFO-HPLC测定了水中酞酸酯。本文采用DLLME-SFO前处理方法并结合高效液相色谱-紫外/荧光检测技术,建立了测定地表水中16种多环芳烃和6种酞酸酯的分析方法。
1 实验部分
1.1 仪器、试剂与材料
Agilent 1200型高效液相色谱仪(美国Agilent公司),配紫外和荧光检测器;TDL-4013离心机(上海安亭科学仪器厂); Vortex Genie 2涡旋振荡器(美国Scientific公司)。

1.2 标准溶液配制
用娃哈哈纯净水配制含多环芳烃20 μg/L、酞酸酯1 000 μg/L的标准工作溶液。将此标准工作溶液用去离子水逐级稀释成含多环芳烃0.006 4、0.032、0.16、0.80、4.0 μg/L,含酞酸酯0.32、1.6、8.0、40、200 μg/L的系列标准工作溶液。
1.3 色谱条件
色谱柱为多环芳烃专用柱(SUPELCOSILTMLC-PAH, 150 mm×4.6 mm, 5 μm);柱温:25 ℃;流动相A:乙腈,流动相B:去离子水;流速:2 mL/min。梯度洗脱程序:0~10 min, 50%A~64%A; 10~24 min, 64%A~100%A; 24~29 min, 100%A; 29~30 min, 100%A~50%A, 30~36 min, 50%A。进样量:10 μL。AcL和6种酞酸酯采用紫外检测,检测波长为224 nm;其余15种PAHs采用荧光检测,其激发波长和发射波长见表1。
1.4 水样的萃取过程
准确移取5.0 mL水样,置于10 mL含有0.2 g NaCl的具塞玻璃离心管中,振荡使NaCl溶解;然后用1 mL注射器将500 μL甲醇(含10 μL十二醇)迅速注入离心管中,涡旋振荡2 min后,以4 000 r/min的转速离心5 min,此时萃取剂形成漂浮液珠于液面上方。将离心管置于0 ℃冰水浴中冷却5 min,萃取剂冷凝形成固体黏附在管壁上。将水溶液弃去,用干净的滤纸吸干管壁上的水分。用20 μL甲醇复溶固体,振荡均匀,待测定。
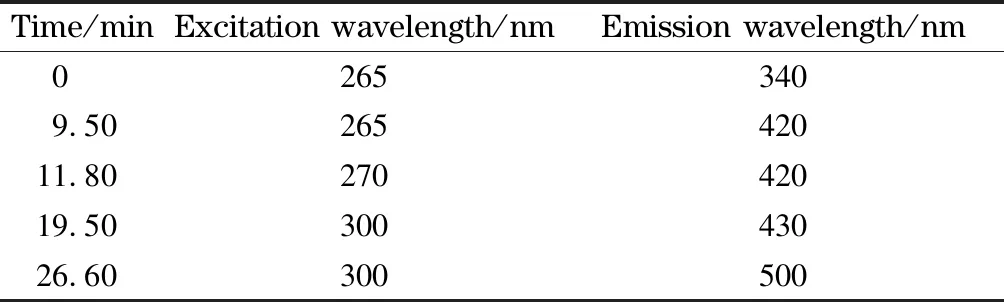
表 1 荧光检测的激发和发射波长

图 1 多环芳烃和酞酸酯的色谱图Fig. 1 Chromatograms of polycyclic aromatic hydrocarbons (PAHs) and phthalate esters (PAEs) a. fluorescence detection; b. UV detection. 1. dimethyl phthalate (DMP); 2. diethyl phthalate (DEP); 3. naphthalene (NaP); 4 acenaphthylene (AcL); 5. acenaphthene (Ace); 6. fluorine (Flu); 7. butyl benzyl phthalate (BBP); 8. dibutyl phthalate (DBP); 9. phenanthrene (PhA); 10. anthracene (AnT); 11. fluoranthene (FluA); 12. pyrene (pyr); 13. benzo[a]anthracene (BaA); 14. chrysene (Chr); 15. benzo[b]fluoranthene (BbF); 16. di(2-ethylhexyl)phthalate (DEHP); 17. benzo[k]fluoranthene (BkF); 18. dioctyl phthalate (DOP); 19. benzo[a]pyrene (BaP); 20. dibenzo[a,h]anthracene (DbA); 21. benzo[g,h,i]perylene (BghiP); 22. indenol[1,2,3-c,d]pyrene (InP).
2 结果与讨论
2.1 分离优化及检测方法的选择
16种多环芳烃中除苊烯外均有荧光,可采用荧光检测,苊烯和6种酞酸酯无荧光,但在紫外波长224 nm下有较强的吸收峰。因此需要通过优化流动相,使目标化合物达到分离,从而实现16种多环芳烃和6种酞酸酯的荧光、紫外同时测定。实验中以乙腈-水为流动相采用梯度洗脱,22种目标化合物实现了基线分离(见图1)。
2.2 萃取条件的优化
以5.00 mL含多环芳烃(4.00 μg/L)和酞酸酯(50 μg/L)的混合标准溶液为供试溶液,以目标化合物的峰面积为萃取效率指标,考察了萃取溶剂的种类和用量、分散溶剂的种类和用量、氯化钠的用量、涡旋振荡时间等因素对萃取效率的影响。
2.2.1萃取溶剂的种类和用量
低毒、难溶于水、易溶于分散溶剂、密度比水轻且熔点接近或低于室温是凝固漂浮有机液滴-分散液液微萃取选择萃取溶剂的标准。基于此,本文考察了十一醇(熔点19 ℃)、十二醇(熔点24 ℃)两种萃取溶剂的萃取效率。实验结果显示,十二醇的萃取效率高于十一醇。这是因为十一醇的熔点相对较低,凝固的液滴易于熔化破碎,不易与水相分离,导致萃取回收率低。因此本实验采用十二醇为萃取溶剂,并进一步考察了十二醇的用量对萃取效率的影响。如图2a所示,随着十二醇用量的增加多环芳烃的萃取效率开始下降。这是因为虽然增加萃取溶剂的用量可以使更多的多环芳烃被萃取出来,但随着用量的增大,多环芳烃在有机相中的浓度也开始下降,进而导致检测信号的下降。如图2b所示,相对分子质量较大的邻苯二甲酸苄基丁基酯、邻苯二甲酸二丁酯、邻苯二甲酸二(2-乙基己基)酯和邻苯二甲酸二辛酯在水中溶解度较小,所以萃取效率的影响和多环芳烃相似;相对分子质量较小的邻苯二甲酸二甲酯、二乙酯在水中的溶解度比其他4种相对分子质量较大的酞酸酯在水中的溶解度要高出千倍以上[20],随十二醇用量的增加,一方面它们被萃取到十二醇中的量显著增加,另一方面萃取溶剂体积的增大也会导致目标化合物的浓度下降,但前者起主导作用,因而导致邻苯二甲酸二甲酯、二乙酯萃取效率随十二醇用量的增加而增大。基于以上实验结果,实验最终将十二醇用量设为10 μL。
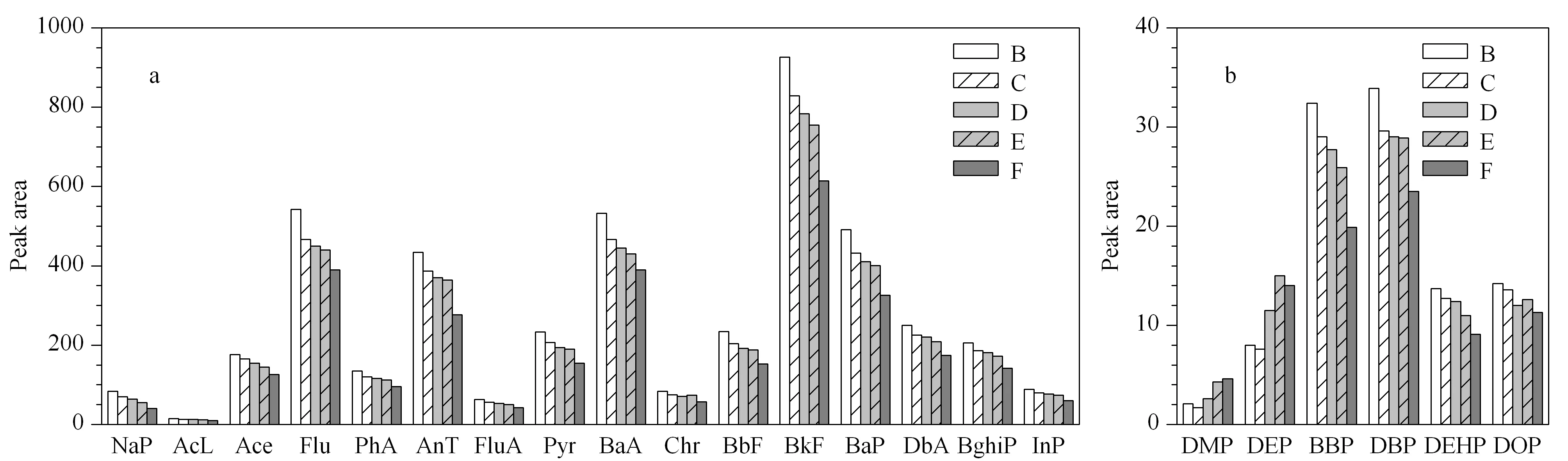
图 2 萃取溶剂的体积对(a)PAHs和(b)PAEs萃取效率的影响Fig. 2 Effect of volumes of extractive solvents on the extraction efficiencies of (a) PAHs and (b) PAEsDispersive solvent: 400 μL methanol; m(NaCl): 0.2 g; vortex oscillation time: 2 min.

图 3 分散溶剂的体积对(a)PAHs和(b)PAEs萃取效率的影响Fig. 3 Effect of volumes of dispersive solvents on the extraction efficiencies of (a) PAHs and (b) PAEsExtractive solvent: 10 μL 1-dodecanol; m(NaCl): 0.2 g; vortex oscillation time: 2 min.
2.2.2分散剂的种类和用量
在分散液液微萃取中,分散剂是影响萃取效率的一个重要因素。所用分散剂必须与水相和萃取溶剂均有良好的互溶性,才能最大限度地增加萃取溶剂与水相的接触面积,增大萃取效率。本文考察了符合上述条件的4种溶剂(甲醇、乙醇、乙腈及丙酮)作为分散溶剂时对萃取效率的影响。结果表明,以甲醇为分散剂时目标化合物的萃取效率最高。
以甲醇为分散剂进一步考察了其用量(300~800 μg/L)对萃取效率的影响。如图3所示,甲醇用量对多环芳烃和酞酸酯萃取效率的影响趋势几乎是一致的,当甲醇体积小于500 μL时,随着甲醇体积的增加,萃取溶剂与水相的接触面积增大,萃取效率增加;但当甲醇大于500 μL时,过多的分散剂又增大了目标化合物在水相的溶解度,导致萃取效率下降。因此本实验选择甲醇用量为500 μL。
2.2.3NaCl的用量及涡旋振荡时间
液液萃取过程中通常加入可溶性盐以增大水相的离子强度,从而提高目标化合物的萃取效率。为此考察了5 mL水样中加入0.1、0.15、0.2、0.25、0.3 g NaCl对萃取效率的影响。实验结果表明,当NaCl的用量小于0.2 g时,萃取效率随NaCl用量的增加而增大;当NaCl用量大于0.2 g时,萃取效率变化不大。故实验中选择NaCl加入量为0.2 g。
涡旋振荡可以加快萃取平衡的建立,因而实验考察了不同涡旋振荡时间对萃取效率的影响。结果表明,当涡旋振荡时间大于2 min时,萃取效率达到稳定状态。
根据以上实验结果,本方法的萃取条件为:以10 μL十二醇为萃取溶剂,500 μL甲醇为分散溶剂,NaCl用量为0.2 g,涡旋振荡时间2 min。
2.3 方法学考察
在优化的萃取条件下,对5 mL含有不同质量浓度的多环芳烃和酞酸酯系列混合标准溶液进行凝固漂浮有机液滴-液液微萃取,然后荧光、紫外同时测定。以质量浓度(C, μg/L)对峰面积(A)绘制校正曲线,得到22种目标化合物的线性方程、相关系数(r)及线性范围(见表2)。以S/N=3和S/N=10时目标化合物的浓度定义方法的检出限和定量限。以自来水为基质添加高、中、低3个水平的混合标准溶液进行加标回收率测定,每个水平平行测定3次,结果见表2。
结果表明,目标化合物的线性关系良好,线性相关系数均大于0.99;基质加标回收率为60.2%~113.5%,相对标准偏差为1.9%~14.3%;多环芳烃和酞酸酯的检出限分别为0.002~0.07 μg/L和0.2~2.2 μg/L,定量限分别为0.006~0.23 μg/L和0.8~7.4 μg/L。
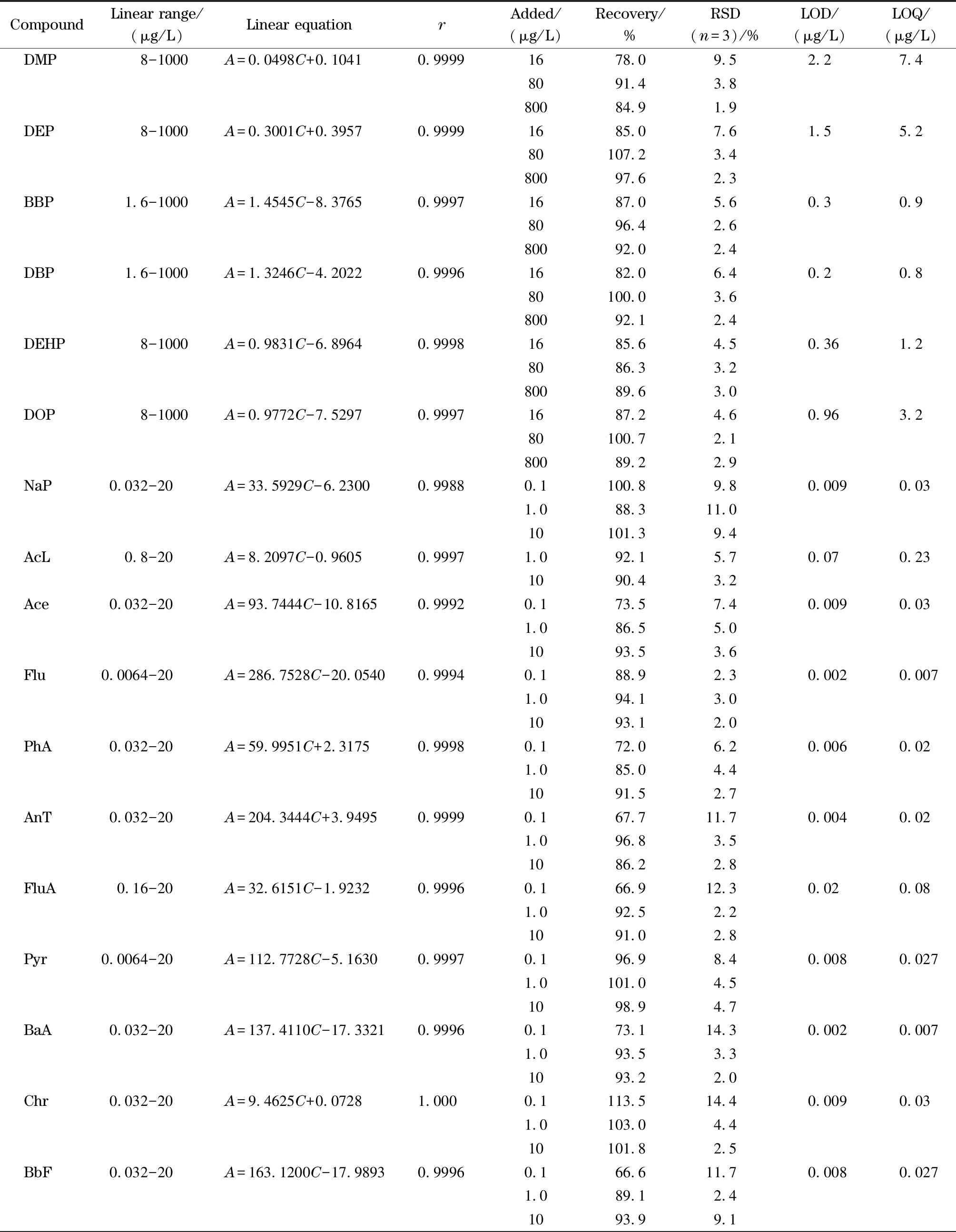
表 2 目标化合物的线性范围、线性方程、相关系数、加标回收率、精密度、检出限及定量限

表 2 (续)
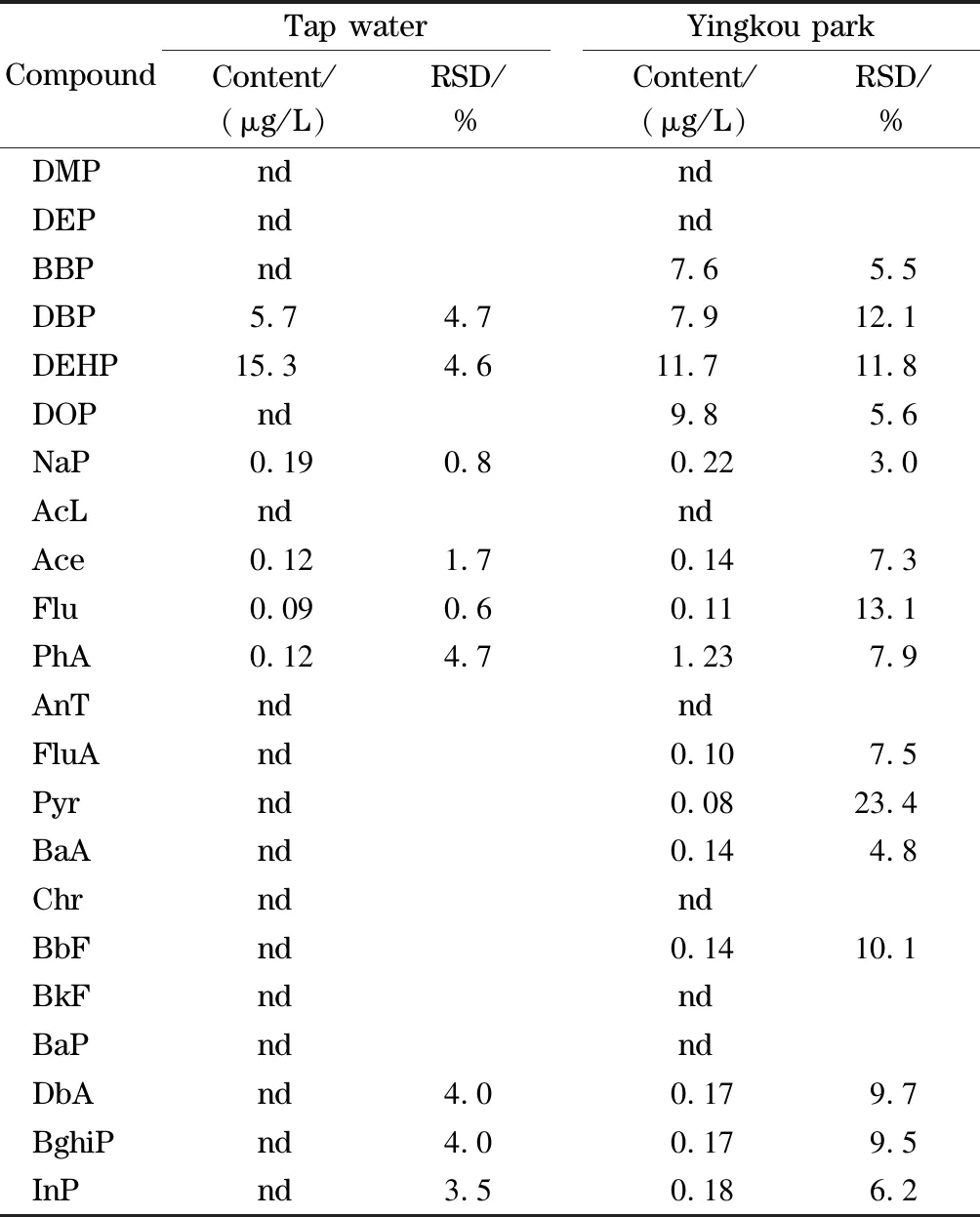
表 3 实际样品的检测结果(n=3)
2.4 实际样品测定
用建立的凝固漂浮有机液滴-分散液液微萃取-高效液相色谱分析方法对辽河(营口公园)水样和实验室自来水样进行测定,测定结果见表3。结果显示,自来水中检出萘、苊、芴、菲、邻苯二甲酸二丁酯及邻苯二甲酸二(2-乙基己基)酯等化合物,其余目标化合物未检出;而辽河营口公园水样中除邻苯二甲酸二甲酯、邻苯二甲酸二乙酯、苊烯、蒽、屈、苯并[k]荧蒽及苯并[a]芘等化合物未检出外,其余目标化合物均检出。
3 结论
本文建立了凝固漂浮有机液滴-分散液液微萃取结合高效液相色谱同时测定地表水中16种多环芳烃和6种酞酸酯的分析方法。该方法简便、快速,环境友好,成本低廉且灵敏度高,用于实际样品加标测定,回收率结果满意。
