玻璃体腔内注射雷珠单抗治疗脉络膜新生血管的临床疗效研究
2020-09-23王皎皎
张 丹 王皎皎
武警重庆总队医院眼科,重庆市 400061
脉络膜新生血管(Choroidal neovascularization,CNV)是一种病理性增生性改变,异常生长的脉络膜毛细血管移行并穿透视网膜色素上皮层(Retinal pigment epithelium,RPE),生长于视网膜神经上皮下,故又称为视网膜下新生血管[1],常出现于黄斑部,导致中心视力不可逆性严重损害,因此,CNV的诊治就显得极其重要,且需要长期有效治疗抑制新生血管使其消退或形成瘢痕。CNV形成原因不明,可能与局部组织的缺血缺氧、炎症反应密切相关,不同疾病均可形成CNV,比如年龄相关性黄斑变性[2]、病理性近视[3]、中心性渗出性脉络膜视网膜病变[4]、特发性息肉状脉络膜血管病变[5]等。研究发现[6]这些疾病形成CNV,均有相同的病理过程,表现为血管内皮生长因子(Vascular endothelial growth factor,VEGF)的表达明显高于正常,VEGF可促进血管内皮细胞激活,激活的血管内皮细胞发生移行和增生,逐步形成异常的新生血管管腔及血管外膜,因其血管结构不完整,常发生液体渗漏并积聚在视网膜内,导致视网膜局部微环境改变,引起不可逆转的视网膜功能结构损害和永久性视力丧失。但临床上CNV治疗棘手,近年来玻璃体腔内注射抗VEGF药物已成为治疗CNV的主要方法,国内外大量研究[7]证实抗VEGF 药物可抑制人体内VEGF所有亚型的表达,阻止新生血管的生长,减轻渗漏,从而改善视功能。本文通过探讨玻璃体腔内注射雷珠单抗连续3针、单独1针治疗黄斑部脉络膜新生血管的临床疗效差异,探寻黄斑部CNV有效持久的最佳治疗方法。
1 对象和方法
1.1 观察对象 本研究经医院医学伦理委员会审核批准,选取2017年1月1日—2019年1月1日于我院治疗的47眼黄斑部CNV患者,进行回顾性分析比较,根据雷珠单抗玻璃体腔注射次数不同,将雷珠单抗连续治疗3针的23眼患者设为观察组,雷珠单抗治疗1针的24眼患者设为对照组。观察组男12眼,女11眼,年龄40~88(64±13)岁,病程1~3个月,平均病程(1.82±0.23)个月; 对照组男13眼,女11眼,年龄42~87(65±12)岁,病程1~3个月,平均病程(1.79±0.22)个月。纳入标准:(1)采用荧光素眼底血管造影术(Fluorescein fundus angiography,FFA)和吲哚菁绿血管造影(Indocyanine green angiography,ICGA)检查CNV有渗漏,继发于黄斑中心凹下或旁中心凹(<2 500μm内);(2)光学相干断层扫描(Optical coherence tomography,OCT)检查RPE层断裂,局部纺锤状增厚和边界清楚的高反射区。排除标准:合并角膜病、白内障、玻璃体积血等影响疗效观察者,严重心、肺等内脏功能不全不能配合眼部治疗及检查者。两组患者性别、年龄、屈光度、病程等基本资料比较,差异无统计学意义(P>0.05),有可比性。
1.2 治疗方法 两组患者治疗前后处理和玻璃体腔注射雷珠单抗(瑞士Novartis Pharma Stein AG,注册证号:S20170003)方法相同,但治疗次数不同:治疗前3d患眼采用盐酸左氧氟沙星滴眼液滴眼(辰欣佛都药业有限公司,国药准字H20150022)4次/d,玻璃体内注射在眼科手术室内完成,常规消毒铺巾,盐酸奥布卡因滴眼液(参天制药株式会社,国药准字J20160094)表面麻醉,用0.5%聚维酮碘溶液常规洗眼,在颞下方角膜缘后3.5~4mm处进针,采用30号针头沿球心方向刺入眼内,进针深度约4mm,确保针尖位于玻璃体腔后缓慢注射雷珠单抗(0.5mg/0.05ml),出针后对穿刺点进行1min的压迫,无菌敷料包扎患眼,术后2h、术后1d检测眼压、眼部情况,术后24h打开敷料,给予溴芬酸钠滴眼液(辰欣佛都药业有限公司,国药准字H20150022)2次/d,妥布霉素地塞米松滴眼液(比利时S.A.Alcon Couvreur N.V.,国药准字H20080661) 4次/d,妥布霉素地塞米松眼膏(比利时S.A.Alcon Couvreur N.V.,国药准字H20160337)1次/晚,治疗1周停药;观察组患者采用雷珠单抗治疗连续3针,中间间隔1个月,对照组患者采用雷珠单抗治疗1针。
1.3 观察指标 比较治疗前、治疗后1个月及3个月两组患者患眼视力状况;采用OCT检查分析治疗前后CNV的图像特征,测量黄斑区视网膜的厚度、CNV突破RPE层的宽度、高度,观察黄斑水肿是否消退或减轻,CNV是否消退或减轻;采用FFA/ICGA检查比较CNV渗漏情况;并比较两组患者不良反应发生情况。
2 结果
2.1 两组患者视力情况比较 记录两组患者治疗后1个月、3个月视力提高两行及以上眼、稳定眼、下降两行及以上眼,观察组患者治疗后1个月、3个月视力提高高于对照组、差异有统计学意义(P<0.05),观察组患者治疗后3个月视力下降低于对照组、差异有统计学意义(P<0.05)。见表1。
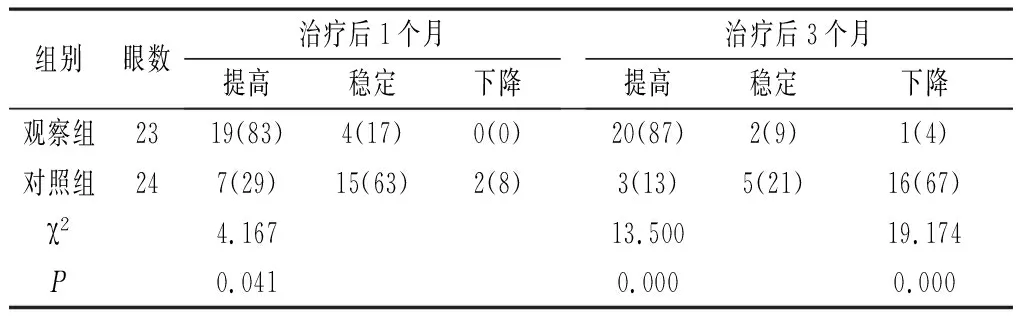
表1 两组治疗后1个月、3个月视力变化[n(%)]
2.2 两组患者OCT检查黄斑区视网膜厚度比较 两组患者治疗前黄斑区视网膜厚度相比较,差异无统计学意义(P>0.05),见表2、图1A、图2A;治疗后1个月,两组患者视网膜下液部分吸收,观察组黄斑区视网膜厚度显著低于对照组,差异有统计学意义(P<0.05),见表2、图1B、图2B;治疗后3个月:观察组黄斑区视网膜下液完全吸收,对照组视网膜下液则增多,观察组黄斑区视网膜厚度显著低于对照组,差异有统计学意义(P<0.05),见表2、图1C、图2C;观察组治疗后1个月、3个月黄斑区视网膜厚度相比较,差异无统计学意义(P>0.05),见表2、图1B、图1C;对照组治疗后3个月黄斑区视网膜厚度高于本组治疗后1个月,差异有统计学意义(P<0.05),见表2、图2B、图2C。
表2 两组患者治疗前、治疗后1个月及3个月黄斑区视网膜厚度比较

图1 观察组患者黄斑区视网膜厚度治疗前后比较
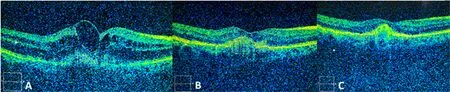
图2 对照组患者黄斑区视网膜厚度治疗前后比较
2.3 两组患者OCT 检查治疗前、治疗后1个月及3个月CNV突破RPE层的宽度、高度的比较 两组治疗前CNV突破RPE层的宽度、高度相比,差异无统计学意义(P>0.05),见表3、图1A、图2A;观察组治疗后1个月、3个月CNV突破RPE层的宽度、高度均显著低于对照组,差异有统计学意义(P<0.05),见表3、图1B、图1C、图2 B、图2C;观察组治疗后1个月、3个月CNV突破RPE层的宽度、高度相比,差异有统计学意义(P<0.05),见表3、图1B、图1C;对照组治疗后3个月CNV突破RPE层的高度高于本组治疗后1个月,差异有统计学意义(P<0.05),见表3、图2B、图2C,宽度相比差异无统计学意义(P>0.05),见表3、图2B、图2C。
表3 两组患者治疗前、治疗后1个月、治疗后3个月CNV突破RPE的宽度、高度比较
2.4 两组患者FFA/ICGA检查渗漏情况比较 记录两组患者治疗后1个月、3个月CNV停止渗漏眼、减少渗漏眼、未停止渗漏眼,观察组患者治疗后1个月、3个月停止渗漏眼高于对照组、差异有统计学意义(P<0.05),见表4,观察组患者治疗后3个月未停止渗漏眼低于对照组、差异有统计学意义(P<0.05),见表4。将观察组治疗后3个月FFA检查与OCT检查相互对照,发现停止渗漏患者外界膜层均完整、RPE层部分完整,渗漏减少患者外界膜层欠完整、RPE层部分完整,见图3。
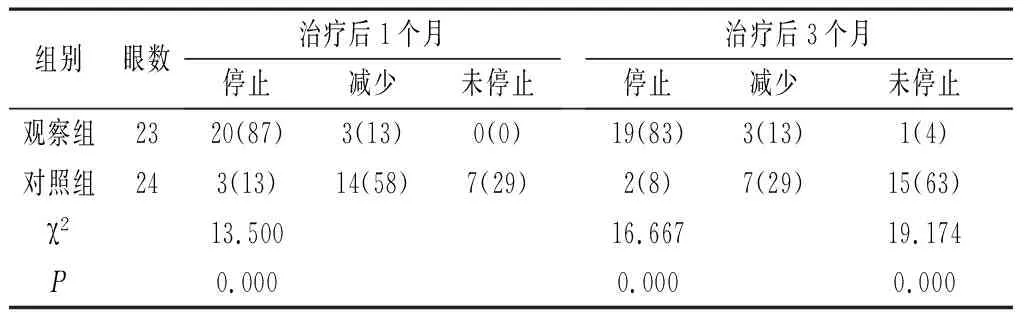
表4 两组患者治疗后1个月、3个月FFA/ ICGA检查CNV渗漏情况[n(%)]
2.5 两组患者不良反应发生率比较 观察治疗期间,所有患者均未发现角膜损伤、炎症反应、高眼压、玻璃体积血、视网膜出血及视网膜脱离等眼部不良反应。
3 讨论
众所周知,CNV是诸多眼底疾病共同的病理改变[8],CNV引起的渗出、水肿、出血及增生可导致视网膜病理性损害,若发生在黄斑区,则严重破坏黄斑区正常视功能结构,造成不可逆性严重视力障碍,甚至失明。CNV形成原因不明,其发生发展进程中受多种信号通路影响[9],研究报道[10-12]有VEGF信号通路、Wnt 信号通路、Shh(Sonic hedgehog) 信号通路、转化生长因子(Transforming growth factor,TGF)-β/Smad 信号通路和Notch 信号通路等,更有学者进一步证实[13-14]众多信号通路均可直接或间接上调VEGF表达,说明VEGF在CNV形成过程中至关重要,VEGF是一种人自身产生的生化物质,为高度特异性促血管内皮生长因子,可促进血管内皮细胞激活、迁移、增殖和血管形成。近年来,认为黄斑部视网膜缺血缺氧及炎症反应可能是形成黄斑CNV的主要原因,缺血缺氧导致VEGF产生,成为形成CNV的启动因素,VEGF激活脉络膜毛细血管内皮细胞,内皮细胞移行增生形成异常新生血管,而新生血管管腔结构不健全,容易产生出血或渗出,引起明显血管渗漏,破坏视网膜微环境,损害黄斑部视网膜正常组织结构,所以黄斑部CNV一旦出现,将对黄斑中心凹功能产生严重损害,导致中心视力不可逆性下降,影响患者日常生活,需要及时治疗。

图3 观察组治疗后3个月FFA检查与OCT检查对照
综合目前CNV的治疗方法,玻璃体腔内注射抗VEGF药物已成为治疗黄斑CNV的主力军[15],并已取得较好临床疗效。2012年,美国食品药品管理局批准雷珠单抗用于湿性老年性黄斑病变的治疗,雷珠单抗是一种新型的抗新生血管生成靶向治疗药物,同时也是一种人源化的重组单克隆抗体片段(Fab)[16],作用位点广,可靶向抑制人VEGF所有亚型的表达。与以往药物相比,雷珠单抗分子量小,玻璃体腔内注射雷珠单抗后,其对视网膜组织穿透力及渗透性更强,生物利用度高,有研究报道可达50%~60%[17]。雷珠单抗可竞争性结合VEGF,使蛋白水解酶的活性降低,减轻基底膜和内皮细胞外基质的异常降解[18],促进视网膜内外环境逐渐修复,减少出血、渗出及水肿,同时能有效抑制VEGF的表达,进而抑制CNV形成。本研究中两组治疗后均可以减轻黄斑水肿、抑制新生血管生长。有研究报道[19]视网膜RPE层和外界膜功能结构逐渐修复至少需要8周以上,但雷珠单抗在玻璃体内的平均消除半衰期为9d左右,作用时间短暂,单次治疗无法满足外层视网膜修复时间,治疗后CNV复发率高,需再次治疗,本研究亦显示连续3针疗效明显优于1针,更利于患者CNV持续消退和视力的稳定,与文献报道结果相同[20-21]。雷珠单抗的持续治疗,可以长久有效抑制CNV,使CNV渗漏持续有效减少、甚至消失,黄斑区及其周围视网膜组织内积液逐渐被吸收,病灶处视网膜的外界膜和脉络膜的Bruch膜得到恢复,结合本研究中FFA/ICGA检查与OCT检查结果,可以观察到随着视网膜RPE层、外界膜以及Bruch膜的逐渐修复,CNV病情持续好转,视力逐渐改善,表明RPE层或外界膜完整性对于评估CNV持续治疗和预后有重要意义,甚至可以不需要行有创的FFA/ICGA检查,仅通过OCT检查观察外界膜、RPE层是否修复,即可评估CNV的治疗效果和是否继续治疗,同时研究中显示,对照组治疗后3个月,CNV复发,CNV突破RPE层的高度与治疗后1个月相比增加,且有统计学意义,宽度改变无统计学意义,所以对于评估病情进展CNV突破RPE层的高度较宽度更有意义,但因本研究选取样本量有限、观察指标少,故研究结果适用范围有限,仍需多中心、大样本量、多指标的长期随访研究观察验证。
总之,雷珠单抗可有效抑制CNV的进展,显著改善CNV患者的视力,提高生活质量,但CNV可复发,需重复治疗,且雷珠单抗注射的最佳时机和最佳针数还不确定,本次研究选取病例数少,不足以代表所有病患情况,期待更大样本及更深入的研究。目前CNV形成的确切病因仍不清楚,需要更深入研究VEGF的上游信号通路来确定最佳的治疗方案,期待新药物和新技术的出现。
