HPLC-ICP-MS联用测定砷各形态的条件优化与应用
2020-09-11郭靖宜
郭靖宜 许 刚
(辽宁省地质矿产研究院有限责任公司 辽宁 沈阳 110032)
前 言
在很久之前我们的祖先就发现了砷的化合物,但是一直到上个世纪人类才开始研究砷的化合物,人类通过饮食将食物与饮用水中的砷富集到体内,研究表明当人类长期饮用砷含量高的水,患皮肤癌与其他内脏癌的概率很高,低含量砷暴露能否致癌是科学家们争论的焦点[1]。尽管如此砷被各大研究机构定为致癌物[2]。
元素在不同形态时,其毒性大小也不相同,在砷的各化合物中,AsB以及AsC对人类没有危害,有机砷形态存在时毒性很小,而无机砷形态存在时毒性最大,因此在研究砷元素在动物体内的生理与毒理作用,需要分析砷元素各个形态[3~5]。单一的仪器或技术显然不能满足要求。
自20世纪80年代,仪器联用被Chesterfield提出,之后仪器联用技术发展进入快车道,许珺辉等采用高效液相色谱分离样品,使用氢化物发生原子荧光光谱法测定了尿液中砷元素的四种形态,Ma Ming-sheng等[6]用同样的方法分析了尿液中砷的四种形态,并取得了一定的效果,而国内外专家认为元素形态分离发展最完善的技术是HPLC-ICP-MS联用,因此本文采用HPLC与ICP-MS联用,对两种分析样品中砷元素的各形态进行定性与定量分析[7~8]。
1 实验部分
1.1 实验材料、试剂
砷标准物质:三价砷酸根(AsO33-)、五价砷酸根(AsO43-)、一甲基砷、二甲基砷、砷甜菜碱(AsB)、砷胆碱(AsC);四丁基氢氧化氨(TBAH),丙二酸,甲醇(色谱纯)。
1.2 实验仪器
1.2.1H P L C仪器工作条件
Waters626型高效液相装置,以μm Kromasil硅胶为填料的反相C18色谱柱(150mm×4.6mm id)用于色谱的分离。
最佳流动相组成:18.8mM四丁基氢氧化氨,2mM丙二酸,4%甲醇(PH=5.95),流速:1ml.min-1进样量:25μL。
1.2.2I C P-MS操作条件
采用Thermo公司的Xseries2型ICP-MS系统,配有Scott玻璃同心雾化器,由于用ICP-MS作为检测器,砷的检测受到所用载气Ar与Cl原子的干扰,所以要用碰撞反应池技术来测定[9],具体参数见表1。
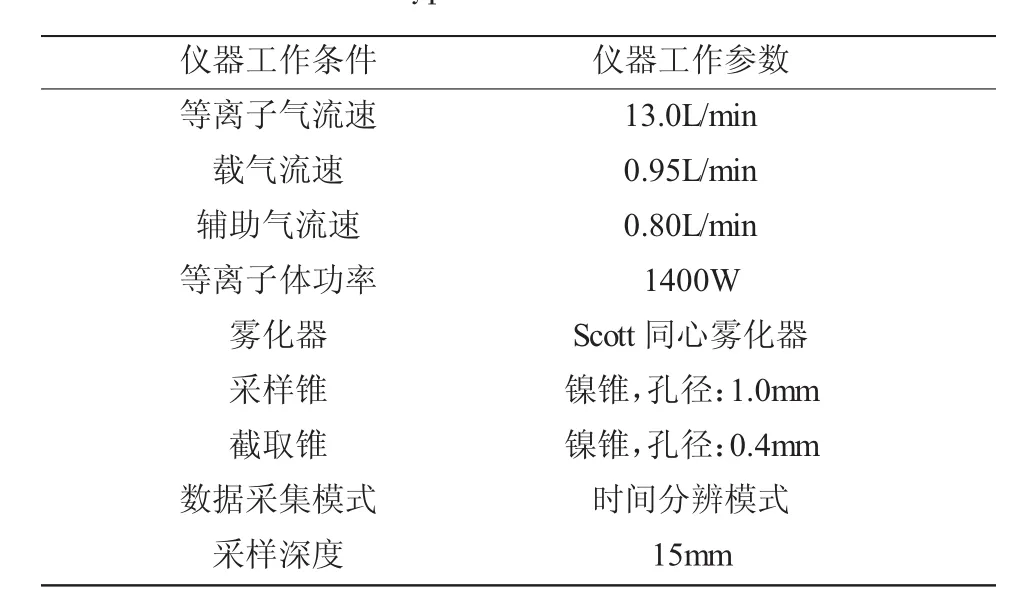
表1 典型的ICP-MS条件Table 1 The typical conditions for ICP-MS
1.3 样品的采集及前处理
1.3.1 人体尿样
尿样是经过ICP-MS测定后重金属含量较高的样品(尤其是总砷的含量),因为采集后不能及时分析,因此加少量酸后于-30℃冷藏。分析前解冻,样品不用稀释直接用一次性注射器经PhenoIilenex 0.45μm孔径的有机滤膜过滤。
1.3.2 环境水样
水样采自沈阳浑河河水,样品采集时分六点采样,每处的样品首先经过滤膜过滤,然后集中装入经过二次水多次洗涤的PE瓶中。因为采回来的样品是直接进行分析的,因此不需冷藏,只需加少量酸酸化后用一次性注射器经PhenoIilenex 0.45μm孔径的有机滤膜过滤。
1.4 实验设计及具体操作
1.4.1 标准配制
用购买国家标准配制成1mg/ml的六种砷的储备液,于棕色容量瓶内冷藏。分析前用millpore系统净化的水(18.2MΩ)将贮备液配制成10ng/ml的混合标准和六种砷的单标,作为建立标准曲线的标准溶液。
1.4.2 砷形态分析方法
首先用ICP-MS对砷含量较高的人体尿液进行砷总量的测定。通过一根PEEK管将Waters626型高效液相色谱的出口端与ICP-MS的进样口相连,采用时间分辨模式(TRA)来监控被分析物信号[10~11]。
用混合标准和单标来确定六种砷的保留时间,然后用微量注射器将经过处理后的人体尿液与浑河河水注入25μl的进样环,每个样品平行3次,并做了两个不同浓度的加标回收实验,同样重复3次。最后根据峰面积积分来计算每种形态的含量和加标回收率,从而检验整个分析方法可行性。
2 结果和讨论
2.1 色谱条件的优化
2.1.1T B A H浓度的影响
四丁基氢氧化氨(TBAH)在流动相作为离子对试剂。其浓度的大小决定砷各形态的分离程度,实验中逐步增加TBAH的浓度,当其浓度增加到18.8mM时,即可消除As(Ⅲ)和DMA的峰重叠,同样也可消除As(Ⅴ)与MMA的重叠[12],因此最终流动相中TBAH的浓度18.8mM见图1。

图1 TBAH浓度对砷形态保留时间的影响Fig.1 The effect of TBAH concentration on the retention time of arsenic species
2.1.2 丙二酸浓度的优化

图2 丙二酸的浓度对砷形态保留时间的影响Fig.2 The effect of malonic acid concentration on the retention time of arsenic species
流动相中的缓冲溶液一般是用来分离酸性和碱性分析物的,不同的分析物缓冲液的种类和浓度也不同[13]。在砷形态研究中经常使用丙二酸作为缓冲液。丙二酸浓度不同,每种砷形态保留时间也不相同,在实验中不断增加丙二酸的浓度,随着丙二酸浓度的增加,As(V)的保留时间显著的缩短。当丙二酸的浓度为1mol/L时As(V)的保留时间的变化趋于平和,当丙二酸的浓度为2mmol/L可以使As(V)和砷的其他形态得到有效分离,最终确定丙二酸的浓度为2mmol/L见图2。
2.1.3 甲醇浓度的影响
在流动相中加入少量甲醇可以增强ICP-MS检测砷信号的灵敏度。在实验时分别在流动相中加入0%~4%(V/V)的甲醇,图3所示,加入不同量甲醇对砷各形态的保留时间并没有显著的影响。但是,考虑到甲醇浓度会影响砷各形态信号的强度,因此确定甲醇的最佳加入量为4%(V/V)。

图3 甲醇浓度对砷各形态保留时间的影响Fig.3 The effect of methanol concentration on the retention time of various arsenic species
2.2实际样品的分析
2.2.1混合标准中砷形态的确定
用优化好的色谱分离条件对10ng/mL的单标和混合标准进行分析,分别测定三次来确定每种砷形态的出峰时间,从而根据峰面积建立标准曲线,见图4。

图4 10ng/mL时六种砷形态混合标准的色谱峰(从左至右依次为:AsC,AsB,As(III),DMA,MMA,As(V)Fig.4 The chromatographic peaks of the mixed standard of six arsenic species with a concentration of 10ng/mL(From left to right:AsC,AsB,As(III),DMA,MMA and As(V)
2.2.2 尿液中砷形态的分析
采用优化的色谱分离条件对人体尿液中的砷形态进行分析,通过标准的出峰位置来确定尿液中所含砷的形态。首先测定了样品中所含砷的总量,而砷各形态含量的总和相对于总量的比值为97%;对样品平行测定三次,相对标准偏差小于3%,取其浓度平均值。测定出样品中含有三种形态的有机砷,其含量列于表2,同时设计了两个浓度的加标回收率的实验。图5是尿液中所含砷各种形态的色谱峰,图6则是加入10ng/ml的混合标准的色谱峰。
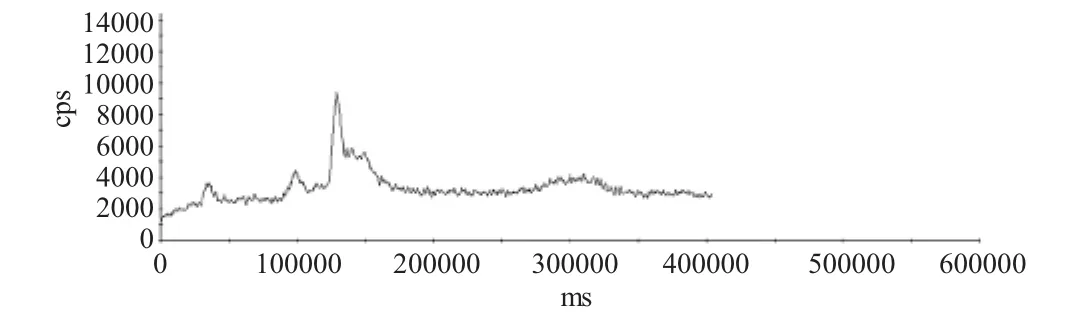
图5 尿液中的砷形态的色谱峰Fig.5 The chromatographic peaks of the arsenic species in urine

图6 加标为10ng/ml的尿液的色谱峰Fig.6 The chromatographic peaks of the urine with a standard concentration of 10ng/mL
2.2.3 浑河河水中砷形态的分析
浑河河水属于环境水样,通过三次平行测定,样品中没有检测出砷的任何形态。ICP-MS对浑河和水中砷的总量进行测定同样未检出。
2.3 加标回收率实验
由于没有标准物质,为了验证整个分析方法的可行性,设计了两个浓度梯度的加标回收实验,其回收率都在99.8%~110%之间,这说明该分析方法在一定程度上还是具有可信度的。人体尿样与浑河河水中各形态砷的含量以及加标回收率列于表2。

表2 尿液和浑河河水中各种砷形态的含量、总砷含量及加标回收率Table 2 The contents of various arsenic species,total arsenic content,and the standard recovery rate in urine and water from Hunhe River
3 结论
尝试采用反相离子对高效液相色谱-电感耦合等离子体质谱(HPLC-ICP-MS)联用测定砷元素的各种形态,并对色谱条件进行了一系列的优化,最终成功地分离了沈阳浑河河水样和尿样中As(Ⅲ)、As(Ⅴ)、MMA、DMA四种砷化合物,取得了理想的实验效果。
