基于葫芦脲衍生物超分子聚合物的构建与性能
2020-09-11王秀丽王巧纯
王秀丽, 王巧纯
(华东理工大学化学与分子工程学院,精细化工研究所,结构可控先进功能材料及其制备教育部重点实验室,上海 200237)
超分子聚合物是小分子间通过非共价作用形成的一类聚合物,常见的非共价相互作用包括金属配位键、氢键、范德华力、π-π 堆积等[1-6]。由于超分子聚合物具有独特的物化性质,它在分析检测、新型材料、生物医药、化学催化等诸多领域都有着潜在的应用价值[7-12]。其中,作为离子检测的材料,超分子聚合物受到了广泛的关注[13]。例如,魏太保课题组利用官能团化的柱[5]芳烃构建了一种超分子聚合物[14],该聚合物对Fe3+、Cr3+、Hg2+、Cu2+有显著的荧光响应,并且具有优异的可分离回收性能。然而,超分子聚合物用于离子检测的报道仍存在一些局限性,如:大多数检测是在有机溶剂或者水和有机溶剂的混合溶剂中进行的,这对环境和生物体中的离子检测十分不利。因此,在水溶液中构建用于检测离子的超分子聚合物对于扩展超分子聚合物在生物和环境方面的应用有着重大意义。
葫芦脲(CB[n])是一种水溶性大环分子,具有高度的对称性和刚性。它的两个端口由许多极性羰基组成,可以通过静电作用或氢键作用与客体分子结合[15-16],常用的客体分子包括多种阳离子,特别是质子化的有机胺[17],因此CB[n]是在水溶液中构建超分子聚合物的理想单体。例如,黎占亭课题组利用CB[8]和4,4’-联吡啶-1 鎓在水溶液中构建了一种具有蜂窝孔状的单层超分子聚合物[18]。赵新课题组利用CB[8]与四苯乙烯衍生物构建了一种具有聚集诱导发光性质的超分子聚合物[19]。本课题组也报道了一种葫芦脲类似物,即十甲基取代亚甲基桥葫芦[5]脲(Me10TD[5]),利用其可与质子化的有机胺以1∶2的物质的量之比结合并且具有较大的结合常数的优点[20],在水溶液中成功地构建了多种超分子聚合物[21-22]。
本文利用具有荧光性质的1,3,6,8-四(4-氨基苯基)芘盐酸盐1 和Me10TD[5]在水溶液中构建了一种超分子聚合物。利用1 和Me10TD[5]形成超分子聚合物时荧光淬灭,而外加Ba2+使聚合物结构破坏,1 重新游离从而使荧光恢复的特点,该聚合物实现了在水溶液中选择性地检测Ba2+,这项研究为环境和生物系统中重金属离子的检测提供了新思路。
1 实验部分
1.1 原料和试剂
1,3,6,8-四溴芘、4-氨基苯硼酸频哪醇酯、四三苯基膦钯均为分析纯,购于北京华威锐科化工有限公司;草酰氯、尿素(Urea)、乙酸均为分析纯,购于上海麦克林生化科技有限公司;无水碳酸钾、1,4-二氧六环、三乙胺(TEA)、氯化钡、氯化铜、氯化亚铁、氯化镁均为分析纯,购于上海百灵威化学科技有限公司;无水甲醇(φ=98%)、浓盐酸(w=37%),购自上海泰坦科技股份有限公司;二甲亚砜(DMSO)、二氯甲烷(DCM)、无水乙醚、丙酮、氯化钠、氯化钙、氯化锌、磷酸氢二钠、磷酸二氢钠均为分析纯,购于上海泰坦科技股份有限公司;氯化钯、氯化镉、氯化镍、氯化锰、氯化钴均为分析纯,购于萨恩化学技术(上海)有限公司。
1.2 测试与表征
核磁共振谱图(1H-NMR,13C-NMR)测试:Brüker AM-400 核磁共振波谱仪(内标物为TMS,瑞士布鲁克公司);质谱测试:LCT Premier XE 质谱仪(美国沃特世公司);动态光散射实验(DLS):ZEN3600 粒度仪(美国马尔文公司);荧光光谱测试:Cary Eclipse 荧光仪(使用宽度为1 cm 的石英池,美国瓦里安公司);透射电子显微镜(TEM)测试:JEM-2100 型透射电子显微镜(日本捷欧路公司);荧光量子产率测试:FLS1000 荧光光谱仪(英国爱丁堡公司)。TEM测量的样品是通过将混合液滴在云母片上并通过旋涂干燥制备。
1.3 实验步骤
图1 示出了1 的合成及其与Me10TD[5]自组装形成超分子聚合物的示意图。
1.3.1 1,3,6,8-四氨基芘(PTTA)的合成 称量1,3,6,8-四溴芘1.0 g(1.93 mmol)、4-氨基苯硼酸频哪醇酯2.0 g(9.1 mmol)、四三苯基膦钯0.21 g(0.2 mmol)、无水碳酸钾1.45 g(10.5 mmol)于250 mL 圆底烧瓶中,加入45 mL 1,4-二氧六环和15 mL 水,在氩气的保护下于115 ℃反应3 d。反应结束,加入35 mL 水并充分搅拌。抽滤,滤饼用甲醇洗涤、干燥,得到0.71 g黄色固体,产率为65%。1H-NMR(400 MHz,DMSO-d6,298 K,δ):8.12(s,4 H),7.78(s,2 H),7.33(d,J= 8.4 Hz,8 H),6.77(d,J=8.4 Hz,8 H),5.30(s,8 H)。m.p.245~247 °C。
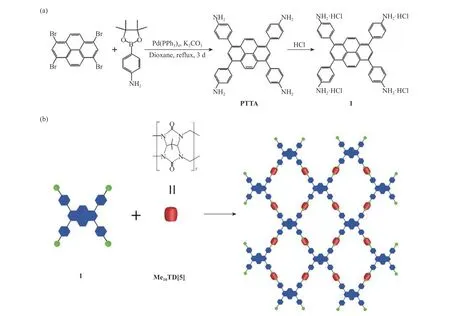
图1 1 的合成及其与Me10TD[5]自组装形成超分子聚合物Fig.1 Synthesis of 1 and its self-assembly with Me10TD[5] into supramolecular polymer
1.3.2 1 的 合 成 将100 mg(0.18 mmol)PTTA 在100 mL 水中超声处理10 min,然后加入10 mL 浓盐酸搅拌,得到澄清的黄色溶液。将溶液进行减压浓缩至体积约1 mL,加入50 mL 甲醇,有沉淀析出。过滤收集所得沉淀物并用50 mL甲醇洗涤,得到黄色粉末状固体112 mg,产率为90%。1H-NMR(400 MHz,D2O,298 K,TMS,δ):8.09(s,4 H),8.05(s,2 H),7.74(d,J= 8 Hz,8 H),7.53(d,J= 8 Hz,8 H);13CNMR(100 MHz,D2O,298 K,TMS):δ148.18,137.10,131.04, 127.55, 126.68, 126.10, 124.41, 113.92;MS(ESI):m/z567.254 7([M + H]+计算值:567.254 9)。1.3.3 Me10TD[5]的合成步骤 Me10TD[5]的合成完全按照参考文献[20]的方法进行。
2 结果与讨论
2.1 1 与Me10TD[5]自组装行为的核磁研究
当1 和Me10TD[5]在水中以1∶2 的物质的量之比(c1= 2.0×10−3mol/L)混合时,溶液变浑浊,说明1 可以与Me10TD[5]结合形成沉淀析出。我们对不同物质的量之比的 1 (c1= 2.0 × 10−3mol/L)和Me10TD[5]的混合液进行核磁测试。当 1 和Me10TD[5]的物质的量之比低于1∶2 时(图2(a)),只能观察到Me10TD[5]的质子信号;当 1 和Me10TD[5]以物质的量之比等于1∶2 混合时几乎观察不到质子信号(图2(b));当 1 和Me10TD[5]以物质的量之比高于1∶2 混合时,只能观察到 1 的质子信号(图2(c))。上述结果表明 1 与Me10TD[5]在水溶液中以1∶2 的物质的量之比混合时形成了几乎不溶的物质。
2.2 1 与Me10TD[5]自组装行为的荧光研究

图2 1 和Me10TD[5]混合后的核磁谱图Fig.2 1H-NMR spectra of the mixture of 1 and Me10TD[5]
为了进一步探索1 和Me10TD[5]的结合行为,研究了1 和Me10TD[5]在结合前后荧光发射光谱的变化。如图3 所示,当1 与Me10TD[5]在水溶液中以1∶2 的物质的量之比混合时,1 的荧光强度显著降低,仪器测出荧光量子产率也从4.73%降低至0.72%,且最大发射波长从421 nm 红移到510 nm。这是因为1 和Me10TD[5]结合后产生层状堆叠,1 分子间的距离减小,发生分子间相互作用,进而导致最大发射波长的红移[23]。而1 分子间的距离减少又导致其产生的荧光被邻近的分子吸收,使荧光发生淬灭[24]。为了确定两者的结合比,采用381 nm 激发光波长(文中荧光实验均采用381 nm 激发光波长)测量发射光波长421 nm 处荧光强度的变化量(ΔF),用ΔF绘制出Job’s plot 图像(1 和Me10TD[5]的总浓度为2.0 × 10−5mol/L),如图4(a)所示,从图中可以看出1 和Me10TD[5]的物质的量之比为1∶2。此外,用Me10TD[5]在水中滴定1,通过421 nm 波长处荧光强度的变化进行非线性拟合(c1=2.0× 10−5mol/L),利用Thordarson 报道的公式[25]可以计算出1 和Me10TD[5]之间结合常数(Ka)为(7.1 ± 0.7)× 104L/mol,如图4(b)所示。

图3 1 和1+Me10TD[5]的荧光光谱(c1 = 1.0 × 10−5 mol/L)Fig.3 Fluorescence spectra of 1 and 1 + Me10TD[5] (c1 = 1.0 ×10−5 mol/L)
2.3 1 与Me10TD[5]自组装的粒径研究
DLS 可以测出聚合物在水溶液中的流体动力学直径(Dh)。将不同浓度的1 和Me10TD[5]以1∶2 的物质的量之比混合,并用DLS 测定其粒径分布。当1 的浓度分别为6.0 × 10−7,2.0 × 10−6,2.0 × 10−5mol/L和2.0 × 10−4mol/L 时,对应的Dh 分别为38,142,190 nm和531 nm(如图5 所示)。这些结果表明,1 与Me10TD[5]至少可以在10−6mol/L 的数量级浓度下自组装形成超分子聚合物。且随着单体浓度的增加,Dh 增加,这是超分子聚合物形成的典型特征。

图4 (a)荧光法测得的Job’s plot 图像;(b)荧光滴定实验测得的非线性拟合曲线(c1 = 2.0 × 10−5 mol/L)Fig.4 (a) Job's plot image measured by fluorescence experiment; and (b) Non-linear fitting-curve by fluorescence titration experiment (c1 = 2.0 ×10−5 mol/L)
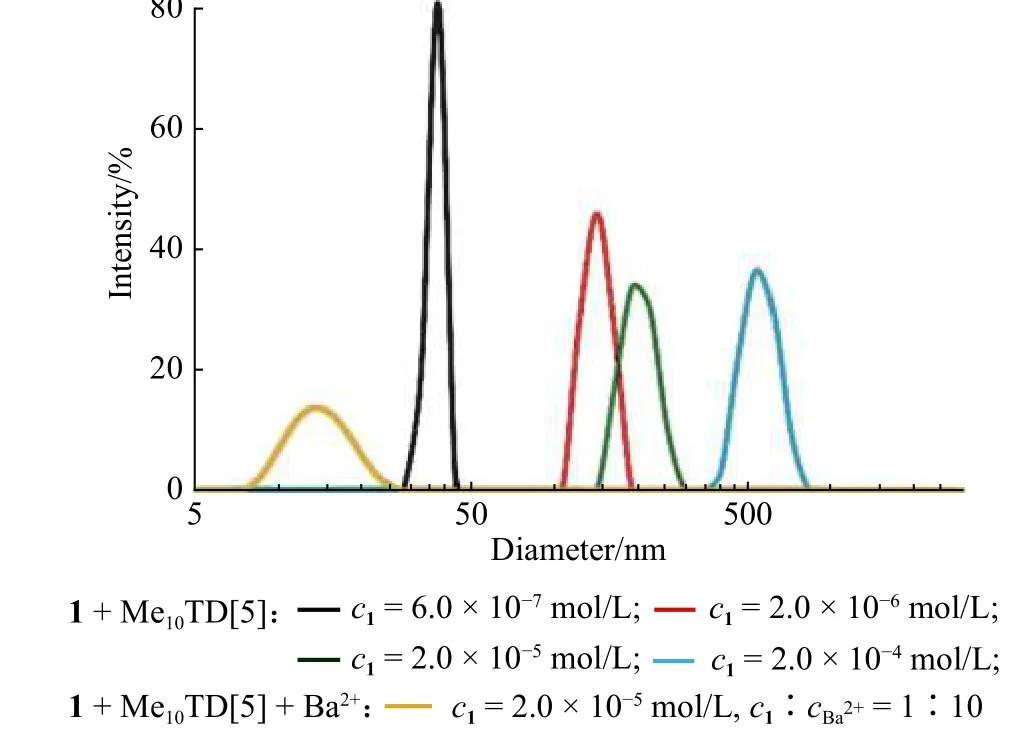
图5 不同浓度下1 与Me10TD[5]混合物的DLS 测试结果Fig.5 DLS results of the mixture of 1 and Me10TD[5] atdifferent concentrations
2.4 1 与Me10TD[5]自组装的形貌研究
采用TEM 对聚合物的形貌进行了观察,如图6所示,1 和Me10TD[5]的物质的量之比为1∶2 的混合液在云母片表面上呈现出膜结构,进一步表明了超分子聚合物的形成。
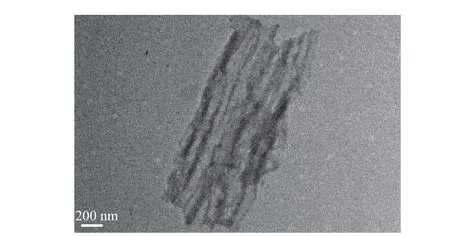
图6 超分子聚合物的透射电镜图(c1 = 2.0 × 10−5 mol/L)Fig.6 TEM image of the supramolecular polymer (c1 = 2.0 ×10−5 mol/L)
2.5 超分子聚合物对Ba2+的检测研究
葫芦脲的端口羰基可以和金属阳离子作用,因此外加与葫芦脲结合力更强的金属阳离子可以破坏原有的超分子聚合物结构,进而引起体系光学性质的改变[26]。图7 示出了聚合物溶液加入Na+(1 与Na+的物质的量之比为1∶10)前后荧光的变化。因为Na+对体系荧光基本无影响(见图7),且在pH =6.0 时聚合物结构稳定(见图8),所以我们用pH = 6.0的NaH2PO4/ Na2HPO4缓冲液进行聚合物溶液的配制,并用于聚合物的性能测试。
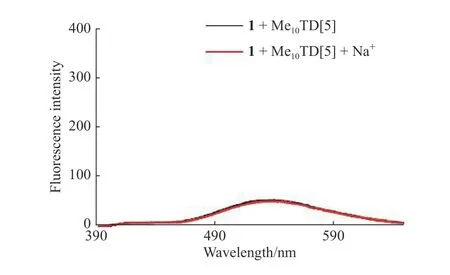
图7 聚合物溶液加入Na+前后荧光的变化(c1 = 1.0 ×10−5 mol/L)Fig.7 Fluorescence change before and after adding Na+ to the polymer solution (c1 = 1.0 × 10−5 mol/L)
配制1 和Me10TD[5]的物质的量之比为1∶2 的混合液,然后分别加入相同浓度(1.0×10−4mol/L)的不同离子,记录421 nm 波长下的荧光(激发光波长381 nm)变化,如图9 所示。从图中可以看出,加入Ba2+后体系荧光显著增强,加入其他离子荧光强度变化不明显或变化较小。这是因为1 和Me10TD[5]形成超分子聚合物后引起荧光淬灭,而加入的Ba2+与Me10TD[5]有着更强的结合力,导致聚合物结构破坏,1 重新游离,从而荧光恢复。DLS 结果(图5)也证实了这一结论:在聚合物溶液中加入Ba2+,使1 与Ba2+的物质的量之比为1∶10 时,Dh 由190 nm减小至13 nm。因此,1 和Me10TD[5]形成的超分子聚合物对Ba2+的检测有较好的选择性。
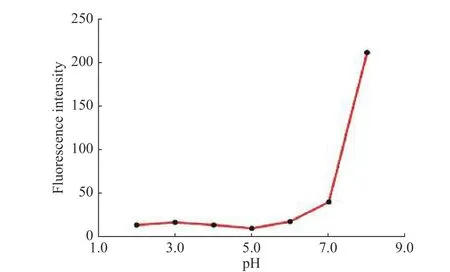
图8 聚合物溶液421 nm 波长处荧光强度随pH 的变化(c1 = 1.0 × 10−5 mol/L)Fig.8 Change of fluorescence intensity of polymer solution at 421 nm with pH (c1 = 1.0 × 10−5 mol/L)
为了研究1 和Me10TD[5]形成的超分子聚合物对Ba2+检测的抗干扰性,配制1 和Me10TD[5]的物质的量之比为1∶2 的混合液(c1= 1.0 × 10−5mol/L),先分别加入浓度相同(1.0 × 10−4mol/L)的不同离子,测定在421 nm 波长下的荧光强度。然后再分别加入浓度相同的Ba2+,测定在421 nm 波长下的荧光强度,结果如图10 所示。从图中可以看出,在其他离子的存在下,Ba2+的加入仍使体系的荧光强度有较大的变化。因此,1 和Me10TD[5]形成的超分子聚合物对Ba2+的检测具有一定的抗干扰能力。
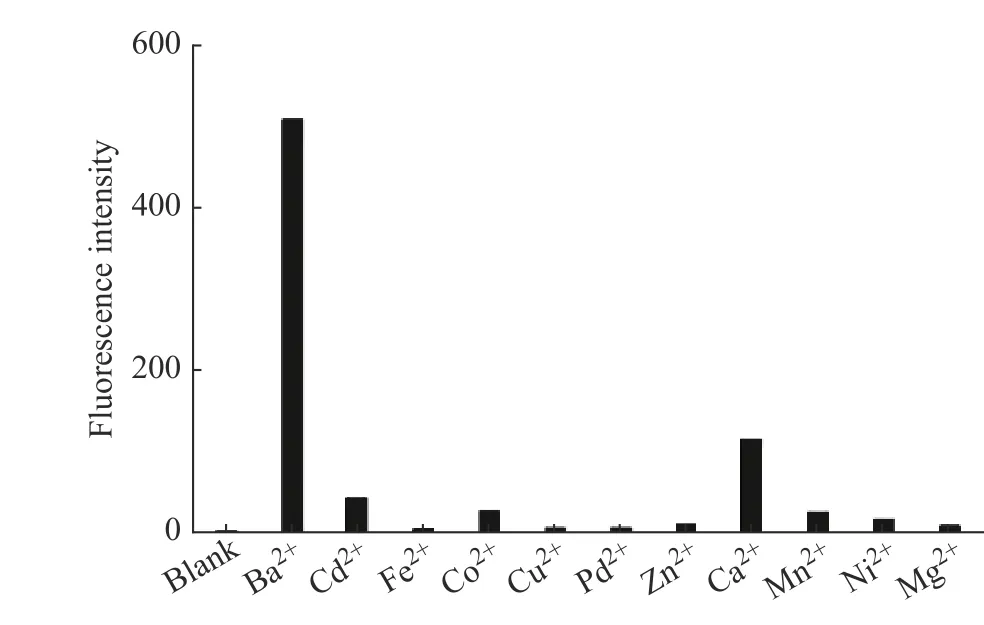
图9 超分子聚合物对Ba2+检测的选择性(c1 = 1.0 × 10−5 mol/L)Fig.9 Selectivity of supramolecular polymers to Ba2+ detection(c1 = 1.0 × 10−5 mol/L)
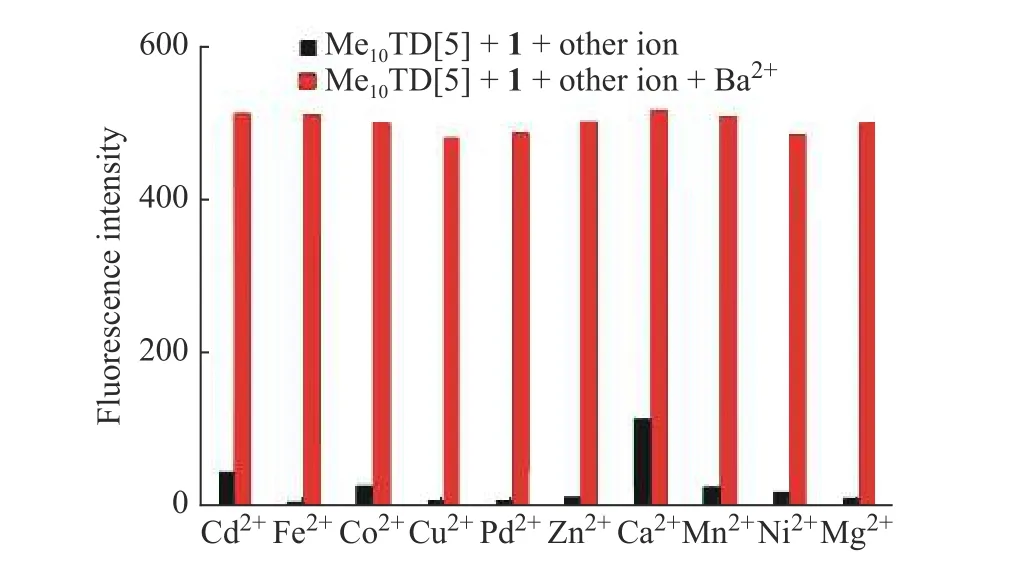
图10 超分子聚合物对Ba2+检测的抗干扰性Fig.10 Anti-interference of supramolecular polymers to Ba2+detection
为了研究1 和Me10TD[5]形成的超分子聚合物对Ba2+检测的灵敏性,进行了定量荧光滴定实验。配制1 和Me10TD[5]的物质的量之比为1∶2 的混合液(c1= 1.0 × 10−5mol/L),然后逐渐加入Ba2+,绘制出荧光强度随Ba2+浓度的变化曲线,如图11 所示。结果表明,Ba2+浓度在10~60 μmol/L 时,Ba2+的浓度与体系的荧光强度有着良好的线性关系,利用3σ/S公式[27](其中σ为样品的标准偏差,S为拟合直线的斜率)计算出检出限为7.6×10−6mol/L。
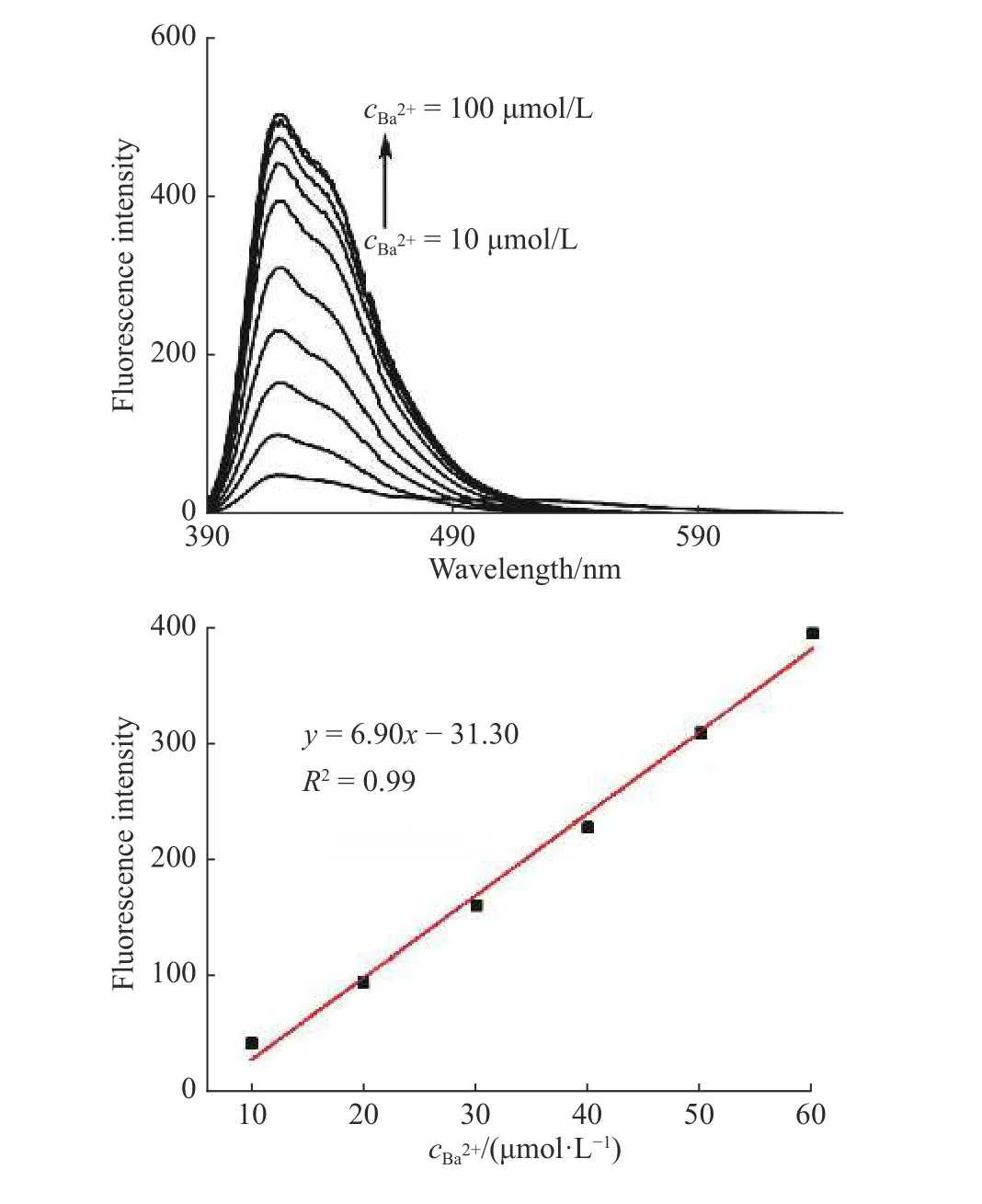
图11 超分子聚合物检测Ba2+的荧光滴定实验Fig.11 Fluorescence titration experiment for detection of Ba2+ by supramolecular polymer
3 结 论
(1)1,3,6,8-四(4-氨基苯基)芘盐酸盐1 可以和葫芦[5]脲类似物(Me10TD[5])在水溶液中自组装形成超分子聚合物。该超分子聚合物的结构可以通过多种表征手段,如1H-NMR、荧光发射光谱、DLS 和TEM加以表征。
(2)通过绘制Job’s plot 图像得到1 和Me10TD[5]两者结合的物质的量之比为1∶2,非线性拟合曲线表明两者的结合常数为(7.1 ± 0.7)× 104L/mol。
(3)在聚合物溶液中加入Ba2+可以使体系荧光明显增强,而加入其他离子体系荧光变化不明显或变化较小。所以该聚合物可以用作水溶液中Ba2+的检测,且具有良好的选择性和一定的抗干扰能力。定量荧光滴定实验表明该聚合物水溶液对Ba2+的检出限为7.6 × 10−6mol/L。
