蒸馏—萃取联合法再生镀钌废液中的三氯化钌
2020-09-10邵莹王琪周全法
邵莹 王琪 周全法

摘要:传统氧化蒸馏工艺回收钌废液中钌的损失率较高,试验优化了氧化蒸馏工艺,并采用萃取法处理蒸余液。探讨了蒸馏温度、氧化剂用量、吸收剂,以及预氧化剂、萃取剂体积分数、萃取相比、反萃条件等因素对钌回收率的影响。结果表明:在蒸馏温度80 ℃下,以KMnO4-H2SO4为氧化剂,6 mol/L HCl为吸收剂,蒸馏时间为1 h,钌蒸馏回收率最高达到89.0 %;再生蒸余液时,在萃取剂为30 %N503,萃取相比为1,反萃剂为2 mol/L NaOH溶液,反萃相比为1的最佳条件下,反萃率达到80.4 %。蒸馏—萃取联合法再生钌的总回收率达到96.9 %,比单一蒸馏法提高了7.9百分点,有效提高了钌的再生利用率。
关键词:氧化蒸馏;萃取;反萃;镀钌废液;三氯化钌
中图分类号:TQ340.68
文章编号:1001-1277(2020)02-0077-04
文献标志码:Adoi:10.11792/hj20200217
引 言
三氯化钌(RuCl3)主要用于金属阳极钌涂层和加氢催化剂的制备。固体三氯化钌有2种晶型:α型和β型,β-RuCl3可溶并具有活性。当RuCl3中钌含量过高时,有可能生成难溶、无活性的α-RuCl3。因此,固体RuCl3中钌质量分数要求在 35 %~38 %[1-2]。
钌废料来源多样,体系庞杂,其再生方法各异[3]。钌废液中钌再生工艺有蒸馏吸收法[4-6]、氢还原法[7-8]、乙醇还原法[9]及其他方法[10]。蒸馏吸收法相对成熟,其操作方便、过程简单。但是,蒸馏吸收过程中常伴有四氧化钌的挥发,且时间越长损失越多。为弥补该技术的不足,缩短蒸馏时间,采用蒸馏—萃取联合法再生镀钌废液中的三氯化钌,并探讨了工艺条件对三氯化钌回收率的影响。
1 试验部分
1.1 材料与仪器
主要材料:镀钌废液(来源于某电镀厂,经测定钌质量浓度为5.53 g/L,以RuO2-4形式存在,无其他金属杂质);高锰酸钾、正辛醇(江苏盛强功能化学股份有限公司);磺化煤油/260号溶剂油、N503(郑州勤实科技有限公司);试剂均为分析纯。
主要仪器:HH电热恒温数显水浴锅(江苏金坛市大仪器厂);T6紫外可见分光光度计(北京普析通用仪器有限责任公司)。
1.2 工艺流程
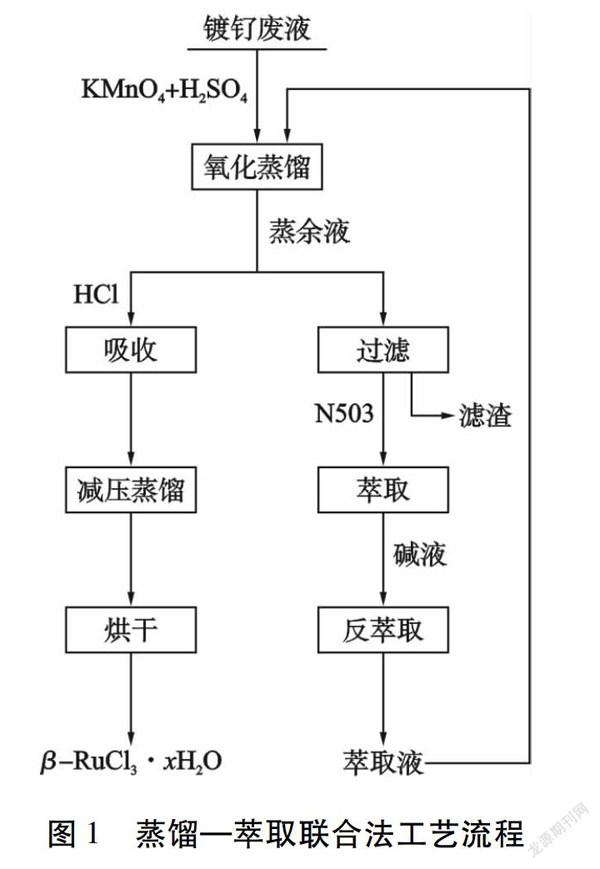
蒸馏—萃取联合法再生镀钌废液中RuCl3的工艺流程如图1所示。
1.3 蒸馏及萃取过程
1.3.1 蒸馏过程
取30 mL镀钌废液、1 g KMnO4于250 mL三口烧瓶中,从分液漏斗中缓慢加入8 mL H2SO4,在80 ℃下蒸馏1 h,蒸馏出的RuO4气体用6 mol/L HCl吸收,生成的RuCl3盐酸溶液在50 ℃~80 ℃下减压蒸馏至黏稠状,于100 ℃烘箱中烘干,称量β-RuCl3·xH2O晶体的质量。
蒸馏化学反应式[11]为:
5RuO2-4+2MnO-4+16H+△
5RuO4↑+2Mn2++8H2O,
3RuO2-4+2MnO-4+8H+△
3RuO4↑+2MnO2↓+4H2O。
吸收化学反应式[11]为:
2RuO4+16HCl
2RuCl3↓+8H2O+5Cl2↑。
蒸餾时间长,RuO4损失增多;蒸馏时间不足,蒸余液中有钌残留。为提高钌回收率,进一步采用萃取法对蒸余液进行处理。
1.3.2 萃取过程
1)钌(Ⅳ)的预氧化。在盐酸体系中,钌主要以Ru(Ⅲ)、Ru(Ⅳ)形式存在。胺类萃取剂对Ru(Ⅳ)选择性高,蒸余液中的钌须转化成四价钌络阴离子[RuCl2-6]才能得到理想的萃取效果[11]。处理过程为:过滤氧化蒸馏后的蒸余液,除去MnO2滤渣,滤液定容至100 mL容量瓶。移取20 mL蒸余液,加入约1.5 g NaOH调节pH至碱性,加入5 mL 10 % NaClO及1 g NaCl,搅拌至溶解,加入10 mL HCl,在80 ℃水浴保温30 min,备用。
2)萃取与反萃取。胺类萃取剂对Ru(Ⅳ)的萃取能力依次为季胺>叔胺>仲胺>伯胺[12],因此选用N503(季胺)萃取蒸余液中的钌。碱溶液(如NaOH或KOH)或还原剂(如亚硫酸、氧化亚砷)皆可有效地从有机相中反萃钌[13]。碱液价格低廉、环保、易获得,因此选用NaOH溶液作为反萃剂。
萃取化学反应式为:
5R1R3N+Cl-+2RuCl2-6
(R1R3N+)5(RuCl2-6)2·Cl-+4Cl-。
反萃取化学反应式为:
(R1R3N+)5(RuCl2-6)2·Cl-+5NaOH
2Na2(RuCl6)+5(R1R3N+)·OH-+NaCl。
处理过程为:以磺化煤油为稀释剂,正辛醇为破乳剂,分别配制不同体积分数的N503萃取剂。为保持萃取过程中酸的稳定,将有机相与等体积3 mol/L HCl溶液振荡3~4次,至水相酸度不变,取出有机相备用。将35 mL处理过的蒸余液与等体积上述有机相置于125 mL分液漏斗中,振荡15 min,静置分层,弃去水相。有机相中加入35 mL 2 mol/L NaOH溶液,振荡15 min,静置后测定水相中的钌,计算钌萃取率。
1.4 钌的分析
采用硫脲分光光度法测定镀钌废液、蒸余液及萃取液中的钌,显色体系为Ru-硫脲,硫脲溶液为显色剂,乙醇为显色助剂,在λ=620 nm处,以试剂为空白,测定钌。蒸馏得到的β-RuCl3·xH2O晶体中的钌采用重量法测定,以锌粒为还原剂还原钌粉。
2 结果与讨论
2.1 蒸馏工艺条件
2.1.1 蒸馏温度
以KMnO4-H2SO4为氧化剂,6 mol/L HCl为吸收剂,蒸馏时间为1 h,考察蒸馏温度对钌蒸馏回收率的影响,结果如图2所示。由图2可知:蒸馏温度为80 ℃时,蒸馏回收率达到最高,为89.0 %。当蒸馏温度为65 ℃~80 ℃,蒸馏回收率随温度升高而升高;蒸馏温度高于80 ℃,蒸馏回收率反而降低。这是由于水蒸气蒸发导致吸收液浓度降低,而RuO4生成速度过快,未能及时被吸收即随尾气排出,使蒸馏回收率降低。因此,选择蒸馏温度为80 ℃。
2.1.2 氧化剂用量
Ru8+/Ru4+的标准电位为1.4 V,可选氧化剂有KMnO4、NaClO、NaClO4和K2Cr2O7。试验比较了这4种氧化剂对钌的氧化效果,结果为:KMnO4>NaClO4>NaClO>K2Cr2O7,因此选择KMnO4作为氧化剂。
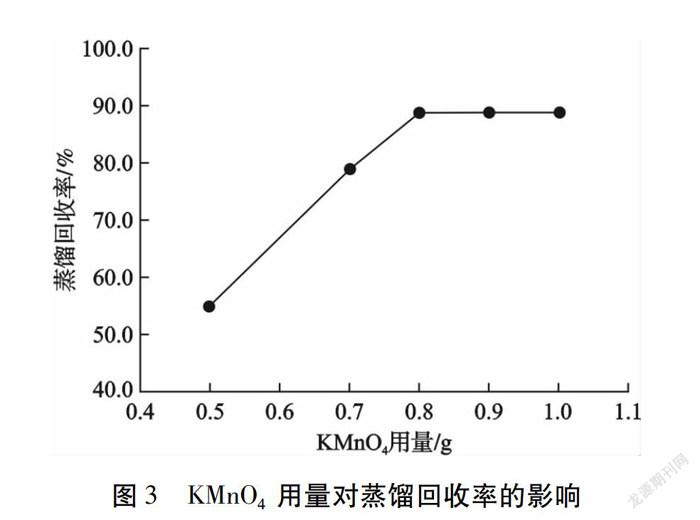
以H2SO4为酸性介质,6 mol/L HCl为吸收剂,蒸馏温度为80 ℃,蒸馏时间为1 h,探讨KMnO4用量对钌蒸馏回收率的影响,结果如图3所示。由图3可知:蒸馏回收率随KMnO4用量的增加而增大。当KMnO4用量高于0.8 g后,蒸馏回收率变化不大,试验选择KMnO4用量为0.8 g。此外,在酸性条件下,随着镀钌废液中的钌被氧化成RuO4,KMnO4分解,酸逐渐消耗,pH增大,致使氧化剂氧化性降低,反应速率下降甚至停止。因此,蒸馏时应适当补充酸与氧化剂,使反应能够反应完全。
2.1.3 吸收剂的选择
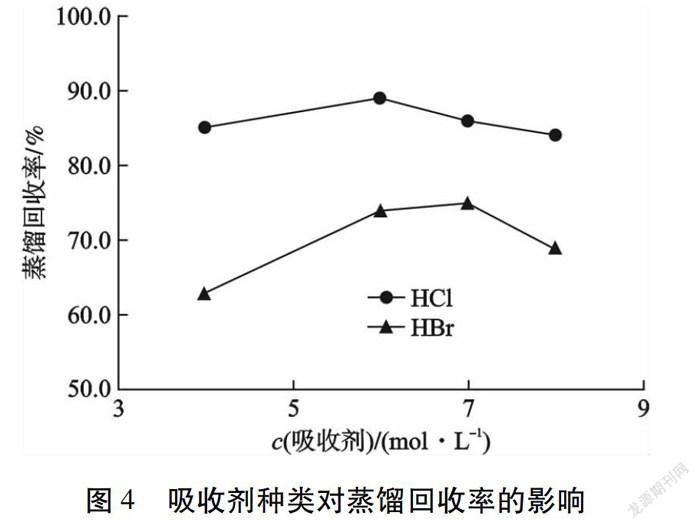
在蒸馏温度为80 ℃,KMnO4-H2SO4为氧化剂,蒸馏时间为1 h条件下,比较HCl和HBr对蒸馏液的吸收效果,结果如图4所示。由图4可知:HCl吸收液效果优于HBr。当HCl浓度为6 mol/L时,蒸馏回收率最高为89.0 %。在酸性条件下,HBr稳定性较差,HBr吸收钌的饱和度低于HCl,因此HCl吸收效果好。当HCl浓度低于6 mol/L时,随酸度增加,蒸馏回收率增大,直至饱和;HCl浓度过高,挥发出的HCl气体与蒸馏出的RuO4生成黑色固体RuCl3凝结于管壁,用硫脲-HCl溶液冲洗可生成蓝色络合物[14]。综合考虑,选择6 mol/L HCl作为RuO4的吸收剂。
在蒸馏温度为80 ℃,KMnO4-H2SO4为氧化剂,6 mol/L HCl为吸收剂,蒸馏时间为1 h条件下,蒸馏回收率可达到89.0 %。蒸余液经过滤定容后,测得钌质量浓度为494 mg/L,用于萃取工艺条件的研究。
2.2 萃取工艺条件
2.2.1 预氧化剂的选择
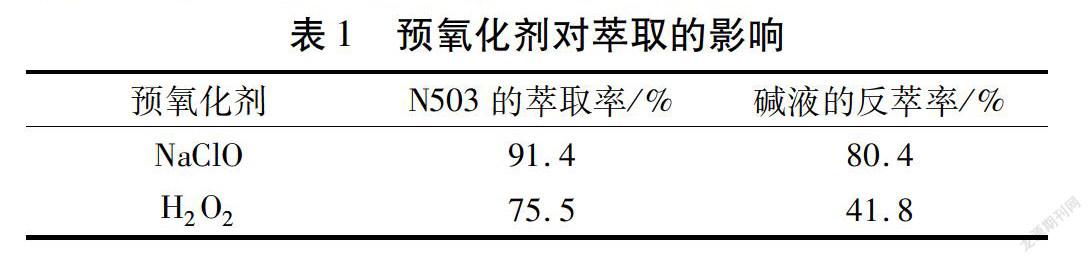
当萃取剂为30 %N503,萃取相比为1,反萃剂为2 mol/L NaOH溶液,反萃相比为1时,考察不同预氧化剂对萃取的影响,结果如表1所示。
由表1可知:相同条件下,NaClO作为预氧化剂时,萃取率与反萃率较高,说明NaClO预氧化的效果优于H2O2。由于H2O2为两性化合物,致使生成的RuCl2-6不稳定,萃取率较低。综上,试验选用10 %NaClO作為钌的预氧化剂,同时加入NaCl,是为了增强RuCl2-6的稳定性。
2.2.2 萃取剂体积分数
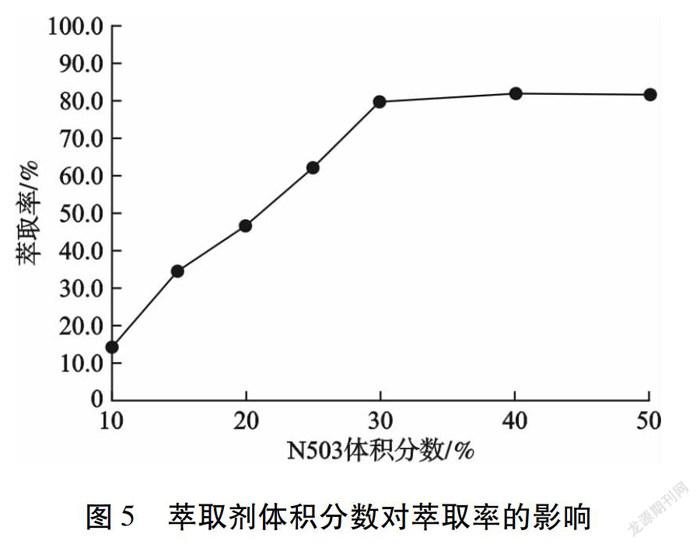
以磺化煤油为稀释剂,正辛醇为破乳剂,配制不同体积分数N503对等体积的蒸余液进行萃取。当萃取相比为1,反萃剂为2 mol/L NaOH溶液,反萃相比为1时,萃取剂体积分数对钌萃取率的影响如图5所示。由图5可知:当N503体积分数低于30 %时,萃取率随体积分数增加而增大;当N503体积分数达到30 %后,萃取率仍有提高,但幅度不大,且分相时间明显增长。这是因为萃取剂体积分数增加,有机相密度增大,萃取速率降低,导致分相时间延长。因此,N503最佳体积分数为30 %。
2.2.3 萃取相比
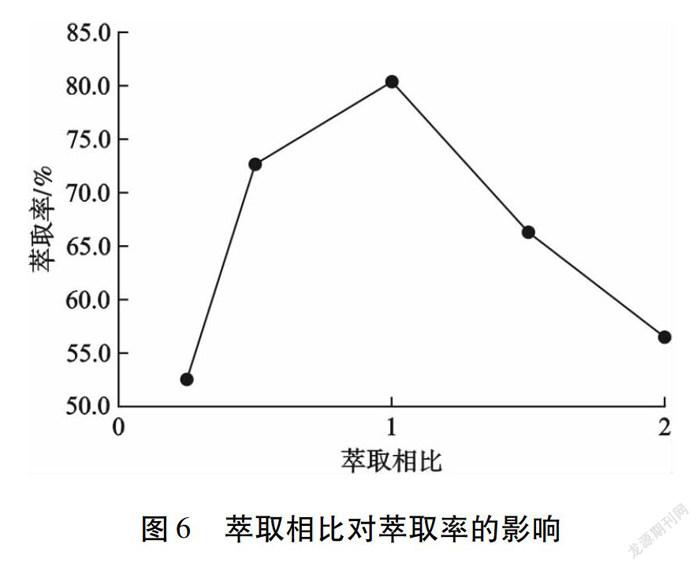
10 %NaClO为预氧化剂氧化Ru(Ⅳ),萃取剂为30 %N503,反萃剂为2 mol/L NaOH溶液,反萃相比为1,不同萃取相比(O/A)对钌萃取率的影响如图6所示。由图6可知:当萃取相比小于1时,随萃取相比增加,萃取率增大,分相时间缩短;当萃取相比为1时,萃取率达到峰值,为80.4 %;当萃取相比大于1时,萃取率随萃取相比增大而降低,且分相时间增长,萃取困难。综合考虑分相性能与萃取率,最佳萃取相比为1。
2.2.4 反萃条件
10 %NaClO为预氧化剂氧化Ru(Ⅳ),萃取剂为30 %N503,萃取相比为1,反萃剂为NaOH溶液,反萃相比为1,考察2~4 mol/L NaOH溶液对钌反萃率的影响。试验结果表明,碱液浓度对钌反萃率影响不大。综合考虑反萃率及分相效果,试验确定2 mol/L NaOH溶液作为反萃剂。
控制NaOH溶液浓度为2 mol/L,其他条件不变,改变反萃相比,比较钌反萃率。试验结果表明:随着反萃相比增大,钌反萃率逐渐增大。当反萃相比大于1时,钌的反萃取趋于饱和。因此,试验选择反萃相比为1,此时钌反萃率为80.4 %。
2.3 钌的分析
采用重量法测得蒸馏得到的β-RuCl3·xH2O晶体中钌质量分数为38.8 %,与理论值35 %~38 %相一致[1]。
3 结 论
1)试验确定了氧化蒸馏法回收镀钌废液中三氯化钌的最佳工艺条件:蒸馏温度为80 ℃,蒸馏时间为1 h,以KMnO4-H2SO4为氧化剂,6 mol/L HCl为吸收剂,减压蒸馏温度为50 ℃~75 ℃。最佳工艺条件下,三氯化钌的蒸馏回收率可达到89.0 %,蒸馏得到的β-RuCl3·xH2O晶体中钌质量分数为38.8 %(理论值为35 %~38 %)。
2)试验确定了萃取法处理蒸余液的最佳工艺条件:以10 %NaClO为预氧化剂氧化Ru(Ⅳ),萃取剂为30 %N503,萃取相比为1,反萃剂为2 mol/L NaOH溶液,反萃相比为1,钌反萃率达到80.4 %。
3)试验优化了传统氧化蒸馏法制备三氯化钌的工艺条件,与单一蒸馏法相比,蒸馏—萃取联合法再生钌的总回收率达到了96.9 %,提高了7.9百分点,钌回收率得到了有效提高。
[参考文献]
[1] 霍春光.三氯化钌产品的质量控制[J].氯碱工业,2000(9):23-24.
[2] BERNARDIS F L,GRANT R A,SHERRINGTON D C.A review of methods of separation of the platinum-group metals through their chloro-complexes[J].Reactive and Functional Polymers,2005,65(3):205-217.
[3] 杨红艳.复杂二次资源物料中钌的富集方法及ICP-AES测定技术研究[D].昆明:昆明贵金属研究所,2012.
[4] 刘利,崔文权,潘鑫.废钌/氧化铝催化剂中钌的回收研究[J].无机盐工业,2010,42(5):48-49,55.
[5] 赵喜太.回收贵金属钌工艺技术的研究[D].沈阳:东北大学,2010.
[6] 杜继山.碱熔法回收废钌炭中的钌[J].化工管理,2016(13):201.
[7] 郁丰善.蒸馏-吸收重量法测定高含量钌废料中的钌[J].中国资源综合利用,2015,33(11):21-23.
[8] 郭俊梅,韩守礼,谭文进,等.氢还原重量法测定三氯化钌产品中钌的含量[J].中国无机分析化学,2014,4(3):44-51.
[9] 赵鹏,姚燕燕,田晓珍,等.醇热还原法制备纳米金属钌颗粒[J].中国有色金属学报,2004,14(11):1 953-1 957.
[10] GALOV J,HEJDA S,STAVREK P,at el.Pervaporation of(R)/(S)-methyl 3-hydroxybutyrate(ΣMHB) from a mixture containing an ionic liquid,methanol and Ru catalyst[J].Separation and Purification Technology,2019,222:45-52.
[11] 贺小塘.钌的氯配合物及其分离提纯理论基础[J].有色金属(冶炼部分),2016(11):39-42.
[12] 余建民,刘时杰.胺类萃取剂在贵金属溶剂萃取中的应用[J].贵金属,1996,17(1):51-57.
[13] 余建民.贵金属分离与精炼工艺学[M].北京:化学工业出版社,2010:264.
[14] 管有祥.碱熔解-硫脲比色法快速测定钌碳催化剂中的钌[J].贵金属,2010,31(3):52-55.
Distillation-extraction joint method for regeneration
of ruthenium trichloride in ruthenium plating liquid waste
Shao Ying,Wang Qi,Zhou Quanfa
(College of Chemistry and Environmental Engineering,Jiangsu University of Technology)
Abstract:The traditional oxidation distillation process for ruthenium recovery from ruthenium liquid waste was optimized because the loss rate of ruthenium is high,and the distillation residue was treated by extraction.The effects of distillation temperature,oxidant dosage,absorbent and pre-oxidation and extraction agent volume fraction,O/A and reverse extraction conditions on ruthenium recovery were discussed.The results show that with KMnO4-H2SO4 as oxidant and 6 mol/L HCl as absorbent,the ruthenium yield reached 89.0 % at the distillation temperature of 80 ℃ for 1 h.With the distillation residue regenerated,the reverse extraction rate reaches 80.4 % when the volume fraction of extractant N503 is 30 %,the O/A is 1,the reverse extraction agent is 2 mol/L NaOH,and the reverse O/A is 1.The total recovery of ruthenium recovered by the joint distillation and extraction method was 96.9 %,which was 7.9 percen-tage points higher than that of the single distillation method,thus effectively improving the regeneration utilization rate of ruthenium.
Keywords:oxidation distillation;extraction;reverse extraction;ruthenium plating liquid waste;ruthenium trichloride
收稿日期:2019-06-24; 修回日期:2020-02-01
基金项目:国家重点研发计划项目(2018YFC1902503-2);江苏省研究生科研与实践创新计划项目(SJCX18_0996)
作者简介:邵 莹(1994—),女,江苏宜兴人,硕士研究生,研究方向为资源循环利用;江苏省常州市钟楼区中吴大道1801號,江苏理工学院化学与环境工程学院,213001;E-mail:2933036842@qq.com
