基于核心素养培养的高中化学教学方法研究
2020-09-10陈志刚
陈志刚
【摘要】笔者在深入学习研究高考试题的基础上,在教学实践中有意识地进行实证教学、建构思维和合作探究等教学方法对学生进行核心素养的培养。期待学生在解答高考题和面对未来的生活都能游刃有余。
【关键词】核心素养;高中化学;教学方法
化学学科核心素养是指学生在学习化学学科的过程中逐渐形成的品格、关键能力和正确的价值观念。2017年版普通高中化学课程标准指出宏观辨识与微观探析、变化观念与平衡思想、证据推理与模型认知、科学探究与创新意识、科学态度与社会责任,是化学学科的核心素养。课标中所提出的化学学科核心素养,反映的是“社会主义核心价值观下化学学科育人的基本要求”[1]。作为一线教师,我们需要在教学实践研究和探讨培养学生化学学科核心素养的途径和策略。基于核心素养的培养,笔者在分析2020年江苏高考化学试卷题目的过程中谈谈研究高中化学教学的几点做法,以期与各位同行交流。
一、实证教学培养证据推理意识
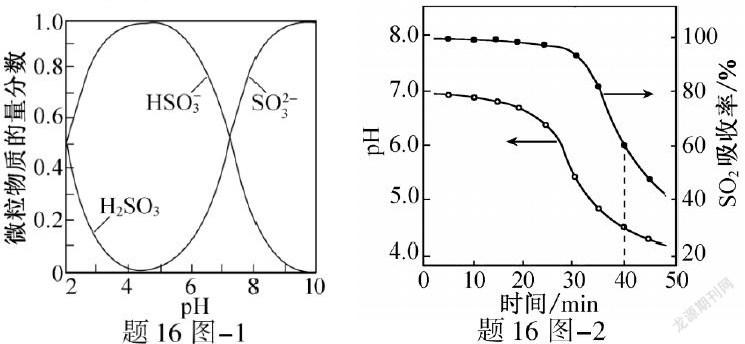
(2020年江苏高考化学16)[2]吸收工厂烟气中的SO2,能有效减少SO2对空气的污染。氨水、ZnO水悬浊液吸收烟气中SO2后经O2催化氧化,可得到硫酸盐。已知:室温下,ZnSO3微溶于水,Zn(HSO3)2易溶于水;溶液中H2SO3、、的物质的量分数随pH的分布如题16图−1所示。(1)氨水吸收SO2。向氨水中通入少量SO2,主要反应的离子方程式为▲;当通入SO2至溶液pH=6时,溶液中浓度最大的阴离子是▲(填化学式)。(2)ZnO水悬浊液吸收SO2。向ZnO水悬浊液中匀速缓慢通入SO2,在开始吸收的40min内,SO2吸收率、溶液pH均经历了从几乎不变到迅速降低的变化(见题16图−2)。溶液pH几乎不变阶段,要产物是▲(填化学式);SO2吸收率迅速降低阶段,主要反应的离子方程式为▲。
(3)O2催化氧化。其他条件相同时,调节吸收SO2得到溶液的pH在4.5~6.5范围内,pH越低生成速率越大,其主要原因是▲;随着氧化的进行,溶液的pH将▲(填“增大”、“减小”或“不变”)。
从16题我们可以看出高考题会出现对化学方程式书写进行考察的题目,有的方程式是我们熟悉的,有些是没有见过的陌生情景下的方程式的书写,方程式的书写当然不是纯考哪位学生的记忆力好,更侧重于化学素养的考察。素养不是一朝一夕形成的,是在三年的学习中逐渐形成的。在方程式的教学中,笔者一直坚持采用实证的教学方法,学习新的方程时通过化学实验检验反应能否发生,通过理论分析预测可能的产物,通过化学实验确认产物,理论分析生成此产物的原因,通过观察法或者氧化还原反应化合价升降法配平化学反应方程式,
所有的化学方程式的反应物和生成物均来自于化学实验,在这个学习过程中变纯机械记忆方程式的方法为证据推理理解的方法,可培养学生的证据推理意识。16题(1)向氨水中通入少量SO2时,SO2与氨水反应生成亚硫酸铵,反应的离子方程式为2NH3+H2O+SO2=2+(或2NH3·H2O+SO2=2++H2O);(2)反应开始时,悬浊液中的ZnO大量吸收SO2,生成微溶于水的ZnSO3,此时溶液pH几乎不变;一旦ZnO完全反应生成ZnSO3后,ZnSO3继续吸收SO2生成易溶于水的Zn(HSO3)2,此时溶液pH逐渐变小,SO2的吸收率逐渐降低,这一过程的离子方程式为ZnSO3+SO2+H2O=Zn2++2(或ZnO+2SO2+H2O=Zn2++2)(3)pH值大于6.5时,S(IV)以微溶物ZnSO3形式存在,使S(IV)不利于与O2接触,反应速率慢;pH降低,S(IV)的主要以形式溶于水中,与O2充分接触。因而pH降低有生成速率增大;随着反应的不断进行,大量的反应生成,反应的离子方程式为2+O2=2+2H+,随着反应的不断进行,有大量的氢离子生成,导致氢离子浓度增大,溶液pH减小。虽然我们教学中没有默写或者精心仔细的讲解过这三个方程式2NH3+H2O+SO2=2+、ZnSO3+SO2+H2O=Zn2++2、2+O2=2+2H+,但我相信大部分学生都可以正确写出来。这三个方程式对知识的考察类似于逐渐向氢氧化钠中通入CO2或者将CO2不断通入澄清石灰中,通过实验现象和理论分析,相信学生们都能知道通入少量CO2的生成碳酸盐,再通入CO2会生成碳酸氢盐,利用第三个方程式分析解答题,也不难,因為在学习SO2的性质时,用这个方程式解释为什么时间越久酸雨酸性越强。
二、建构思维模型,培养模型认知
成功解答16题,还需要学生们细心地读图,在教学实践中,笔者会和学生们一起构建一个解答图像题的思维模型,以题16图−1为例,需要看图像的横纵坐标,从图中可以看出,是溶液中H2SO3、、的物质的量分数随pH的分布,曲线的起点、拐点、最高点、交叉点、终点及曲线的变化趋势,横坐标相同时如何分析纵坐标的变化,纵坐标相同时如何分析横坐标,很多因素影响曲线变化时如何控制变量只分析一种因素的影响,建构解答图像题的模板,构建图像解答的思维模型。当然,在教学中还可以建立多种多样的思维模型,比如解答平衡移动题时构建“平衡移动原理模型”,学习物质的量时建立微观的NA和宏观的M之间的计算模型,计算题中的质量守恒、化合价升降相等、差量法等计算模型。
三、合作探究,培养科学探究意识
2020年江苏高考化学19最后一题中需要学生们设计实验方案,顺利解答这个问题学生有一定的探究意识。在平时的教学中,笔者有意识地让学生进行合作探究,学生们以小组讨论的形式分析讨论,如学习制取漂白液的反应时,笔者会出问题:将氯水加入含有酚酞的氢氧化钠溶液中,红色褪去,请问褪色原因,以小组为单位设计实验方案证明你的推测,在这个过程中,学生们需要开动脑筋,在熟悉次氯酸强氧化性漂白和氢氧化钠和氯气反应的基础上思考可能的原因并加以验证。平时积攒了能力,在考试答题中才能游刃有余。
参考文献:
[1]中华人民共和国教育部.普通高中化学课程标准(2017年版).北京:人民教育出版社,2018
[2]2020年江苏高考化学试卷
湖北省孝感高级中学 432000
