以无机元素为特征指标的太和贡椿指纹图谱研究
2020-09-10张德欣郭斌刘艳芳杨永学廖洪梅
张德欣 郭斌 刘艳芳 杨永学 廖洪梅



摘要:以4种常量元素和4种微量元素为特征指标,研究了其基本含量,在国标方法的基础上进行了改进,建立了原子吸收分光光度法测定K,Na,Ca,Mg,Fe,Zn,Mn,Cu的测定方法,指出太和贡椿中矿物元素含量丰度依次为K,Na,Ca,Zn,Fe,Mg,Mn,Cu;并与其他产地的香椿进行了差异性分析,为太和贡椿建立以矿物元素为参数的特征指纹图谱,提供了借鉴。
关键词:太和贡椿;矿物元素;含量;指纹图谱
中图分类号:O65 文献标志码:A doi:10.16693/j.cnki.1671-9646(X).2020.02.047
Abstract:In this study,four major elements and four trace elements were taken as the characteristic indexes,and their basic contents were studied. Based on the national standard method,an improved method for the determination of K,Na,Ca,Mg,Fe,Zn,Mn,Cu by atomic absorption spectrophotometry was established. It was pointed out that the abundance of mineral elements in Taihe tribute toon was K,Na,Ca,Zn,Fe,Mg,Mn,Cu,and compared with the Chinese toon produced in other places,it provides a reference for establishing the characteristic fingerprint of Chinese toon in Taihe with mineral elements as parameters.
Key words:Taihe tribute toon;mineral elements;content;fingerprints
0 引言
香椿(Toona sinensis)又名香椿芽、香桩头、大红椿树、椿天等,在安徽地区也有叫春苗。中国人食用香椿久已成习,尤其在谷雨前采摘的椿芽,更是香鲜脆嫩、清香扑鼻,食之能使人提神、明目。椿芽营养丰富,并具有食疗作用[1],主治外感风寒、风湿痹痛、胃痛、痢疾等。据《中国中药大全》记载,椿芽可防止咳嗽、嘶哑、水土不服及妊娠反应等症状。香椿的生理学功效与其矿物质元素的含量也具有密切的关联性[2]。太和香椿[3]历史悠久。唐代曾用此物作贡礼,清朝被御封为“贡椿”,名扬天下,是安徽省特产名品。太和椿芽营养物质含量极为丰富,所含有的营养物质都为人体所需要,具有很高的药用价值。
太和贡椿生产基地主要分布在颍河沿岸的河床漫滩冲积的沙淤两合土和少量沙土的乡镇。实践表明,青沙土、两合土为香椿适生土壤,淤土次之,黑土生长较差。树木品种、适宜的生长土壤和优越的气候条件,是造就地方名优土特产品的先决条件。是太和贡椿与其他地区的香椿存在差异性的决定因素,也是分析太和贡椿“特征指纹图谱”的先决物质条件。
当前,对于太和贡椿这一“安徽省特产名品”,则缺乏相应的研究和原产地保护措施。旨在通过检测多种微量元素的含量探讨并建立太和贡椿中人体必需微量元素种类、含量,以及对太和贡椿品质的影响规律,探知以太和贡椿中各种微量元素种类及含量为基础指标的太和贡椿质量品质等级评价体系,初步建立以钙、镁、磷、钠、钾、铁、碘、硒、锌、锰等常微量元素和含量为主导指标的太和贡椿特征“指纹特征”图谱,保护地方特产声誉。引导椿农产业化种植,加快香椿种植的集约化、产业化进程,提高椿农收入,尽快脱贫致富,以及为后续的香椿系列产品开发提供技术支持。
1 材料与方法
1.1 材料
香椿芽A號,2019年4月14日采于安徽太和县香椿良种采穗园,桩头芽叶数9~11支,芽头鲜嫩,色泽油光,肉质肥厚;香椿芽B号,2019年4月 15日采于亳州市谯城区双沟镇秦大园自然村,桩头芽叶数6~9支,色泽较深,肉质稍干瘦。2种产品直线南北距离约60 km(A产品在南,B产品在北)。
1.2 仪器与试剂
Thermo型超低温冷冻冷藏冰箱、DZ-280/2SD型小型多功能真空封装机,东莞市金桥科技电器制造有限公司产品;METTLER TOLEDO型电子天平,梅特勒-托利多集团产品;IM-82002型电子天平,诸暨市超泽衡器设备有限公司产品;DHG-9040A型电热恒温鼓风干燥箱,宁波江南仪器厂产品;KDN-08型消化炉,上海昕瑞仪器仪表有限公司产品;EPED-10TS型实验室级超纯水机,南京易普易达科技发展有限公司产品;TAS-990型原子吸收分光光度仪(配GF-990石墨炉电源),北京普析通用仪器有限公司产品。
K,Na,Ca,Mg,Fe,Zn,Mn,Cu标准溶液,国家有色金属及电子材料分析测试中心提供,标准值为1 000 μg/mL;硝酸、高氯酸、氯化铯、盐酸、氧化镧,国药集团化学试剂有限公司提供。
所有玻璃仪器均以硝酸(1+5)浸泡24 h以上,用自来水反复冲洗,最后用蒸馏水冲洗,晾干后方可使用。
1.3 样品保存与处理
1.3.1 样品保存[4]
采集的新鲜样品立即分装于薄膜保鲜袋中,每袋约200 g,用真空封装机抽真空封装,放置在超低温冷藏冰箱中速冻至-50 ℃,并在该温度下保藏,备用。
1.3.2 样品消化
将新鲜的椿芽在日光下晒干,粉碎机粉碎,过60目筛,精密称取约5.000 g(精确至0.000 1 g),置消化管中,参照GB 5009.91—2017标准5.2.3湿式消解法消化,称取的样品置消化管中,加硝酸20 mL,高氯酸1 mL,在消化炉上逐步加热消解,条件为120 ℃/0.5~1.0 h升至180 ℃/2~4 h,再升至220 ℃持续加热,若在消化过程中液体过少或者消化液呈棕褐色,则适量补加硝酸,直至消解至冒白烟、消化液呈无色透明或略带黄色,视为消化完全,取出消化管,冷却至室温。然后以2%硝酸溶液定容至250 mL容量瓶中,备用。同时做空白试验。
1.4 标准溶液的制备
将标准溶液用质量分数2%硝酸梯度稀释,首先配成质量浓度100 μg/mL的储备液;然后再测定时,再按对应的国标方法将储备液稀释成对应质量浓度的标准工作液。其中,K,Na,Ca,Fe标准工作液的质量浓度为100.0 μg/mL;Mg,Zn,Mn,Cu标准工作液的质量浓度为10.0 μg/mL。
1.5 测定方法
1.5.1 水分含量测定
基本方法参照GB 5009.3-2016[5];采用两步法:称取新鲜的椿芽样品约500 g(精确到0.01 g),自然条件下风干20 h以上(试验采用35℃日光下晾晒20 h以上),达到安全水分以下,称质量。粉碎机粉碎,过60目筛,混匀,贮于干净的棕色磨口瓶中备用。后续用105 ℃恒质量法测定自然干燥的水分,根据自然晾晒失水和恒质量法测定的水分含量,计算新鲜椿芽样品的水分含量。
后续的各矿物元素含量,依据样品水分含量,折算成干物质含量计。
1.5.2 K,Na的测定
测定方法参照GB 5009.91—2017[6]。
1.5.3 Ca的测定
测定方法参照GB 5009.92—2016[7]。
1.5.4 Fe的測定
测定方法参照GB 5009.90—2016[8]。
1.5.5 Mg的测定
测定方法参照GB 5009.241—2017[9]。
1.5.6 Zn的测定
测定方法参照GB 5009.14—2017[10]。
1.5.7 Mn的测定
测定方法参照GB 5009.242—2017[11]。
1.5.8 Cu的测定
测定方法参照GB 5009.13—2017[12]。
调整仪器参数,待仪器稳定后,将标准系列溶液样品处理液(做3个平行样)与试剂空白分别依次导入仪器,进行测定。
1.6 各元素测定的仪器工作参数
各元素测定仪器工作参数见表1。
2 结果与分析
2.1 样品消解
在按照1.3.2的样品消解过程中,都按湿法消解的操作方法,大同小异却略有差异,主要表现在取样量要求、加入硝酸和高氯酸的比例,试验采用一次消化测定多种元素的方法,提高了试验效率。
2.2 线性范围
在进行条件优化的前提下,进样系统依次导入标准溶液系列、待测样品和试剂空白样,仪器自动绘制标准曲线,得到各元素的线性方程和相关系数。结果表明,K,Na,Ca,Fe在0~200 μg/mL,相关系数R2≥0.999 5;Mg,Zn,Mn,Cu在0~20 μg/mL的范围内R2≥0.995 0,线性关系良好。
各元素测定线性关系见表2。
2.3 方法检出限[13]
以标准序列质量浓度梯度最接近于“0”的质量浓度梯度值,连续进样12次,得出测定值,计算测定值的标准偏差、样品测定平均值,按下式计算方法检出限值:
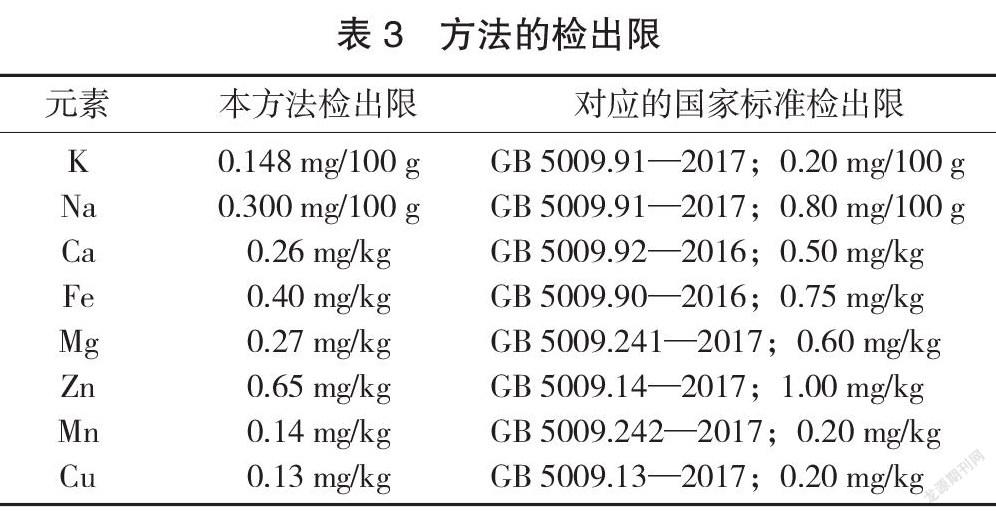
方法的检出限见表3。
由表3可以看出,对上述7种元素的检测限低于对应的国家检测标准检出限值,证明能够满足分析测定要求。
2.4 方法稳定性
准确移取在“1.3”“1.4”项下制备并与4 ℃保存的供试样品,分别于24,48,72,96,120 h做相关元素的重复测定,计算测定结果的平均值和RSD值,结果显示,各元素测定值的RSD值均小于5%,表明该消解方法和保存措施在一定的时间范围内,具有较好的稳定性。
2.5 重复性试验
对在4 ℃密闭保存的供试样品,按照同样的样品处理和测定方法,平行测定5次,计算各元素的平均含量和RSD,结果显示RSD均小于5%,表明该测定方法重复性良好。
2.6 精密度和加标回收试验
在4 ℃密闭保存的供试样品,经“1.4”项下方法再次制备,在供试样品中精密加入各元素标准溶液(加入量为标准曲线第3个定量点的标准溶液对应的元素质量),按“1.5”项下方法进行测定,平行试验5次,根据测定结果计算加标回收率。结果表明,加标回收率为98.7%~102.6%,RSD范围为 0.975%~1.350%,说明该方法具有良好的精密度。
2.7 样品分析测定结果
2.7.1 样品水分含量
采用两步法对样品中的水分含量进行了测定。
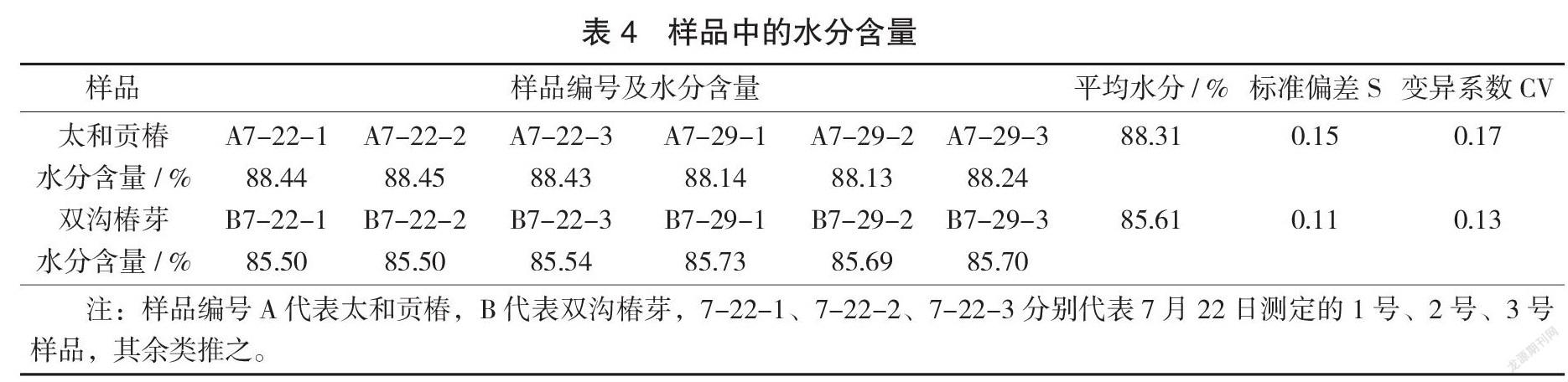
样品中的水分含量见表4。
由表4可以看出,在同期采集的样品中,太和贡椿比雙沟椿芽水分高出约2.7%,这说明太和贡椿更加脆嫩,形态更坚挺,口感也更好。
2.7.2 检测矿物质元素含量
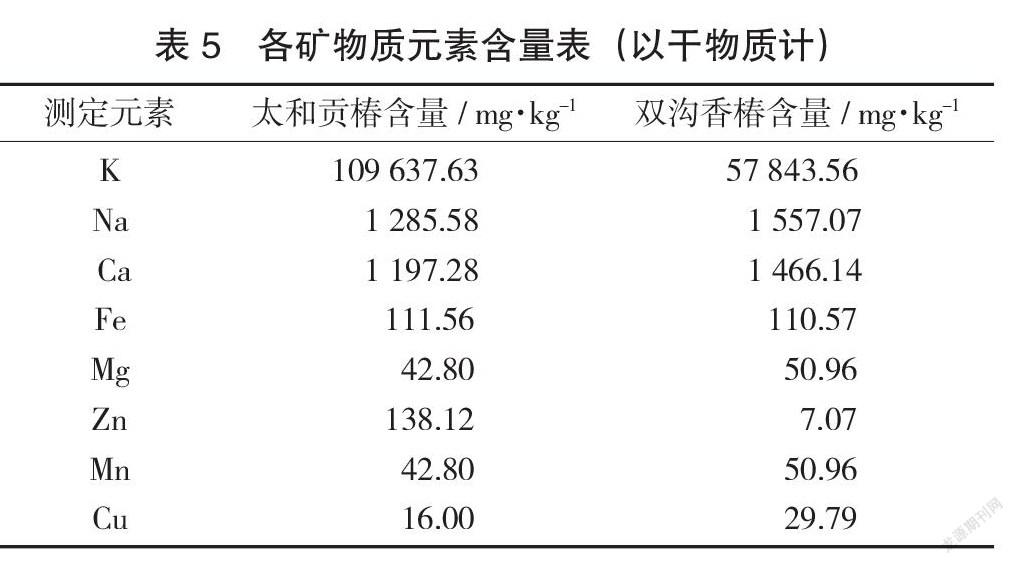
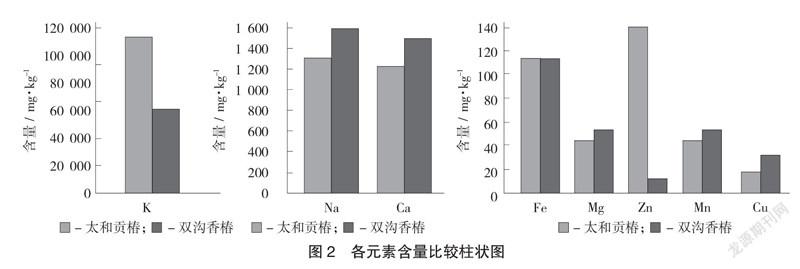
各矿物质元素含量表(以干物质计)见表5,各元素含量比较柱状图见图2。
以上测定结果表明:
(1)太和贡椿水分含量显著高于同期的双沟香椿,是保证其具有良好脆度和口感的重要因素。
(2)以测定的8种常量、微量元素为分析判断基础,太和贡椿最丰富的矿物质元素是K,含量为109.6×103 mg/kg(以干物质计,下同),其他元素按丰度计,依次为Na 1 285.6 mg/kg,Ca 1 197.3 mg/kg,Zn 138.1 mg/kg,Fe 111.6 mg/kg,Mg 42.8 mg/kg,Mn 42.8 mg/kg,Cu 16.0 mg/kg。
与对照测定的亳州双沟香椿相比较,太和贡椿的K和Zn含量,明显高出双沟香椿。其中,太和贡椿的K和Zn含量分别是双沟香椿的1.90倍和19.54倍;这可能是太和贡椿与其他香椿品质具有显著差异性的重要因素之一。
(3)太和贡椿Ca元素含量低于双沟香椿约20%,可以解释为何太和贡椿具有良好的脆度和口感;在Mg,Mn,Cu 3种元素含量方面,虽然2种样品略有差异性,但相对差距不是十分悬殊且都是低含量水平,尚无法说明其对太和贡椿品质贡献度的影响度。
(4)在不讨论黄酮类等其他生理活性物质对太和贡椿的保健作用的贡献度的前提下,揭示太和贡椿的高K和高Zn含量,对于说明太和贡椿的保健作用也是有正向效应的。K可以形成某些酶(果糖激酶、磷酸丙酮酸转磷酸酶等)的辅因子[14];作为细胞内液的主要阳离子,对于维持细胞的完整性十分重要。钾也是钠泵的组成部分。在生物膜上,钾离子和钠离子的交换,往往与一些重要的生理过程有关,如神经冲动的传递,以及肌肉的收缩。心脏的正常搏动有赖于钠、钾等离子的协同作用。碳水化合物和蛋白质的代谢也需要钾的帮助。钾和钠一样,对于身体维持电位差和渗透压、维持电解质平衡具有关键作用。
锌作为体内多种酶和活性蛋白质维持结构稳定和生物活性的必要因子,其生理功能极其重要且多样。例如,锌是稳定细胞膜结构的重要因素、对于预防自由基伤害和维持正常免疫功能也是必需的;锌还参与胰岛素的合成和释放,以及甲状腺激素的作用;锌因参与维A在视觉细胞中的转运和转化为视黄醛的过程而为形成正常视力所必需;锌是味蕾当中味觉蛋白的成分,因此为正常的味觉功能所必需;锌是DNA合成的必要因素,所有细胞的分裂和增殖均需要锌的帮助等。通过上述分析,有理由相信,太和贡椿的高K和高Zn的微量元素含量特征,是形成太和贡椿优秀食品质量特征的重要因子。
(5)以上的8种元素组成,可以认定为以矿物质元素为考量指标的太和贡椿特征指纹图谱。
3 结论
(1)分析的8种元素的组成关系,从一个角度揭示了太和贡椿的产品特征,为太和贡椿原产地保护奠定了化学(成分)特征图谱的部分基础。
(2)结合常量组分分析、包括黄酮类化合物在内的其他生理活性物质测定,可以进一步揭示和完善太和贡椿的化学(成分)特征图谱,结合太和贡椿的生物特征图谱,建立太和贡椿的原产地保护方案和产品分级标准,奠定良好的基础,为这一地方名特产品的产业化发展提供技术支持。
(3)研究具有一定的局限性。一是对于功能性元素(如P,I,Se等)若干常、微量元素没有涉及;二是对有害元素(如Pb,Hg,As,Cr等)尚未涉及;三是测定样品和参比样本数量较少,今后有待于进一步深入研究和探讨,以期丰富相关数据,对于太和贡椿质量评价体系的建立提供更有力的数据支撑。
参考文献:
赵天会. 香椿不同部位药理作用研究[J]. 吉林农业科技学院学报,2018,27(4):8-9,46.
丁素君. 微波消解-ICP-MS测定香椿芽中微量元素含量[J]. 食品研究与开发,2016,37(14):128-130.
杨京霞,李 静,吴婷,等. 太和香椿水提物对秀丽隐杆线虫生物学特征的影响及清除自由基作用的研究[J]. 食品工业科技,2016,30(11):328-331.
胡新,刘小丽,何梦雅,等. 香椿采后生理学变化及其保鲜技术研究进展[J]. 食品与发酵工业,2019,45 (11):286-289.
中华人民共和国国家卫生和计划生育委员会. GB 5009.3—2016食品安全国家标准 食品中水分的测定[S]. 北京:中国标准出版社,2016.
国家卫生和计划生育委员会,国家食品药品监督管理总局. GB 5009.91—2017食品安全国家标准 食品中钾、钠的测定[S]. 北京:中国标准出版社,2017.
国家卫生和计划生育委员会,国家食品药品监督管理总局. GB 5009.92—2016食品安全国家标准 食品中钙的测定[S]. 北京:中国标准出版社,2016.
国家卫生和计划生育委员会,国家食品药品监督管理总局. GB 5009.90—2016食品安全国家标准 食品中铁的测定[S]. 北京:中国标准出版社,2016.
国家卫生和计划生育委员会,国家食品药品监督管理总局. GB 5009.241—2017食品安全国家标准 食品中镁的测定[S]. 北京:中国标准出版社,2017.
国家卫生和计划生育委员会,国家食品药品监督管理总局. GB 5009.14—2017食品安全国家标准 食品中锌的测定[S]. 北京:中国标准出版社,2017.
国家卫生和计划生育委员会,国家食品药品监督管理总局. GB 5009.242—2017食品安全国家标准 食品中锰的测定[S]. 北京:中国标准出版社,2017.
国家卫生和计划生育委员会,国家食品药品监督管理总局. GB 5009.13—2017食品安全国家标准 食品中铜的测定[S]. 北京:中国标准出版社,2017.
吕涛,冯奇. 分析方法检出限的确定[J]. 漯河职业技术学院学报,2007(4):191-192.
范志红. 食物营养与配餐[M]. 北京:中国农业大学出版社,2017:100-109. ◇
