肺部超声在老年肺切除术后患者血管外肺水的评估价值
2020-09-04王研孙思庆周本昊姜迎厚杜成
王研 孙思庆 周本昊 姜迎厚 杜成
血管外肺水(Extravascular Lung Water,EVLW)是肺内血管外的全部液体,取决于肺毛细血管静水压力、肺毛细血管通透性、血浆胶体渗透压、淋巴循环等因素。肺切除术后,由于低氧、液体过负荷、炎症反应、肺循环阻力增加、单肺通气导致肺损伤等众多因素,导致EVLW增加。EVLW增加临床上表现为肺水肿、气体交换受损、呼吸衰竭,并可能导致术后患者急性肺损伤,死亡率20%~100%[1]。
肺切除术后围术期容易出现肺水肿、肺不张、肺部感染等肺部并发症。老年患者心肺代偿功能差,免疫功能下降,可能合并其他基础疾病等原因,导致老年患者围术期更易出现上述并发症。而此类并发症的发生发展往往伴随着血管外肺水的增加。
对于肺切除术后患者EVLW进行早期可靠的评估,并作出及时的处理,可以降低术后并发症的风险。目前用于监测EVLW的方法包括:脉搏指示连续心排出量(PICCO)、CT、胸片、放射性核素等,因其有创性、操作繁琐、准确性不高等因素限制其使用。据报道[2-3],EVLW与通过肺部超声(LUS)评估的B线相关。但对于肺切除术后这类特殊的患者,缺乏相关研究报道。本研究通过部超声对老年肺切除术患者围术期的EVLW进行评估。
资料与方法
一、 一般资料
收集2018年08月-2019年08月收住本院ICU的肺切除术后患者53例。依据手术类型将所有入组患者分为两组,肺叶切除术和亚肺叶切除术。记录患者一般资料、手术时间、APACHEⅡ评分、围术期氧合指数、围术期出入量、既往病史等。术后常规每日行床边X线胸片检查。常规每日进行肺部听诊。本研究符合医学伦理学标准,且经过医院伦理学委员会批准,家属签署知情同意书。
二、 纳入和排除标准
1 纳入标准
(1)≥65岁;(2)计划为治疗目的的选择性肺叶切除术或亚肺叶切除术;(3)美国麻醉医师协会(ASA)评分≤3分;(4)纽约心脏协会(NYHA)评分≤Ⅱ分。
2 排除标准
(1)既往肺纤维化或间质性肺疾;(2)近期胸外科手术;(3)不能按时进行肺部超声;(4)术后需要机械通气;(5)因皮下气肿、过度肥胖等因素导致无法获得清晰的超声图像。
三、方法
1 术前评估
包括详细的病史、血气分析、12导联心电图、肺活量测定、超声心动图,排除右心室负荷过重、左心室舒张功能障碍和心脏功能障碍。
2 麻醉过程
常规术中监测心电图;置入桡动脉导管,以保证持续监测血压;置入颈内静脉置管。麻醉药物选用丙泊酚、咪达唑仑、舒芬太尼、阿曲库铵。所有手术均选用单肺通气(One-lung Ventilation,OLV):置入大小合适的双腔支气管导管,并最终通过利用纤维支气管镜确定两肺分隔。
3 手术过程
所有手术均采用标准后外侧开胸或胸腔镜(Video-Assisted Thoracic Surgery,VATS)。所有手术均包括系统淋巴结切除。所有患者术后立即拔管,术后未再插管。术后常规转入ICU,所有患者常规采用目标导向限制性补液策略(Goal-directed Fluid Restriction,GDFR)。(具体措施如下:围术期术前所有患者均统一禁食禁饮时间,术中麻醉期间采用胸科手术麻醉仅补充生理需要量和术中丢失量,术中补液速度维持在3~5mL/kg/h,术中血压若出现下降,必要时予以血管活性药维持循环稳定。术中采用脉搏压变异度(PPV)行目标导向容量管理监测,术中维持PPV在5~7%,并维持术中循环、尿量、内环境稳定。术后通过超声监测下腔静脉变异指数等方法维持容量稳定。)
4 肺部超声评估
入组患者超声评估经超声培训合格的ICU医师进行并解释,对于患者病情不知晓。入组患者于术前1天、术后第1天、术后第4天进行肺部超声评估。为了避免术中操作、术侧引流管放置以及术侧皮下气肿等因素对于实验结果的干扰,所有肺部超声评估均针对健侧半胸。超声设备:便携彩色多普勒超声诊断仪VⅣID q(GENERAL ELECTRIC,美国)。评估过程:端坐位,同侧手置于颈部后方。采用6分区法[4]:以腋前线、腋后线将健侧半胸分为前、中、后三个区域,以第3肋为界分为六个区域(图1),记录各区域B线,并参照最新国际肺部超声评分表[5]进行半定量评分(见表1、图2)。
四、统计方法
应用SPSS 25.0软件进行统计分析。计数资料采用频数和构成比进行描述,采用行*列表资料的卡方检验。计量资料进行正态检验后,正态分布采用均数±标准差描述,组间比较采用独立样本t检验;非正态分布采用中位数和四分位间距进行描述,组间比较采用秩和检验。重复测定数据采用两因素重复测量的方差分析。P<0.05提示差异有统计学意义
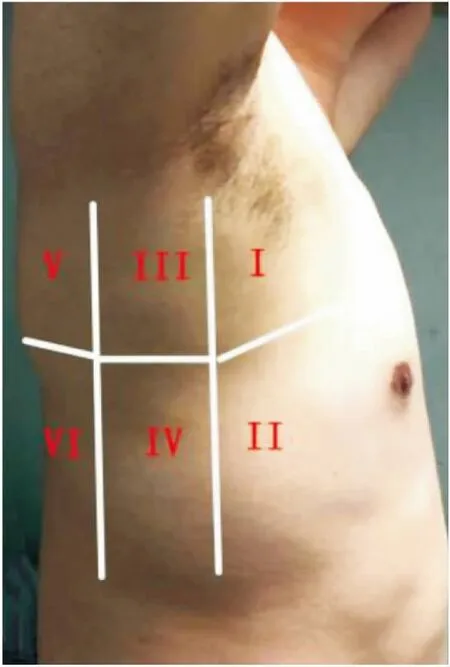
图1 六分区法超声评估

表1 肺部B线半定量评分表

图2 肺部B线半定量评分示例
结 果
一、入院患者一般资料
入院患者组间比较:年龄、性别、既往病史、BMI、APACHEⅡ评分、术侧等均无差异(P均>0.05)。所有患者均顺利完成手术,肺叶切除组的手术时间长于亚肺叶切除组,差异具有统计学差异(P=0.009)(见表2)。术后康复中,仅有1例术后出现肺栓塞,经过抗凝后推迟出院,其余均按时出院。
二、B线及氧合指数在围手术的价值
采用不同术式的老年患者,肺叶切除的B线指数明显高于亚肺叶切除组,差异具有统计学意义(F=4.780,P=0.033)(见图3)。术后1d,患者的B线指数均明显升高,而到4d时明显下降(F=183.047,P<0.01)。术式和时间之间存在交互效应,肺叶切除组术后升高幅度较大(F=3.238,P=0.043)。
术后老年患者氧合指数均于术后1d降低,4d逐渐回升(F=29.380,P<0.01)。术式和时间之间无明显交互效应,不同术式间比较氧合指数也无明显差异(P均>0.05)。
相关性分析:B线指数与氧合指数中度负相关,具有统计学意义(r=-0.408,P<0.01)。
讨 论
因为肺内富含空气,肺部一直使用超声较少。
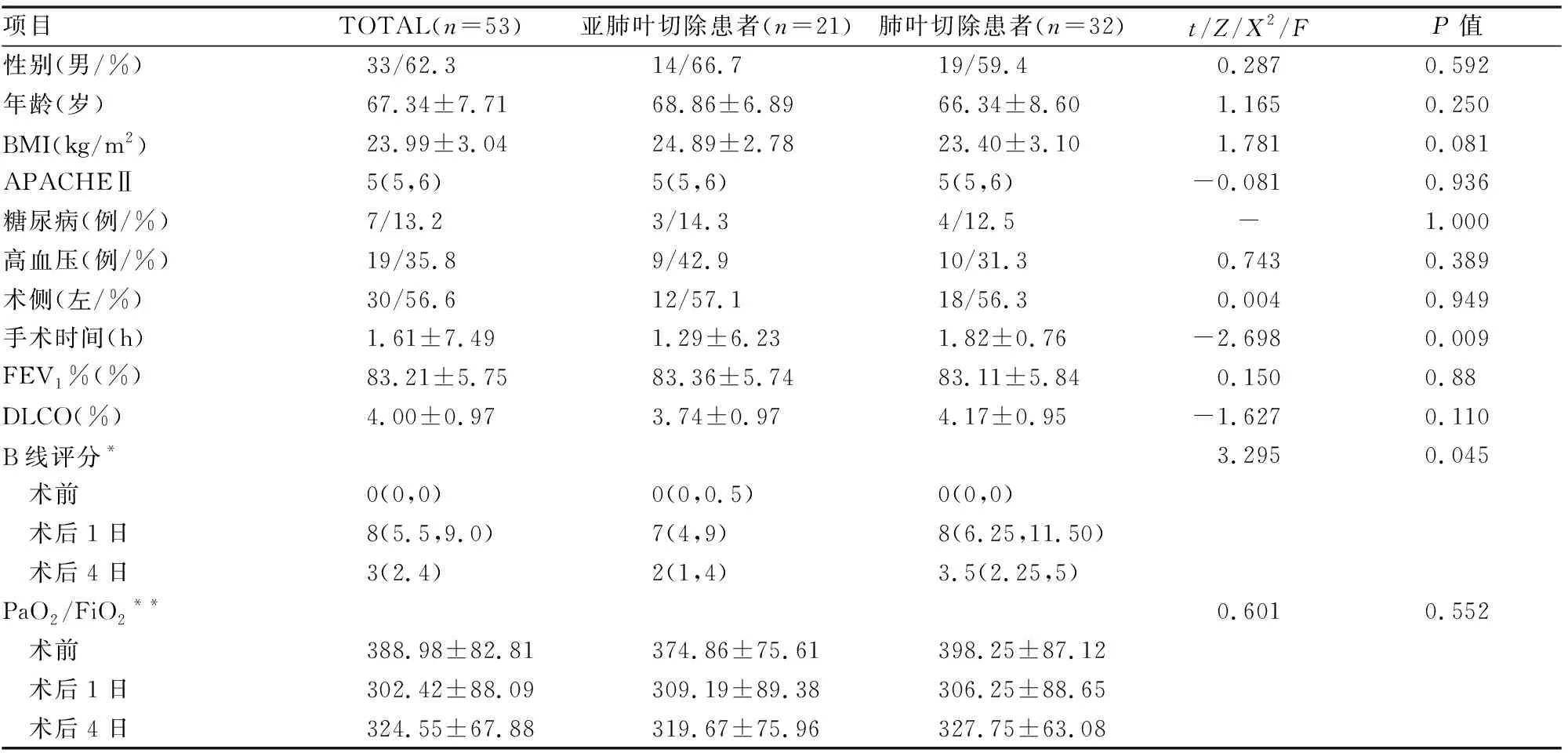
表2 入选患者一般情况
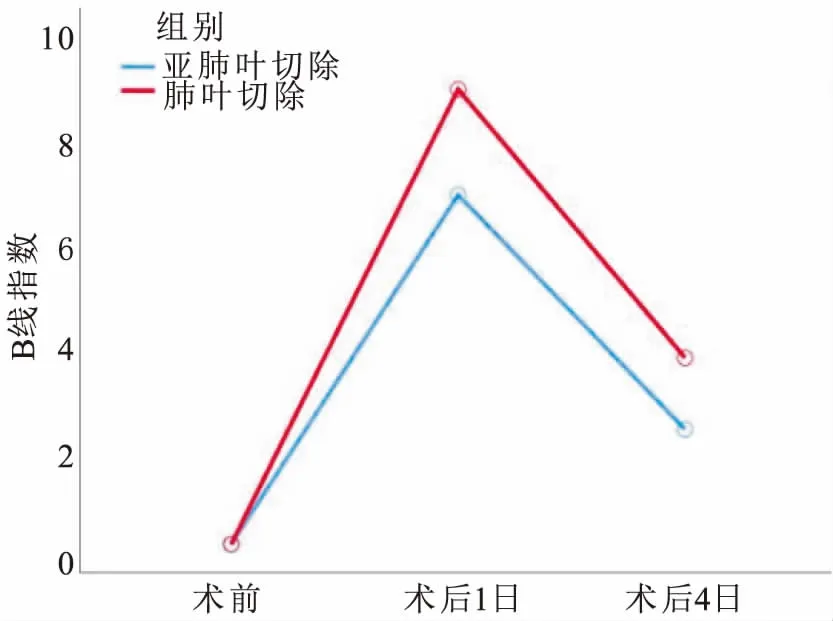
图3 组间围手术期B线评分的估计值
近年来随着肺部超声研究的深入,发现肺内气/水之间不同的比例导致了各种超声征象并用来诊断不同的肺部疾病[6]。其中B线,又称彗尾征( comet-tail sign),被认为是由于水肿、慢性间质性疾病等原因导致小叶间隔增厚而产生的伪像[7]。近年来,国内外学者通过动物尸检称重[8]、PICCO测EVLWI数值[9]、定量CT等不同方法证实了B线征可以用于量化血管外肺水、评估肺水肿的严重程度,是评估半定量评估肺水肿的可靠手段之一。本研究显示B线指数在围术期变化趋势与氧合指数趋于一致,体现了肺切除术患者围术期健侧肺水肿的发生发展吸收的全过程。
本研究结果中可以看出肺切除术后患者血管外肺水较术前明显增加,究其原因有以下几条。
一、肺切除术后由于肺动脉的主要分支破坏,分流血量的减少;肺血管床损失,肺循环阻力增加等原因,病人除呼吸功能受损外,右心的后负荷明显增加。肺叶组的B线评分高于亚肺叶组,不难发现损伤肺组织范围与EVLW相关。
二、围术期不恰当的补液。液体过负荷导致肺毛细血管静水压升高,引起EVLW的增加。
三、OLV引起气压伤、通气/血流比例失调、炎症反应等[10]可能机制导致健侧肺损伤,引起EVLW的增加。上述两点可以从围术期出入量、手术时间与B线评分之间的关系中得到印证。
四、本研究人群为老年患者,基础心肺储备功能差,其并发高血压、糖尿病比率高,肺血管通透性差等。
血管外肺水的增加导致肺顺应性下降、肺泡氧交换障碍引起术后低氧、肺部感染等一系列并发症。但目前临床上缺乏早期评价肺水肿的指标。单纯的肺部听诊准确性差[11],胸部X线存在明显滞后的时效性[12],经PICCO测量EVLW理论上来说准确性最高,但因其有创、繁琐、费用高等弊端,临床上难以推广使用。本研究中,肺部超声对B线的测量可以从术后第1天就可以发现血管外肺水的情况,较胸片较早。究其原因,我们认为B线是由于小叶间隔水肿引起的超声伪影,从原理上说是早于肺部啰音以及胸片改变的。B线的出现提示检测窗中的肺水增多,而本研究在术前1d所有患者均行肺部超声检查,结果B线分值均为0,提示术前患者均不存在肺水肿、肺不张、肺部感染等肺部并发症。而术后肺水的增多,可以表明肺局部通气-血流屏障可能存在破坏,这也是术后肺部并发症发生的病理生理学基础,也是后期发生肺水肿、肺不张、肺部感染等肺部并发症的机制。超声检测可以更加早期以及简便的发现这一现象,早期发现即意味着早期诊断、早期处理,从而降低此类患者围术期并发症的风险。因此超声指导下的血管外肺水监测的诊断效能较高,值得推广。
本研究同样存在一定的局限性。首先这是一项单中心研究;其次由于入组样本量少,未能发现B线指数升高与并发症之间的关系;第三缺乏PICCO、CT、尸检称重等公认方法的印证。同时需要注意到肺叶切除组的手术时间明显长于亚肺叶切除组,可能给结果带来额外的偏差,因此进一步扩大样本量、加深相关研究显得尤为重要。
结 论
肺部超声可以早期发现血管外肺水的增加,进而为胸外科围术期危重患者的早期识别、早期处理提供可能,降低此类患者的并发症风险。
