电感耦合等离子体质谱法测定注射用氯化钠中的19种元素杂质
2020-09-04邱晟张健
邱 晟 张 健
(苏州大学 药学院,江苏 苏州 215123)
元素杂质在人体内的蓄积会给患者带来严重危害。元素杂质中毒可能会引起患者脑部和骨骼病变,心血管疾病,神经系统疾病,胃肠道功能紊乱或者贫血。因此控制药品中元素杂质的含量尤为重要。大容量注射液每日使用量大,向人体带入金属元素的风险也较高。氯化钠作为大容量注射剂的常用原料,对其进行相应的控制对于从源头堵住金属杂质非常重要。本文介绍了一种对药用氯化钠中金属元素进行测试的方法。
1 仪器与试剂
1.1 仪器
电感耦合等离子体质谱仪(NexIon 350X,珀金埃尔默),超纯水机(Q10,密理博)。
1.2 试剂
多元素标准溶液(含铝Al,砷As,硼B,钡Ba,铍Be,铋Bi,镉Cd,钴Co,铬Cr,铜Cu,铁Fe,镓Ga,锂Li,镁Mg,锰Mn,镍Ni,铅Pb,锑Sb,锡Sn,锶Sr,钛Ti,钒V,锌Zn元素,批号:176035-1,国家有色金属及电子材料分析测试中心);汞单元素标准溶液(批号:17C021-3,国家有色金属及电子材料分析测试中心);钼单元素标准溶液(批号:18091,中国计量院);内标标准溶液(铋Bi,锗Ge,铟In,锂7Li,钪Sc,铽Tb,钇Y)(批号:CL3-188MKBY1,珀金埃尔默);高纯硝酸(批号:B1435118,默克)。
2 方法与结果
2.1 鉴别需要控制的元素
ICH Q3D[1]是元素杂质控制的指导原则,其对金属元素种类和限度都有相应的说明。美国药典(USP)〈232〉[2]和欧洲药典(EP)5.20[3]做出了相应的协调。而根据常用的应用场景,我们选定0.9%的氯化钠注射液作为元素杂质控制的目标制剂,如表1所示。根据其要求,氯化钠注射液属于注射给药途径,需要评估Cd,Pb,As,Hg,Co,V,Ni,Li,Sb,Cu这10种元素(用*标出)。Fe,Mn,Ti,Mo,Cr是不锈钢中常见的金属元素,而不锈钢在药品的生产中经常涉及。Al,Li,Sn是塑料中可能采用的添加剂/催化剂,而塑料常用于相关产品的包装,所以在方法中也需做相应的考察。Ba则是药用氯化钠在精制过程中常见的添加剂[4],用于除去氯化钠中的杂质。
2.2 每日允许暴露量与浓度限度的转换
ICH Q3D协调了24种元素的每日允许暴露量(Permitted Daily Exposure,PDE)。按照ICH Q3D对于注射剂的要求,氯化钠注射液属于临床实践确定日剂量可能超过2 L的产品。按照ICH Q3D的要求,如果日剂量超过2 L就以2 L计算。因此氯化钠注射液以2 L计算相应的限度。
2.3 分析方法的要求
ICH Q3D未对用于元素杂质分析的方法有详细要求,但是在USP〈233〉和EP 2.4.20中都有涉及。它们的要求相似,均为在50%~150%的限度范围内满足准确度70%~150%的回收率要求,精密度RSD≤20%。
2.4 测试方法的优化
由于测试需要的目标浓度较低(如As的目标浓度为0.5ppb),所以我们采用了动能歧视(Kinetic Energy Discrimination,KED)模式,带内标校正的标准加入法。
2.4.1 测量模式的选择与干扰的排除
ICP-MS最常见的干扰是多原子离子(Polyatomic Ion,PAI)干扰[5]。而这些干扰主要由氯化钠(Na,Cl),水(H,O)硝酸(H,N,O)和氩气(Ar)带入。常见的的干扰见表2。
动能歧视模式(kinetic energy discrimination,KED)可以用来消除待测多原子离子的干扰。原理是根据分子离子的横截面积通常比待测离子的大,与碰撞器相互撞击的机会大。被击碎产生的低质量数离子由于多次碰撞而失去大部分动能,而待测离子由于受到的撞击几率小,动能降低较少,因此最后进入质量分析器的待测离子较多而产生干扰的多原子离子较少。
标准加入法的选用,可以降低基质干扰,消除样品与对照品的差异性[6]。内标校正则可以进一步校正响应信号的波动。由于测试需要的灵敏度较高,所以采用带内标校正的标准加入法来进行测定。这些均可通过ICP-MS系统的软件自动完成。
2.4.2 Hg与Pb的残留
Hg在电感耦合等离子质谱(inductively coupled plasma massspectrometry,ICP-MS)中容易吸附而残留[7]。常用的做法是加入一定量Au或者较高浓度的盐酸。而Pb则需要一定浓度的酸才可以清洗干净。因此,本文采用加入200 ppb Au标液,将含有200 ppb Au的1%HNO3作为清洗液,且将线性最高点控制在0.5 μg/L,以抑制Hg在ICP-MS的系统中的残留。
2.5 分析方法
2.5.1 仪器参数
仪器的参数设定见下表3和表4。

表3 仪器的参数设定表Ⅰ
表4 仪器的参数设定表Ⅱ
2.5.2 标准溶液配制
精密量取氯化钠适量制成0.45%的氯化钠的1%HNO3溶液,加入多元素标准溶液适量,并用1%HNO3稀释至50 mL。具体标准溶液配置见表5。
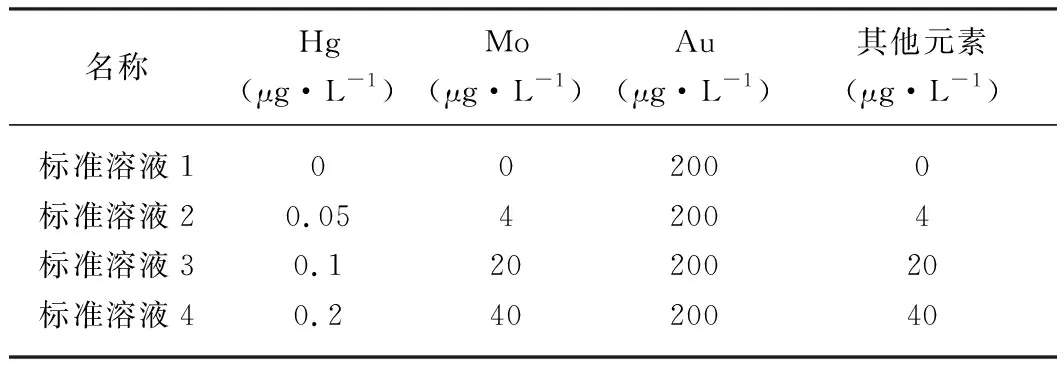
表5 标准溶液配置表
2.5.3 内标溶液配制
取内标标准液用1%HNO3稀释成10 μg·L-1的内标溶液。
2.5.4 供试品溶液配制
精密量取氯化钠适量制成0.45%的氯化钠的1%HNO3溶液。
2.5.5 测试方法
以含200 ppb Au的1%HNO3为清洗液,采用蠕动泵在线加内标的方法,分别进样标准溶液,以待测元素的响应与内标元素相应的比值为纵坐标,以待测元素的浓度为横坐标,采用机器的自带软件进行计算得到校准曲线,并用该曲线计算结果。
2.6 方法验证
2.6.1 线性
分别用标准品溶液适量制成表6所示的线性溶液。以待测元素的响应与内标元素相应的比值为纵坐标,以待测元素的浓度为横坐标,采用机器的自带软件进行计算,结果见表7。

表6 线性溶液配置表
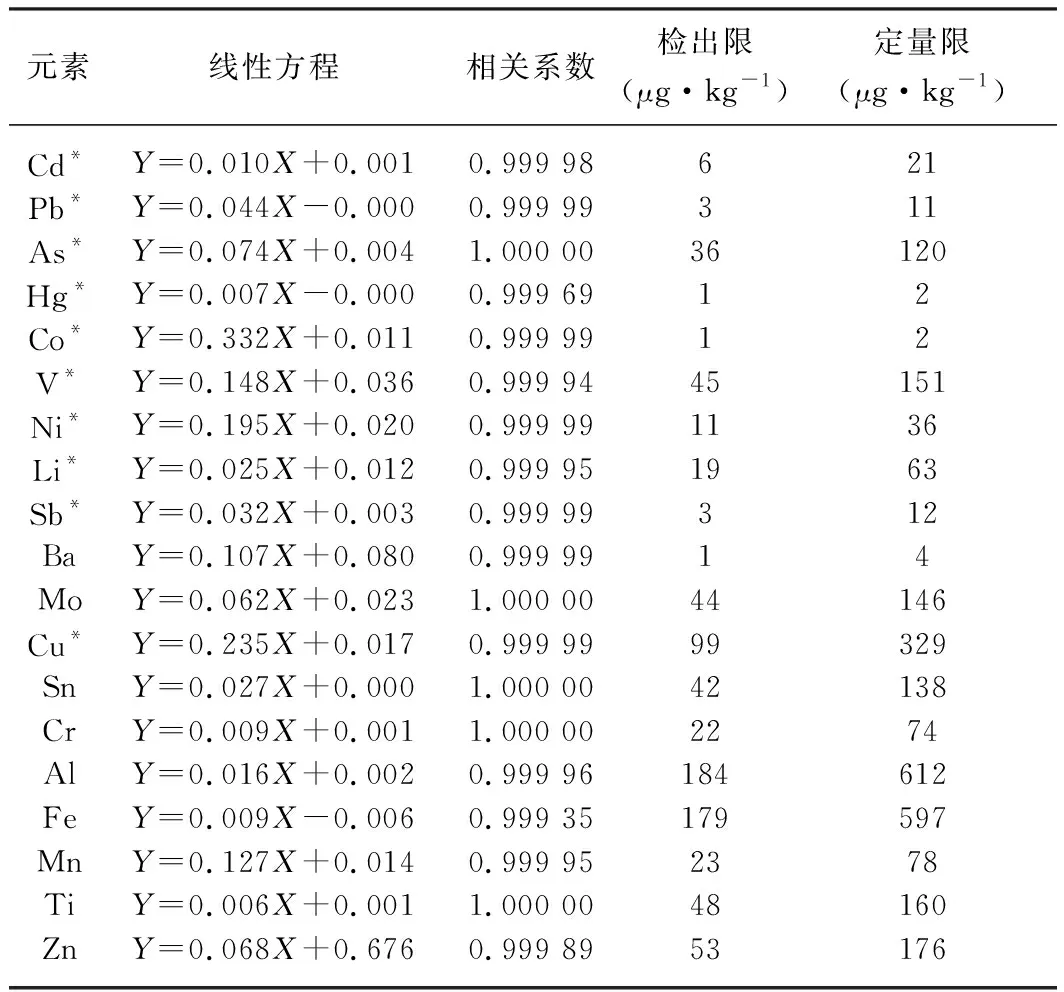
表7 线性与检出限、定量限结果表
2.6.2 检出限与定量限
参考中国药典2015年版电感耦合等离子体质谱法,以8次连续测定空白样品溶液响应值的3倍标准偏差(3SD)所对应的待测元素浓度作为检测限;以连续测定空白溶液响应值的10倍标准偏差(10SD)所对应的待测元素浓度作为定量限。结果见表7。
2.6.3 准确度与精密度
取待测元素对照品适量,加入供试品溶液至50 mL,每个浓度配制三份。测定结果见表8。

表8 准确度与精密度测定结果(n=3)
2.7 样品的测定
四个厂家的四批样品按照本方法进行测试,结果见表9。
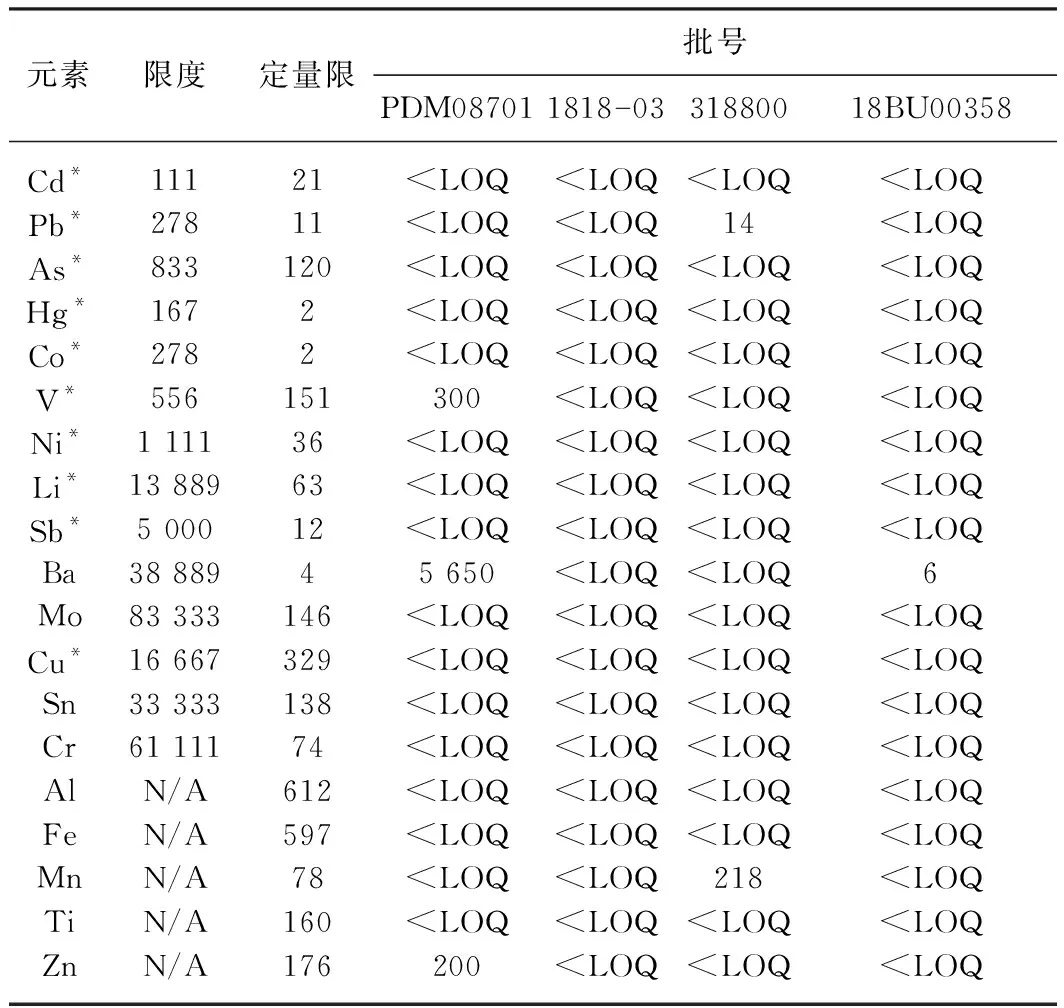
表9 样品测定结果
3 讨论
本方法样品溶液被配置成0.45%,相当于0.9%氯化钠注射液浓度的1/2,这样的浓度既避免了过度稀释导致的无法满足检测限的要求,又避免了过高的盐浓度对与检测器和进样系统寿命的影响。此方法也可以用于0.9%氯化钠注射液成品的检测。
笔者曾分别尝试标准模式(STD)和KED模式,带内标校准的标准曲线法。但因为检测的要求过高(1类与2A类元素定量限需小于5 g/L),无法满足同时测定所有元素的测定要求。
为保证测定结果的准确性,准确度考察从0.25 ppb开始。结果表明所有元素的准确度和精密度均可满足美国药典〈233〉和欧洲药典2.4.20的要求。
批次样品测定的结果均符合ICH Q3D的限度要求,但有一批次的钒V超出了控制阈值(限度的30%),需要后续关注。个别批次Ba的结果证实Ba可能在生产中添加,在日后应监测。
