三种盐类超细水雾抑制管道内甲烷-空气预混气爆炸的差异性*
2020-08-26贾海林翟汝鹏李第辉项海军杨永钦
贾海林,翟汝鹏,李第辉,项海军,杨永钦
(1. 河南理工大学河南省瓦斯地质与瓦斯治理重点实验室-省部共建国家重点实验室培育基地,河南 焦作 454000;2. 河南理工大学安全科学与工程学院,河南 焦作 454000)
随着生态环保意识的提高,使用清洁能源代替煤炭资源受到了极大重视[1]。各地区也都积极地实施煤改气工程,然而天然气富集区向燃气需求区输送过程中敷设的长距离管网存在一定的安全风险,有引发管网爆炸事故的风险,如2014 年高雄燃气管网爆炸,2018 年波士顿的燃气管网爆炸。
针对预混气燃爆机理及传播特性的研究已经卓有成效[2-5]。陈鹏等[6]研究发现甲烷/空气预混气爆炸受遮挡物影响会出现火焰逆流并持续加速现象。周宁等[7]通过改变遮挡物的间距及阻塞比发现遮挡物间距为管长1 倍时,丙烷/空气预混气爆炸火焰加速明显。为了抑制预混气爆炸危害,细水雾或含添加剂细水雾常被应用于燃爆场所[8-14]。裴蓓等[15]研究CO2和超细水雾协同抑制甲烷/空气预混气爆炸时,发现CO2能够有效弥补超细水雾的不足。纪虹等[16]研究了不同雾通量的超细水雾降解与抑制甲烷爆炸的特性,认为随着雾通量的增大,甲烷的降解速率会加快;管道内爆炸超压、平均压升速率呈现下降的趋势。Rui 等[17]研究了不同体积分数的超细水雾对不同浓度甲烷爆炸的抑制作用。Modak 等[18]认为粒径小的细水雾较粒径大的细水雾的抑制效率高。杨克等[19]对比分析了含不同浓度草酸钾的超细水雾对甲烷的抑爆特性,发现浓度为2%草酸钾抑爆效果最佳。Joseph 等[20]认为含NaCl、KCl 和KHCO3的细水雾可有效提高灭火效率,而含(NH4)2HPO4细水雾的灭火效果不佳。余明高等[21-22]开展了含MgCl2、FeCl2细水雾和含NaCl 的荷电超细水雾抑制单管瓦斯爆炸的实验,发现含添加剂细水雾和带荷电的超细水雾均能抑制和降低爆炸传播速度和火焰温度。Gan 等[23]进行了含NaCl 和NaHCO3细水雾对PMMA 粉尘爆炸抑制实验,指出含添加剂细水雾能够降低火焰传播速度、最高温度和升温速率。陈晓坤等[24]通过比较单管道内含NaHCO3、KCl 细水雾与纯水细水雾的抑爆性能,认为含添加剂超细水雾抑爆效率显著。Cao 等[25-27]开展了含NaCl 超细水雾抑制密闭管道内不同浓度甲烷/空气的爆炸实验,结果表明添加NaCl 可以明显改善超细水雾的冷却作用和吸热效果。
综合前人研究发现,关于细水雾抑制预混气爆炸的实验主要集中在单段管道,且细水雾粒径多为Ⅱ级,对于预混气爆炸跨越至后续管网的传播特性、抑爆规律以及盐类超细水雾的综合作用的研究相对较少。针对现实中燃气采用管道输运这一现状,搭建两节管道预混气爆炸传播及抑爆实验系统,开展不同种类、不同盐类质量分数及不同雾通量盐类超细水雾抑制甲烷体积分数为9.5%的甲烷-空气预混气的爆炸实验,分析不同工况下爆炸超压、火焰锋面及火焰平均传播速度的变化,以期研究结果可为燃气安全输运及燃爆事故预防提供指导。
1 管道预混气爆炸传播及抑爆系统
1.1 实验系统组成及功能
为研究和对比分析管道预混气爆炸特征和盐类超细水雾的抑爆效果,自主搭建了两节管道预混气爆炸传播及抑爆实验系统(见图1),该系统由预混气配置单元、管道预混气爆炸单元、爆炸超压及火焰信息采集单元和超细水雾雾化单元组成。预混气配置单元包括空压机、高纯高压甲烷气体存储钢瓶、阀门、耐高压树脂软管、快速接头、质量流量计等组成。管道预混气爆炸单元由两段长度为50 cm、截面为10 cm×10 cm、耐压2 MPa 的有机玻璃管道(A、B)和点火系统组成。管道A、B 采用法兰连接并在连接处用PVC膜将其分隔,然后将密封胶垫置于PVC 膜外侧,确保管道连接的密闭性。管道A 的右端采用不锈钢钢板密闭,钢板上分别设置有点火器、高频压力传感器和进气阀门预留孔。管道B 左端采用PVC 膜密封,作为预混气爆炸时的泄压口。点火系统采用陶瓷钨棒材料制成的点火电极和HE119 系列的高能点火器,点火器间距为5 mm,放电电压为6 kV,工作频率为50 Hz。爆炸超压及火焰信息采集单元由高频压力传感器、USB-1608FS 型数据采集卡、M310 型高速摄像机和计算机组成。高频压力传感器工作范围为-0.1~0.2 MPa,响应时间为0.2 ms,精度为0.25%。高速摄像机最短曝光时间不长于1 μs,最高分辨率为1 024×1 024。实验过程中信号采集频率均为15 kHz,选取的拍摄频率为3 200 s-1。为准确测定起爆时间,将RL-1 型光电传感器置于管道A 的外侧,探头倾斜放置并指向点火电极。超细水雾雾化系统由超声雾化装置、密闭树脂储水箱及水雾导流管组成,其中压电陶瓷雾化片的雾化速率约为4.2 mL/min,工作频率为1 700 kHz。实验系统可实现以下功能:(1)研究不同类型、不同体积分数预混气在不同管段的爆炸超压、火焰锋面传播特性;(2)分析不同雾通量纯水超细水雾抑制预混气爆炸的弱化效果;(3)开展不同类型、不同盐类质量分数、不同雾通量盐类超细水雾抑制预混气爆炸的抑制实验。

图1 两节管道预混气爆炸及抑爆实验系统Fig.1 Experimental system for the premixed gas explosion and explosion suppression in a two-section pipeline
1.2 超细水雾粒径分布测定
水雾粒径采用相位多普勒激光测速仪进行测量。该仪器主要应用于雾化测量以及气固两相测量,主要由激光器、发射(接收)光路系统、信号处理系统、全自动位移系统和数据处理系统构成。粒径测量范围为0.3~7 000 μm,测量精度为±0.5 μm。实验中盐类超细水雾的水雾粒径分布见图2。由图2 可知,粒径总体分布在0~20 μm,且水雾粒径大部分在0~10 μm。根据NFPA750 标准中细水雾的分级分类[28]可知,90%以上的细水雾粒径小于200 μm 被定义为第Ⅰ级。秦俊等[29]认为水雾平均粒径的索太尔平均直径小于50 μm 的可以称为超细水雾。因此,本实验雾化系统所产生的水雾可称为超细水雾。
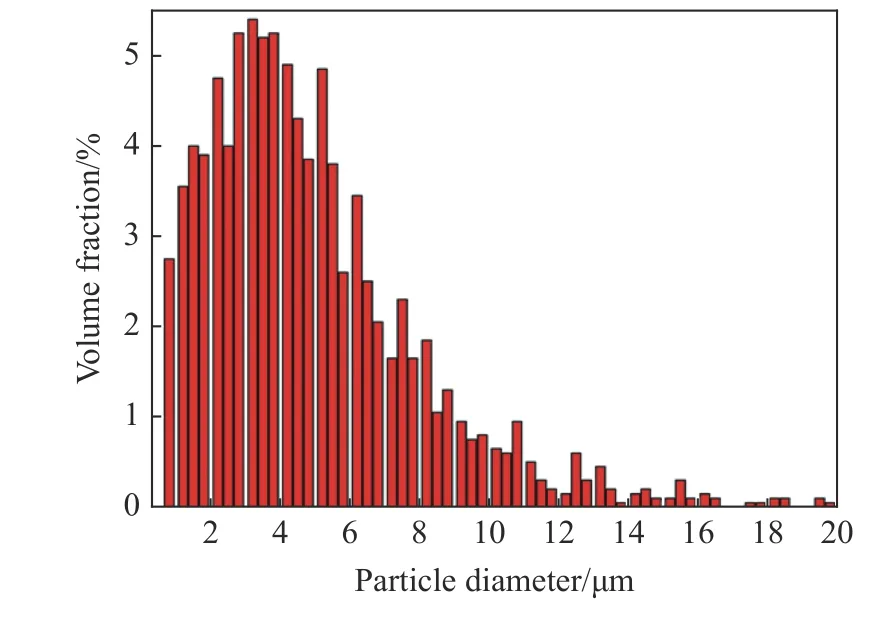
图2 超声雾化产生的细水雾粒径分布Fig.2 Particle diameter distribution of water mist generated by ultrasonic atomization
1.3 实验工况及过程
实验前预先分别配置盐类质量分数为2%、4%、6%和8%的NaCl、MgCl2和NaHCO3溶液。为使爆炸单元管道A、B 内预混气(CH4与空气的混合气体)的化学当量比为9.5%,实验配气基于分压法计算管道A、B 内需要的通气量。实验过程:(1)检查仪器并调试,确保测试系统处于待机状态;(2)将PVC 薄膜紧贴于管道A 和B 之间、管道B 末端,之后同时打开管道A、B 的进气阀和出气阀,通入4 倍于管道容积的预混气体于管道A、B 中,充气时间设定为8 min,保证管道内部气体置换完全;(3)保持管道B 与超声雾化装置间的进气阀处于开启状态,并启动超声雾化装置;(4)按照不同的工况通入相应的水雾量(0、2.1、4.2、6.3 和8.4 mL),充气和管道B 内通细水雾全部结束后,关闭进气阀和出气阀,启动点火器,同时采集压力数据并存储拍摄到的火焰图像;(5)重复上述步骤,进行下一次实验,每次实验前需将拆卸下的管道B 用吹风机吹干,每组工况重复3~5 次。
2 预混气爆炸及抑爆实验分析
2.1 不同盐类超细水雾对爆炸超压振荡曲线及最大超压峰值的影响
不同水雾通入量和不同盐类质量分数的盐类超细水雾抑制甲烷体积分数为9.5%的甲烷-空气预混气的爆炸超压p 曲线及最大超压pmax变化情况如图3~6 所示。提取图3(a)、4(a)和5(a)不同工况下的爆炸超压最大值,计算同一雾通量V、不同盐类质量分数w 下的最大爆炸超压变化值Δpmax以及增幅η,汇总在表1~3 中。

图3 NaCl 超细水雾对甲烷体积分数为9.5%的甲烷-空气预混气的爆炸超压振荡曲线及最大超压峰值的影响Fig.3 Explosion overpressure-time curves and the maximum explosion overpressures affected by water mists containing NaCl for premixed methane-air mixture with the methane volume fraction of 9.5%
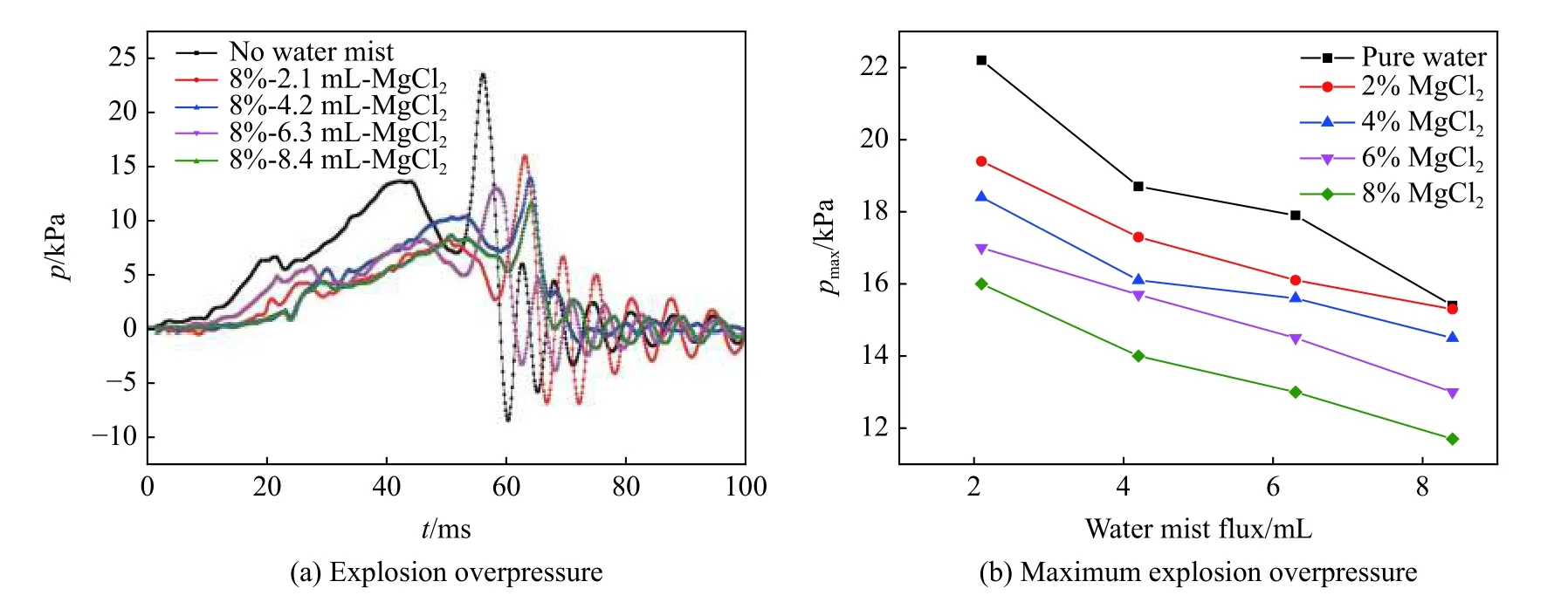
图4 MgCl2 超细水雾对甲烷体积分数为9.5%的甲烷-空气预混气的爆炸超压振荡曲线及最大超压峰值的影响Fig.4 Explosion overpressure-time curves and the maximum explosion overpressures affected by water mists containing MgCl2 for premixed methane-air mixture with the methane volume fraction of 9.5%
观察图3(a)、4(a)和5(a)知,随着时间的推移,爆炸超压曲线呈现出多个峰值。爆炸超压曲线在达到最大值前出现2 个波峰:第1 个波峰是由于爆炸形成的前驱压力波冲破管道A、B 间的薄膜后泄压引起的,使超压呈现先上升后下降的趋势;第2 个波峰是由于前驱压力波冲破管道B 左端的薄膜泄压造成的。末端管道破膜后未燃预混气因管道压力骤变而卷吸进入爆炸反应区,导致爆炸火焰继续向末端管道传播,前驱压力波使得末端管道的薄膜再次进一步破裂。当爆炸反应所产生的能量与周围环境吸收而消耗的能量相等时,爆炸超压处于最大峰值,对应于图3(a)、4(a)和5(a)的最大峰值,也即第3 个波峰。之后,随着器壁的冷却效应、周围环境等因素消耗的能量大于反应所放出的能量时,压力呈现下降趋势。

图5 NaHCO3 超细水雾对甲烷体积分数为9.5%的甲烷-空气预混气的爆炸超压振荡曲线及最大超压峰值的影响Fig.5 Explosion overpressure-time curves and the maximum explosion overpressures affected by water mists containing NaHCO3 for premixed methane-air mixture with the methane volume fraction of 9.5%

图6 雾通量均为8.4 mL、盐类质量分数不同的不同盐类超细水雾作用下爆炸超压变化的差异性Fig.6 Differences of the explosion overpressures affected by ultrafine water mists with three different salts and different salt mass fractions under the same mist flux

表1 NaCl 超细水雾作用下最大爆炸超压的变化Table 1 Changes of the maximum explosion overpressures under the suppression of ultrafine water mists containing NaCl

表2 含NaHCO3 超细水雾作用下最大爆炸超压的变化Table 2 Changes of the maximum explosion overpressure under the suppression of ultrafine water mists containing NaHCO3

表3 MgCl2 超细水雾作用下最大爆炸超压的变化Table 3 Changes of the maximum explosion overpressures under the suppression of ultrafine water mists containing MgCl2
分析表1~3 可知,对于相同雾通量和盐类质量分数的超细水雾,NaCl 超细水雾的抑爆效果最好,MgCl2超细水雾次之,NaHCO3超细水雾抑爆效果最差。例如:在盐类质量分数均为8%,分别含NaCl、MgCl2和NaHCO3的3 种超细水雾作用下,雾通量为4.2 mL 时,最大爆炸超压分别为13.9、14.0 和16.6 kPa;雾通量为8.4 ml 时,最大爆炸超压分别为9.9、11.7 和12.8 kPa。与无超细水雾下的最大爆炸超压(记为pmax,1,由图3 知pmax,1为23.5 kPa)相比,降幅分别达到40.9%、40.5%、29.4%和57.9%、50.2%、45.6%;与纯超细水雾下的最大爆炸超压(记为pmax,2,相应数值见表1~3)相比,降幅分别达到25.7%、25.1%、11.2%和35.7%、24%、16.9%。NaCl 超细水雾作用下的pmax,8.4和pmax,1的差值约为pmax,8.4和pmax,2差值的2.5 倍,而盐类质量分数为2%和4%的NaHCO3超细水雾作用下的pmax,4.2相对于pmax,2要弱得多,最大爆炸超压下降比例仅从0.5%增加到2.1%。盐类超细水雾均会使最大爆炸超压峰值有所降低的原因有3 方面:(1)管道A 内爆炸反应引发的前驱压力波致使管道A 与管道B 之间的PVC 薄膜发生破裂,从而诱导未反应区内可燃气体进入爆炸反应区,促进管道B 内的爆炸反应进行,此时管道B 内的超细水雾通过汽化吸收火焰的热量,降低火焰温度和燃烧速率,且汽化产生的水蒸气能够稀释预混气体,削弱反应区的热辐射强度;(2)汽化后析出的NaCl、MgCl2和NaHCO3晶体同样可以吸收火焰阵面热量,并随着盐类质量分数和水雾量的增加,削弱热辐射强度和阻隔热传递能力不断增强;(3)分散于反应区的NaCl、MgCl2和NaHCO3离子气相组分会同甲烷-空气预混气爆炸反应产生的高能自由基发生碰撞和自由基消亡反应,极大降低了高能自由基参与链式反应的几率,高能自由基的消耗使得爆炸链式反应增长速度减降低,进而爆炸被抑制。
分析图3(b)、4(b)和5(b)可知,同一雾通量、同一盐类、不同质量分数的超细水雾作用下,当质量分数从0%增加至8%,爆炸超压峰值随着质量分数的增大显著降低,这表明超细水雾中盐类质量分数的增大能有利于增强抑爆效果。同一盐类、同一质量分数、不同雾通量的超细水雾作用下,当雾通量从2.1 ml增加至8.4 ml,爆炸超压峰值随着雾通量的增大而减小,近似呈线性负相关趋势下降,且爆炸超压曲线上升缓慢,这表明盐类超细水雾雾通量的增大能显著提高抑爆效果。

2.2 不同盐类超细水雾对火焰锋面位置和火焰平均传播速度的影响
由前述分析可知,随着水雾通入量和盐类质量分数的增大,综合抑爆效果会逐渐增强。为了分析3 种盐类超细水雾对管道B 内火焰锋面位置和火焰传播速度的影响,提取了雾通量均为8.4 mL、盐类质量分数不同的不同盐类超细水雾作用下火焰峰面到达管道B 末端的时间tter,计算了相对于无细水雾作用下火焰峰面到达管道B 末端的延迟时间Δt 以及相应的延迟幅度ξ,汇总于表4。选取雾通量均为8.4 mL、盐类质量分数均为8%的不同盐类超细水雾作用下管道B 内的火焰锋面位置和火焰平均传播速度进行分析,详见图7~8。
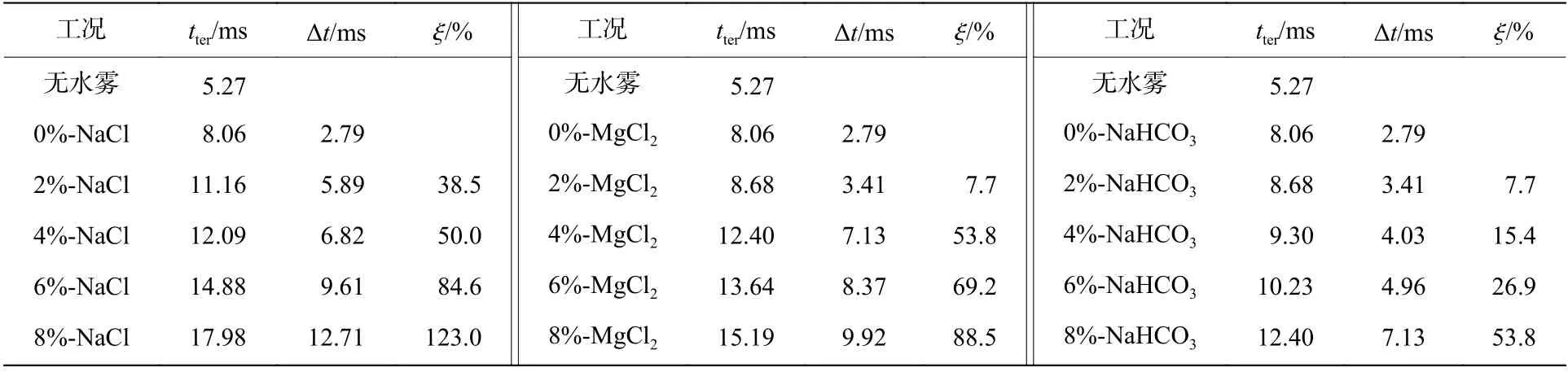
表4 不同工况下3 种盐类超细水雾作用下火焰峰面到达管道末端的时间Table 4 Times for the flame front to arrive at the terminal end of pipe B affected by three ultrafine water mists with different salts under different working conditions

图7 不同盐类超细水雾作用下管道B 内爆炸火焰锋面位置的变化Fig.7 Changes of explosive flame front positions in pipe B affected by different ultrafine water mists
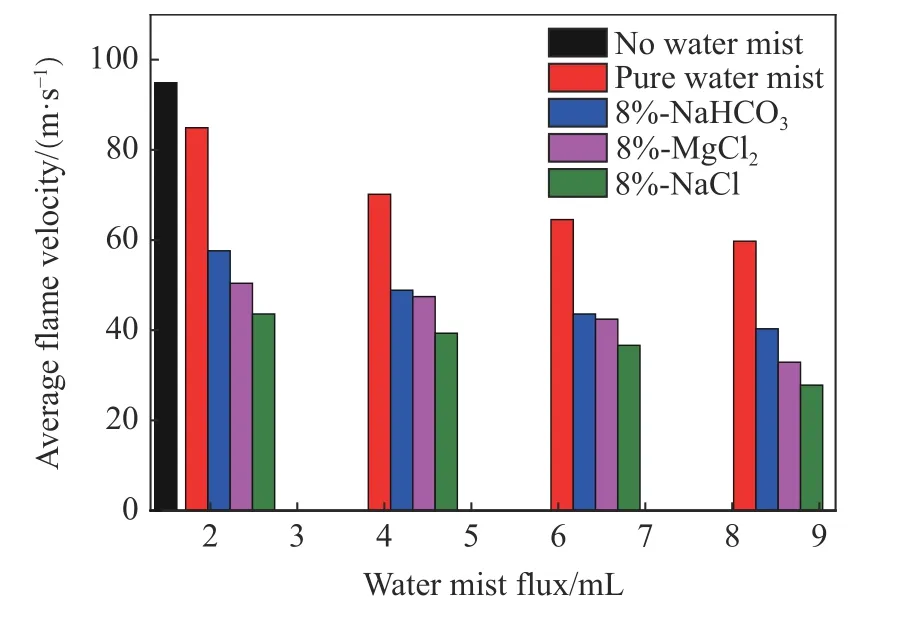
图8 不同盐类超细水雾作用下管道B 内爆炸火焰平均传播速度的变化Fig.8 Changes of average propagation velocities of explosion flames in pipe B affected by different ultrafine water mists
分析图7 和表4 可知,无细水雾作用下,火焰锋面位置呈斜率较大的线性趋势快速上升,火焰锋面穿越B 区到达管道末端仅需5.27 ms,纯水超细水雾作用下需8.06 ms。3 种盐类超细水雾作用下火焰锋面位置呈震荡曲线的形状缓慢上升,火焰到达管道B 末端的时间延长,分别延迟至12.40 ms(NaHCO3)、15.19 ms(MgCl2)和17.98 ms(NaCl),延迟幅度较纯水超细水雾作用下达到了53.8%(NaHCO3)、88.5%(MgCl2)和123.0%(NaCl)。总体来说,这3 种盐类超细水雾对爆炸超压和火焰锋面均有一定抑制效果,但NaCl 超细水雾的抑制效率最高,MgCl2超细水雾的抑制效率次之,NaHCO3超细水雾的抑制效率最低。
观察图7 发现,火焰在管道B 内传播时,火焰锋面位置出现下降-上升-再下降的传播现象。NaCl 超细水雾作用下火焰锋面在0.62 ms 时出现第1 次后退,火焰锋面在4.34 ms 时后退较显著,火焰锋面在10.23 ms 时发生急剧后退。MgCl2、NaHCO3超细水雾作用下,火焰锋面出现第1 次后退的时间分别为1.24 和2.48 ms,火焰锋面出现显著后退的时间分别为9.92 和9.61 ms。相比来说,NaCl 超细水雾作用下火焰锋面显著后退发生较早,NaCl 超细水雾作用下火焰锋面后退现象共出现了5 次,而MgCl2、NaHCO3超细水雾作用下火焰锋面分别出现了4 次和2 次后退。这也证明了盐类超细水雾可以有效延缓火焰阵面的推进速度,延长了火焰阵面传播至管道B 末端的时间。
观察图8 可知,无细水雾作用下管道B 内火焰平均传播速度为94.88 m/s。当雾通量为8.4 mL 时,3 种盐类超细水雾作用下,管道B 内火焰平均传播速度分别下降至27.81 m/s(NaCl)、32.92 m/s(MgCl2)和40.32 m/s(NaHCO3),下降率分别达到70.7%、65.3%和57.5%。这表明在雾通量和盐类质量分数相同的情况下,NaCl 超细水雾作用下管道B 内火焰平均传播速度最小,MgCl2超细水雾作用下次之,NaHCO3超细水雾作用下最大。在盐类质量分数相同、雾通量不同的情况下,管道B 内火焰平均传播速度同样遵循前述规律。盐类超细水雾作用下火焰锋面出现延迟后退的原因在于:管道A、B 之间的薄膜类似于传播过程的障碍物,爆炸后的破膜作用造成火焰面发生褶皱变形,火焰阵面的燃烧面积被拉伸;当火焰演化传播时,褶皱变形的火焰阵面被进一步分离成小火焰团;之后,在管道B 传播时盐类超细水雾会包络这些爆炸火焰及分离的小火焰团,在高温作用下盐类超细水雾形成的水蒸气和析出的盐类微小晶体吸收了火焰团前锋的大量热量,削弱了主体火焰对前锋火焰团的辐射热,使得前锋火焰团会反复窒息熄灭,导致火焰前锋由火焰团转为主体火焰作为主锋面,继而使得火焰锋面出现不同次数后退。
3 不同盐类超细水雾抑爆机理
3.1 盐类超细水雾的抑爆作用
盐类超细水雾是通过物理和化学的双重作用达到抑爆效果的,选取雾通量均为8.4 mL、盐类质量分数均为8%、不同盐类超细水雾作用下管道B 内的火焰图像见图9。分析图9 可知,爆炸前驱波穿越管道A 并破膜后进入管道B,此时盐类超细水雾在高压气流驱使下快速进入爆炸反应区,盐类超细水雾的回流能撕裂火焰团阵面,由于具有较大的比表面积,增大了对火焰团的包裹性,弱化了反应区和未燃区之间的热传递。根据阿伦尼乌斯公式[30]可知,这会降低火焰前沿温度和预混气的爆炸反应速率,且导致火焰团前锋被分割成体积不均的小火焰团,使得管道B 内的火焰形貌呈内凹外凸的演化结构。盐离子随着超细水雾的蒸发会以微小的晶体析出,析出量随着盐类质量分数的增大而增多。卷吸作用下微小的盐离子晶体分散于管道B 内的爆炸反应区,一方面吸收火焰热量,增强吸热能力;另一方面高温下气相分解出的盐离子能销毁爆炸反应区的活性自由基(OH·和H·等),中断链式反应,而且会因为盐离子的焰色反应,造成火焰亮度有所增强。此外,盐离子会与活性自由基发生碰撞,使得高活性的自由基在能量交换过程中失去活性。
3.2 不同盐类超细水雾抑爆差异性
添加剂种类的不同,爆炸反应区内盐离子与高能自由基相互作用也有所差异,作用路径见图10。分析图10 可知,钠离子、镁离子和氯离子在第三体作用下能消耗大量的活性自由基,Na+与OH-结合产生氢氧化钠,成为主要消耗活性基团(H·和OH·)的中间产物,Mg2+与OH-结合生成氢氧化镁,氢氧化镁在高温下分解的氧化镁具有较大的表面能,能够吸附高活性基团(H·),终止相关的链式反应[31]。H·和OH·在Cl-的催化作用下生成大量的水分子。NaHCO3受热分解的氧化钠和水蒸气反应生成氢氧化钠,氢氧化钠通过捕获活性基团(H·和OH·),使得链式反应中的高能自由基减少,降低爆炸强度。同时水分子作为第三体基元M 催化H·和OH·反应( 2 H+H2O →H2+H2O,H+OH+M →H2O+M ),促进水分子进一步增多,正反馈效应降低支链反应。

图10 三种盐类超细水雾抑爆机理Fig.10 Explosion suppression mechanism by three ultrafine water mists with different salts
其主要基元反应过程如下:
Na+OH+M →NaOH+M, NaOH+H →Na+H2O,
NaOH+OH →NaO+H2O, H+OH+Cl →H2O+Cl
Mg+OH+M →Mg(OH)2+M, Mg(OH)2+H →Mg+H2O,
Cl+Cl+M →Cl2+M, H+OH+Cl →H2O+Cl
NaHCO3→Na2CO3+H2O+CO2, Na2CO3→Na2O+CO2
Na2O+H2O →NaOH, NaO+H →Na+OH
4 结 论
利用自行搭建的两节管道瓦斯爆炸传播及抑爆实验系统,模拟分析了管道瓦斯爆炸跨越至后续管网的爆炸传播特性以及不同种类、不同盐类质量分数及不同雾通量盐类超细水雾抑爆效果。通过实验分析和理论研究,主要获得了以下结论:
(1)甲烷体积分数为9.5%的甲烷-空气预混气爆炸在盐类(NaHCO3、MgCl2和NaCl)超细水雾作用下爆炸超压振荡曲线缓慢上升,抑爆效果优于纯水超细水雾。随着盐类超细水雾的盐类质量分数和雾通量的增大,含NaCl 超细水雾抑制效能相对最优。在雾通量均为8.4 mL,盐类质量分数均为8%的3 种盐类超细水雾作用下的最大爆炸超压峰值较无超细水雾工况下降幅度分别达到45.6%(NaHCO3)、50.2%(MgCl2)和57.9%(NaCl)。
(2)盐类超细水雾作用下,火焰锋面穿越B 区到达管道B 末端的时间较无细水雾和纯水超细水雾作用下出现延迟且火焰锋面在管道中传播时呈现不同次数的后退现象。在盐类超细水雾的盐类质量分数均为8% 和和雾通量均为8.4 mL 的情况下,NaCl 超细水雾作用下火焰锋面出现了5 次后退现象,MgCl2和NaHCO3超细水雾作用下火焰锋面仅分别出现了4 次和2 次后退现象。
(3)盐类超细水雾对火焰平均传播速度和爆炸超压的影响规律趋于一致,盐类质量分数为8%的情况下,随着盐类超细水雾雾通量的增大,火焰到达管道B 末端的时间延迟,管道B 段内的火焰平均传播速度呈阶梯下降趋势。与无超细水雾作用下的火焰平均传播速度(94.88 m/s)相比,分别下降了57.5%(NaHCO3)、65.3%(MgCl2)和70.7%(NaCl),火焰到达管道末端时间分别延迟至17.98 ms(NaCl)、15.19 ms(MgCl2)和12.4 ms(NaHCO3)。

