膜解剖在腹腔镜胃癌根治术中的作用
2020-08-24丁闯
丁闯
胃癌全球发病率居恶性肿瘤第5 位,死亡率居第3 位,严重威胁人类健康[1]。胃癌的治疗逐步从扩大的手术切除和淋巴结骨骼化廓清到规范化和标准化时代,标准胃癌D2 根治术强调沿胃周血管的淋巴清扫,膜解剖理论则强调膜间隙的寻找和系膜的完整切除[2]。本文通过对比分析2017年12月~2018年6月在膜解剖理论指导下完成腹腔镜胃癌根治术和在传统血管导向下完成腹腔镜胃癌根治术,探讨膜解剖在胃癌根治术中的疗效及安全性。现报告如下。
1 资料与方法
1.1 一般资料 选择本院2017年12月~2018年6月经评估适合行腹腔镜下根治性全胃切除手术的47例胃癌患者,根据指导方法不同分为A组(23例)和B组(24例)。两组患者一般资料比较差异无统计学意义(P>0.05),具有可比性。见表1。纳入标准:①肿瘤位于胃体中上部及贲门;②影像学检查综合评估无远处转移;③pTNM 分期Ⅱa~ⅢB 期;④术前未接受新辅助放化疗。排除标准:①合并严重重要脏器疾病;②姑息手术者;③急诊手术确定胃癌者;④临床资料不完善者。本研究经本院伦理委员会批准通过,研究对象均签署知情同意书。
表1 两组患者一般资料比较(n,±s)

表1 两组患者一般资料比较(n,±s)
注:两组比较,P>0.05
1.2 手术方法
1.2.1 A组 在膜解剖理论指导下行腹腔镜胃癌根治术。向左沿胃系膜与横结肠系膜间隙游离至结肠脾区,并沿胰腺尾部向脾门分离,掀起胃网膜左系膜,然后向胰腺尾部及脾门游离,结扎并切断胃网膜左动脉,清扫No.4sb组淋巴结。向右沿胃结肠系膜间隙游离至胃网膜右系膜根部(见图1),清扫No.06组淋巴结,提拉胃胰皱襞,予胰腺上缘打开胰腺背膜,进入胰后间隙,向右掀起肝总动脉表面系膜(见图2),清扫No.09、08a、07组淋巴结。向左掀起脾动脉表面系膜(见图3),向膈肌及脾门方向扩展,清扫第11组淋巴结。以胃网膜左系膜根部、胃网膜左动脉为起点,沿脾动静脉分支掀起血管表面系膜(见图4),由近及远清扫第10组淋巴结。向上清扫脾门时结扎胃短动、静脉,顺势清扫第2组淋巴结。
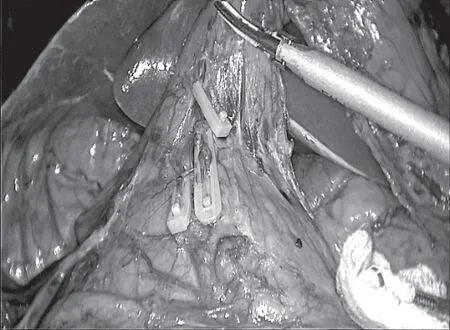
图1 幽门下区域

图2 胰腺上缘右侧区域

图3 胰腺上缘左侧区域
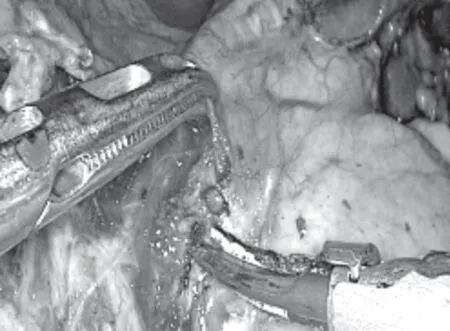
图4 胰尾上缘区域
1.2.2 B组 在传统血管导向下行腹腔镜胃癌根治术。从横结肠中部以超声刀离断大网膜,沿横结肠系膜前叶下分离,向右侧至结肠肝区分离裸化胃网膜右动脉,根部上锁扣后切断,清扫N06组淋巴结,打开肝十二指肠韧带被膜,裸化肝固有动脉、胃十二指肠及肝总动脉,在胃右动脉根部上锁扣后切断,同时清扫第N05、N12、N08组淋巴结,暴露腹腔动脉、脾动脉及胃左动静脉,于根部上锁扣,清扫N07、N09、N11组淋巴结,沿肝下缘清扫小网膜至贲门右侧,清扫N01、N03组淋巴结。游离大网膜至结肠脾区,切断胃网膜左动静脉,沿着脾门周围血管清扫第N10组淋巴结,游离贲门区,裸化食管下段,完成N02组淋巴结的清扫。
1.3 观察指标 比较两组各项手术治疗指标(手术时间、术中出血量、淋巴结清扫数目、肛门排气时间);术后进行为期3~24 个月的随访,比较两组1、2年的生存率。
1.4 统计学方法 采用SPSS23.0 统计学软件对研究数据进行统计分析。计量资料以均数 ± 标准差(±s)表示,采用t 检验;计数资料以率(%)表示,采用χ2检验。P<0.05 表示差异具有统计学意义。
2 结果
2.1 两组各项手术治疗指标比较 A组手术时间短于B组,术中出血量少于B组,差异具有统计学意义(P<0.05);两组淋巴结清扫数目、肛门排气时间比较差异无统计学意义(P>0.05)。见表2。
表2 两组各项手术治疗指标比较(±s)

表2 两组各项手术治疗指标比较(±s)
注:与B组比较,aP<0.05
2.2 两组术后生存情况比较 两组1、2年生存率比较差异无统计学意义(P>0.05)。见表3。

表3 两组术后生存情况比较[n(%)]
3 讨论
目前,腹腔镜胃癌根治术多是在腹腔镜下完成胃周淋巴结的清扫,采用上腹部小切口进行消化道重建[3]。对于腹腔镜胃癌根治术的主要争议在于:淋巴结清扫的不彻底[4]。淋巴结清扫的彻底性是胃癌根治术成败的关键,淋巴结的彻底清扫不仅能够提高手术疗效,还有助于胃癌的病理分期,从而为术后放化疗提供临床依据[5]。
传统的D2 根治术理论认为:胃壁各层的淋巴管网大体上与胃周血管伴行并汇入胃周的淋巴系统,故胃癌淋巴结清扫也是胃周血管的暴露与裸化过程[6]。但血管周围淋巴结清扫的边界,血管前后面的范围的模糊定义给腹腔镜下胃癌淋巴结的清扫带来了争议[7]。龚建平[8]则认为:胃在发育中先后倒卧于后腹壁或其他器官系膜上,胃及周围血管、淋巴结和淋巴管网连同其周围的脂肪结缔组织被一个膜样“信封”所包绕,该区域形成独立空间,其中可能有除直接侵犯、腹膜播散、血行转移和淋巴扩散以外的第五转移,也是胃背侧系膜近胃端系膜完整切除的边界。沿着膜桥进入膜间隙(即胃癌根治切除的边界)将膜连同包裹内的脂肪淋巴组织一并清除,膜间隙是结直肠Tolds 间隙在胰腺前面的胰前间隙和背面的胰后间隙的延续,继续向上进入Gerota 筋膜前间隙。该间隙入路避免了传统术式沿着肝总动脉或脾动脉剥除淋巴结时创面的渗血。
本研究结果显示,A组手术时间(170.35±41.16)min短于B组的(223.47±51.37)min,术中出血量(55.36±23.25)ml 少于B组的(87.41±26.61)ml,差异具有统计学意义(P<0.05)。说明膜解剖相较于传统血管导向,操作时间更短,造成的术中出血量更少。分析原因认为,对于淋巴结肿大融合成团的患者,沿传统动脉血管剥离时很容易走错层面,进入淋巴组织内,膜的破裂,脂肪淋巴组织的泄露[9]。不仅导致淋巴结的残留,清扫不彻底,也会引起创面渗血,影响术野。两组淋巴结清扫数目、肛门排气时间比较差异无统计学意义(P>0.05)。两组1、2年生存率比较差异无统计学意义(P>0.05)。表明腹解剖与传统腔镜手术相比,手术的效果和远期生存差异不明显。分析淋巴结无统计学差异的原因:①样本量相对较少,结果具有一定的局限性。②在传统腹腔镜手术中,虽然没有按膜解剖来操作,但传统经验方法,顺着血管裸化时,无意间完成了部分膜解剖的过程[10]。
综上所述,在膜解剖指导下行腹腔镜下胃癌根治术,不仅能缩短手术时间,减少出血量,而且为临床操作者提供一种膜间隙意识,是一种很好的术式选择,具有较高的应用及推广价值。
