基于门静脉压力梯度等多因素的肝硬化门静脉高压食管静脉曲张破裂出血风险评估初步探讨
2020-08-19孙世蒙牟玉珍于海东李玉彪马存凯雷振武
孙世蒙,牟玉珍,于海东,李玉彪,马存凯,雷振武
食管胃底静脉曲张是肝硬化门静脉高压最常见的并发症之一,其破裂出血是导致肝硬化门静脉高压患者死亡的主要原因[1]。门静脉高压在侧支循环形成和曲张静脉破裂出血中起决定性作用。食管胃底静脉曲张出血前准确预测门静脉压力梯度(portal pressure gradient,PPG)并选择合适治疗方法是提高门静脉高压症患者生存期的关键。本研究尝试通过分析PPG、食管静脉曲张程度、胃冠状静脉直径、门静脉直径及肝纤维化等指标在肝硬化门静脉高压患者食管静脉曲张破裂出血评估中的作用,优化食管静脉曲张出血预防和治疗。
1 材料与方法
1.1 一般资料
收集2017年1月至2019年3月青海大学附属医院收治的153例门静脉高压患者临床资料。患者入组标准:①符合BavenoⅥ共识中肝硬化门静脉高压诊断标准[2];②拟行颈静脉肝内门体分流术(TIPS)。排除标准:①严重肝功能障碍、凝血功能障碍、肾功能不全;②伴有肝性脑病;③门静脉、脾静脉、肠系膜上静脉血栓形成;④并发肝癌;⑤门静脉海绵样变性;⑥非肝硬化门静脉高压症。根据入组和排除标准,共纳入患者106例。按照TIPS术前有无食管曲张静脉破裂出血分组。出血组62例,其中男43例,女 19 例;年龄 39~73岁,平均(48.79±20.12)岁。未出血组44例,其中男27例,女17例;年龄31~65 岁,平均(46.77±17.35)岁。 所有患者均完善术前PPG检测、影像学资料、实验室检查、胃镜检查、核医学肝纤维化检测、门静脉造影等;门静脉CTV和DSA测量患者门静脉直径、胃冠状静脉直径及数量;胃镜下检测食管静脉曲张程度及数量。本研究经医院伦理委员会审核批准。
1.2 PPG检测方法
通过TIPS放置导管直接检测门静脉和肝静脉自由压。常规右颈部消毒、铺巾,穿刺右颈内静脉成功后,置入RUPS-100型TIPS穿刺套装(美国Cook公司),沿鞘送入导管至肝静脉作造影,以腋中线平心脏水平为零点检测肝静脉压力(手测法,重复3次,取均值);DSA导引下穿刺门静脉,导管置入至门静脉主干,检测门静脉自由压(方法同上)。随后完成TIPS治疗。
1.3 核医学肝纤维化检测
术前空腹6 h抽取外周静脉血,Snibe-MAGLUMI 4 000型全自动化学发光分析仪检测肝纤维化指标——透明质酸钠(HA)、层粘连蛋白(LN)、Ⅲ型前胶原氨基端肽(PⅢNP)、Ⅳ型胶原(ⅣC)。
1.4 食管静脉曲张分级
根据2016年中华医学会肝病学分会《肝硬化门静脉高压食管胃静脉曲张出血的防治指南》[3],将患者食管静脉曲张分为3级:轻度(G1)——食管静脉曲张呈直线形或略有迂曲,无食管静脉曲张红色征;中度(G2)——食管静脉曲张呈直线形或略有迂曲,有红色征,或食管静脉曲张呈蛇形迂曲隆起,但无红色征;重度(G3)——食管静脉曲张呈蛇形迂曲隆起,有红色征,或食管静脉曲张呈串珠状、结节状或瘤状。
1.5 术后随访
术后1~2周,1、3、6个月进行常规体检、实验室检查(血细胞分析、肝肾功能、凝血功能等)和影像学检查(腹部CT/MR、门静脉CTV、门静脉彩色超声)。
1.6 统计学方法
采用SPSS 21.0软件进行统计学分析。计量资料以均数±标准差(x±s)表示,对比用独立样本t检验、多元性线性回归分析,分类资料回归分析用受试者工作特征曲线(ROC);计数资料以百分比(%)表示,对比用卡方检验,等级资料对比用秩和检验,检验标准:α=0.05。
2 结果
两组患者性别、年龄比较,差异无统计学意义(P>0.05);伴腹水、肝功能 Child-Pugh 分级、胃冠状静脉直径、食管静脉曲张程度、门静脉直径、PPG指标比较,差异均有统计学差异(P<0.05),见表1。两组患者核医学肝纤维化指标中HA、PⅢNP、ⅣC比较,差异均有统计学意义(P<0.05),出血组均显著高于未出血组;LN差异无统计学意义(P>0.05),见表2。
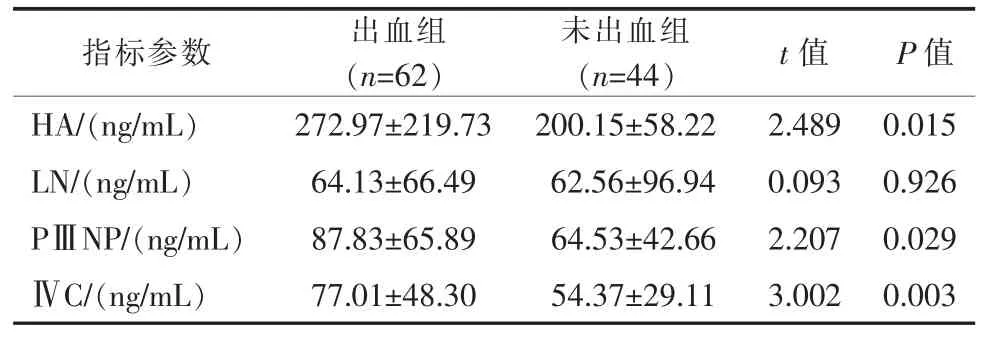
表2 两组患者肝纤维化指标比较 x±s
门静脉高压食管静脉曲张破裂出血多因素评分结果见表3。PPG、Child-Pugh分级、胃冠状静脉直径、门静脉直径、门静脉高压食管静脉曲张破裂出血多因素评分的95%CI及灵敏度、特异度见表4、图1。

表3 门静脉高压食管静脉曲张破裂出血多因素评分

表4 ROC曲线下面积分析结果
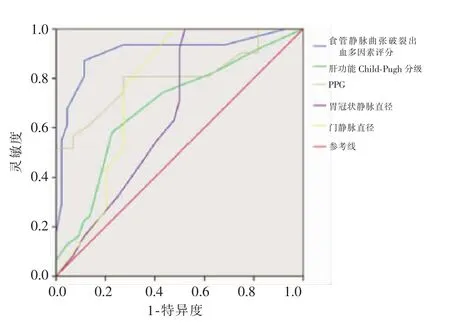
图1 多因素评分等预测食管静脉曲张破裂出血ROC
3 讨论
食管胃底静脉曲张破裂出血是肝硬化门静脉高压症最严重的并发症之一,是影响患者生存和预后的关键因素。林志鹏等[4]研究显示PPG和食管静脉曲张程度是预测食管胃底静脉曲张破裂出血的危险因素,PPG>12 mmHg时曲张静脉破裂出血风险增大。Abraldes等[5]研究显示肝功能 Child-Pugh C级患者食管静脉曲张程度明显大于A级患者,表明肝功能状态与食管静脉曲张出血相关。但研究发现Child-Pugh A级患者伴有重度静脉曲张和红色征时出血风险明显高于C级患者,表明食管静脉曲张严重程度是影响出血的关键因素之一[6]。 Hino 等[7]研究发现胃冠状静脉直径>6.5 mm时静脉曲张破裂出血风险大;腹水是肝硬化失代偿期最常见临床表现,治疗有一定复杂性与难治性。Wadhawan等[8]研究显示伴发腹水患者PPG显著高于无腹水患者(P=0.02),表明腹水也是食管静脉曲张破裂出血高危因素之一。因此,肝硬化门静脉高压患者静脉破裂出血由多因素引起,如何综合评估相关危险因素,提高破裂出血预测,对改善患者预后、选择合适治疗方法具有重要意义。
本研究结果显示出血组、未出血组患者伴腹水、Child-Pugh分级、食管静脉曲张程度、胃冠状静脉直径、门静脉直径、PPG参数差异均有统计学意义(P<0.05),表明这些因素是肝硬化门静脉高压静脉曲张破裂出血的高危因素,与既往文献报道一致。肝纤维化指标可在一定程度上反映肝硬化程度,HA主要由肝间质细胞合成,由肝内皮细胞吸收、分解,当肝实质细胞损伤或肝纤维化进展,其吸收和分解能力减退。LN由肝内皮细胞和上皮细胞合成,肝硬化门静脉高压时LN增多,沉积于肝窦周间隙,影响肝脏微循环。PⅢNP在机体发生炎症坏死时明显增高,可反应体内胶原合成情况,对判断肝纤维化和肝硬化程度有重要意义。ⅣC是肝血窦基底膜的主要成分,其含量增高严重影响肝脏微循环。本研究结果显示出血组、未出血组患者HA、PⅢNP、ⅣC差异均有统计学意义(P<0.05),表明肝纤维化指标可在一定程度上预测静脉曲张破裂出血。
Wang 等[9]报道通过既往出血情况、病史、食管静脉曲张程度评估食管静脉出血风险的方法,但由于出血情况、病史指标含有较多主观信息,难以准确判断,可能造成不同患者差异。本研究通过观察并总结既往文献研究结果[10-13],提出一种评估门静脉高压食管胃底静脉曲张破裂出血的多因素评分方法(表3),即以既往是否出血、PPG、食管静脉曲张程度、胃冠状静脉直径、门静脉直径、Child-Pugh分级为评分参数,以提高预测出血风险水平。本研究结果显示,门静脉高压食管静脉曲张破裂出血多因素评分、Child-Pugh分级、PPG>17、胃冠状静脉直径、门静脉直径的ROC曲线下面积分别为0.906(0.844~0.968)、0.686(0.583~0.790)、0.803(0.720~0.885)、0.665(0.550~0.780)、0.763(0.657~0.869),提示门静脉高压食管静脉曲张破裂出血多因素评分预测食管静脉曲张破裂出血的灵敏度和特异度比PPG>17、Child-Pugh分级、胃冠状静脉直径、门静脉直径更高。多因素评分是一种比较客观的评分方法,其参数均为多因素分析后的相关危险因素。这为肝硬化门静脉高压患者不同治疗提供了参考,如β受体阻滞剂可通过降低每分钟心输出量和内脏血流降低门静脉压,其疗效可通过检测PPG变化结合多因素评分中的肝功能情况进行评估,肝功能较差患者往往不能耐受,而对于多因素评分较高患者,内镜下治疗不能降低PPG,且再次出血风险较高。本研究认为,对多因素评分较低患者可给予内镜下治疗,对多因素评分较高患者,早期可给予TIPS治疗。
总之,综合Child-Pugh分级、胃冠状静脉直径、门静脉直径、食管静脉曲张程度、既往出血及PPG的多因素评分评估肝硬化食管静脉曲张破裂出血,较单一因素评估具有更好的灵敏度和特异度。对静脉曲张高危患者中HA、PⅢNP、ⅣC明显增高患者进行早期干预,可能会降低破裂出血风险。但仍需大样本、多中心研究进一步证实。
