根皮素与根皮苷对酪氨酸酶的抑制机制
2020-08-19陈健敏黄子尧黄玮玥李青莲冉梦楠阮志鹏金楠
陈健敏,黄子尧,黄玮玥,李青莲,冉梦楠,阮志鹏,金楠
(1 莆田学院药学与医学技术学院,福建 莆田 351100;2 药物分析与检验医学福建省高校重点实验室,福建 莆田 351100)
酪氨酸酶(EC 1.14.18.1)是一种多功能的金属酶,广泛存在于微生物、动植物及人体中[1]。近年来酪氨酸酶抑制剂的研究开发越来越受到关注,它们在农业方面(杀虫剂和果蔬褐变抑制剂)和医药化妆品领域(皮肤美白剂)具有巨大的应用潜力。虽然已有大量的研究报道了从天然植物来源或人工合成的方法中开发具有潜在价值和安全的酪氨酸酶抑制剂[2],但只有很少一部分具有应用价值且满足安全需求。因此,开发高效低毒的酪氨酸酶抑制剂的科研任务依然繁重,已成为目前的研究热点之一。
根皮素(phloretin)最早发现于1835年,是从苹果树的根皮、果实及叶中分离得到的天然二氢查耳酮类化合物[3-4]。从结构上看,根皮素是一种缺乏杂环C环和缺少α-β双键的类苯基丙烷化合物。这样的结构特点使它成为柔性分子,能够和许多生物大分子结合[5]。药理研究表明,根皮素及其衍生物具有抗病毒、抗菌、抗肿瘤、抗炎和类雌性激素等作用[5-6]。近年来有人发现根皮素能够抑制人类表皮黑素细胞中酪氨酸酶的活性[7]。最近,科学家又发现根皮素及其衍生物能够在体外有效地抑制酪氨酸酶活性[8-11]。
因此,根皮素在农业和医药化妆品领域具有广阔的应用前景。然而,根皮素在植物中的含量较低,而根皮苷是根皮素的糖基化产物,易于从苹果、海棠等植物中大量获取,根皮苷(phlorezin)是根皮素的很好的一种替代品。但是,到目前为止,根皮苷是否具有酪氨酸酶抑制活性,若有抑制活性,与根皮素抑制机理有何异同,二者抑制酪氨酸酶的分子机制如何;根皮素中起到抑制作用的基团是4-羟基苯基(4-Hydroxyphenyl)还是2,4,6-三羟基苯基(2,4,6-trihydroxyphenyl);这些问题都尚未进行研究。为此,本研究拟采用紫外光谱法、荧光光谱法、高效液相色谱法和分子对接技术对比研究根皮素、根皮苷和根皮酚(phloroglucinol,根皮素的酶解产物)的酪氨酸酶抑制活性和抑制机制,为根皮素和根皮苷的进一步开发和应用提供理论依据和数据支持。
1 材料与方法
1.1 材料
试剂:根皮素(批号:D1122 A)、根皮苷(批号:K176926)和根皮酚(批号:K177822)纯度均为98.5%以上,购于开来生物科技有限公司。酪氨酸酶(来源于蘑菇,批号:BDP1041,比活力为500 U/mg),L-多巴(批号:J1417049)、L-酪氨酸(H1408317)、曲酸(K1418056)和二甲基亚砜(DMSO,批号:J66947)均购自上海晶纯生化科技股份有限公司。本实验中的其它试剂均为分析纯。
仪器:UV2550 紫外可见分光光度计,日本岛津;Spectrofluorometer FS5荧光分光光度计,英国爱丁堡;Agilent 1200高效液相色谱仪,美国安捷伦;Milli-Q-Plus超纯水发生器,德国赛多利斯;PHS-3C 型酸度计,上海雷磁。
1.2 方法
1.2.1 酪氨酸酶单双酚酶活性测定
参考文献[12]的方法并做修改。测定双酚酶活性时以0.5 mmol·L-1L-多巴为底物,测定酪氨酸酶单酚酶活性时以0.5 mmol·L-1的L-酪氨酸作为底物,均用0.05 mol·L-1的磷酸缓冲液(pH=6.8)配制。取试管A1、A2、A3,分别加入2.8 mL底物溶液,28 ℃预热10 min后,A2和A3加入100 μL抑制剂溶液,A1加入等体积溶剂(DMSO)。混匀后,A1,A2加入100 μL酪氨酸酶溶液,A3加入100 μL磷酸缓冲溶液,摇匀,反应10 min时测定A475,平行测定3次。
根据公式酶活性/%=[(A2-A3)/A1]×100% 计算出相应抑制剂下的酶活性。(A1:底物,酪氨酸酶在样品溶剂存在下反应10 min的吸光度值;A2:底物,酪氨酸酶在抑制剂存在下反应10 min的吸光度值;A3:底物,抑制剂反应10 min的吸光度值)。对于单酚酶活性测试,抑制剂若具有双酚酶活性,仅用上述方法不能测定单酚酶抑制作用。只能采用以下方法,抑制剂(不同浓度)与酪氨酸酶分别加入预热10 min的酪氨酸溶液中,随着时间变化记录吸光度值的变化,前2 min内每0.5 min记录一次,之后每1 min记录一次,直至30 min,然后绘制以时间为横坐标,吸光度值为纵坐标的关系图,从图中得到酶反应的迟滞时间和曲线斜率的变化,判断抑制剂是否具有单酚酶抑制作用。
1.2.2 酪氨酸酶底物识别
从单双酚酶活性抑制动力学曲线可以看出,根皮素与根皮苷在低浓度对酪氨酸酶有激活作用。产生这种现象的原因可能是因为根皮素和根皮苷本身就是一种底物。为此,本实验将探索二者是否为酪氨酸酶底物。
将根皮素(或根皮苷)在存在酶作用或不存在酶作用的情况下,每隔5 min,分别对其进行紫外光谱扫描,扫描范围为200~800 nm。简单来说,使用包含166.67 μmol·L-1根皮素(或根皮苷)的PBS(50 mmol·L-1,pH=6.8)3 mL作为底物,向其中加入酪氨酸酶,使其终浓度为13.33 U·mL-1。不加酪氨酸酶的溶液作为空白对照,在相同的条件下每隔5 min进行光谱扫描。
1.2.3 高效液相色谱法测定
为了进一步保证实验结果的可靠性,用高效液相色谱法测试根皮素(或根皮苷)在酶作用下的含量变化。将66.67 μmol·L-1的根皮素(或根皮苷)与酶(33.33 U·mL-1)反应10、 20、30、60和120 min后的样品取出测试。收集的样品用0.22 μm的滤膜过滤后用高效液相色谱法测试。
检测条件如下,色谱柱:Agilent XDB C18 色谱柱(250 mm × 4.6 mm ×5 μm);柱温:30 ℃;进样体积:20 μL;流动相:乙腈-0.05%磷酸水溶液(40:60,V/V);流速:1 mL·min-1;检测波长:286 nm。
1.2.4 荧光光谱测定
荧光光谱采用Spectrofluorometer FS5荧光分光光度计采集。将2 mL 400 U·mL-1的酪氨酸酶加入到石英比色皿中,扫描酪氨酸酶内在荧光光谱,然后每次加入100 μL 0.2 mmol·L-1的根皮素(根皮苷或根皮酚,以DMSO作为溶剂配制),摇匀后静置5 min使其平衡后,扫描光谱。采用280 nm激发,扫描速度与电压都为默认值,分别在298 K和304 K温度下扫描各样品在290~500 nm处的发射光谱。抑制剂的浓度范围控制在0~66.67 μmol·L-1,磷酸缓冲液作为空白背景扣除,不含抑制剂的溶剂(DMSO)作为阴性对照。
1.2.5 分子对接
采用AutoDock (4.2.6)软件研究根皮素和根皮苷与酪氨酸酶之间的相互作用,参考之前使用的方法[13]。首先从https://pubchem.ncbi.nlm.nih.gov/网站上下载蘑菇酪氨酸酶(PDB ID:2Y9X)及配体(根皮素和根皮苷)的3D结构文件,然后用Chem 3D软件将其转化成PDB格式。
利用AutoDockTools 1.5.4对酪氨酸酶大分子(受体)进行处理(包括去除水,加氢等),并保存为pdbqt文件;根皮素和根皮苷也使用同样方法保存为pdbqt文件;设置x、y、z 轴值为4.827、28.489和92.878,使盒子(Grid box)处于酶催化活性中心,整个酶催化活性中心均在盒子之内,盒子大小为60×60×60,一个网格的间距是0.375 Å。
利用Autogrid计算格点的能量分数,采用拉马克遗传算法(Lamarckian genetic algorithm)进行对接运算,并设定运算次数为100次。一般结合能量最低时的对接结果就是大分子与配体结合最稳定的结构,将对接结果保存为PDB格式,利用PyMoL软件查看最佳构象并制图,再用LIGPLOT+(1.4.5) 研究疏水相互作用。
1.2.6 数据统计分析
所有试验数据均重复3次(n=3),采用Microsoft Office Excel 2007数据分析工具进行处理,并用Duncan多重比较(SSR 法)检验各处理平均数之间的差异显著性(P<0.05)。试验数据以平均值±标准差(Mean±SD)表示,采用Origin Pro 8.5 软件作图。
2 结果
2.1 抑制剂对酪氨酸酶单酚酶活性的影响
以L-酪氨酸为底物,在不存在和存在不同浓度的抑制剂的情况下,酪氨酸酶催化反应的进行曲线见图1。如图1D所示,曲酸(kojic acid)作为阳性对照,开始时,产物的形成量缓慢地上升,到一定时间后成直线上升,反应体系达到恒定的斜率,说明反应达到稳定态。直线外推得到横轴截距为抑制剂浓度的增大而延长,稳态的酶活力(直线部分的斜率)也随着抑制剂浓度的增大而下降,这说明曲酸对酪氨酸酶催化酪氨酸的迟滞时间和稳态酶活力均有影响。
实验结果表明曲酸对酪氨酸酶的单酚酶活性有显著的抑制作用。然而,从图1A和1B来看,从迟滞时间和稳态酶活力来看,根皮素和根皮苷表现出在低浓度对酪氨酸酶是激活的,而高浓度呈现抑制,尤其是根皮苷的表现更为明显。而图1C则表明,根皮酚对单酚酶的迟滞时间没有影响,但是随着浓度的升高使得稳态酶活力逐渐下降,说明根皮酚具有单酚酶抑制活性。
根皮素具有根皮酚结构(2,4,6-三羟基苯基),因此根皮素本应该和根皮酚一样表现出单酚酶抑制作用,但是却在低浓度时产生激活的作用。这可能是因为根皮素的另一个结构(4-羟基苯基),它是类似酪氨酸的单酚结构,很可能成为酪氨酸酶的底物,而且生成的产物在475 nm也有吸收,从而造成了激活酶活性的假象。根皮素与根皮酚另一个不同的地方是,根皮素对单酚酶的迟滞时间有显著影响,而根皮酚没有影响,这说明根皮素影响迟滞时间的基团并不是根皮酚结构。
有报道根皮素因具有2,6-二羟基苯乙酮结构(2,6-dihydroxyacetophenone)而具有特殊的还原性[14],具有还原性的物质(如抗坏血酸)能够影响迟滞时间[15],因此根皮素对单酚酶迟滞时间的影响可能来自这个基团。根皮苷的结构与根皮素相近,只是在其根皮酚结构上多了个糖基,应该会因为空间位阻的原因,影响其单酚酶抑制活性,但对比图1 A和1B,发现其抑制作用似乎比根皮素更强。这个问题与根皮素和根皮酚是否真的是酪氨酸酶底物,二者的氧化产物是否对酶活性测试产生干扰有关,接下来将会再设计实验进行探索。
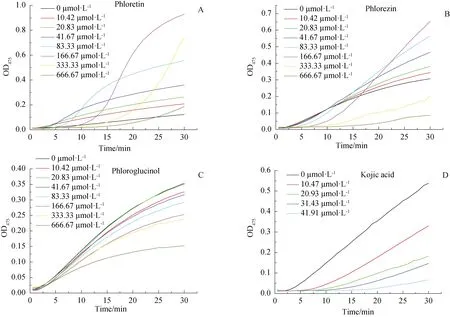
图1 根皮素、根皮苷和根皮酚对酪氨酸酶单酚酶抑制作用的进程曲线
2.2 抑制剂对酪氨酸酶双酚酶活性的影响
以L-多巴为底物,测定不同浓度的抑制剂对酪氨酸酶的双酚酶活性的抑制作用,以曲酸作为阳性对照。结果如图2所示,根皮素和根皮苷在低浓度时,酶的活性大于100%,抑制剂表现出激活的作用;当浓度较大时,这二者有具有较强的双酚酶抑制作用;根皮酚随着浓度的增大表现出有一定的激活作用,说明其没有双酚酶抑制作用。根皮素和根皮苷在低浓度表现出激活作用,推测可能的原因是:二者确实能够激活酶的活性;二者可能是酪氨酸酶的底物,氧化产物与多巴色素相似,在475 nm有吸收,从而从表观上看,是激活作用。具体何种原因,接下来将专门设计实验进行探索。曲酸、根皮素和根皮苷导致双酚酶活力下降一半所需的抑制剂浓度(IC50)分别为83.11、169.36和707.14 μmol·L-1。这些结果说明根皮素比曲酸抑制能力弱,大约为其的一半,但是其又比根皮苷的更强,大约强4倍。根据根皮素与根皮苷的结构,根皮素的一个酚羟基被糖苷基取代便成了根皮苷,这样的结构差异导致根皮苷的抑制活性大幅度下降,可能是因为空间位阻的影响使得根皮苷与酪氨酸酶的结合能力降低了,最终导致抑制活性下降。这一推测将采用分子对接技术进一步进行验证。
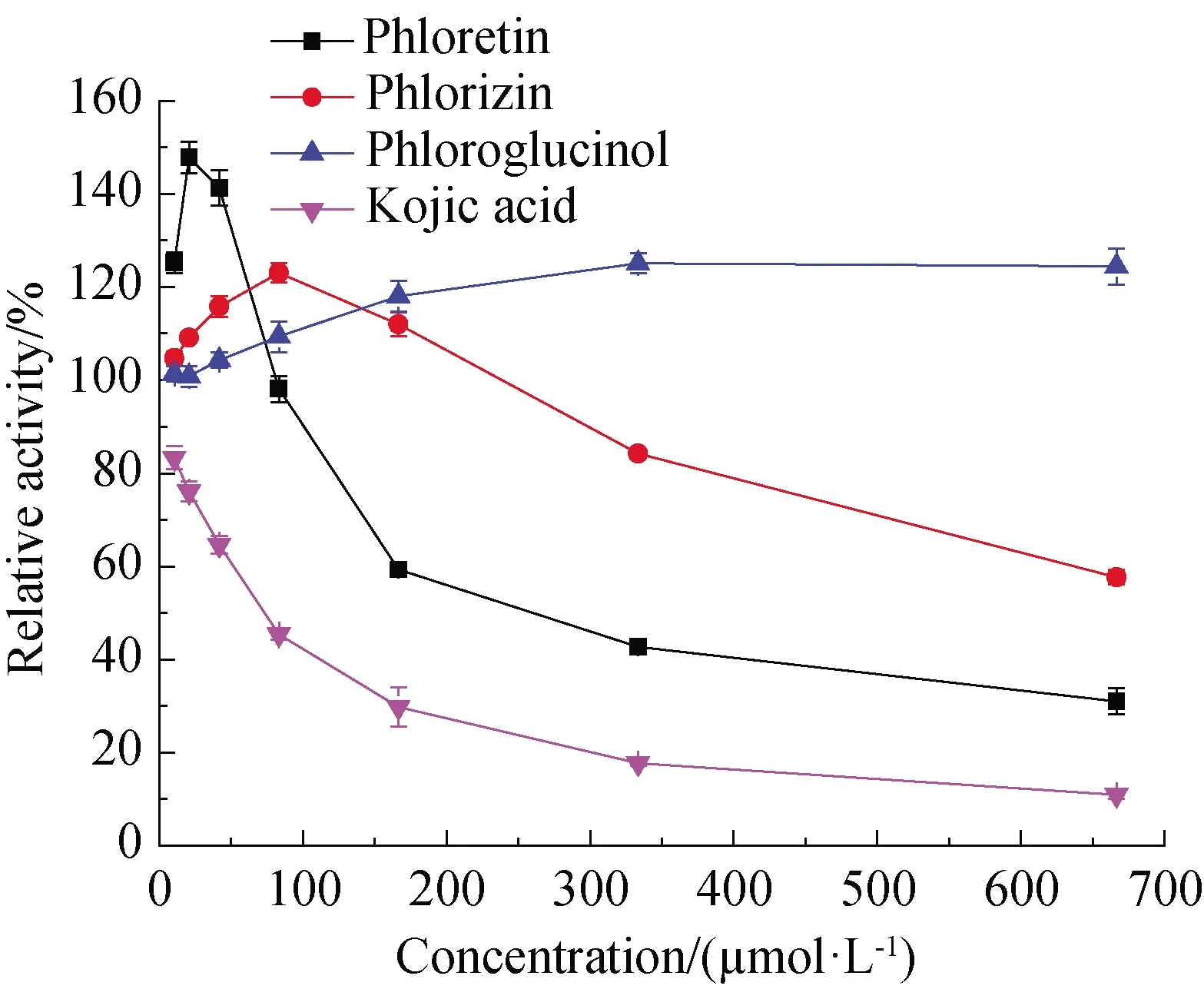
图2 根皮素、根皮苷和根皮酚对酪氨酸酶二酚酶活力的影响
2.3 酪氨酸酶底物识别
单双酚酶活性测试的结果说明根皮素和根皮苷很可能是酪氨酸酶的底物,为了验证这一可能,让根皮素、根皮苷和根皮酚(166.67 μmol·L-1)分别与酪氨酸酶(13.33 U·mL-1)进行反应,每隔5 min扫描一次紫外光谱,结果如图3 A、3C 和3E所示。从图3A可以看出,根皮素自身在288 nm有特征的最大吸收峰,随着时间的延长,该吸收峰逐渐下降,而在475 nm处本来没有吸收峰,也随着时间的延长,显著增大,这结果说明根皮素确实可能是一种底物,与酪氨酸酶反应后生成了其他物质,从而引起了根皮素紫外光谱的变化,另有根皮素自身(没有酶参与下)随时间变化的光谱图(各个时间点光谱重合,因篇幅原因未能列出),说明光谱变化并不是因为其自身的光降解引起的。如图3C所示,根皮苷自身在286 nm 和321 nm有特征的双峰吸收,随着时间的延长,该双峰吸收强度逐渐下降,而且其自身(没有酶参与下)随时间变化的光谱不变,说明根皮苷可能也是一种底物,与酪氨酸酶反应生成其他物质,从而消耗了根皮苷的量,导致其双峰吸收逐渐下降。图3E则表明根皮酚并不是酪氨酸酶的底物。
为了进一步探明这三者是否酪氨酸酶底物以及作为底物反应的动力学特征,以及是否会影响单双酚酶测试的结果,设计如下实验。制备不同浓度的抑制剂,分别在酪氨酸酶的作用下,记录475 nm处的吸光度随时间变化情况。从图3B可以看出,随着根皮素浓度的增大,根皮素与酪氨酸酶反应的稳态速率(图中所示曲线的线性斜率)逐渐升高,但是当根皮素的浓度达到166.67 μmol·L-1以上时,稳态速率又开始逐渐下降。这说明了根皮素在低浓度时主要是作为酪氨酸酶的底物,但当浓度达到一定程度就能够抑制酪氨酸酶的活性。从图3D中可以看出,根皮苷与根皮素具有同样的性质。而图3F则进一步表明根皮酚确实不是底物。根皮素和根皮苷在475 nm有吸收,因此在用单双酚酶活性测试抑制剂的抑制活性时便有干扰,当浓度较低时,根皮素和根皮苷作为一种底物起主要作用,所以表现出激活作用,而在高浓度时表现出抑制作用,这些结论与单双酚酶活性测试结果一致。同时对比图3B和3D,可以发现在475 nm的吸光度值,根皮素比根皮苷强得多,因此单酚酶活性测试的结果中,根皮素受到干扰的程度更大。图3G是采用高效液相色谱法,测试抑制剂与酪氨酸酶反应后的损耗率,从定量的角度进一步证明它们是否为底物。从图中可以看出根皮素在10 min之后,在酪氨酸酶的作用下的损耗率已基本达到100%,而根皮苷则在1 h后才达到100%,这说明二者确实是底物,而且根皮素与酪氨酸酶的酶促反应速率远大于根皮苷,或者说亲和力更强。而根皮酚也进一步被证实其并非酪氨酸酶底物。这些结果说明根皮素和根皮苷是酪氨酸酶的底物,而且其被酪氨酸酶氧化的基团为4-羟基苯基,而不是2,4,6-三羟基苯基(根皮酚结构);根皮苷上的糖基影响了其作为底物对酪氨酸酶的亲和力。
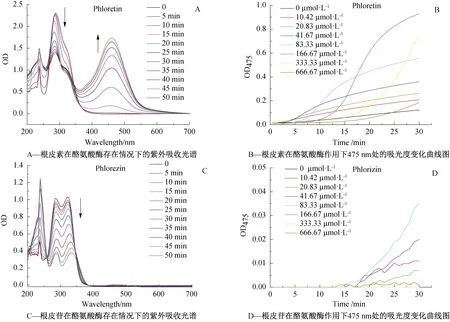
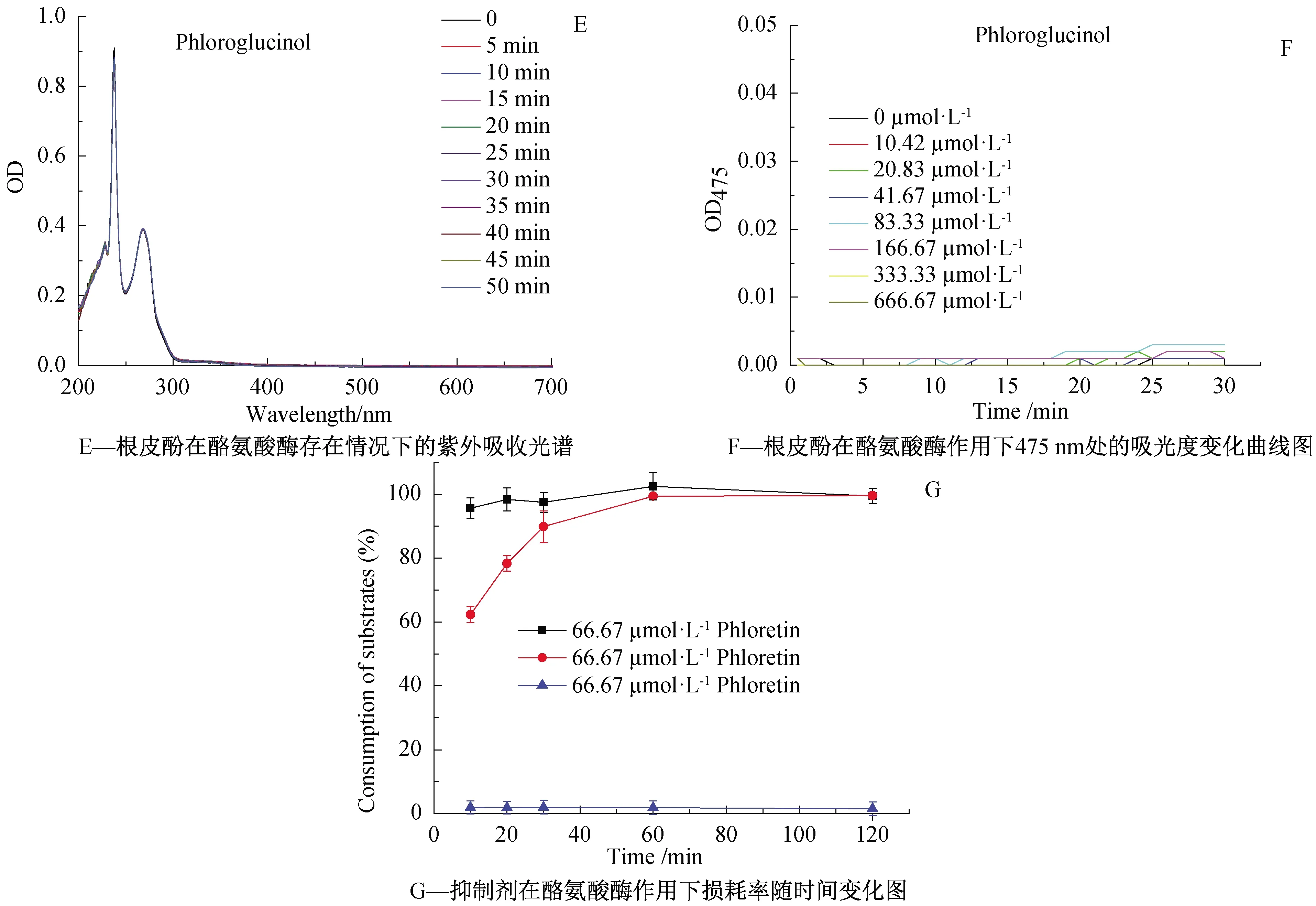
图3 抑制剂对酪氨酸酶双酚酶活性的影响及底物识别试验
2.4 荧光光谱法研究抑制剂与酪氨酸酶的相互作用
2.4.1 抑制剂对酪氨酸酶的荧光猝灭作用
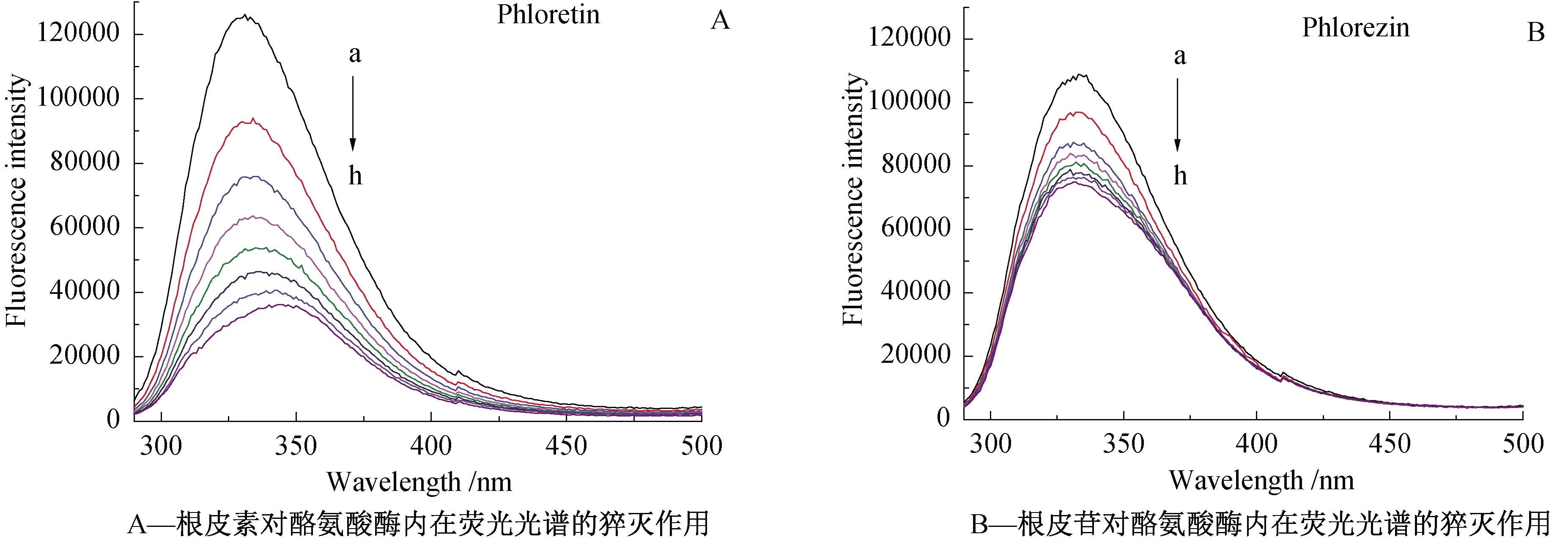
酪氨酸酶含有色氨酸、酪氨酸、苯丙氨酸等氨基酸残基,具有内在荧光特性,所以采用荧光猝灭实验研究其与小分子之间的相互作用也常见报道[16]。图4 A和4B所示为温度298 K时,不同浓度抑制剂(分别为根皮素和根皮苷)存在下,酪氨酸酶的荧光发射光谱。a-h曲线的抑制剂浓度分别为0、9.52、18.18、26.09、33.33、40.00、46.15和51.85 μmol·L-1。随根皮素和根皮苷浓度的增加,酪氨酸酶的荧光强度呈单调性降低,表明二者与酪氨酸酶相互作用后,对其荧光产生猝灭作用[17]。酪氨酸酶的最大发射波长为331 nm,加入根皮素后,酪氨酸酶的最大发射波长发生了蓝移(345 nm),表明根皮素与酪氨酸酶相互作用时,改变发生荧光猝灭的氨基酸残基(色氨酸等)的疏水性环境。与此不同的是,加入根皮苷后,并没有发生明显的红移或蓝移,表明根皮苷并未改变荧光猝灭的氨基酸残基(色氨酸等)的疏水性环境。对比根皮素和根皮苷对酪氨酸酶的荧光猝灭作用,可以发现根皮素的猝灭作用比根皮苷明显更强,主要原因也可能是根皮苷的糖基的空间位阻影响了其与酶的相互作用。图4C和4D分别为根皮酚和溶剂(DMSO)逐渐加入酪氨酸酶的荧光发射光谱,从图中可以看出二者的光谱并没有什么明显差异,这说明根皮酚并不显著引起荧光猝灭。
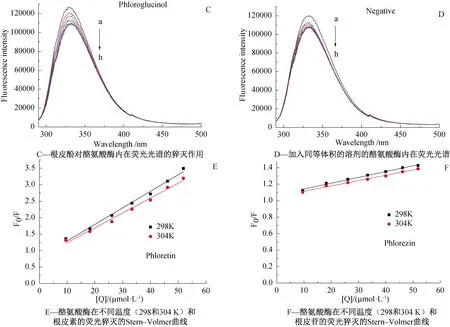
图4 抑制剂对酪氨酸酶的荧光猝灭作用及机理
2.4.2 抑制剂对酪氨酸酶的荧光猝灭机理
荧光猝灭可分为动态猝灭和静态猝灭两种。蛋白质与小分子结合后其荧光强度的变化可由式(1)的Stern-volmer方程表示:
F0/F=1+Kqτ0[Q]=1+Ksv[Q]
(1)
F0为荧光物质的初始荧光强度;F为相互作用后荧光物质的荧光强度;Kq为双分子猝灭过程的速率常数,L·mol-1·s-1;Ksv为Stern-Volmer方程猝灭常数,L·mol-1;τ0为猝灭剂不存在时生物大分子的荧光平均寿命,一般为10-8s;[Q]为荧光淬灭剂的浓度。
分别将根皮素和根皮苷的浓度[Q]对F0/F-1作图,结果发现,F0/F-1与[Q]呈良好的线性关系。由此计算的Stern-Volmer方程及其猝灭常数Ksv见表1。由表1可知,随着温度的升高,Ksv减小,可判断根皮素和根皮苷对酪氨酸酶的荧光猝灭方式都属于静态猝灭。根据得到的不同温度下的抑制剂猝灭常数Ksv,及其与Kq的关系,可求得298和304 K下对应的Kq,根皮素的Kq分别为5.02×1012和4.52×1012L·mol-1·s-1,根皮苷的Kq分别为7.06×1011和6.45×1011L·mol-1·s-1,远大于生物分子的最大碰撞扩散速率常数(2. 0×1010L·mol-1·s-1)[18],由此可进一步判断,根皮素和根皮苷对酪氨酸酶的荧光猝灭是由于其与酪氨酸酶形成了无荧光或者荧光信号较弱的复合物而引起的静态猝灭。而且,根皮素的Ksv和Kq值均比根皮苷的大,证明根皮素与酪氨酸酶的亲和能力比根皮苷更强,形成的复合物更稳定。这与酪氨酸酶底物识别的实验结果一致,原因可能也在于根皮苷的糖基(空间位阻)。
2.4.3 抑制剂与酪氨酸酶的结合常数和结合位点数
为进一步计算根皮素和根皮苷的结合常数和结合位点,静态猝灭中,假定它们之间有n 个独立的结合位点,我们描述结合常数与荧光强度、猝灭剂浓度以及结合位点数之间的关系可用式(2)所示的双对数方程:
(2)
在不同温度下,以不同浓度的根皮素和根皮苷对应酪氨酸酶荧光光谱的log [Q]值对log[(F0-F)/F]作双对数图,并进行线性回归,由所得直线的斜率和截距可计算得到根皮素和根皮苷与酪氨酸酶的结合位点数和结合常数(表1)。由表1可知,根皮素和根皮苷与酪氨酸酶的结合位点数都约为1,表明根皮素和根皮苷与酪氨酸酶的结合只有一类独立的结合位点[19]。根皮素的结合常数均比根皮苷的更大,之所以随着温度的升高而减小,是由于根皮素和根皮苷对酪氨酸酶的猝灭机理是静态猝灭,温度升高不利于复合物的稳定,因此结合常数减小。
2.4.4 抑制剂与酪氨酸酶相互作用力类型
小分子与蛋白质的作用力类型主要包括氢键、范德华力、静电作用力和疏水相互作用。通过研究根皮素和根皮苷与酪氨酸酶相互作用的结合自由能(ΔG)、焓变(ΔH)、和熵变(ΔS)等热力学参数可探究作用力类型。温度变化不大时,结合作用的焓变和熵变可以近似看做常数。根据之前求得的298和304 K下得到的结合常数以及公式(3)和(4)求解出各项参数,结果见表1。
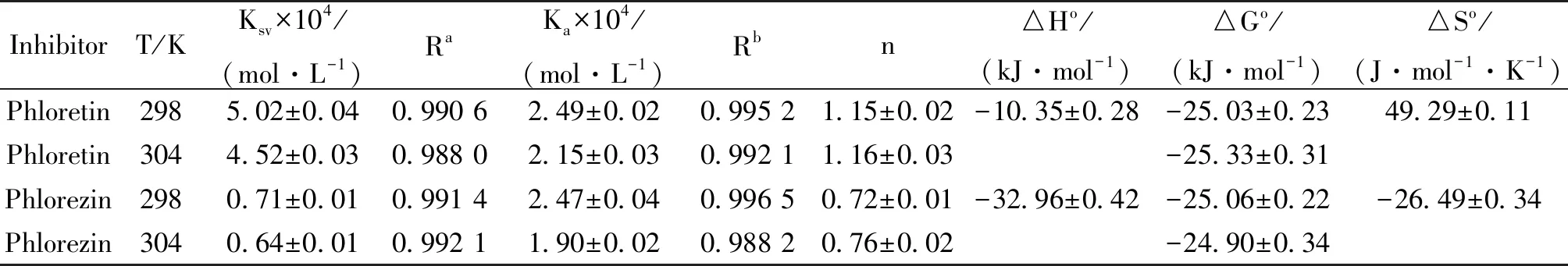
表1 根皮素和根皮苷与酪氨酸酶在不同温度下相互作用的荧光猝灭常数Ksv, 结合常数Ka,键合位点数n和相关的热动力学参数
(3)
Go=Ho-TSo,
(4)
式中,K为对应温度下的结合常数(L·mol-1);R为理想气体常数(8. 314 J·mol-1·K-1)。结果显示,298与304 K下根皮素和根皮苷与酪氨酸酶的结合自由能分别为-25.03±0.23、-25.33±0.31 kJ·mol-1和-25.06±0.22、-24.90±0.34 kJ·mol-1,自由能均为负值,说明根皮素和根皮苷与酪氨酸酶的相互作用是自发进行。
根皮素与酪氨酸酶相互作用过程的熵变ΔS为49.29 J·mol-1·K-1,ΔS为正值,表明二者相互作用中存在疏水作用。另外,计算所得体系的焓变(ΔH) 为-10.35 kJ·mol-1,焓变为负值说明根皮素与酪氨酸酶相互作用时有氢键作用发生。由此可说明根皮素与酪氨酸酶形成的复合物中,氢键与疏水作用力起着至关重要的作用。根皮苷与酪氨酸酶相互作用过程的熵变ΔS为-26.49 J·mol-1·K-1,ΔS为负值,说明有范德华力作用[20]。计算所得体系的焓变(ΔH) 为-32.96 kJ·mol-1,焓变为负值说明根皮苷与酪氨酸酶相互作用时有氢键作用发生。结果说明根皮苷与酪氨酸酶形成的复合物中,主要是氢键和范德华力的作用。
2.5 分子对接
利用分子对接软件Autodock (4.2.6)分别构建了根皮素和根皮苷与酪氨酸酶的对接模型,图5A(surface)和5B(carton)展示了根皮素与酪氨酸酶的对接模式和氢键相互作用。酪氨酸酶的活性中心由2个铜离子和6个与之相连的组氨酸残基(His-61、His-85、His-94、His-259、His-263和His-296)组成[21]。由图5 A可见根皮素在酪氨酸酶的活性中心内,结合能为-5.12 kcal·mol-1。图5B中展示了根皮素与酪氨酸酶结合的氢键作用(黄色虚线),由图可见共与6个氨基酸残基形成氢键作用(共6个),包括ASN-260 (1)、VAL-283 (1)、GLY-281 (1)、HIS-85 (1)、HIS-94 (1) 和 HIS-259 (1)。图5C和5D显示,根皮苷并没有整个分子进入活性中心,只有4-羟基苯基在中心内,而另外一部分在中心外,最佳构象的结合能为-3.99 kcal·mol-1。图5D显示了根皮苷与酪氨酸酶结合,并与4个极性氨基酸残基发生氢键作用(共7个),包括:HIS-244 (2)、MET280(1)、HIS-85(2)和ASN-81(2)。从图5E和5F来看,根皮素和根皮苷与酪氨酸酶有很强的疏水作用,根皮素与酪氨酸酶上的16个残基有疏水作用,而根皮苷只与13个残基有疏水作用。从结合能的大小来看,根皮素比根皮苷更容易与酪氨酸酶结合,结合主要通过氢键和疏水作用,因此二者与酪氨酸酶结合中,疏水作用占主导地位。分子对接结果表明根皮素和根皮苷与底物识别实验和荧光猝灭实验结果一致。从对接结果和前面的实验结果可推测,根皮素和根皮苷抑制酪氨酸酶活性存在以下4个方面的机制:①根皮素和根皮苷在活性中心部位的存在可能形成空间位阻效应,阻碍其他酶底物进入酶活性中心;②根皮素和根皮苷与酪氨酸酶之间的相互作用,可能影响酪氨酸酶的活性中心空间构象,导致酪氨酸酶活性受到影响;③根皮素和根皮苷作为一种底物,起到竞争性抑制;④根皮素和根皮苷具有特殊的2,6-二羟基苯乙酮结构,对单酚酶的迟滞时间有影响。

图5 分子对接分析抑制剂与酪氨酸酶的相互作用
3 讨论
本研究深入探讨了根皮素和根皮苷对酪氨酸酶活性抑制和机制。单双酚酶抑制动力学实验结果表明,根皮素和根皮苷对单酚酶活性有抑制作用(延长迟滞时间并减小稳态酶活力),单酚酶活性抑制来源于2,6-二羟基苯乙酮和2,4,6-三羟基苯基结构;双酚酶活性抑制(IC50)分别为169.36和707.14 μmol·L-1,说明根皮素比根皮苷具有更强的双酚酶抑制作用(糖基位阻原因);底物识别实验结果证明根皮素和根皮苷都是酪氨酸酶的底物,而且根皮素比根皮苷(糖基位阻原因)与酪氨酸酶具有更强的亲和力;荧光光谱实验结果表明,根皮素和根皮苷对酪氨酸酶产生静态荧光猝灭,并分别通过氢键和疏水相互作用与氢键和范德华力作用,与酪氨酸酶形成稳定的复合物,根皮素形成的复合物更加稳定。分子对接实验结果进一步表明:根皮素与酪氨酸酶残基(ASN-260,VAL-283,GLY-281,HIS-85,HIS-94和HIS-259) 形成了6个稳定的氢键和16个残基形成疏水作用(最佳构象结合能为-5.12 kcal·mol-1),而根皮苷与酪氨酸酶残基(HIS-244,MET280,HIS-85和ASN-81) 形成了7个稳定的氢键和13个残基形成疏水作用(最佳构象结合能为-3.99 kcal·mol-1),根皮苷的糖基影响了其与酶的结合。综上,根皮苷的酪氨酸酶抑制活性比根皮素低,主要是因为糖基影响了其与酪氨酸酶的结合,但二者抑制机制相似。这些研究结果有助于根皮素和根皮苷的进一步开发和利用。
