吉利德科学公司Remdesivir专利分析及启示*
2020-08-18朱月仙李姝影
张 娴 朱月仙 李姝影 许 轶
(1.中国科学院成都文献情报中心 知识产权研究咨询中心,成都610041;2.中国科学院大学经济与管理学院图书情报档案管理系,北京100190)
2020年2月1日,《新英格兰医学杂志》(The New England Journal of Medicine,NEJM)在线发表多篇关于COVID-19病例的论文,其中介绍了美国首例新型冠状病毒感染肺炎确诊病例的诊疗过程以及其接受美国吉利德科学公司(Gilead Sciences,Inc.)在研药物 Remdesivir(又名:瑞德西韦、伦地西韦)作为“同情用药”(compassionate use)进行试验性治疗的临床表现。该患者在治疗之后,病情出现了迅速缓解[1]。
Remdesivir是美国吉利德科学公司针对埃博拉病毒开发的一款药物,2020年2月针对埃博拉病毒感染的临床研究在第Ⅲ期阶段。截至2020年2月,Remdesivir尚未在任何国家获得批准上市,其安全性和有效性也未被证实。吉利德公司表示,尽管目前没有抗病毒数据显示Remdesivir对于“新型冠状病毒”(COVID-19)的活性,但其针对其他冠状病毒的有效数据为其带来了希望,在体外和动物模型中,Remdesivir证实了对严重急性呼吸系统综合征(Severe Acute Respiratory Syndrome,SARS)和中东呼吸综合征(Middle East Respiratory Syndrome,MERS)的病毒病原体均有活性,二者与新型冠状病毒在结构上非常相似。吉利德公司于2月1日发布声明,表示正与全球卫生部门紧密合作,通过提供在研药物Remdesivir应用于试验性治疗,以应COVID-19的暴发。目前,吉利德公司与美国食品药品监督管理局(U.S.Food&Drug Administration,FDA)、美国疾病控制和预防中心(U.S.Centers for Disease Control and Prevention,CDC)、美国卫生和公共服务部(U.S.Department of Health and Human Services,DHHS)、中国疾病预防控制中心、中国国家药品监督管理局、世界卫生组织(World Health Organization,WHO)、美国国家过敏和传染病研究所(U.S.National Institute of Allergy and Infectious Diseases,NIAID)等组织机构以及研究人员和临床医生一起,在抗病毒领域贡献其资源,帮助患者和各界共同抗击 COVID-19[2]。
2月2日,中国国家药监局药品评审中心正式受理Remdesivir的临床试验申请。2月5日,由中日友好医院王辰、曹彬团队牵头的Remdesivir治疗2019新型冠状病毒感染临床试验研究在武汉市金银潭医院宣布启动,以评价Remdesivir对新型冠状病毒性肺炎的安全性与有效性[3-5]。2月21日,美国国立卫生研究院(U.S.National Institutes of Health,NIH)和NIAID共同资助了一项针对重症新冠病患的Remdesivir临床试验[6]。
本文从PubChem、Cortellis数据库中获取了吉利德公司关于Remdesivir的9项专利,基于inco-Pat全球专利数据库获取整理了相关信息(数据检索日2020年2月1~5日),希望能为相关研发提供参考。
1 Remdesivir概况
Remdesivir是由吉利德公司开发的一种新型实验性广谱抗病毒药物,被认为可以有效抑制呼吸道上皮细胞中SARS病毒和MERS病毒的复制。Remdesivir属于核苷类似物,是RNA依赖的RNA聚合酶(RdRp)抑制剂,可以通过抑制病毒核酸合成抗病毒。Remdesivir在临床前研究中被发现能够抑制埃博拉病毒一个名叫RdRP的蛋白质——该蛋白质对于埃博拉病毒在人体细胞内的复制繁殖至关重要,因此能够起到很强的病毒抑制作用。
药品名称:瑞德西韦,伦地西韦
研发代码:GS-5734
系统(IUPAC)命名名称:2-ethylbutyl(2S)-2-[[[(2R,3S,4R,5R)-5-(4-aminopyrrolo[2,1-f][1,2,4]triazin-7-yl)-5-cyano-3,4-dihydroxyoxolan-2-yl]methoxy-phenoxyphosphoryl]amino]propanoate
化学物质登记号:1809249-37-3
分子式:C27H35N6O8P
摩尔质量:602.58 g·mol-1
分子靶点:RNA-dependent RNA polymerase(RdRp)
作用机制:RdRp抑制剂;核苷类似物
公司:Gilead Science
最高研发阶段:Ⅱ/Ⅲ期临床
结构式:如图 1[7]所示。
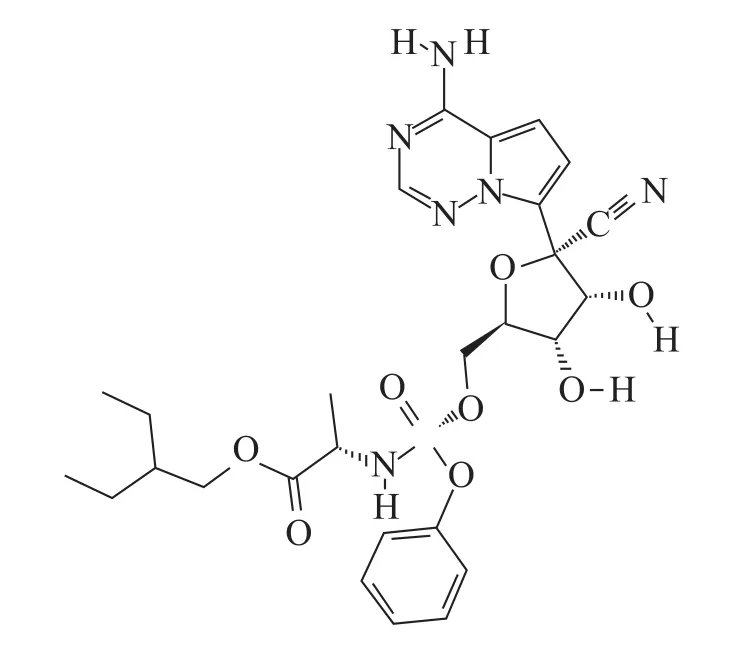
图1 Remdesivir的结构式Fig.1 Structural Formula of Remdesivir
2020年4月29日,中美两国3个研究团队分别发布了各自开展的Remdesivir治疗COVID-19临床试验研究结果,结论各不相同:1)吉利德公司公布的开放标签SIMPLE三期临床试验结果显示,接受5天疗程的患者与接受10天疗程的患者的临床改善相似,说明Remdesivir用药量减半并不影响患者疗效。吉利德公司首席医疗官Merdad Parsey博士认为,该研究结果“补充了NIAID的Remdesivir安慰剂对照研究的数据,并且有助于确定Remdesivir治疗的最佳持续时间。研究表明对于一些患者可采取为期5天的治疗方案,这样可显著增加在当前Remdesivir供应量下能够治疗的患者数量,对当前大流行背景下帮助医院救治更多病患尤为重要”[8]。2)中国医学科学院王辰和中日友好医院的曹彬研究团队在《柳叶刀》杂志发表的关于Remdesivir的全球首项随机双盲安慰剂对照临床试验结果显示,Remdesivir疗法在治疗重症新冠肺炎中与标准疗法相比不具有统计学意义上的显著临床获益。但是,尽管没有统计学意义,但在症状持续时间为10天或更短的患者中,接受Remdesivir的患者比接受安慰剂的患者的临床改善时间更快。不过,在早期治疗患者中对于临床改善时间的减少情况,还需要更大规模的研究加以证实[9]。3)NIAID公布的一项适应性COVID-19治疗试验(the Adaptive COVID-19 Treatment Trial,或称ACTT试验)的初步数据分析结果,认为接受Remdesivir治疗的进展期患者比接受安慰剂治疗的类似患者恢复速度更快,该研究认为Remdesivir在缩短康复时间方面具有明显的积极作用[10]。
中美三个临床试验研究结果的明显差异,再度引发全球对Remdesivir治疗新冠肺炎疗效的热议。业内同行评论,中国开展了全球首个随机双盲、安慰剂对照的临床试验,设计最严谨科学、执行标准最严格规范,对科学评价Remdesivir治疗重症新冠肺炎有一定的借鉴和指导意义。美国试验结果显示具有一定疗效,但研究结果也提示,不能确认Remdesivir对重症的干预有效。综合来看,目前中美试验结果显示Remdesivir并非治疗新冠肺炎的特效药,但可能是一个有效的治疗药物选择,后续还需要基于既有试验的更多临床试验,可利用临床应用的真实试验数据继续补充验证,同时也对患者和医生发挥一定的心理安慰,具有一定的社会意义[11]。
截至5月7日,美国的新冠感染者已逾120万,死亡人数超过7万[12],找到一种可以对抗新冠病毒的治疗药物成为了美国的燃眉之急,在此背景下,美国各方对Remdesivir反响积极。5月1日,美国FDA有条件批准了Remdesivir用于重症新冠肺炎住院患者的紧急使用授权(Emergency Use Authorization,EUA)[13]。同日,吉利德公司宣布已捐赠了全部150万单剂Remdesivir,将在获得紧急授权与监管批准(包括EUA)后免费提供给患者,以10天一个疗程计算,相当于超过14万个疗程。吉利德公司正在多管齐下扩大生产规模,迅速建立能够满足更多临床试验与EUA计划的Remdesivir供应能力。吉利德公司已通过工艺改进大大缩短了从原材料到成品的制造周期,并且通过北美、欧洲和亚洲多家合作伙伴扩充Remdesivir产能,目标是到2020年10月至少生产50万个疗程,到2020年12月生产100万个疗程,2021年如需要还可以生产更多[14]。
2 吉利德公司Remdesivir专利分析
2.1 专利技术市场布局
通过PubChem、Cortellis记录,获知吉利德公司关于 Remdesivir化合物的9项相关专利申请[7,15]。这 9项专利申请通过 INPADOC同族专利布局,共覆盖了全球38个国家与地区。这些专利家族成员的全球分布反映出,吉利德公司对该技术布局最重视的市场依次是美国、澳大利亚、日本、中国、韩国、加拿大、中国台湾,并且吉利德公司很重视专利合作条约(Patent Cooperation Treaty,PCT)途径的利用(表1)。
2.2 专利技术主要内容
吉利德公司于2011年7月22日申请了Remdesivir的最早化合物专利(WO2012012776 A1)。吉利德公司对该化合物专利通过PCT途径在美国、澳大利亚、中国、日本、韩国等全球20多个国家与地区进行了专利布局。其它8项专利技术分别涉及了Remdesivir用于多种病毒感染治疗的相关化合物、药物组合物及其相关制备方法、病毒感染治疗方法等内容,包括化合物结构、化合物及其药物组合物制备方法、合成、晶型、制剂等的保护。
这些专利技术内容反映出,Remdesivir化合物可作为治疗丝状病毒科病毒(马尔堡病毒、埃博拉病毒和Cueva病毒等)、沙粒病毒科病毒(拉沙病毒和胡宁病毒等)、冠状病毒科病毒(SARS、MERS病毒等)、黄病毒科病毒(寨卡病毒等)和副粘病毒科病毒感染的诸多疾病的潜在治疗药物,体现出其广谱抗病毒性的潜力(表2)。
2.3 中国同族专利保护
吉利德公司Remdesivir专利技术在中国共有6件发明专利申请。其中2件已获得授权,其余4件处于实质审查阶段(表3)。
这些专利申请反映出,吉利德公司的Remdesivir化合物专利在中国已经获得专利授权保护,且距离有效期届满还有较长一段时期。对于药物的专利保护而言,化合物专利是其中的重要核心。其他专利申请涉及Remdesivir用于治疗丝状病毒科病毒、沙粒病毒科病毒、冠状病毒科病毒、黄病毒科病毒等多种病毒感染的化合物、组合药物及其制备以及施用治疗方法,当前尚未获得授权。

表1 吉利德科学公司Remdesivir相关专利分布Tab.1 Distribution of the INPADOC Patent Family Members on Remdesivir by Gilead Sciences

表2 吉利德公司Remdesivir相关专利内容Tab.2 Gilead Sciences' Patents on Remdesivir

表3 吉利德公司Remdesivir相关中国专利申请Tab.3 Gilead Sciences' Patents on Remdesivir in China
对该6件中国专利的主要技术内容解析如下。
1)专利名称:用于治疗副黏病毒科病毒感染的方法和化合物


2)专利名称:用于治疗副黏病毒科病毒感染的方法和化合物


3)专利名称:治疗丝状病毒科病毒感染的方法


4)专利名称:制备核糖核苷的方法


5)专利名称:治疗沙粒病毒科和冠状病毒科病毒感染的方法

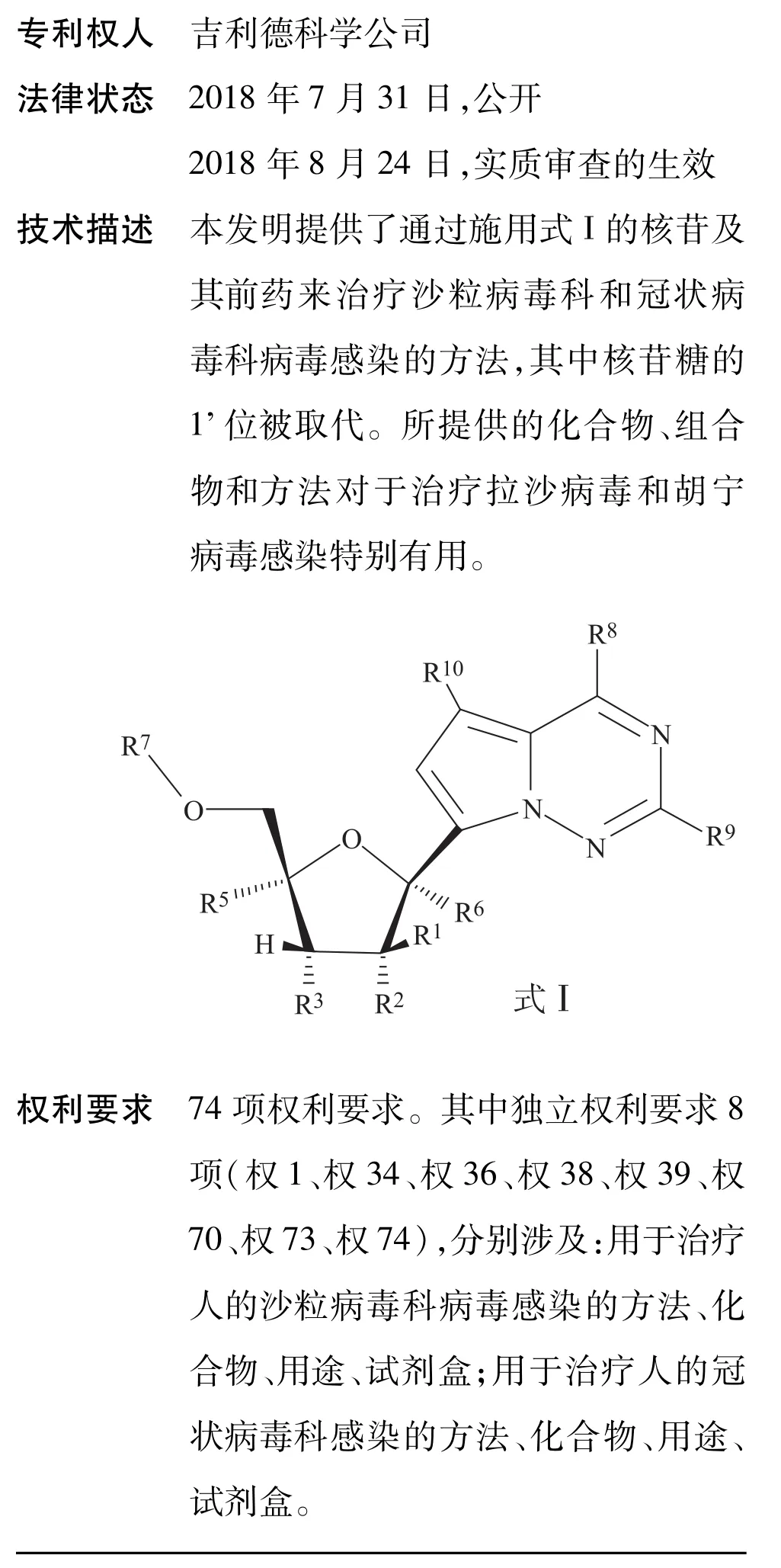
6)专利名称:(S)-2-(((S)-(((2R,3S,4R,5R)-5-(4-氨基吡咯并[2,1-f][1,2,4]三嗪-7-基)-5-氰基-3,4-二羟基四氢呋喃-2-基)甲氧基)(苯氧基)磷酰基)氨基)丙酸-2-乙基丁基酯的结晶形式


3 吉利德公司Remdesivir专利布局策略
吉利德公司从2011年开始Remdesivir专利申请,先后对药用化合物、药物组合物、医疗用途、制备方法、剂型等申请了专利保护,经过近十年的专利布局,逐步构建起了Remdesivir药物的核心技术保护体系。其中,吉利德公司已经获得了化合物专利授权,可以说是掌握了该药物专利保护体系的核心与主导地位。并且,吉利德还获得了该药物治疗副黏病毒科、丝状病毒科、沙粒病毒科和冠状病毒科病毒感染的用途专利权利保护,对该药物抗病毒适应症的广谱应用也已有了比较广泛的技术布局。
此外,吉利德公司对相关试剂盒、冻干组合物、可注射组合物的专利申请活动反映出,公司已开始着手Remdesivir的未来产品化的前瞻布局。可见,尽管当前Remdesivir尚处于在研状态且原计划针对埃博拉病毒感染治疗的研究进展并不理想,但吉利德公司的技术创新活动已经在从基础研发端向商业研发端推进,围绕创新价值全链,由研发驱动创新技术的市场化、产业化。
中国是吉利德公司重点选择的专利保护布局区域之一。吉利德公司关于Remdesivir的化合物类中国同族专利申请已在中国获得授权,还获得了治疗副黏病毒科病毒感染的用途专利权利保护。其它多件专利申请如治疗丝状病毒科、沙粒病毒科、冠状病毒科病毒感染的方法等正处于实质审查阶段。本次Remdesivir直接进入中国开展针对COVID-19的临床三期试验,未来时期,关于Remdesivir制剂、制备方法等产品化专利以及相关外围专利的布局可能还会进一步增强。
吉利德公司Remdesivir专利布局策略见图2。

图2 吉利德科学公司Remdesivir专利布局策略Fig.2 Gilead Sciences' Patent Strategy on Remdesivir
4 对我国新药研发知识产权保护的启示
吉利德公司是目前全球最大的生物制药公司之一,在病毒疾病领域具有全球统治地位,自2014年以来一直保持着全球人类免疫缺陷病毒(HIV)药市场一半以上占有率;开发了首个治愈病毒疾病的特效药,使丙型肝炎(HCV)的药物治愈率提高到90%以上;是甲型和乙型流感治疗药物达菲(Tamiflu)的原研企业。结合吉利德公司关于Remdesivir以及其它药物专利保护情况,总结其专利战略主要特点及对于我国创新药物研发知识产权保护的启示如下。
4.1 密织保护网,掌控主动权
吉利德公司的Remdesivir专利申请特点,反映出吉利德公司对新药研发保护秉持的一以贯之的专利布局策略,即:专利申请布局内容尽可能涉及化合物及衍生物、药物制剂与组合物、制备方法和装置、制药用途、晶体、联合用药等各方面,尤其重视对处于上游的化合物及衍生物专利技术的申请和布局,以掌控药品专利保护的主动权。
因此,新药研发主体应注重尽早申请化合物基础核心专利,再围绕核心专利积极完善包括化合物晶型、制备方法、组合物、治疗用途等专利申请,形成全面覆盖的专利组合网络。注重企业专利分析,重视专利撰写质量与可实施性,保持与竞争对手的相对优势。
4.2 提升创造质量,聚焦目标区域,布防全球市场
吉利德公司专利申请以发明类型为主,从专利家族成员分布来看,约47%发明通过PCT程序进行申请和布局、48%发明在研发地就近申请布局,非常重视利用PCT途径开展全球市场布局。不仅是Remdesivir,当前吉利德公司大部分专利的预计保护期届满日处于未来10~16年,专利技术生命力旺盛[16]。吉利德公司早期产品并不太重视中国市场专利布局,后来基于中国巨大市场潜力的考虑,对于核心技术基本都会通过PCT途径进入中国申请,例如公司的热点产品如Tenofovir(替诺福韦酯)、Sofosbuvir(索非布韦)等的化合物、晶型、制剂等核心专利。
因此,新药研发主体应重视一类新药研发,重视前瞻性、战略性的新方法、新技术、新策略的研究,加强多学科、多种技术方法的交汇融合与综合集成,不断更新药物的研发理念,提升知识产权成果创造质量,为产业发展提供高质量的创新成果与技术储备。并且,聚焦目标市场定位,开展重点区域布局,加强全球推广利用。
4.3 灵活运用策略,加强运营
吉利德公司注重综合利用多种手段保护和运用企业知识产权。企业不仅注重对创新成果申请专利权保护,同时还注重运用商业秘密、技术秘密等非专利手段保护企业内部创新知识,通过与合作伙伴、员工、顾问和供应商签订保密协议的方式防止侵权纠纷等。例如,作为公司脂质体技术关键组成的大量脂质体制造专业知识就是作为商业秘密而非专利形式来进行保护的。吉利德公司尤其注重对知识产权成果的有效运营,通过专利转让、技术许可、特许使用等方式,促进研发成果的活跃应用,维持在竞争对手中的竞合优势,保障了企业创新技术供给与商业运营前景的巨大潜力与长足发展空间。
因此,新药研发主体应注重加大知识产权布局与多种策略的灵活运用。在新药研发过程中,应建立科学、系统和规范的知识产权管理体系。规范和完善新药研发过程涉及的各项知识产权的操作——如药品专利链接、药品数据保护、专利期延长、优先权、临时专利申请、分案申请、专利复审无效、诉前禁令、商业秘密等,将知识产权制度与药品技术创新进行有效衔接,发挥药品知识产权保护的最大效应,切实提高产品附加值和技术创新水平。
4.4 加快资本市场融合,加速产业化进程
吉利德公司于1995年研发出首款新药Vistide后就联合投资人开始大手笔收购行动,奠定了高速发展的基础,此后多次通过研发或并购不断壮大产品线与研发管线的部署运用,特别是借助激进主动的专利收购策略实现了企业的跨越式发展,堪称利用资本运作扶持产业发展的典范。
因此,我国新药研发主体,尤其是科研院所类机构等,应重视与产业界合作,加快创新药科研项目与社会资本的融合。以产品化、产业化为导向,提升新药知识产权的运营能力,在自主研发的同时,根据对市场情况及药物发展前景的预判,通过多种方式实现知识产权资产的转移转化。借助资本市场介入来打通前期基础研究、应用研究和后期产业化之间的瓶颈,畅通药物研发管线,为科研成果顺利转向医药企业后期研发和产业化奠定基础,助推通过创新研发驱动产业发展。
