经颅多普勒超声无创性评价颅脑创伤患者颅内压的临床研究
2020-08-07常涛高立杨彦龙李立宏
常涛 高立 杨彦龙 李立宏
根据《颅脑创伤救治指南》推荐的治疗策略,以颅内压(ICP)< 20 mm Hg(1 mm Hg=0.133 kPa)、脑灌注压(CPP)60 ~70 mm Hg为目标的导向治疗可有效降低重型颅脑创伤(sTBI)患者的病死率[1-2];而有创性颅内压监测作为颅内压监测的“金标准”则是颅脑创伤患者颅内压目标导向治疗的决策基础,然而由于颅内出血、感染等与操作相关的并发症,加之费用昂贵、零点漂移等因素大大限制了该项技术的临床推广应用[3-4]。经颅多普勒超声(TCD)是一种无创性检查技术,近年广泛应用于神经危重症患者,通过对脑血流量和颅内压的监测与评估,指导临床管理,尤其对于在特殊环境下无法实施有创性颅内压监测的患者,TCD 可识别脑低灌注状态,有助于早期恢复脑血流[5-6]。然而,视神经鞘直径(ONSD)和搏动指数(PI)这两项TCD 无创性评估颅内压的指标,与颅内压间的相关性及其预测颅内压增高的能力目前尚未得到充分研究,本研究以空军军医大学唐都医院神经外科重症监护中心近年治疗的68例颅脑创伤患者为观察对象,回顾分析所有患者的诊断与治疗过程,以探讨TCD 无创性评估颅内压的敏感性、特异性和诊断准确性。
对象与方法
一、研究对象
1.纳入标准 (1)闭合性颅脑创伤。(2)年龄>16 岁。(3)创伤至入院时间 ≤ 24 h。(4)入院时Glasgow昏迷量表(GCS)评分≥4分。(5)入院后接受开颅血肿清除术并留置有创性颅内压监测探头。(6)经TCD 无创性评估视神经鞘和大脑中动脉(MCA),并获得高质量图像。(7)术后重症监护管理时间≥1 周。(8)患者及其家属对监测项目知情并签署知情同意书。
2.排除标准 (1)开放性颅脑创伤。(2)颅脑创伤合并视神经损伤或既往有视神经病变。(3)GCS评分为3分或为脑疝晚期。(4)接受过头颈部血管病变并行支架植入术。(5)既往有开颅手术史。(6)无法获得高质量TCD图像。
3.一般资料 选择2018年1月至2019年3月在我院神经外科重症监护中心住院治疗的68 例颅脑创伤患者,男性46例,女性22例;年龄16 ~68 岁,平均(46.17±16.87)岁;创伤至入院时间1 ~20 h,中位时间7.00(5.00,18.50)h;入院至手术时间4 ~ 36 h,中位时间13(8,28)h。致伤原因为车祸伤(51 例占75%)、跌落伤(13 例占19.12%)、坠物砸伤(4 例占5.88%)。入院时 GCS 评分 4 ~ 11 分,平均(6.59±2.45)分;单侧脑疝形成者25 例(36.76%),双侧脑疝形成6 例(8.82%),无脑疝形成37 例(54.41%);脑挫裂伤35 例(51.47%),脑实质血肿21 例(30.88%),硬膜下血肿7 例(10.29%),硬膜外血肿3 例(4.41%),蛛网膜下腔出血5 例(7.35%),脑梗死4 例(5.88%)。所有患者均行开颅血肿清除术并留置有创性颅内压监测探头,其中 51 例(75%)去除骨瓣,17 例(25%)还纳骨瓣;53 例(77.94%)颅内压探头类型为脑室型,15例(22.06%)为脑实质型。
二、研究方法
1.有创性颅内压监测 所有患者均于血肿清除术中留置有创性颅内压监测探头[脑实质型探头(REF-826631 型)或脑室型探头(REF-826632 型)],购自美国 Codman,Johnson & Johnson Professional 公司。脑实质型探头置于创伤侧或创伤严重侧脑实质内2 ~3 cm,脑室型探头常规经侧脑室额角穿刺点置入脑室内,术后颅内压监测探头留置1 周。以颅内压≥20 mm Hg 为增高,行以颅内压<20 mm Hg、脑灌注压60 ~70 mm Hg为目标的导向治疗。
2.TCD 监测 (1)脑血流监测:采用美国GE 公司生产的LOGIQ-E9 型彩色超声波诊断仪监测双侧大脑中动脉血流量,记录收缩期峰值流速(PSV)、舒张期末流速(EDV)、平均流速(Vm)和搏动指数(PI)。大脑中动脉 Vm < 30 cm/s、EDV < 20 cm/s 且PI > 1.40,诊断为脑缺血。大脑中动脉 Vm 为 120 ~200 cm/s 时,需探查颈内动脉颅外段(eICA),记录Vm,并计算离登指数(LR),LR=MCAVm/eICAVm,以鉴别脑血管充血与脑血管痉挛,大脑中动脉Vm为120 ~ 200 cm/s 并且LR ≤ 3,诊断为脑血管充血;大脑中动脉 Vm 为 120 ~ 200 cm/s 且 LR > 3 或 Vm >200 cm/s,诊断为脑血管痉挛。术后患者每日至少监测1 次脑血流量,若病情变化随时床旁监测并记录数据。(2)ONSD 测量:将 7.50 ~ 10.00 MHz 探头置于视盘后方3 mm,测量ONSD,每只眼球测量2 次,取平均值。以ONSD ≥5 mm 作为预测颅内压增高临界值。
3.统计分析方法 采用SPSS 24.0 统计软件进行数据处理与分析。呈正态分布的计量资料以均数±标准差()表示,非正态分布的计量资料以中位数和四分位数间距[M(P25,P75)]表示。颅内压与ONSD 和PI 的相关性采用Pearson 相关分析。绘制受试者工作特征曲线(ROC 曲线)并计算曲线下面积(AUC),计算 ONSD 和 PI 诊断颅内压增高(ICP ≥20 mm Hg)的灵敏度和特异度。以P≤0.05为差异具有统计学意义。
结 果
Pearson 相关分析显示,术后1 周颅内压与ONSD 呈正相关(r=0.679,P=0.000)。根据颅内压分层(≥ 20 和 < 20 mm Hg),ICP ≥ 20 mm Hg(r=0.665,P=0.000)和 < 20 mm Hg(r=0.358,P=0.006)与ONSD 均呈正相关关系;根据ONSD 分层(≥5和<5 mm),ONSD ≥ 5 mm 时与颅内压呈正相关(r=0.644,P=0.000),< 5mm 时则与颅内压无关联性(r=0.376,P=0.137)。
Pearson 相关分析显示,术后1 周颅内压与PI 呈正相关(r=0.458,P=0.000),且术后不同时期关联性有所不同:术后1 ~2 d(术后早期)二者无关联性(r=-0.055,P=0.705),术后3 ~5 d(脑水肿高峰期;r=0.508,P=0.001)和6 ~ 7 d(脑水肿逐渐消退期;r=0.645,P=0.000)二者均呈正相关。根据颅内压进一步分层,ICP ≥ 20 mm Hg(r=0.716,P=0.000)和15 ~ 20 mm Hg(r=0.705,P=0.000)时与 PI 呈正相关,ICP < 15 mm Hg 时与 PI 无关联性(r=-0.120,P=0.366);根据 PI 分层(≥ 1.20 和 < 1.20),无论 PI ≥1.20(r= 0.350,P= 0.021)或 < 1.20(r= 0.282,P=0.029)与ICP均呈正相关。
根据颅脑创伤患者颅内压、ONSD、PI 测值,假设不同临界点,获得一系列诊断灵敏度和特异度:以灵敏度为纵坐标,1-特异度为横坐标,绘制ROC曲线。该曲线下面积反映的范围即为诊断准确性,越接近 1,ONSD 和 PI 诊断 ICP ≥ 20 mm Hg(颅内压增高)的精确度越高。ONSD 诊断ICP ≥20 mm Hg的曲线下面积为 0.900(95%CI:0.831 ~ 0.969,P=0.000;图1),灵敏度为0.821、特异度0.931,该曲线下面积相对应的ONSD 临界值为5 mm。PI 诊断ICP ≥ 20 mm Hg 的 曲 线 下 面 积 为 0.729(95%CI:0.623 ~ 0.834,P=0.000;图2),灵敏度为0.483、特异度0.860,该曲线下面积对应的PI临界值为1.20。进一步绘制 ONSD ≥ 5 mm 联合 PI ≥ 1.20 诊断 ICP ≥ 20 mm Hg 的 ROC 曲 线 ,曲 线 下 面 积 0.943(95%CI:0.866 ~ 1.000,P=0.000;图3),诊断灵敏度为1.000、特异度0.857,表明ONSD ≥5 mm 联合PI ≥1.20诊断ICP ≥20 mm Hg 的敏感性、特异性和诊断准确性更高。
讨 论

图 1 ROC 曲线显示,ONSD 诊断 ICP ≥ 20 mm Hg 的曲线下面积为0.900(95%CI:0.831 ~ 0.969,P=0.000)Figure 1 ROC showed for prediction ICP ≥20 mm Hg with ONSD, the AUC value was 0.900 (95%CI: 0.831-0.969, P =0.000).

图 2 ROC 曲线显示,PI 诊断 ICP ≥ 20 mm Hg 的曲线下面积为 0.729(95%CI:0.623 ~ 0.834,P=0.000)Figure 2 ROC showed for prediction ICP ≥20 mm Hg with PI, the AUC value was 0.729 (95%CI: 0.623-0.834, P =0.000).
视神经鞘是硬脑膜在视神经管内的延续,健康成人ONSD 为2.20 ~5.00 mm。既往研究显示,颅内压增高(P=0.015)和视神经鞘增宽(P=0.035)均是重型颅脑创伤患者死亡的危险因素[7],因此ONSD理论上可以反映颅内压水平[8]。目前尚缺乏统一的ONSD 诊断颅内压增高的标准,同时缺乏不同颅内压水平下二者的相关性研究。既往研究均以ONSD 5 mm 为诊断颅内压增高(ICP ≥ 20 mm Hg)的阈值[9-11]。在本研究中,Pearson 相关分析显示,术后 1 周颅内压与ONSD 呈正相关关系(r= 0.679,P=0.000),且颅内压增高(ICP ≥20 mm Hg)时二者相关性较颅内压正常(ICP <20 mm Hg)时更加显著(r=0.665 对r=0.358);ROC 曲线显示,ONSD 诊断颅内压增高(ICP ≥20 mm Hg)的曲线下面积为0.900(95%CI:0.831 ~ 0.969,P=0.000),其所对应的临界值即为5 mm。这一结果符合颅脑创伤后的病理生理改变,颅内压越高、ONSD 越宽。Maissan 等[12]的研究显示,颅脑创伤患者气管切开后颅内压升至≥20 mm Hg时,ONSD迅速增至≥5 mm,因此ONSD的增加能够快速、准确地反映颅内压的增高变化。Rajajee 等[13]的研究结果同样支持上述结论,即颅内压增高时ONSD 迅速增加,而颅内压恢复至正常水平时其仍处于增宽水平,因此相较于颅内压的降低,ONSD 的降低具有延迟性,这可能导致根据ONSD 无创性评估颅内压时易引起过度治疗。本研究也进一步证实了ONSD 无创性评估颅内压的延迟性,ONSD ≥5 mm 时与颅内压具有较强的正相关关系(r=0.644,P=0.000),而ONSD < 5 mm 时则与颅内压无关联性(r=0.376,P=0.137);且颅内压正常(ICP <20 mm Hg)时二者相关性弱于颅内压增高(ICP ≥ 20 mm Hg)时(r=0.358 对r=0.665),提示在继发性脑损伤的演变过程中,唯有颅内压增高导致ONSD ≥5 mm时,二者的相关性才显现出来,此时再采取治疗措施可能会延误治疗时机。因此,不同颅内压水平下的ONSD 无创性评估颅内压的准确性有所差异。

图 3 ROC 曲 线 显 示 ,ONSD ≥ 5 mm 联 合 PI ≥ 1.20 诊断ICP ≥ 20 mm Hg 的曲线下面积为 0.943(95%CI:0.866 ~1.000,P=0.000)Figure 3 ROC showed for prediction ICP ≥20 mm Hg with a combination of ONSD ≥ 5 mm and PI ≥ 1.20, the AUC value was 0.943 (95%CI: 0.866-1.000, P=0.000).
在生理状况下,脑血流自动调节(CA)能力正常,颅内压增高可导致脑小血管顺应性扩张,脑血管阻力减小,从而保持脑血流相对稳定[14-15]。PI 可以反映脑血管远端阻力的变化,是评价脑小血管顺应性和弹性的重要指标,其计算公式为:PI=(PSVEDV)/Vm。当脑血流自动调节能力受损时,脑小血管失去扩张能力,颅内压增高导致脑血管阻力增加,PI 进行性升高,脑血流量减少。由此可见,当脑血流自动调节能力受损时,有创性颅内压监测与PI无创性评估颅内压具有较高的一致性[16]。但也有学者对PI与颅内压的相关性持有异议:Bellner等[17]的研究显示,PI 与颅内压呈正相关(r=0.938,P<0.001),PI诊断颅内压增高(ICP >20 mm Hg)的灵敏度为 0.89、特异度 0.92,并推算出 PI > 2.13 时 ICP >22 mm Hg、PI < 1.20 时 ICP < 12 mm Hg。Prunet等[18]认为,PI 可以反映颅内压水平,其诊断颅内压增高(≥20 mm Hg)的ROC 曲线下面积为0.901(95%CI:0.794 ~ 1.000,P< 0.01),灵敏度为 0.800、特异度0.900,其所对应的 PI 临界值为 1.35。de Riva 等[19]则认为PI 并非压力指标,不能准确反映患者颅内压水平。Behrens 等[20]的观点是:颅内压受脑灌注压、心率、脉压差(PP)、脑血管阻力、脑血管顺应性、脑血流自动调节能力等多种因素的影响,并提出计算公式:
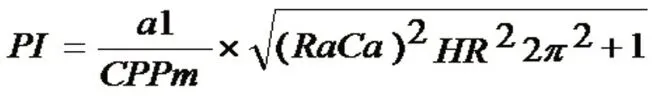
其中,a1 为收缩压与舒张压的差值,CPPm 为平均动脉压,Ra 为脑血管阻力,Ca 为脑血管顺应性,HR 为心率。本研究Pearson 相关分析显示,术后1 周颅内压与PI 具有相对较弱的正相关关系(r=0.458,P=0.000),但是随着颅内压的增高(< 15、15 ~ 20 和 ≥20 mm Hg),二者之间的相关性从无(P=0.366)到有再逐渐增强(r=0.705 对r=0.716);且术后不同时期二者相关性不同,术后1 ~2 天(术后早期)二者无关联性,术后3 ~5 天(脑水肿高峰期)和6 ~7 天(脑水肿逐渐消退期)二者均呈正相关,表明继发性脑损伤越严重、颅内压增高越明显、PI 与颅内压的相关性越强。进一步根据PI 分层,PI ≥1.20 与颅内压的相关性强于PI <1.20(r=0.350对r=0.282)。ROC曲线显示,PI 诊断颅内压增高(ICP ≥ 20 mm Hg)的曲线下面积为0.729(95%CI:0.623~0.834,P=0.000),其所对应的临界值为1.20,表明PI 增加时颅内压增高,应予以紧急干预。提示PI 可以作为颅内压增高、脑灌注压降低的动态指标,而不宜仅从颅内压角度反映其临床价值。
本研究结果还显示,ONSD ≥ 5 mm 联合 PI ≥1.20 诊断颅内压增高(ICP ≥20 mm Hg)的ROC 曲线下面积为0.943(95%CI:0.866 ~ 1.000,P=0.000),均高于ONSD 和PI 单一诊断颅高压增高的曲线下面积。因此我们认为,通过TCD 无创性评估颅内压时,ONSD 增宽联合PI 增加诊断颅内压增高的准确性更高。
TCD 监测参数可以反映颅脑创伤患者脑血流动力学和颅内压改变,当无法开展有创性颅内压监测或怀疑其准确性时,通过合理解读TCD 监测参数,同样可提供治疗依据,但是在解读参数时应了解其所表达的病理生理学意义。本研究存在的局限性:(1)为单中心回顾性研究,样本量较小。(2)颅内压监测应为连续性,而TCD 监测ONSD 和大脑中动脉PI是间断性的,且不同医师进行TCD 监测获取数据时可能存在选择偏倚。(3)一方面部分患者术后保留骨瓣,超声穿透颅骨时发生衰减,相对于去除骨瓣的患者,PI 存在差异;另一方面术后早期眼睑肿胀严重,术后晚期眼睑肿胀消退,使得ONSD 亦存在差异;均可能对研究结论产生一定的影响。今后尚待前瞻性大样本临床研究进一步证实TCD 无创性评估颅内压的可靠性。
利益冲突无
