新情境下电极反应方程式的书写
2020-07-20陕西文政民
◇ 陕西 文政民
电化学知识是中学化学理论的重要组成部分,是历年来高考命题的重点,几乎每年在各个省份的化学试题中都有所涉及.近几年,高考题都侧重于用新型化学电源来考查学生运用电化学理论、氧化还原反应、元素化合物等相关理论知识解决实际问题的能力.
1 理论依据
书写电极反应式要遵循元素守恒和电荷守恒定律,因此,只要能在给定的新情境下判断出电极参与氧化或还原反应的反应物和产物,再根据价态变化判断并写出得失电子数,最后根据溶液的酸碱环境、氢氧元素守恒、电荷守恒,在电极反应方程式的两边分别补上H+、OH-、H2O 即可得到某一电极的电极反应式.
2 书写原则及步骤
书写电极反应式时,无论是原电池还是电解池均可按照以下四步直接写出.
1)写:依据信息及物质所含元素价态变化写出氧化剂(还原剂)及还原产物.
2)标:依据物质所含原子数及化合价升降数标出氧化剂(还原剂)得到(或失去)的电子数.
3)配:依据反应介质酸碱环境及电荷守恒配平离子.
4)补:依据质量守恒及反应体系补充物质.
3 典型示例
3.1 新型化学电源电极反应式的书写
例1某科研小组用电化学方法使NH4HS变废为宝(硫酸铵化肥),设计方案如图1所示,写出该电池负极的电极反应式.
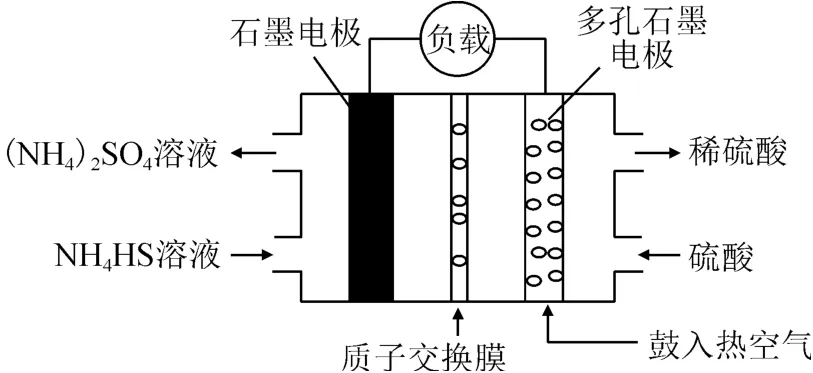
图1
解析
该题以新型化学电源考查原电池电极反应式的书写,根据题中信息,四步书写模式如下.
1)写:原电池负极发生氧化反应,物质所含元素化合价升高,据装置写出:
2)标:根据硫元素化合价变化标出失去的电子数,HS-和中硫元素的化合价分别为-2和+6,故失去电子数为8,即
3)配:题中信息出现有质子交换膜,间接说明了电解质溶液为酸性环境,故可在方程式右边补上H+使左右两边电荷相等,即
4)补:根据元素守恒定律,需要补上水,并将箭头变为等号,即
3.2 燃料电池电极反应式的书写
例2如图2所示,装置Ⅰ为甲烷燃料电池(电解质溶液为KOH),通过装置Ⅱ实现在铁棒上镀铜.
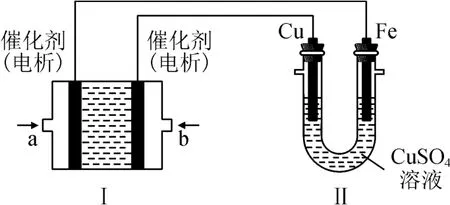
图2
解析
该题考查燃料电池电极反应式的书写,根据题中“通过装置Ⅱ实现在铁棒上镀铜”可知,Fe电极为电解池的阴极,则a为燃料电池负极,通入CH4,b为正极,通入O2.a 极电极反应式分步书写如下.
1)写:负极CH4发生氧化反应,因为是碱性介质,所以氧化产物为,即.
2)标:根据化合价标出失去的电子数,CH4和中碳元素化合价分别为-4和+4,故失去电子数为8,即
3)配:电解质溶液为KOH 溶液,说明电解质溶液为碱性环境,故补上OH-使左右两边电荷数相等,即
4)补:根据元素守恒定律,需要补上水,并将箭头变为等号,即
4 结语
本文通过对电池电极反应式的书写方法进行程序化合理编排,建立和形成了一种行之有效的书写方法,对于学生正确、快速地解题具有一定的指导意义,同时,也为本模块的教学实践提供了一种新的思路.
