以橡子为碳源制备的空心磁性碳纳米球及其吸附性能
2020-07-20武世奎
曹 群 武世奎*,, 李 彦
(1内蒙古医科大学药学院,呼和浩特 010110)
(2北京大学化学与分子工程学院,北京 100871)
0 引 言
纳米材料具有独特的电子结构和磁学、光学、热力学性质及机械性能,在许多领域表现优异[1]。空心纳米球具有比表面积大、密度小、中空等性质[2],其在催化剂[3]、电极材料[4]以及空气净化[5]等领域有着广泛应用。碳基空心材料原料来源广泛、价格低廉[6],其具有化学稳定性好[7-9]、导电性高[10-13]、比表面积大[14-16]、生物相容性好[17]等优点。因此碳基空心纳米球在医药等领域有着潜在应用价值[18-20]。
生物质材料的主要成分是纤维素、半纤维素和木质素,且其取材便利,不需要复杂的前处理,是生产微孔碳的优质原料[21]。同时,生物质原料中含有的杂原子(如N、S等)可能在制备的空心纳米碳球中得以保留,有利于提高材料的性能[22]。目前,以生物质材料为碳源制备多孔碳材料已成为纳米材料研究领域的热点,但制备出具有较高分散性空心碳的纳米球的报道较少。橡子由于其自身缺陷,如淀粉支链度高难以消化吸收,且含有较多的单宁不易除净,限制了其在食品、饮料工业上的利用。利用橡子作为碳源,制备空心纳米球可以增加其利用率。本文报道了一种以生物质材料橡子仁为碳源,制备磁性空心碳纳米球(MHCNS)的方法。通过调节氢氧化钾和醋酸镍添加量和比例实现对MHCNS最终形貌和粒径的控制,经过后处理可以得到具有较高比表面积的MHCNS-2。该工作将为碳基空心纳米球的可控合成和应用提供新的途径。该法制备的MHCNS-2有较高的吸附能力,有望在废水处理和载药领域得到应用。
1 实验部分
1.1 主要材料与试剂
橡子仁采收于内蒙古赤峰市。其它试剂有Ni(CH3COO)2·4H2O(分析纯,国药集团化学试剂有限公司)、KOH(分析纯,天津市化学试剂三厂)、HCl(优级纯,天津市天力士化学试剂有限公司)、NH3·H2O(分析纯,天津市津东天正精细化学试剂厂)、HNO3(优级纯,天津市化学试剂厂)、亚甲基蓝(MB)(分析纯,重庆茂业化学试剂有限公司)。
1.2 MHCNS的制备方法
将2 g橡子仁粉分散于20 mL蒸馏水,在电磁搅拌下缓慢加入15 mL含有2 g Ni(CH3COO)2的水溶液,搅拌1h后,缓慢滴加10 mL含有0.8 g KOH的水溶液,继续搅拌30 min。混合液置于80℃水浴上加热除去部分水分,糊状物转移至刚玉坩埚中。坩埚置于密闭反应釜中,用箱式电阻炉加热到900℃煅烧2 h,得到黑色固体。将产物研碎后用蒸馏水洗涤 至 中 性,再用1 mol·L−1HCl浸泡过夜 ,除去MHCNS外部的可溶性杂质,用蒸馏水洗涤至中性,得到产物MHCNS-1。向产物MHCNS-1中加入1 mL浓HNO3和19 mL浓NH3·H2O,混合均匀,在聚四氟乙烯内衬的反应釜中以170℃加热24 h,去除MHCNS-1内部的大部分Ni(OH)2和Ni,产物用蒸馏水洗涤至中性,干燥即得产物MHCNS-2。
1.3 表 征
使用粉末X射线衍射(XRD)对样品的结构进行表征,仪器为Rigaku D/MAX 2400,CuKα辐射,λ=0.154 06 nm,管电压40 kV,管电流250 mA,扫描速度 5(°)·min−1,扫描范围为 5°~90°)。通过扫描电镜(SEM,S4800,工作电压10 kV)和透射电镜(TEM,JEM-2100,工作电压100 kV)对样品的尺寸、形貌和显微结构进行表征。在库尔特SA 3100表面积分析仪上获得了77 K的N2吸附−脱附等温线。在300 K下,使用振动样品磁强计(VSM,美国Quantum Design)测定样品的磁性。
1.4 染料吸附试验
在室温下,将浓度分别为35、60、75和100 mg·L−1的MB溶液500 mL分别与10 mg MHCNS-2混合后,在100 r·min−1条件下恒温振荡,测定吸附前后染料浓度,确定染料去除率。每隔一段时间量取3 mL混合液过滤,利用紫外分光光度计测出滤液在664 nm处的吸光度,然后将测出的吸光度代入MB溶液的标准曲线,测定残余染料浓度,直至达到吸附平衡。吸附量(qe,mg·g−1)可由质量平衡方程(1)计算:

其中c0为吸附前染料溶液的初始浓度(mg·L−1),c为MB溶液剩余质量浓度(mg·L−1),V为染料的取用体积(mL),m为MHCNS-2的投加量(g)。
1.5 MHCNS-2的载药-释药性能
1.5.1 标准曲线
以0.4%的氢氧化钠溶液作溶剂,配制一定浓度的布洛芬溶液,经全波长扫描测定布洛芬的吸光度,以确定最大吸收波长。布洛芬在265与273 nm的波长处有最大吸收,选取265 nm为测量波长。分别配制0.1、0.2、0.3、0.4、0.5 mg·mL−1的布洛芬溶液,测定其吸光度值,以浓度(c)为横坐标,吸光度(A)为纵坐标,作出A对c的关系图,并对其进行线性拟合,得到布洛芬的标准曲线图。
1.5.2 MHCNS-2的载药动力学吸附测试
准确称量10 mg MHCNS-2于棕色瓶中,加入15 mL浓度为2 mg·mL−1的布洛芬溶液,在恒温振荡器中以 25℃、180 r·min−1的条件进行载药实验。每隔一定时间,取一定量的上清液经0.45µm的滤头过滤,采用紫外−可见分光光度计(UV-Vis)测试布洛芬的吸光度,根据标准曲线换算布洛芬的浓度,再根据式(2)计算出不同时间的载药量Qt(mg·g−1)。

其中:m1表示溶液中布洛芬的含量(mg);ct表示t时间的布洛芬浓度(mg·mL−1);Vt表示t时间反应溶液的体积(mL);m2表示加入的MHCNS-2的质量(mg)。
1.5.3 MHCNS-2的释药性能测试
将20 mg载有布洛芬26.4 mg的MHCNS-2分散在5 mL的磷酸缓冲溶液(PBS,pH=7.4)中,再置于截留量为3400D的透析袋中,并将透析袋置于15 mL的PBS中。在恒温振荡器中以37 ℃、160 r·min−1的条件进行避光载药实验。每隔一定时间,取1 mL的上清液经0.45µm的滤头过滤,同时取1 mL的PBS补充于烧杯中,采用紫外−可见分光光度计(UV-Vis)测试布洛芬的吸光度,根据标准曲线换算布洛芬的浓度,再根据式(3)计算出不同时间的累积释药率。

其中:E表示累积释药率;V0为溶液的总体积(20 mL);V1为每次取样的体积(1 mL);ci表示第i次取样时,溶液中布洛芬的质量浓度(mg·mL−1);n为取样次数;M表示加入的装有布洛芬的MHCNS-2的总质量(mg);X表示空心碳纳米球对布洛芬的载药率(%)。
2 结果与讨论
2.1 MHCNS样品的表征
MHCNS样品的XRD图如图1所示。由XRD可知,两样品衍射峰的位置分别与C、Ni、Ni(OH)2的标准图(PDF No.26-1076,04-0850,14-0117)一致,说明样品中含有C、Ni与Ni(OH)2。经HCl浸泡MHCNS-1样品Ni(OH)2和Ni的衍射峰较强,说明颗粒内部仍有大量Ni(OH)2和Ni存在。由MHCNS-2的XRD图中衍射峰高度可知,用HNO3与NH3·H2O处理后样品中C的比例增加,Ni与Ni(OH)2的比例下降。说明MHCNS-1样品经HNO3与NH3·H2O处理后可通过HNO3的氧化作用和NH3·H2O的配位反应除去颗粒内部残留的大部分Ni(OH)2和Ni,得到MHCNS-2。

图1 MHCNS的XRD图Fig.1 XRD patterns of MHCNS
由MHCNS-2样品的SEM图(图2a)可知,产物为粒径均匀、分散性良好的球体,直径为20~40 nm。插图为样品的粒径分布图,由图可知,样品直径主要分布在20~40 nm之间,平均粒径为30 nm。由MHCNS-2样品的SEM图(图2b)可以观察到其表面粗糙并有一些球形凸起。由TEM图(图2c)可知,MHCNS-2样品具有空心结构,直径20~40 nm,壁厚3~5 nm。其HRTEM图(图2d)显示,MHCNS-2外壁的晶格条纹0.34 nm对应C的(002)晶面,内部颗粒的晶格条纹分别为0.20和0.27 nm,对应Ni(111)和β-Ni(OH)2(100)。该结果表明,MHCNS-2样品为包含了一些Ni和β-Ni(OH)2的空心碳壳结构。
2.2 影响MHCNS形貌的因素
通过分析产物的FESEM,发现煅烧温度及Ni(CH3COO)2和KOH投料比是影响产物形貌的重要因素。我们分析了700、800、900及1 000℃下不同投料比得到的产物形貌。结果显示:700℃时,产物形貌不均匀,2种投料比(3∶1和5∶2)下均产生了多孔碳结构,未见球状碳纳米结构产生(图3a、b)。这可能是因为温度较低时Ni对碳元素的吸附−脱附作用较弱[23]。800℃时,虽然也能形成球状碳纳米结构(图3c、d),但形貌并不均匀。而900℃时,投料比为3∶1时,如图3e所示产物为多孔碳结构;投料比为5∶2时,产物为均匀的球状纳米结构(图3f)。这一结果表明KOH和Ni2+共同影响了橡子煅烧产物的形貌。1 000℃时,产物的形貌不均匀,可能是高温下碳纳米球结构被破坏(图3g、h)。

图2 MHCNS的(a、b)SEM图、粒径分布图(a的插图)、(c)TEM图和(d)HRTEM图Fig.2 (a,b)SEMimage,particle size distribution(inset in a),(c)TEM image and(d)HRTEM image of MHCNS

图3 温度和投料比对产物形貌的影响Fig.3 Effect of temperature and mass ratio of Ni(CH3COO)2to KOH on the morphology of product
KOH在高比表面积碳材料的制备过程起到了造孔剂的作用[24]。在橡子仁粉(图4a)中只添加KOH,仅能得到较大的块状结构(图4b)。考虑到Ni(CH3COO)2和KOH的配合是形成均匀球状碳纳米结构的关键,除了投料比,Ni(CH3COO)2和KOH用量对产物形貌也会有一定影响。如上所述,Ni(CH3COO)2和KOH添加量分别为2和0.8 g时(投料比5∶2),得到分散性较好的MHCNS(图3f)。维持Ni(CH3COO)2和KOH投料比,减少用量时(1和0.45 g),产物形成均匀的多孔结构(图4c)。进一步降低Ni(CH3COO)2和KOH用量(0.5和0.225 g),产物会形成不均匀的棒状碳纳米结构(图4d)。综上所述,当Ni(CH3COO)2与KOH的比例为5∶2,添加量为2和0.8 g,且煅烧温度为900℃时可获得均匀的MHCNS。

图4 (a)橡子仁粉的形貌;900℃时Ni(CH3COO)2和KOH用量对产物形貌的影响:(b)只添加KOH;mNi(Ac)∶2mKOH=5∶2,添加量分别为(c)1与0.45 g,(d)0.5与0.225 g时,产物的形貌Fig.4 (a)Morphology of acorn powder;Effect of the addition amount of Ni(CH3COO)2and KOH on the morphology of product:(b)only KOH added;mNi(Ac)∶2mKOH=5∶2,wherein the addition amount is(c)1 and 0.45 g,(d)0.5 and 0.225 g,respectively
2.3 MHCNS的形成机理

图5 MHCNS的形成机理Fig.5 Formation mechanism of MHCNS
图5为MHCNS的生长机理图。首先,在搅拌过程中Ni(CH3COO)2中的Ni2+均匀地穿插在橡子仁粉末中。加入KOH后,继续搅拌,OH−与Ni2+在橡子仁粉中反应形成Ni(OH)2。煅烧的过程中,插在橡子仁粉中的氢氧化镍纳米球被还原为金属镍纳米球。镍纳米球在高温下与碳原子形成碳化物,并在降温的过程中析出碳原子,在金属镍纳米球表面形成碳壳。控制煅烧温度与投料比可得到粒径均匀的MHCNS,此时所得到的产物表面与内部皆存在大量Ni(OH)2和金属Ni。用HCl可除去表面的Ni(OH)2与Ni,再用HNO3与NH3·H2O的混合溶液,在聚四氟乙烯内衬的反应釜中加热去除内部的Ni(OH)2与Ni。产物大部分为中空的碳纳米球,包含有少量Ni(OH)2与Ni,形成粒径均匀的磁性空心碳纳米球。
2.4 MHCNS样品的BET比表面与磁性
图6为样品MHCNS-2的N2吸附−脱附测试结果,插图为通过BJH法得到的孔径分布图。孔径分布图中,在20 nm处有强度较弱的宽峰,可能对应MHCNS-2的内径;在1~5 nm处有尖锐峰,可能对应球壁上存在的小孔。BET法计算的结果表明,MHCNS-2 具有较大的比表面积(642 m2·g−1)。图 6b显示了在300 K下测量的MHCNS-1与MHCNS-2的磁滞回线,插图为磁滞回线的局部放大图。结果显示,样品MHCNS-1的磁饱和磁化强度Ms为15.02 emu·g−1,矫顽力Hc为 83.66 Oe;样品 MHCNS-2 的磁饱和磁化强度Ms为 0.73 emu·g−1,矫顽力Hc为 39.26 Oe。由磁饱和强度的变化可知,MHCNS-1样品经过处理除去颗粒内部残留的Ni(OH)2和Ni,得到MHCNS-2。

图6 (a)MHCNS-2的N2吸附−脱附分析和BJH孔径分布(插图);(b)MHCNS的磁滞回线Fig.6 (a)N2adsorption-desorption analysis and BJH pore size distribution(Inset)of MHCNS-2;(b)Hysteresis loop of MHCNS
2.5 MHCNS样品的染料吸附试验
在37℃下,MHCNS-2样品在不同时间,对不同浓度的MB溶液进行吸附实验,得到不同浓度MB溶液吸附时间与吸附量曲线图,如图7所示。由图7可知,在初始阶段,MB溶液初始浓度较大,MHCNS-2吸附染料速率较快;随后吸附速率逐渐减慢,3 h达到吸附平衡。同时,随着MB溶液初始浓度的增加,平衡吸附量增加,当MB溶液浓度为100 mg·L−1时,吸附量可以达到185 mg·g−1。图7中的插图显示了用MHCNS-2除去染料溶液前后的对比照片,说明样品具有较强的磁性,且可用磁铁实现分离。
吸附动力学一级模型和二级模型分别用一级动力学方程(4)和二级动力学方程(5)[25-26]描述为:

式中,k1为一级反应的速率常数(min−1);k2为二级反应的速率常数(g·mg−1·min−1);qt为t时刻的吸附量(mg·g−1),qe为平衡时刻的最大吸附量(mg·g−1)。
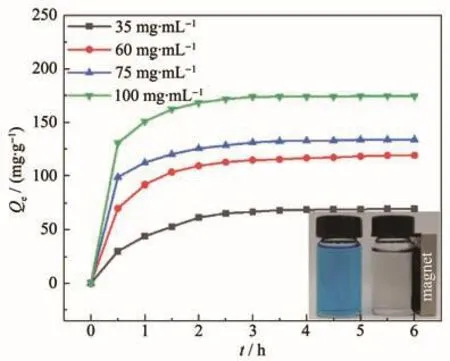
图7 MHCNS-2对不同浓度MB溶液的吸附时间和吸附量Fig.7 Adsorption time and adsorption amount of MHCNS-2 to different concentrations of MB solution
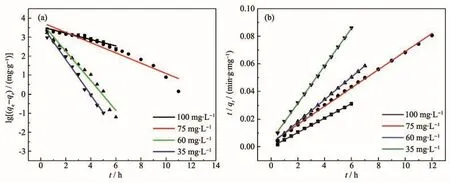
图8 MHCNS-2对MB溶液吸附的(a)准一级动力学模型和(b)准二级动力学模型的线性拟合Fig.8 (a)Linear fitting of pseudo-first-order kinetics model and(b)pseudo-second-order kinetics model for MHCNS-2 adsorption to MB solution

表1 MHCNS-2对MB溶液吸附的准一级动力学与准二级动力学参数Table 1 Pseudo-first-order kinetics and pseudo-second-order kinetic parameters for MHCNS-2 adsorption to MB solution
按照准一级动力学方程,以 ln(qe−qt)对t作图(图 8a),对数据进行线性拟合,由直线斜率可以得到MHCNS-2对不同浓度MB溶液吸附的一级动力学参数;按照准二级动力学方程,以t/qt对t作图(图8b),对数据进行线性拟合,得到MHCNS-2对不同浓度MB溶液吸附的二级动力学参数。所得参数均列于表1中。由表1可知,准一级动力学拟合数据中R2>0.80;准二级动力学拟合数据中R2>0.99。因此,MHCNS-2对MB溶液的吸附过程与准二级动力学模型更相符。
2.6 MHCNS-2的载药-释药试验
在25℃下MHCNS-2对布洛芬的动力学吸附曲线如图9a所示。在吸附开始时,MHCNS-2对布洛芬的吸附量随着时间的增大而快速增大,随后吸附量增长逐渐缓慢直至趋于稳定,在12 h基本达到平衡,载药率为44%。
在37℃下,载药MHCNS-2的释药曲线如图9b所示。随着时间的变化,布洛芬缓慢释放,在12 h达到平衡,累积释药率约为70%。

图9 MHCNS-2的(a)载药曲线与(b)释药曲线Fig.9 (a)Drug loading and(b)drug release curve of MHCNS-2
3 结 论
在密闭容器中,用简单的高温煅烧法制备了球形的MHCNS,经后处理得到的样品MHCNS-2结构均匀、分散性好。Ni(CH3COO)2与KOH的添加比例以及煅烧温度对于MHCNS的形貌有着很大影响。该样品可用于废水中有机污染物的去除,并在作为药物载体方面具有一定的应用前景。
