磷石膏矿化CO2反应体系调控碳酸钙晶型的过程参数研究
2020-07-16谢安帝朱家骅彭玉凤
谢安帝,李 季,朱家骅,葛 敬,吴 林,彭玉凤,卢 蔚
(四川大学 化学工程学院,四川 成都 610065)
湿法磷酸工业产生大量固废磷石膏,严重污染环境,磷石膏的资源化利用亟待解决[1]。CO2的过度排放引发温室效应,对全球气候和环境的影响愈发明显[2]。利用磷石膏矿化CO2,生产高附加值(NH4)2SO4和CaCO3,以废治废,是实现CO2减排和磷石膏资源化利用的绿色低碳技术路线[3]。该过程的主要反应发生在CaSO4· 2H2O-NH3-CO2-H2O 三相反应体系中:

产物CaCO3有方解石、文石、球霰石3 种可能的结晶形态,其热力学稳定性依次降低[4]。目前产物CaCO3呈方解石、球霰石等混合晶型,仅可作为水泥原料,经济效益较低。球霰石型碳酸钙通常为球形多孔颗粒,比表面积大,粒径分布均匀,所以常用来改善产品物理性能和填充性能[5];同时,其良好的生物相容性和可降解性,在药物控释载体、仿生材料制备等生物医学领域显示出巨大的发展潜力[6-7]。如能实现球霰石型碳酸钙的定向结晶,可以大大提升产物CaCO3的经济附加值。
目前,球霰石型碳酸钙的制备方法主要有仿生矿化法[8]、单分子膜法[9]、复分解法[10]、超声分散法[11]等。但这些制备方法过程较为复杂,实验条件要求较高,且产率较低,工业应用成本高,难度大。对于磷石膏矿化CO2体系,薛潇[12]等通过添加不同浓度的乙二胺(EDA),成功合成了球霰石型碳酸钙。SONG X F[13]等以脱硫石膏矿化CO2为基础,向体系中加入聚丙烯酸(PAA),控制CaCO3晶型为方解石。虽然体系产物晶型得到了控制,但添加剂的使用,增加了成本和后续分离难度,不利于工程化应用。在类似体系的研究中,CaCO3的晶型与形貌会受反应过程参数影响,如:温度、pH 值、压力、溶液饱和度等[14-17]。如果利用磷石膏矿化CO2反应体系自身特点,实现产物晶型调控,将有工程实际应用价值。
研究磷石膏矿化CO2三相反应体系的温度、氨浓度、CO2流量等过程参数对碳酸钙晶型的影响,为不外加添加剂的前提下直接制备纯净球霰石型碳酸钙提供基础数据和实验依据。
1 实验材料和方法
1.1 实验试剂与仪器
试剂:二水硫酸钙、氨水、二氧化碳、无水乙醇、去离子水。
仪器:电热恒温水浴锅(SINO TECH, XOSC-15D);悬臂式搅拌器(IKA® EUROSTAR 20 digital);蠕动泵(Kamoer, KCP-C);pH 计(Rex,PHSJ-4F);pH 电极(Rex, E-301-D);电子天平(SHANGPING, FA1004N); 电 热 恒 温 干 燥 箱(BOXUN, GZX- 9146MBE); X 射 线 衍 射 仪(SHIMADZU,XRD-6000);扫描电子显微镜(JEOL,JSM-6360LV);可见分光光度计(YUANXI,723N)。
1.2 样品制备与表征

图1 实验装置
实验装置见图1。在原料罐中配制w(CaSO4·2H2O)为1%,w(NH3)分别为2%、4%、6%、8%的原料。将容积为1 L 的连续反应容器置于超级恒温水浴中。循环水温度设置为15 ~35 ℃,设置搅拌转速500 r/min,调节CO2流量100 ~350 mL/min。以停留时间60 min 调节浆液体积流量为16.66 mL/min。反应稳定后取样,利用真空泵过滤得到产物碳酸钙,经去离子水和无水乙醇洗涤后,放入60 ℃恒温干燥箱中干燥2 h,然后于干燥器中保存。
采用Malvern 型激光粒度分析仪分析样品粒度。采用扫描电子显微镜(SEM)观察样品的形貌与结构。采用D/Max2500型转靶X射线多晶衍射仪(XRD)分析样品的物相晶型。采用可见分光光度计测定反应液中硫酸根含量。
2 结果与讨论
2.1 氨浓度对产物碳酸钙晶型的影响
在CaSO4· 2H2O-NH3-CO2-H2O 三相反应体系下,改变氨浓度会生成不同形貌和结构的碳酸钙晶体,见图2。由图2可知,当w(NH3)为2%时,产物主要是立方体型小颗粒的团聚物,说明产物主要为方解石型碳酸钙;当w(NH3)为4%时,立方体型颗粒群大量消失,晶体呈球状团聚物,晶体表面粗糙并且伴随着立方体型颗粒;当w(NH3)为6%时,表面立方体型颗粒进一步减少,表面趋于平整;当w(NH3)升高至8%时,晶体完全表现为球状颗粒的团聚物,颗粒表面平整,说明产物主要为球霰石型碳酸钙。

图2 不同氨浓度下碳酸钙结晶SEM图
产物碳酸钙的XRD谱图如图3所示。将样品的谱图与标准谱图进行比对,发现样品谱图和标准谱图的峰一一对应,没有其他的衍射峰,说明样品中只含有方解石和球霰石,纯度较高。球霰石的(110)晶面对应的衍射角2θ=24.90°,方解石的(104)晶面对应的衍射角2θ=29.40°。

图3 不同氨浓度下碳酸钙结晶XRD图
晶体中球霰石和方解石的质量分数可以根据XRD数据计算得到[18]。通过计算得到对应条件下球霰石和方解石的质量分数如表1所示。

表1 不同氨浓度下碳酸钙产物晶型特征
由表1可知,当CO2流量为250 mL/min、温度为25 ℃时,若w(NH3)大于4%,球霰石的质量分数均大于90%。由此可得出在CaSO4·2H2O-NH3-CO2-H2O三相反应体系下,氨浓度会影响产物碳酸钙的晶型,且随着氨浓度的增加,球霰石的含量增加。
2.2 温度对产物碳酸钙晶型的影响
在CaSO4· 2H2O-NH3-CO2-H2O 三相反应体系下,不同的温度也会诱导形成不同形貌和结构的碳酸钙晶体,通过计算得到对应条件下球霰石和方解石的质量分数如表2所示。

表2 不同温度下所得碳酸钙产物晶型特征
由表2 可知,当w(NH3)为6%、CO2流量为250 mL/min、温度为15 ℃时,产物碳酸钙中球霰石占比超过97%;当温度升至25 ℃时,球霰石含量略微减少,仍超过95%;但当温度为30 ℃时,球霰石质量分数迅速减少,小于40%;当温度升至35 ℃,球霰石质量分数小于5%,方解石为产物碳酸钙的主要晶型。
2.3 CO2流量对产物碳酸钙晶型的影响
在CaSO4· 2H2O-NH3-CO2-H2O 溶解-结晶耦合反应体系下,不同的CO2流量也会诱导形成不同形貌和结构的碳酸钙晶体,其中球霰石和方解石的质量分数如表3 所示。

表3 不同CO2流量下所得碳酸钙产物晶型特征
由表3可知,当w(NH3)为4%、温度为25 ℃、CO2流量为100 mL/min 时,产物中没有球霰石,为单纯的方解石;当CO2流量为150 mL/min 时,球霰石开始出现,但占比小于30%;当CO2流量增大至250 mL/min 时,球霰石占比接近95%;当CO2流量继续增大至350 mL/min 时,球霰石占比略有下降,但仍超过90%,可能是因为当CO2流量大于250 mL/min时,CO2的吸收率降低[19]。
2.4 最佳实验条件
在温度为25 ℃、w(NH3)为8%、CO2流量为250 mL/min时成功制备出球霰石占比达到99%、表面平整的球形微孔球霰石型碳酸钙,如图4 所示。表征结果表明这种球霰石颗粒是由尺寸更小的球霰石颗粒聚集而成,粒径在5 μm左右。
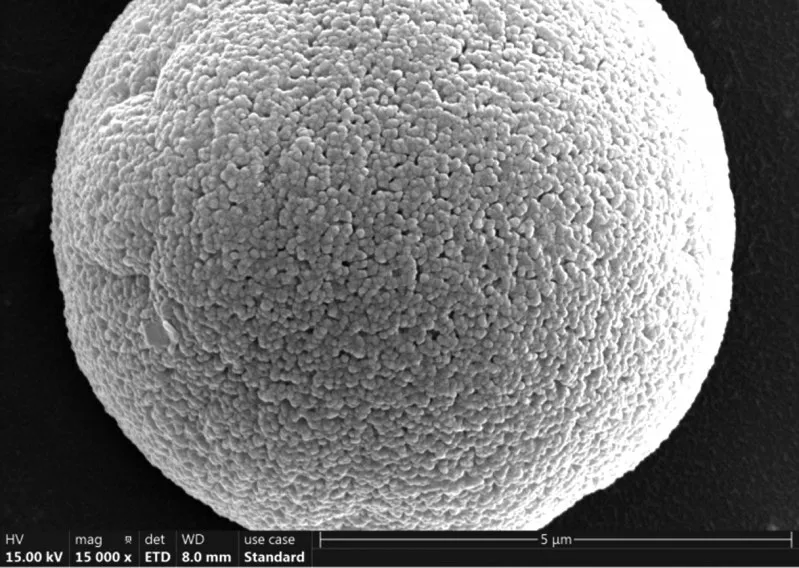
图4 温度25 ℃、w(NH3)8%、CO2流量为250 mL/min时制备的碳酸钙
3 结论
在CaSO4· 2H2O-NH3-CO2-H2O 三相体系中,研究体系的温度、CO2流量、氨浓度等反应参数对CaCO3结晶形貌的影响规律。当温度大于30 ℃、CO2
流量小于150 mL/min 或w(NH3)低于2%时,主要产物为方解石型碳酸钙。在温度为25 ℃、w(NH3)为8%、CO2流量为250 mL/min 时,成功制备纯度99%的球形微孔球霰石型碳酸钙,为磷石膏矿化CO2反应体系直接制备纯净球霰石提供了基础数据和实验依据,证实了磷石膏矿化CO2反应体系直接制备纯净球霰石的可行性。
