基质辅助激光解析质谱成像可视化分析三七皂苷空间分布
2020-07-14刘芳赵瀚森孙公伟宋哲徐富建马明英张四纯
刘芳 赵瀚森 孙公伟 宋哲 徐富建 马明英 张四纯
摘要根据2,5二羟基苯甲酸(DHB)、 α氰基4羟基肉桂酸(CHCA)、石墨烯(GR)、氧化石墨烯(GO)和碳纳米管(CNT)5种基质混合人参皂苷Rg1、人参皂苷Rb1以及三七皂苷R1 3种标准品得到的质谱信号,选取DHB为基质。将20 μm厚度的三七根茎冷冻切片真空干燥40 min后,在循环60次、喷雾强度30%、喷雾时间1 s、孵育时间40 s、干燥时间60 s的条件下,将DHB均匀覆盖于切面。质谱数据采集质量范围为m/z 0~1500 Da,使用PEG600进行质荷比校准,以1000 Hz频率的正离子反射模式进行基质辅助激光解吸质谱成像(MALDIMSI),观察到10种皂苷在三七根茎木栓层、韧皮部、木质部以及髓部的3种空间分布情况,同时对质谱数据进行t分布领域嵌入算法分析(tSNE),实现了2年生和3年生三七根茎的区分。本研究为三七根茎组织中代谢物的表征提供了原位、可视化的方法,也为三七根茎的特异性提取提供了有价值的信息。
关键词基质辅助激光解吸电离; 质谱成像; 三七根茎; 皂苷
1引 言
三七(Panax notoginseng (Burk.) F. H. Chen)是五加科人参属中的一种药食同源植物[1,2],具有活血化瘀、止血、消肿止痛的功效。研究发现,三七还具有抗肿瘤、提高机体免疫力和防治心脑血管疾病等药理作用[3]。三七的主要活性成分是一系列三萜类皂苷。目前,从三七中已分离得到七十多种皂苷,均为达玛烷型四环三萜类化合物,按结构可分为原人参二醇型(Protopanaxadiol,PPD)和原人参三醇型(Protopanaxatriol, PPT)[4]。
目前,市场上常见的三七为2年生和3年生两种。因产地、年限及部位的不同,皂苷种类及含量也呈现出差异性。不同产地总皂苷和单体皂苷的含量存在显著差异[5~7],三七皂苷含量与生长年限之间有明显的相关性[8,9]。沙孟晨等[10]对三七植株不同部位的5种皂苷进行了测定,发现不同部位的化学成分存在差异,根茎中5种皂苷的含量最高。
对三七的研究常采用色谱质谱联用的方法[11,12],但该方法无法给出各种成分在三七植株分布的信息。基质辅助激光解吸质谱成像(Matrixassisted laser desorption/ionization mass spectrometry imaging, MALDIMSI)是一种分子可视化技术,测定时,分析物从样品表面原位离子化,借助质谱的化学特异性,在一个实验中可同时获取多种分析物的离子图像,直接呈现其分子结构和空间分布信息,非常适用于复杂体系的样品分布分析[13,14]。MALDIMSI提供的大量信息,也为研究者从多角度解决复杂的生物系统问题提供了可能性。研究人员利用MALDIMSI对芍药根[15]、甘草[16]、银杏叶[[17,18]、人参[19]等药用植物中代谢产物的分布进行了研究,并结合分布情况,对植物防御和生物合成途径进行了探讨。本研究在比较不同基质的基础上,选择DHB作为基质,采用手指回温的方式对整株三七中皂苷含量最高的新鲜根茎进行冷冻切片,利用MALDIMSI技术获得了皂苷的空间分布信息,为特异性提取及代谢物研究提供了有价值的信息。
2实验部分
2.1仪器与试剂
UltrafleXtreme基质辅助激光解吸飞行时间质谱(德国Bruker Daltonics公司),配备Nd:YAG激光器(波长为355 nm),FlexAnalysis 3.4和FlexImaging 3.0软件;自动基质喷雾仪ImagePrep(德国Bruker Daltonics公司);CM1950冷冻切片机(德国Leica Microsystems公司);AL204电子天平(梅特勒托利多仪器有限公司);DS2510DTH超声波清洗器(上海生析超声仪器有限公司);MXS旋涡混匀仪(美国Scilogex公司);超纯水系统(Millipore公司)。
2,5二羟基苯甲酸(DHB)、α氰基4羟基肉桂酸(CHCA)、三氟乙酸(TFA)、多聚L赖氨酸(Sigma公司);乙醇(天津市永大化学试剂有限公司);乙腈(赛默飞世尔科技中国有限公司);冷冻包埋剂OCT (Sakura公司);人参皂苷Rg1、人參皂苷Rb1、三七皂苷R1(上海源叶生物科技有限公司);石墨烯(GR)、氧化石墨烯(GO)和碳纳米管(CNT)购于苏州碳丰石墨烯科技有限公司。三七采挖于云南省文山州砚山县三七种植基地。
2.2标准溶液和基质的配制
用乙腈水(1∶1,V/V)及0.1% TFA混合溶液将人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1标准品均配制成2 mg/mL的溶液,DHB和CHCA配制成30 mg/mL的溶液,4℃保存。GR、GO及CNT均各取2 mg悬浮于1 mL乙醇中,超声处理3 min后使用[20]。
2.3样品的制备
将清洗干净后的新鲜三七根状组织于-80℃储存,备用。冷冻切片时,使用OCT作为粘合剂,将三七固定于冷冻切片机的样品架上,在20℃下,采用手指回温的方式获取组织切片。组织切片厚度<20 μm时,三七组织结构容易断裂或出现空洞;厚度≥20 μm的切片组织结构完整,厚薄均匀。考虑到组织切片越薄,图谱质量越好,故选取样品的切片厚度为20 μm。切片热融紧贴于用0.1%(w/V)多聚L赖氨酸水溶液处理过的导电玻璃上[21],随后将样品切片真空干燥40 min。用ImagePrep将基质均匀的覆盖于样品切片上。ImagePrep的仪器参数为:循环60次,喷雾强度30%,喷雾时间1 s,孵育时间40 s,干燥时间60 s。
2.4质谱成像(MALDIMSI)和数据处理
质谱成像采用UltrafleXtreme基质辅助激光解吸飞行时间质谱仪,以1000 Hz频率的正离子反射模式获得数据。仪器扫描步长为200 μm,激光能量强度为40%,激光设定数据采集的质量范围为m/z 0~1500, 使用PEG600进行质荷比校准。
获得的质谱数据使用FlexAnalysis 3.4进行平滑和基线校正处理;成像结果利用FlexImaging 3.0软件对获得的质谱进行总离子流归一化(TIC)处理,随后利用t分布领域嵌入算法(tSNE)對质谱数据进行分析。
3结果与讨论
3.1基质种类的选择
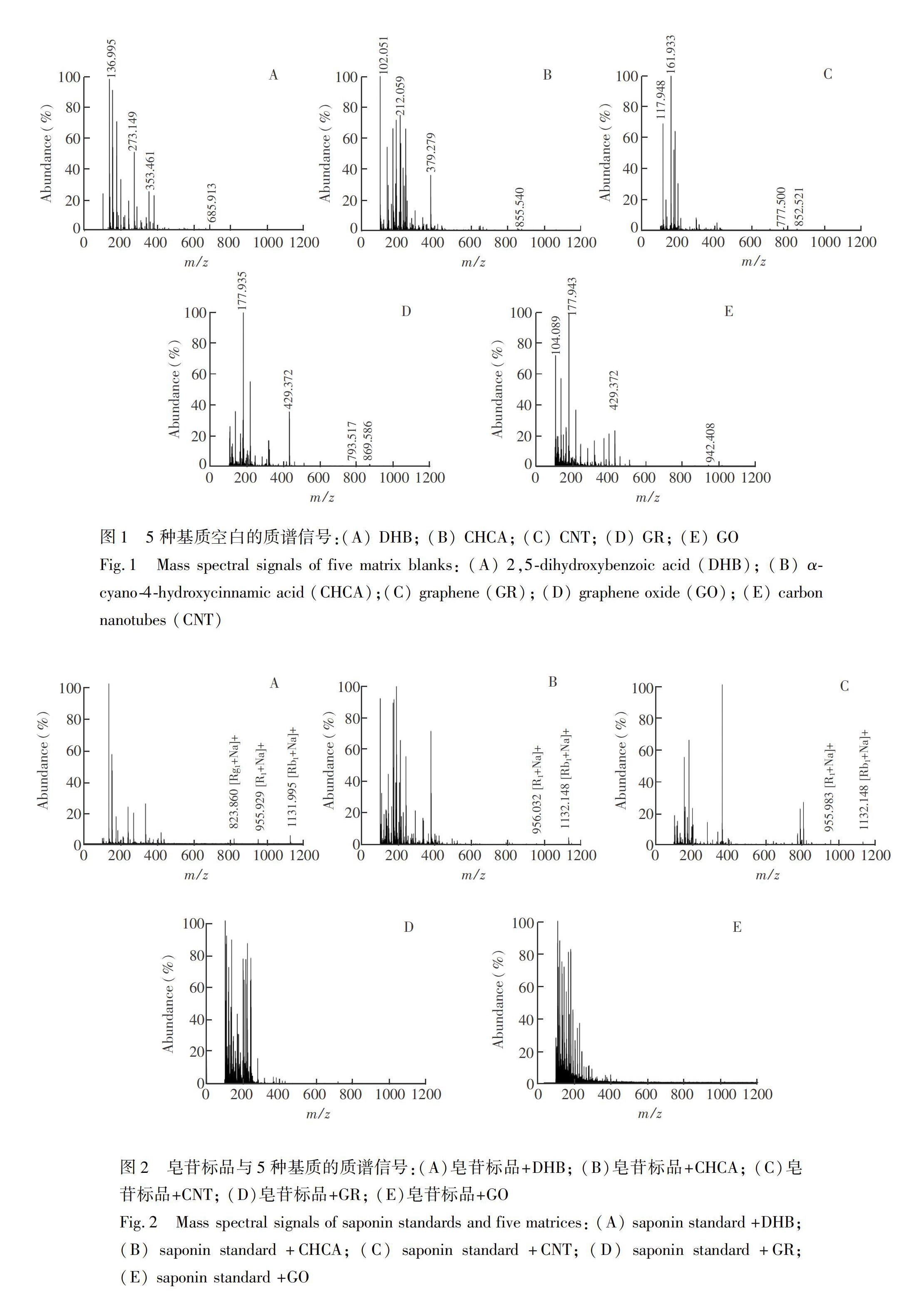
比较DHB、CHCA、GR、GO以及CNT分别作为基质时人参皂苷Rg1、三七皂苷R1和人参皂苷Rb1 3种皂苷标准品的质谱信号。由图1可见, 5种基质中除DHB基质峰都在800 Da以下,其余4种基质在800 Da以上仍出现基质峰。由图2可见, DHB作为基质可以检测到m/z 823.860、955.929、1131.995处3种皂苷的[M+Na]+峰,另外4种基质只能检测到两种皂苷的峰或3种均不出峰。考虑到排除基质干扰的同时,获得最佳的检测灵敏度,选择DHB作为基质。
3.2三七皂苷MALDIMSI的识别和成像分析
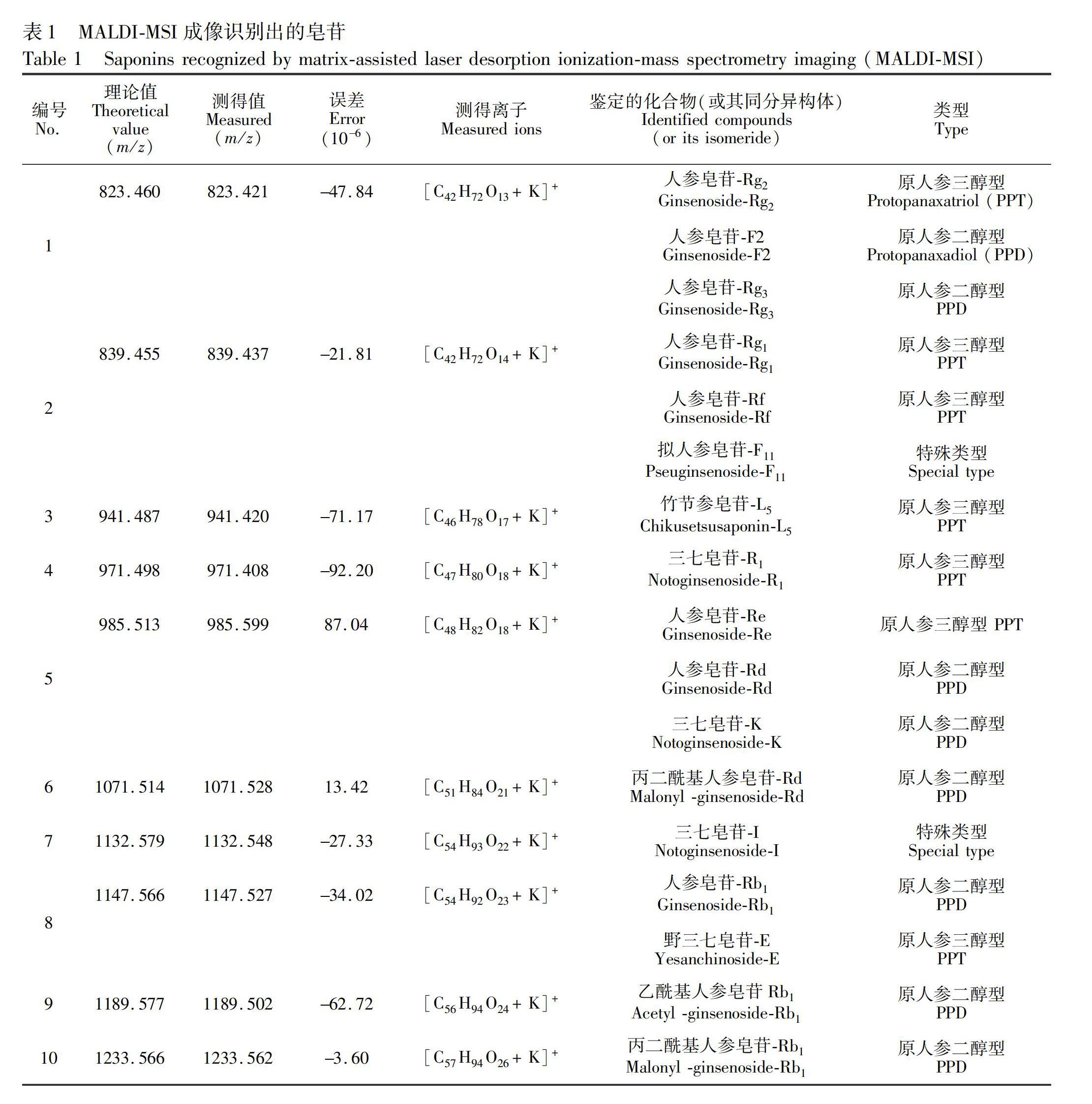
按照上述选定的实验条件,对三七根茎部分组织切片进行了MALDI成像分析。根据测到的质谱峰,参照文献[22~34]已报导的三七根茎中皂苷的成分,并与人参皂苷Rg1、Rb1和三七皂苷R1标准品质荷比进行对照,对信号峰进行了归属(表1)。
三七根茎的MALDI谱图中,所有的皂苷都是以钾加合离子的形式出现。K+在植物体内参与了糖类的运输,而糖类也是皂苷主要结构的一部分,这也与三七是典型的喜钾植物相吻合。
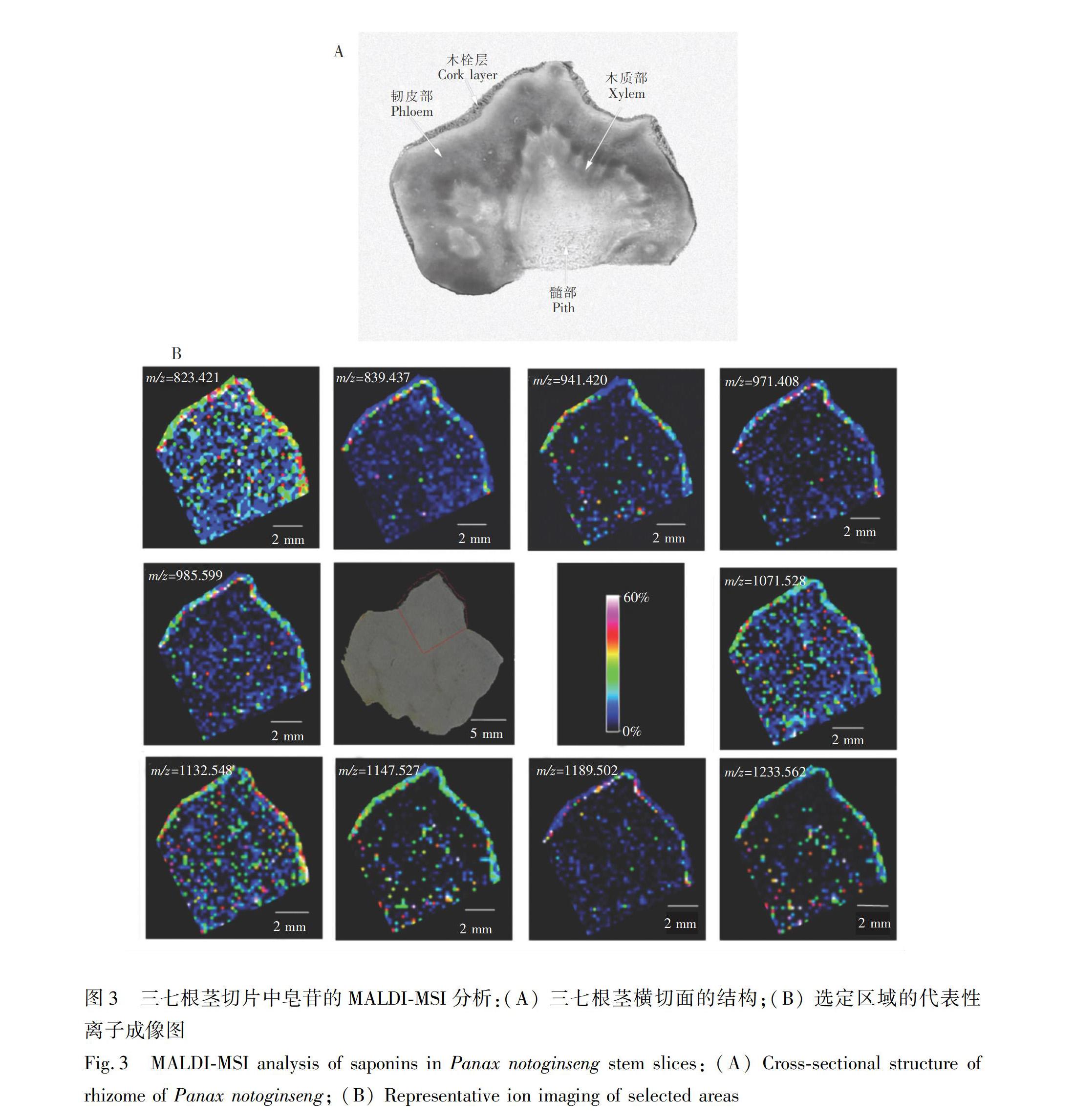
由图3可见,根茎中鉴定出的三七皂苷均呈现出在木栓部分布较集中的特点。这与三萜皂苷类化合物具有防御环境胁迫和病虫害等危害的功能相关。
3.3三七根茎皂苷的生物代谢合成途径与分布
在三七根茎的MALDI成像图中, 人参皂苷Rb1在木质部和髓部均有分布,人参皂苷Rg1和三七皂苷R1几乎只存在于木栓层。人参皂苷Rg1和三七皂苷R1属于原人参三醇型皂苷,人参皂苷Rb1则属于原人参二醇型皂苷。这两类皂苷在植物体中都是先经过甲羟戊酸(Mevalonate, MVA)或糖酵解(EmbdenMeyerhofParnas, MEP)途径合成异戊烯基焦磷酸(Isopentenyl pyrophosphate, IPP)或二甲基烯丙基焦磷酸(Dimethylallyl pyrophosphate, DMAPP); IPP或DMPP又通过异戊烯基转移酶和萜类环化酶的催化合成2,3氧化鲨烯(2,3Oxidosqualene); 2,3氧化鲨烯依次经过环化、羟基化、糖基化修饰,最终形成达玛烷型三七皂苷[35]。在此合成过程中,2,3氧化鲨烯是三七皂苷生物合成的共同前体,它的环化过程是各种三萜生物合成多样化的第一步。原人参二醇型是2,3氧化鲨烯在达玛烯二醇合成酶(DammarenediolHsynthase, DS)催化作用下先生成达玛烯二醇(Dammarenedio1Ⅱ),然后细胞色素P450单加氧酶基因CYP716U1参与达玛烯二醇C12位的羟基化所产生的。若细胞色素P450单加氧酶基因CYP716S1v2在原人参二醇C6位继续羟基化,即可产生原人参三醇型。在糖基转移酶(Glycosyltransferase/UDPglycosyltransferase, GT/UGT)作用下,一个或几个单糖添加到原人参三醇上,形成了人参皂苷Rg1和三七皂苷R1;添加到原人参二醇上,形成了人参皂苷Rb1[36,37]。
人参皂苷Rg1和三七皂苷R1的合成途径相同,分布也相同;人参皂苷Rb1的合成途径与人参皂苷Rg1和三七皂苷R1不同,分布也呈现差异性,这表明皂苷的分布与其生物代谢途径合成途径有关联。因此,有望通过MALDI成像探讨皂苷类化合物的生物代谢合成途径。
3.4不同年份根茎的区分
质谱成像具有高通量的特点,提供了不同样品的大量质谱信息。成像分析表明,三七根茎中的皂苷主要分布在木栓层,选取市售常见2年生和3年生三七根茎木栓层皂苷的质谱数据进行t分布领域嵌入算法分析(tSNE)。如图4所示,tSNE通过对样本数据降维后,可以明确显示出两种年份三七根茎质谱数据的聚类状况,实现了2年生与3年生根茎的区分。
4结 论
通过基质的优化实现了对三七根茎冷冻切片的MALDIMSI分析,检测到10种皂苷,并得到其分布信息。基于MALDIMSI直接分析的优势,检测到了极不稳定的酰基化皂苷(丙二酰基人参皂苷Rd和丙二酰基人参皂苷Rb1),获取了多种皂苷可视化空间分布信息,有助于探讨生物代谢合成途径。在此基础上,基于MALDIMSI数据,通过tSNE将2年生与3年生的三七根茎进行区分。本方法为三七组分的特异性提取提供了有价值的信息,也为了解三七代谢物的合成途径提供了重要线索。
致 谢本研究得到中国科学院化学研究所聂宗秀和刘会会的帮助,谨此致谢。
References
1Chinese Pharmacopoeia Commission. Pharmacopoeia of the People's Republic of China. 2015 ( Part 1) . Beijing: China Medical Science Press, 2015: 11-12
国家药典委员会. 中华人民共和国药典2015年版一部. 北京: 中国医药科技出版社, 2015: 11-12
2Han L F, Sakah K J, Liu L L, Kojo A, Wang T, Zhang Y. Chin. Herb. Med.,2014, 6(2): 159-163
3SUN FengZhi, SUN MingJiang, LU XuXiao. J. Med. Res., 2013, 42(9): 24-26
孙凤志, 孫明江, 吕旭潇. 医学研究杂志, 2013, 42(9): 24-26
4ZHANG JingJing, LIU GuiQin, WANG QingPeng, LI LanJie. J. Liaocheng Univ. Nat. Sci. Ed., 2018, 31(2): 43-52
张静静, 刘桂芹, 王庆鹏, 李兰杰. 聊城大学学报(自然科学版), 2018, 31(2): 43-52
5Guan J, Lai C M, Li S P. J. Pharm. Biomed. Anal.,2007, 44(4): 996-1000
6SUN YuQin, XIANG FeiJun, ZENG Jiang, LIU YunZhi, ZHU YunFei, CHEN YiJun, WANG ChaoLiang. J. Wenshan Univ., 2013, 26(6): 8-10
孙玉琴, 向飞军, 曾 江, 刘云芝, 朱云飞, 陈昱君, 王朝梁. 文山学院学报, 2013, 26(6): 8-10,
7Dong T T, Cui X M, Song Z H, Zhao K J, Ji Z N, Lo C K, Tsim K W. J. Agric. Food Chem.,2003, 51(16): 4617-4623
8XU Shuai, ZHAO ChangLing, CHEN ZhongJian, PAN YanBing, WEI FuGang, XIAO XingLei. Chin. Agric. Sci. Bull., 2018, 34(7): 13-17
徐 率, 赵昶灵, 陈中坚, 潘彦冰, 魏富刚, 肖兴磊. 中国农学通报, 2018, 34(7): 13-17
9CUI XiuMing, CHEN ZhongJian, WANG ChaoLiang, ZENG Jiang. Chin. J. Chin. Mater. Med., 2001, 26(1): 24-25
崔秀明, 陈中坚, 王朝梁, 曾 江. 中国中药杂志, 2001, 26(1): 24-25
10SHA MengChen, ZHOU YongFeng, ZHANG HaiZhu, LI Yang, QIN Qin. Mod. Chin. Med., 2018, 20(7): 832-836
沙孟晨, 周永峰, 张海珠, 李 杨, 秦 琴. 中国现代中药, 2018, 20(7): 832-836
11Ma C, Guan H D, Ju Z C, Li S P, Deng G, Zhang Y P, Lin Q Y, Cheng X M, Yang L, Wang Z T, Wang C H. J. Sep. Sci., 2019, 42(8): 1550-1563
12Yao C L, Pan H Q, Wang H, Yao S, Yang W Z, Hou J J, Jin Q H, Wu W Y, Guo D A. J. Chromatogr. A, 2018, 1538: 34-44
13HE HuiXin, CHEN LuLu, QIN Liang, LIU YaQin, WANG XiaoDong. Sci. Sin. Vitae,2017, 47(10): 1043-1064
何慧欣, 陈路路, 秦 亮, 刘亚琴, 王晓东. 中国科学: 生命科学, 2017, 47(10): 1043-1064
14SUN Jie, HE Qing, XUE JinJuan, XIONG CaiQiao, LIU HuiHui, CHEN SuMing, NIE ZongXiu. Sci. Sin. Chim., 2016, 46(10): 1119-1125
孙 洁, 何 清, 薛晋娟, 熊彩侨, 刘会会, 陈素明, 聂宗秀. 中国科学: 化学, 2016, 46(10): 1119-1125
15Li B, Bhandari D R, Rmpp A, Spengler B. Sci. Rep., 2016, 6: 36074
16Li B, Bhandari D R, Janfelt C, Rmpp A, Spengler B. Plant J., 2014, 80(1): 161-171
17Beck S, Stengel J. Phytochemistry, 2016, 130(2016): 201-206
18Li B, Neumann E K, Ge J, Gao W, Yang H, Li P, Sweedler J V. Plant Cell Environ., 2018, 41(11): 2693-2703
19Taira S, Ikeda R, Yokota N, Osaka I, Sakamoto M, Kato M, Sahashi Y. Am. J. Chin. Med., 2010, 38(3): 485-493
20Dong X L, Cheng J S, Li J H, Wang Y S. Anal. Chem., 2010, 82(14): 6208-6214
21Bai H R, Wang S J, Liu J J, Gao D, Jiang Y Y, Liu H X, Cai Z W. J. Chromatogr. B,2016, 1026(2016): 263-271
22Chen J T, Li H Z, Wang D, Zhang Y J, Yang C R. Helv. Chim. Acta, 2006, 89(7): 1442-1448
23Yoshikawa M, Murakami T, Ueno T, Hirokawa N, Yashiro K, Murakami N, Yamahara J, Matsuda H, Saijoh R, Tanaka O. Chem. Pharm. Bull., 1997, 45(6): 1056-1062
24WANG Qiu, FENG YiFan, RUI Wen, ZHONG YanMei, GUO Jiao. Nat. Prod. Res. Dev., 2014, 26(8): 1233-1239
王 邱, 冯毅凡, 芮 雯, 钟艳梅, 郭 姣. 天然产物研究与开发, 2014, 26(8): 1233-1239
25ZHAO Jing, QIN ZhenXian, PENG Bing, LIU YongGang, LIU Yong. J. Chin. Mass. Spectr. Soc., 2017, 38(1): 97-108
赵 静, 秦振娴, 彭 冰, 刘永刚, 刘 勇. 质谱学报, 2017, 38(1): 97-108
26XU Wen, QIU XiaoHui, ZHANG Jing, ZHU DaYuan, YANG YiMing, LU ChuanJian. Acta. Pharm. Sin., 2012, 47(6): 773-778
徐 文, 丘小惠, 张 靖, 朱大元, 杨一鸣, 卢传坚. 药学学报, 2012, 47(6): 773-778
27ZHOU Yu, SONG FengRui, LIU ShuYing, LI XiangGao. Acta. Chim. Sinica, 1998, 56(3): 298-301
周 雨, 宋凤瑞, 刘淑莹, 李向高. 化学学报, 1998, 56(3): 298-301
28LU RuMei, HUANG ZhiQi, LI Bing, WEI JianHua, ZHONG ZhenGuo. Chin. J. Exp. Tradit. Med. Form., 2016, (7): 62-64
盧汝梅, 黄志其, 李 兵, 韦建华, 钟振国. 中国实验方剂学杂志, 2016,(7): 62-64
29XIA PengGuo, ZHANG ShunCang, LIANG ZongSuo, QI ZhiHong. Chin. Tradit. Herbal. Drugs, 2014, 45(17): 2564-2570
夏鹏国, 张顺仓, 梁宗锁, 齐志鸿. 中草药, 2014, 45(17): 2564-2570
30BAO JianCai, LIU Gang, CONG DengLi, ZHANG ChongXi. Chin. Tradit. Pat. Med., 2006, 28(2): 246-253
鲍建才, 刘 刚, 丛登立, 张崇禧. 中成药, 2006, 28(2): 246-253
31LI HaiZhou, ZHANG YingJun, YANG ChongRen. Nat. Prod. Res. Dev., 2006, 18(4): 549-554
李海舟, 张颖君, 杨崇仁. 天然产物研究与开发, 2006, 18(4): 549-554
32Dan M, Su M M, Gao X F, Zhao A H, Zhao T, Xie G X, Qiu Y P, Zhou M M, Liu Z, Jia W. Phytochemistry, 2008, 69(11): 2237-2244
33SHEN XiaoJing, LI XiaoBo, SHEN Yong, YANG ShengChao, JIANG WeiWei. Chin. Med, Mat., 2018, 41(08): 1894-1898
沈晓静, 李晓波, 沈 勇, 杨生超, 姜薇薇. 中药材, 2018, 41(08): 1894-1898
34LIU JinHuai, WANG Xuan, CAI ShaoQing, KOMATSU Katsuko, NAMBA Tsuneo. J. Chin. Pharm. Sci., 2004, 13(4): 225-237
刘进怀, 王 璇, 蔡少青, 小松かつ子, 难波恒雄. 中国药学, 2004, 13(4): 225-237
35LI ZeDong, ZHAO RongHua, ZHANG ZhaoChuan, YU Jie, GU Wen, HE Sen, CAO GuanHua. Tradit. Med. Form.,2018, 24(14): 207-213
李泽东, 赵荣华, 张兆传, 俞 捷, 顾 雯, 贺 森, 曹冠华. 中国实验方剂学杂志, 2018, 24(14): 207-213
36Ghosh S. Indian Natl. Sci. Acad., 2016, 82(4): 1189-1210
37Wei R C, Qiu D Y, Wilson I W, Zhao H, Lu S F, Miao J H, Feng S X, Bai L H, Wu Q H, Tu D P, Ma X J, Tang Q. BMC Genomics, 2015, 16(1): 835
