HPLC法测定圣愈汤冻干粉中4个指标成分的含量
2020-07-09董丹华刘玉军李亚男胡祥昊孙平李婷刘菊妍高鹏
董丹华 刘玉军 李亚男 胡祥昊 孙平 李婷 刘菊妍 高鹏


中圖分类号 R284.1 文献标志码 A 文章编号 1001-0408(2020)05-0576-05
DOI 10.6039/j.issn.1001-0408.2020.05.14
摘 要 目的:建立测定圣愈汤冻干粉中阿魏酸、毛蕊花糖苷、藁本内酯、黄芪甲苷含量的方法。方法:采用高效液相色谱法测定3批冻干粉样品4种成分含量。测定阿魏酸、毛蕊花糖苷、藁本内酯的色谱柱为Inertsil ODS-SP C18,流动相为甲醇-0.1%磷酸水溶液,梯度洗脱,流速为1.0 mL/min,检测波长为330 nm,检测器为二极管阵列检测器,柱温为30 ℃,进样量为10 μL;测定黄芪甲苷的色谱柱为Kromasil C18,流动相为乙腈-水(32 ∶ 68,V/V),检测器为蒸发光散射检测器,漂移管温度为100 ℃,载气(空气)流量为2.5 L/min,流速为1.0 mL/min,柱温为30 ℃,进样量为10 μL。结果:阿魏酸、毛蕊花糖苷、藁本内酯和黄芪甲苷进样量线性范围分别为0.050 15~10.03 μg(r=0.999 8)、0.067 80~13.56 μg(r=0.999 9)、0.057 30~11.46 μg(r=0.999 5)、1.128~11.28 μg(r= 0.999 3);检测限分别为2.12×10-4、1.30×10-3、8.02×10-4、1.09×10-3 μg,定量限分别为7.43×10-4、3.87×10-3、2.34×10-3、3.36×10-3 μg;精密度、稳定性(12 h)、重复性试验的RSD均小于2%(n=6);平均加样回收率分别为99.6%(RSD=0.83%,n=6)、100.9%(RSD=1.07%,n=6)、98.8%(RSD=0.84%,n=6)和101.3%(RSD=0.99%,n=6)。3批样品中阿魏酸、毛蕊花糖苷、藁本内酯和黄芪甲苷的含量分别为1.225~1.248、0.413~0.424、0.325~0.332、0.394~0.404 mg/g(批间RSD<1.5%)。结论:建立的含量测定方法稳定性、重复性好,能够快速、准确地测定圣愈汤冻干粉中阿魏酸、毛蕊花糖苷、藁本内酯和黄芪甲苷的含量。
关键词 圣愈汤;冻干粉;高效液相色谱法;阿魏酸;毛蕊花糖苷;藁本内酯;黄芪甲苷;含量测定
Content Determination of 4 Indicator Components in Shengyu Decoction Lyophilized Powder by HPLC
DONG Danhua1,LIU Yujun2,LI Yanan1,HU Xianghao1,SUN Ping1,LI Ting3,LIU Juyan4,GAO Peng1(1.School of Pharmacy, Shandong University of TCM, Jinan 250355, China;2.Chinese Pharmacy of Qihe County Peoples Hospital of Shandong Province, Shandong Dezhou 251100, China;3.Dept. of Pharmacy, Wendeng Osteopathic Hospital of Shandong Province, Shandong Weihai 264400, China;4.Dept. of Technology, Guangzhou Pharmaceutical Group Co., Ltd., Guangzhou 510130, China)
ABSTRACT OBJECTIVE: To establish the content determination method of ferulic acid, verbascoside, ligustilide and astragaloside in Shengyu decoction lyophilized powder. METHODS: HPLC method was adopted to determine 4 components in 3 batches of lyophilized powder. The determination of ferulic acid, verbascoside and ligustilide was performed on Inertsil ODS-SP C18 column with mobile phase consisted of methanol-0.1% phosphoric acid (gradient elution) at the flow rate of 1.0 mL/min; detector was diode array detector; detection wavelength was set at 330 nm; column temperature was 30 ℃, the sample size was 10 μL. The determination of astragaloside was performed on Kromasil C18 column with mobile phase consisted of acetonitrile-water (32 ∶ 68, V/V); detector was evaporative light scattering detector; the drift tube temperature was 100 ℃, the carrier gas (air) flow rate was 2.5 L/min at the flow rate of 1.0 mL/min; column temperature was 30 ℃, the sample size was 10 μL. RESULTS: The linear ranges of ferulic acid, verbascoside, ligustilide and astragaloside were 0.050 15-10.03 μg (r=0.999 8), 0.067 80-13.56 μg (r=0.999 9), 0.057 30-11.46 μg (r=0.999 5), 1.128-11.28 μg (r=0.999 3), respectively. The detection limits were 2.12×10-4, 1.30×10-3, 8.02×10-4, 1.09×10-3 μg, respectively. The limit of quantification were 7.43×10-4, 3.87×10-3, 2.34×10-3, 3.36×10-3 μg, respectively. RSDs of precision, stability (12 h) and reproducibility tests were all lower than 2% (n=6). Average recovery rates were 99.6% (RSD=0.83%, n=6), 100.9% (RSD=1.07%, n=6), 98.8% (RSD=0.84%, n=6) and 101.3% (RSD=0.99%, n=6), respectively. The contents of ferulic acid, verbascoside, ligustilide and astragaloside in 3 batches of samples were 1.225-1.248, 0.413-0.424, 0.325-0.332, 0.394-0.404 mg/g, respectively (RSDs among batches were lower than 1.5%). CONCLUSIONS: Established method is stable, reproducible, rapid and accurate for the content determination of ferulic acid, verbascoside, ligustilide and astragaloside in Shengyu decoction lyophilized powder.
KEYWORDS Shengyu decoction; Lyophilized powder; HPLC; Ferulic acid; Verbascoside; Ligustilide; Astragaloside; Content determination
圣愈汤为经典名方,出自金代李东垣的《兰室秘藏》:“治诸恶疮,血出多而心烦不安,不得睡眠,亡血故也,以此药主之”。此方由生地黄、熟地黄、川芎、人参各三分,当归身、黄芪各五分组成。方中人参、黄芪补气;当归身、生熟地黄、川芎补血滋阴;配合成方,共奏补益气血、活血止痛之效[1-3]。现代药理研究表明,圣愈汤对血液系统具有抗凝作用[1],可改善微循环、改善血液流变学、降血脂、抗动脉粥样硬化[2],还可治疗气血虚证痛经[3],同时对妇科恶性肿瘤并发的贫血症状也有改善效果[4]。圣愈汤中当归和川芎可活血、补血,共有的成分阿魏酸和藁本内酯为主要活性物质[5-8];地黄可滋阴、补血,所含毛蕊花糖苷可促进血虚动物红细胞及血红蛋白的恢复[9];《本草纲目》中称黄芪为“补药之长”,其主要成分黄芪甲苷对心血管系统的作用效果显著[10]。因此,阿魏酸、毛蕊花糖苷、藁本内酯和黄芪甲苷这4个成分均为圣愈汤的重要指标成分。目前,2015年版《中国药典》尚未收载圣愈汤相关制剂,数据库中多收录的是圣愈汤中医辨证论治方面的内容,尚未检索到关于圣愈汤含量测定的研究报道。为了便于制剂保存及最大程度地保持中药汤液的物质一致性,可将圣愈汤采用减压浓缩和冷冻干燥法制备成冻干粉,之后还可加入相应辅料制剂开发成相关的成药制剂。因此,本试验将建立圣愈汤冻干粉中阿魏酸、毛蕊花糖苷、藁本内酯和黄芪甲苷含量的测定方法,为后续的相关研究提供参考。
1 材料
1.1 仪器
LC-2030C型高效液相色谱仪,配有二极管阵列检测器(DAD)、LabSolutions工作站(日本岛津制作所);3300型蒸发光散射检测器(ELSD,美国奥泰科技有限公司);XS105型分析天平(梅特勒-托利多国际贸易有限公司,感量:0.01 mg);YP10002型电子天平(上海光正医疗仪器有限公司,感量:0.01 g);KQ2200DV型数控超声波清洗器(昆山市超声仪器有限公司);H22-X3型电陶炉(九阳股份有限公司);SHB-Ⅲ型循环水式多用真空泵(郑州长城科工贸有限公司);RE 5298A型旋转蒸发仪(上海亚荣生化仪器厂);冷冻干燥机(北京博医康实验仪器有限公司)。
1.2 药品与试剂
阿魏酸(批号:110773-201614,纯度:99.0%)、毛蕊花糖苷(批号:111530-201713,纯度:92.5%)、黄芪甲苷(批号:110781-201314,纯度:95.8%)各对照品均来源于中国食品药品检定研究院;藁本内酯对照品(批号:58546-55,纯度:98.0%)来源于上海雅吉生物科技有限公司;甲醇、磷酸均为色谱纯;纯净水(杭州娃哈哈集团有限公司);生地黄、熟地黄、当归、川芎、人参、黄芪各饮片均经山东中医药大学药学院万鹏教授鉴定为真品,具体信息见表1。
表1 中药饮片信息
2 方法与结果
2.1 冻干粉样品制备
原方记载圣愈汤的制备方法为:“生地黄、熟地黄、川芎、人参各三分,当归身、黄芪各五分,右[父]咀如麻豆大,都作一服,水二大盏,煎至一盏,去粗”[11](“右[父]咀”指用牙齿将上述药材嚼碎)。本试验样品制备方法如下:取已剪成麻豆粒大小(约为黄豆粒~5目大小)的生地黄、熟地黄、川芎、人参饮片各1.24 g,当归身、黄芪饮片各2.06 g,置于砂锅中,加水400 mL,称质量,置于电陶炉上,武火煎煮至沸腾,改用文火保持微沸,至总质量减少200 g,停止加热,趁热用200目尼龙滤布滤过,挤压药渣,得到汤液;汤液用旋转蒸发仪于50 ℃进行减压浓缩,得到浓缩液;将浓缩液置于冷冻干燥机中进行冷冻干燥,得到圣愈汤冻干粉。按上述方法制备3批成方冻干粉,批号分别为190615、190616、190617,质量分别为4.92、5.14、5.07 g。另同法制备阴性样品:取已剪成麻豆粒大小的人参饮片1.24 g、黄芪饮片2.06 g,按上述样品制备方法制备,得到缺生地黄、熟地黄、川芎和当归的阴性冻干粉A,平行3份,混匀,总质量为2.5 g;取已剪成麻豆粒大小的生地黄、熟地黄、川芎、人参饮片各1.24 g,当归身饮片2.06 g,按上述样品制备方法制备,得到缺黄芪的阴性冻干粉B,平行3份,混匀,总质量为11.4 g。
2.2 阿魏酸、毛蕊花糖苷和藁本內酯含量测定方法建立
2.2.1 色谱条件 在文献[12-13]基础上设置本文条件。色谱柱为Inertsil ODS-SP C18(250 mm×4.6 mm,5 μm);流动相为甲醇(A)-0.1%磷酸水溶液(B),采用梯度洗脱(0~8 min,5%A;8~55 min,5%A→27%A;55~57 min,27%A→73%A;57~60 min,73%A→5%A);流速为1.0 mL/min;检测器为DAD,检测波长为330 nm;柱温为30 ℃;进样量为10 μL。
2.2.2 溶液的制备 (1)对照品溶液制备。取阿魏酸、毛蕊花糖苷和藁本内酯对照品,加甲醇制成每1 mL含阿魏酸1.356 mg、毛蕊花糖苷1.003 mg和藁本内酯1.146 mg的混合对照品贮备液;将贮备液以甲醇稀释100倍,得到每1 mL含阿魏酸13.56 μg、毛蕊花糖苷10.03 μg和藁本内酯11.46 μg的混合对照品溶液。(2)供试品溶液制备。取成方冻干粉(批号:190615)约0.5 g,精密称定,置于具塞锥形瓶中,精密加入70%甲醇25 mL,密塞,称定质量,超声30 min(功率:250 W,频率:40 kHz,下同),放冷,再称定质量,用70%甲醇补足减失的质量,摇匀,滤过,取续滤液,即得。(3)阴性样品溶液A制备。取阴性冻干粉A约0.2 g,按上述供试品溶液制备方法制备,即得。
2.2.3 系统适用性试验 分别取“2.2.2”项下混合对照品溶液、供试品溶液和阴性样品溶液A,在“2.2.1”项色谱条件下进样测定,记录色谱图。结果,在该色谱条件下,各峰间分离度均大于1.5,其他成分对待测成分的测定无干扰,理论板数以阿魏酸峰计不低于3 000,色谱图见图1。
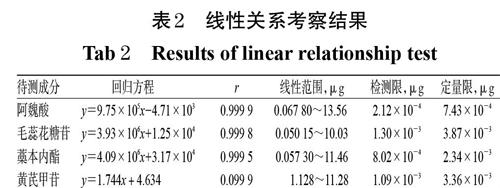
2.2.4 线性关系考察 分别精密吸取“2.2.2”项下混合对照品贮备液0.05、1、2、3、5 mL,置于不同10 mL量瓶中,加70%甲醇稀释制得 5 个不同质量浓度的混合对照品溶液。取“2.2.2”项下混合对照贮备溶液及上述5个质量浓度混合对照品溶液,按“2.2.1”項下色谱条件进样测定,以进样量为横坐标(x)、峰面积为纵坐标(y)分别绘制各成分标准曲线,计算其回归方程。结果,各成分在各自进样量范围内与峰面积的线性关系良好,详见表2。
表2 线性关系考察结果
2.2.5 检测限与定量限考察 精密吸取“2.2.2”项下混合对照品溶液适量,加甲醇倍比稀释后,按“2.2.1”项下色谱条件连续进样测定6次,记录峰面积。当信噪比为3 ∶ 1时,得检测限;当信噪比为10 ∶ 1时,得定量限,结果见表2。
2.2.6 精密度试验 精密吸取“2.2.2”项下混合对照溶液适量,按“2.2.1”项下色谱条件连续进样测定6次,记录色谱图。结果,阿魏酸、毛蕊花糖苷和藁本内酯峰面积的RSD分别为0.52%、0.98%、0.75%(n=6),表明仪器精密度良好。
2.2.7 稳定性试验 取同一供试品溶液(批号:190615),分别于室温条件下放置0、2、5、8、10、12 h时,按“2.2.1”项下色谱条件进样测定,记录色谱图。结果,阿魏酸、毛蕊花糖苷和藁本内酯峰面积的RSD分别为1.02%、0.47%、0.72%(n=6),表明供试品溶液在室温放置12 h内稳定性良好。
2.2.8 重复性试验 取同一批冻干粉样品(批号:190615)6份,按“2.2.2”项下方法制备供试品溶液,按“2.2.1”项下色谱条件进样测定,记录峰面积并按外标法计算各成分含量。结果,阿魏酸、毛蕊花糖苷和藁本内酯平均含量分别为1.246、0.414、0.324 mg/g,RSD分别为0.96%、0.61%、0.55%(n=6),表明方法重复性良好。
2.2.9 加样回收率试验 取冻干粉样品(批号:190615)6份,每份约0.25 g,精密称定,分别置于具塞锥形瓶中,各加入待测成分对照品适量,按“2.2.2”项下方法制备供试品溶液,按“2.2.1”项下色谱条件进样测定,记录峰面积并计算各成分的加样回收率。结果,阿魏酸、毛蕊花糖苷和藁本内酯平均加样回收率分别为99.6%(RSD=0.83%,n=6)、100.9%(RSD=1.07%,n=6)和98.8%(RSD=0.84%,n=6),详见表3。
表3 阿魏酸、毛蕊花糖苷和藁本内酯回收率试验结果(n=6)
2.3 黄芪甲苷含量测定方法建立
2.3.1 色谱条件 色谱柱为Kromasil C18(250 mm×4.6 mm,5 μm);流动相为乙腈-水(32 ∶ 68,V/V);检测器为ELSD,漂移管温度为100 ℃;载气(空气)流量为2.5 L/min;流速为1.0 mL/min;柱温为30 ℃;进样量为10 μL[14]。
2.3.2 溶液的制备 (1)对照品溶液制备。称取黄芪甲苷对照品适量,用甲醇溶解制成每1 ml含黄芪甲苷5.642 mg的对照品贮备液;将该贮备液加甲醇稀释10倍,得到质量浓度为564.2 μg/mL的对照品溶液。(2)供试品溶液制备。取冻干粉约1.0 g,精密称定,置于具塞锥形瓶中,精密加入甲醇50 mL,称定质量,超声处理30 min,放冷,再称定质量,用甲醇补足减失的质量,摇匀,滤过;精密量取续滤液25 mL,蒸干,残渣加水15 mL使溶解;用水饱和的正丁醇振摇提取4次,每次25 mL;合并正丁醇液,用氨试液洗涤2次,每次40 mL;弃去氨液,正丁醇液蒸干,残渣用甲醇溶解,转移至5 mL量瓶中,加甲醇至刻度,摇匀,微孔滤膜(0.22 μm)滤过,取续滤液,即得。(3)阴性样品溶液B制备。取阴性冻干粉B约1.0 g,按上述供试品溶液制备方法制备,即得[15]。
2.3.3 系统适用性试验 分别取“2.3.2”项下混合对照品溶液、供试品溶液和阴性样品溶液B,按“2.3.1”项色谱条件下进样测定,记录色谱图。结果,在该色谱条件下,黄芪甲苷与相邻峰间分离度均大于1.5,其他成分对待测成分的测定无干扰,理论板数以黄芪甲苷计不低于 4 000,色谱图见图2。
2.3.4 线性关系考察 分别精密吸取“2.3.2”项下对照品贮备液0.1、0.2、0.4、0.7、1 mL,置于不同5 mL量瓶中,加甲醇制成6个不同浓度的对照品溶液。按“2.3.1”项色谱条件进样测定,以黄芪甲苷进样量的对数为横坐标(x)、峰面积的对数为纵坐标(y)绘制标准曲线,计算回归方程。结果,黄芪甲苷在进样量范围内线性关系良好,详见表2。
2.3.5 检测限与定量限考察 精密吸取“2.3.2”项下对照品溶液适量,加甲醇倍比稀释后,按“2.3.1”项下色谱条件连续进样测定6次,记录峰面积。当信噪比为3 ∶ 1时,得检测限;当信噪比为10 ∶ 1时,得定量限,结果见表2。
2.3.6 精密度试验 精密吸取“2.3.2”项下对照品溶液适量,按“2.3.1”项下色谱条件连续进样测定6次,记录色谱图。结果,黄芪甲苷峰面积的RSD为0.67%(n=6),表明仪器精密度良好。
2.3.7 稳定性试验 取同一供试品溶液(批号:190615),分别于室温条件下放置0、2、5、8、10、12 h时,按“2.3.1”项下色谱条件进行测定,记录色谱图。结果,黄芪甲苷峰面积的RSD为1.15%(n=6),表明供试品溶液在室温12 h内稳定性良好。
2.3.8 重复性试验 取同一批冻干粉样品(批号:190615)6份,按“2.3.2”项下方法制备供试品溶液,按“2.3.1”项下色谱条件进样测定,记录色谱峰,并按外标法计算含量。结果,黄芪甲苷平均含量为0.398 mg/g,RSD为0.74%(n=6),表明方法重复性良好。
2.3.9 加样回收率试验 取冻干粉样品(批号:190615)6份,每份约0.5 g,精密称定,分别置于具塞锥形瓶中,加入黄芪甲苷对照品溶液适量,按“2.3.2”项下方法制备供试品溶液,按“2.3.1”项下色谱条件进样测定,记录峰面积并计算黄芪甲苷的加樣回收率。结果,黄芪甲苷平均加样回收率为101.3%(RSD=0.99%,n=6),详见表4。
表4 黄芪甲苷回收率试验结果(n=6)
2.4 圣愈汤冻干粉中4个成分的含量测定
2.4.1 阿魏酸、毛蕊花糖苷和藁本内酯的含量测定 取3批冻干粉样品适量,按“2.2.2”项下方法制备成供试品溶液,按“2.2.1”项下色谱条件进样测定,按外标法计算阿魏酸、毛蕊花糖苷和藁本内酯的含量。每批样品平行2份测定。结果,不同批次阿魏酸、毛蕊花糖苷和藁本内酯含量的均一性较好,详见表5。
2.4.2 黄芪甲苷含量测定 取3批冻干粉,按“2.3.2”项下方法制备供试品溶液,每批平行2份,按“2.3.1”项下色谱条件进样,测定黄芪甲苷的含量。结果,不同批次黄芪甲苷含量的均一性较好,详见表5。
表5 3批圣愈汤冻干粉中阿魏酸、毛蕊花糖苷、藁本内酯和黄芪甲苷的含量测定结果(mg/g)
3 讨论
3.1 阿魏酸、毛蕊花糖苷和藁本内酯供试品溶液制备方法的选择
本试验在建立阿魏酸、毛蕊花糖苷和藁本内酯的含量测定方法时,首先考察了甲醇、70%甲醇和50%甲醇3种提取溶剂的提取效果,结果发现70%甲醇对目标成分的提取率更高;另外,考察了超声时间对目标成分提取率的影响,结果发现超声30 min与45、60 min的效果相当。因此,阿魏酸、毛蕊花糖苷和藁本内酯含量测定供试品溶液的制备方法为用70%甲醇超声处理30 min。
3.2 色谱条件的优化
本试验在建立阿魏酸、毛蕊花糖苷和藁本内酯的含量测定方法时,首先用DAD进行了全波长扫描,发现在330 nm波长下基线平稳,主峰相对峰面积较大;又对比了流动相甲醇-水和乙腈-水,发现甲醇-水对毛蕊花糖苷和藁本内酯的分离效果更好,但是导致阿魏酸色谱峰有明显拖尾,故在水相中加入0.1%磷酸,使峰形得以改善;另对不同品牌色谱柱Inertsil ODS-SP C18、Kromasil C18和Cosmosil-5C18-MS-Ⅱ进行了比较,发现采用Inertsil ODS-SP C18时对上述3个目标峰的分离度和峰形更好,而Kromasil C18更适合用于分析黄芪甲苷。
综上所述,本试验建立的同时测定阿魏酸、毛蕊花糖苷、藁本内酯和黄芪甲苷4种成分含量的方法具有重复性好、结果稳定可靠、操作简单等特点,对圣愈汤冻干粉的质量进行整体控制有重要意义。
参考文献
[ 1 ] 赵菊花,祝彼得.圣愈汤的临床应用和实验研究新进展[J].辽宁中医药大学学报,2010,12(12):208-210.
[ 2 ] 唐从耀,田兆华,李怀友,等.圣愈汤对高血压脑出血患者血清HMGB1、BNP、NSE水平的影响[J].中国医药导刊,2018,20(5):271-274.
[ 3 ] 李团网.浅谈圣愈汤治疗气血虚弱型痛经[J].中西医结合心血管病杂志,2016,4(3):176-177.
[ 4 ] 乔小燕,杨树明,蔡焦生.圣愈汤治疗恶性肿瘤化疗后贫血的临床观察[J].光明中医,2010,25(8):1423-1424.
[ 5 ] 韩炜.川芎的化学成分与药理作用研究进展[J].中国现代中药,2017,19(9):1341-1349.
[ 6 ] 杨英来,崔方,胡芳,等.当归补血活血作用的谱效关系研究[J].中国中药杂志,2013,38(22):3923-3927.
[ 7 ] 刘福和,陈少军,倪文娟.川芎中抗血栓活性成分的计算机虚拟筛选研究[J].中国药房,2017,28(16):2182-2186.
[ 8 ] 张来宾,吕洁丽,陈红丽,等.当归中苯酞类成分及其药理作用研究进展[J].中国中药杂志,2016,41(2):168-176.
[ 9 ] 付国辉,杜鑫.地黄化学成分及药理作用研究进展[J].中国医药科学,2015,5(15):39-41.
[10] 聂娟,谢丽华,马港圆,等.中药黄芪的化学成分及药理作用研究进展[J].湖南中医杂志,2018,34(7):228-231.
[11] 吴谦.医宗金鉴[M].北京:人民卫生出版社,1963:332.
[12] 王继陈,韩岚,张艳艳,等.桃红四物汤中6种指标性成分的含量测定[J].安徽中医药大学学报,2019,38(2):80- 84.
[13] 邵长森,张国青,韩真真,等. HPLC法同时测定温经汤中10种活性成分的含量[J].中国药房,2018,29(19):2640- 2643.
[14] 曹庆伟,杜鹃,罗晋平.黄芪甲苷含测方法的优化及对不同产地、不同等级黄芪中黄芪甲苷含量分析[J].中国中药杂志,2019,44(13):2813-2819.
[15] 刘玉军,魏永利,马睿,等.白芪龙胶囊稠膏不同干燥方式的优选[J].中成药,2012,34(3):476-478、486.
(收稿日期:2019-08-26 修回日期:2019-09-20)
(编辑:刘 萍)
