基于美国食品药品监督管理局不良事件报告系统数据库的他克莫司致药品不良反应信号挖掘与分析Δ
2020-07-07余春飞
程 艺,陈 晨,余春飞,陈 乾,陈 力
(1.四川大学华西第二医院药学部/循证药学中心,四川 成都 610041;2.出生缺陷与相关妇儿疾病教育部重点实验室,四川 成都 610041;3.重庆医科大学附属儿童医院药学部/儿童发育疾病研究教育部重点实验室,重庆 400014;4.四川大学华西药学院,四川 成都610041; 5.宜宾市第一人民医院药学部,四川 宜宾 644000)
免疫抑制剂的种类较多且发展非常迅速,从最早的硫唑嘌呤到环孢素A,再到他克莫司,他克莫司现已成为器官移植的首选药物[1]。他克莫司是一种从土壤真菌筑波链霉菌中提取的中性疏水性大环内酯类新型免疫抑制剂[2]。该药可能通过与细胞质内蛋白质结合,形成复合物,竞争性抑制钙调素,以阻止其发挥作用,后者介导T细胞内的钙依赖性抑制信号传递系统,从而阻止一系列淋巴因子基因转录,发挥免疫抑制作用[3-5]。他克莫司有效血药浓度范围窄,而患者药动学个体差异大,其血药浓度受年龄、肝肾功能和药物基因组学等因素影响[6-7]。他克莫司上市以来关于其不良反应报告文献局限,对该类药物不良反应的研究还不够完善。因此,充分探索该药的不良反应十分必要。现利用上市后真实世界的数据以及数据挖掘的方法,对他克莫司致药品不良反应进行研究,即进行不良反应信号检测,充分挖掘他克莫司的不良反应,为临床合理用药提供参考。
1 资料与方法
1.1 资料来源
研究数据为美国食品药品监督管理局(food and drug administration,FDA)不良事件报告系统(FDA adverse event reporting system,FAERS)[8]中自2009年第1季度至2019年第1季度共41个季度的关于他克莫司的不良反应报告。以FDA批准药品及不良反应公众数据库(public dashboard)中药品名称为标准,以他克莫司的通用名“Tacrolimus”做为关键检索词,在FAERS数据库中进行检索。共收集到96 309 例报告,删除其中信息不完全和与药物治疗无关的报告,筛选出其中用药名称为“Tacrolimus”且为首要怀疑药物的报告,最终纳入59 093例。
1.2 信号生成条件与挖掘方法
本研究主要采用的信号检测方法为报告比值比(reporting odds ratio,ROR)法和比例报告比值(proportional reporting ratio,PRR)法,主要计算目标药品不良反应与数据库中对应的药品不良反应等发生之间的关系,若两者之间的关系达到失衡,则提示信号生成,该方法具有较高的可信度和灵敏性。本方法以比例失衡法[8]四格表(见表1)为基础,再用ROR法和PRR法的公式(见表2)计算ROR和PRR。
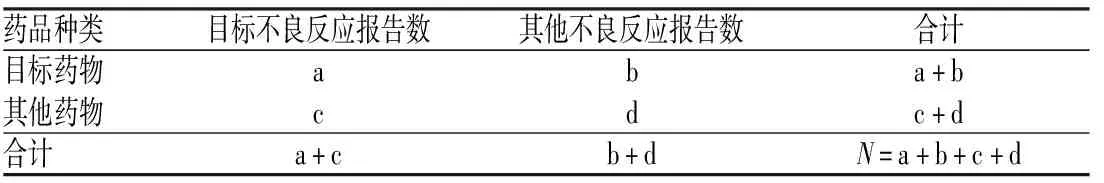
表1 比例失衡法所用四格表
1.3 数据处理
使用Microsoft Excel 2010软件进行统计,并对标准化后的结果进行统计和计算。

表2 ROR法与PRR法的公式及阈值
1.3.1 标准化:采用世界卫生组织(world health organization,WHO)药品不良反应术语集,对每例报告的不良反应名称按照系统和器官进行规范化编码,可以有效减少因药品不良反应报告术语的差异所导致的差异性,提高研究的准确度和可信度[9-10]。采用首选术语(preferred term,PT)。
1.3.2 统计与计算:将上述标准化后的术语进行统计,筛选出报告数>3例的数据,按比例失衡法四宫格(见表1)及ROR法、PRR法的计算公式(见表2),计算表中各值。
1.3.3 筛选:为了避免出现假阳性信号,要求数据同时满足ROR>3和PRR>3且95%CI>1,将不符合条件的数据进行筛除,将符合条件的数据进行排序,以便进行下一步的数据分析。
2 结果
2.1 药品不良反应信号数结果
对检索到的用药名称为“Tacrolimus”(他克莫司)的96 309例报告进行筛选后,得到59 093例报告。对筛选出的报告进行统计后,共获得177个信号。他克莫司致药品不良反应信号强度和报告数居前50位的信号见表3。
2.2 新的药品不良反应信号
将上述二次筛选后的信号与其在WHO药品不良反应术语集累及的系统、器官相对应,结果见表4。
3 讨论
本研究所得的不良反应信号与他克莫司药品说明书和文献研究[11-13]基本一致,主要不良反应表现为肝肾毒性、神经毒性、糖代谢紊乱、心血管并发症、脓肿和感染等。脓肿、感染是接受联合免疫抑制疗法的移植受者常会发生的不良反应,可发生细菌、病毒和真菌等感染。他克莫司肾毒性表现为血浆肌酐急性升高或偶尔进展的慢性肾病,前者可以在降低剂量后大幅度逆转,而后者通常不可逆。心血管并发症主要表现为高血压,其机制可能是通过刺激肾钠氯协同转运蛋白来介导该反应。由肾血管收缩和钠潴留引起的高血压通常在治疗开始后的前几周内发生,减少剂量通常对缓解血压升高有效,但也有可能需要抗高血压药[14]。他克莫司的神经毒性主要表现为震颤、可复性后部脑病综合征和癫痫发作等,其损害较严重,临床药师、医师应重点监护该类不良反应的发生。
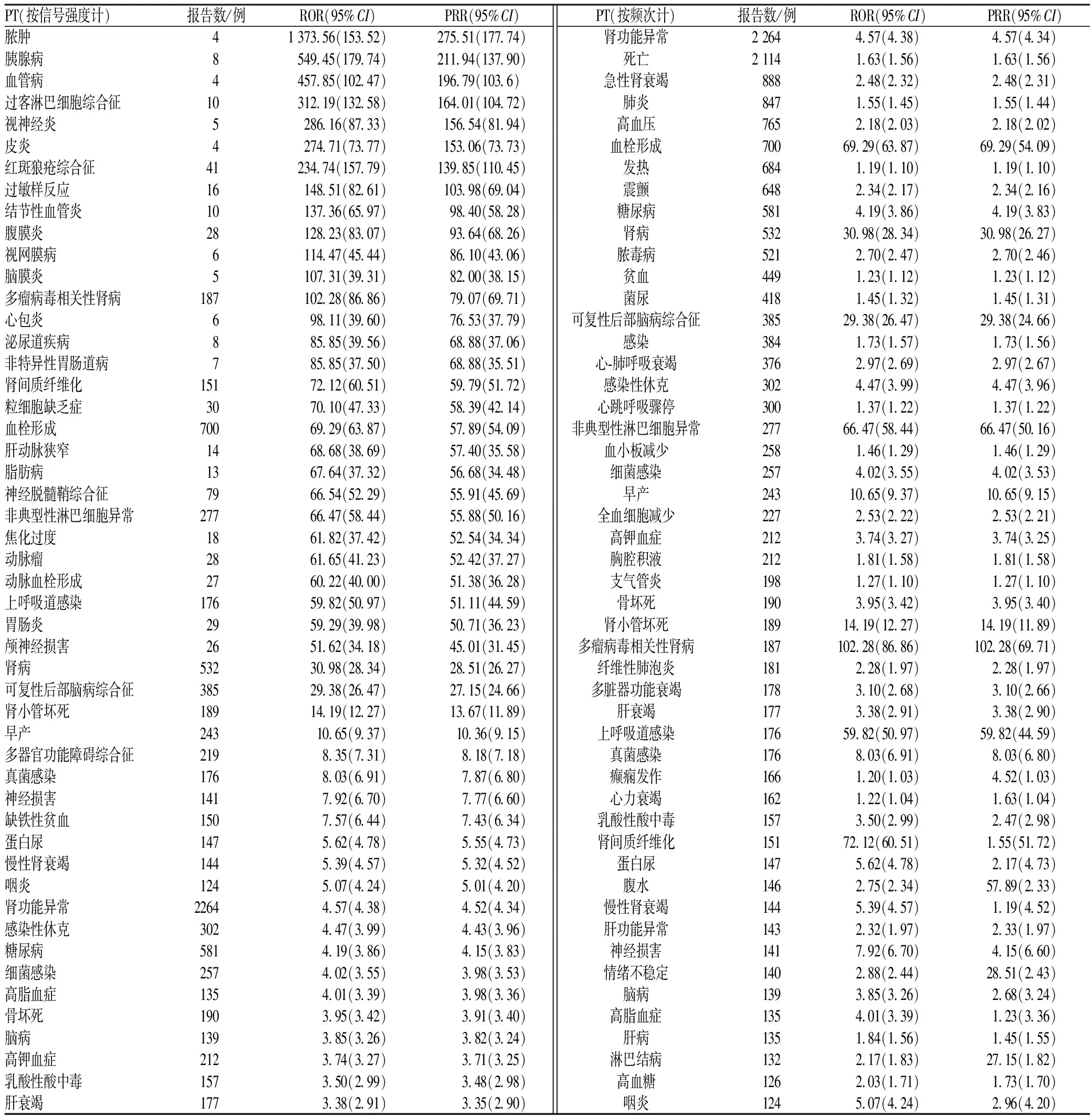
表3 他克莫司致药品不良反应信号强度和报告数居前50位的信号
3.1 新的不良反应
他克莫司所致新的不良反应共涉及8个系统,分别为泌尿系统损害、全身性损害、免疫功能紊乱、呼吸系统损害、白细胞和网状内皮系统异常、肝胆系统损害、肌肉骨骼肌系统损害和胶原组织损害。但大部分与药品说明书中记载的不良反应尚有联系。完全与药品说明书中记载的不良反应无关的信号有骨坏死和纤维性肺泡炎。上述新的不良反应信号需要重点关注。
3.2 研究的局限性
本研究的优点是利用美国FAERS数据库为自发呈报系统,覆盖人群广,数据库容量大[15]。但是,本研究所使用数据仅包含发生不良反应患者的基本信息,存在一定缺陷:(1)患者的诊断不能提供,无法分析药品不良反应与原发疾病的关系;(2)不良反应发生时间特点不能提供,移植患者需长期服用免疫抑制剂,如能明确不良反应的发生主要集中在术后什么阶段,则患者和临床可重点监护此阶段;(3)该数据库不能提供使用他克莫司但未发生不良反应的患者数量,从而无法计算该药整体不良反应发生率[16];(4)报告不够完整、规范导致不同不良反应同种表达或同种不良反应不同表达等,最终与WHO药品不良反应术语集累及的系统、器官相对应时存在差异[17-18];(5)该数据库是针对美国人群,可能与中国人群存在种族差异。

表4 他克莫司致药品不良反应信号与累及器官和(或)系统
注:“*”代表未在他克莫司药品说明书中出现的新的PT
Note:“*” represents new PT that does not include in drug instructions of tacrolimus
本研究所用方法为比例失衡法,该方法简便易行且较为敏感,但容易出现假阳性[19]。同时使用PRR法和ROR法进行计算并提高阈值,筛选出PRR法和ROR法重叠的信号,可以避免假阳性。通过比较他克莫司不良反应信号强度排序和发生频率排序,可以发现他克莫司的不良反应发生次数和经挖掘后得到的信号强度在关联性方面存在着一定程度的差异,如肾功能异常、急性肾衰竭和肺炎等发生频率较高,但信号强度较低,这可能与ROR法和PRR法挖掘药品不良反应的局限性有关。
总之,他克莫司口服给药后吸收不规则,生物利用度差异显著,治疗窗窄。临床用药时,应尽量避免使用对他克莫司代谢干扰大的药物。除药物基因组学因素外,年龄、肝功能和白蛋白水平等对他克莫司血药浓度均有影响。因此,条件允许的情况下,应常规进行血药浓度监测,再根据需要浓度调整剂量,确保安全有效[20]。他克莫司所致不良反应与药品说明书、文献基本一致,其中也发现了维性肺泡炎、骨坏死等新的不良反应,获得了相对真实完整的药品安全信息,可为临床用药提供参考,从而促进临床合理用药。
