应用NAT检测献血者HBsAg ELISA灰区样本的探讨
2020-07-06汪鹏宋晓艳张瑞萍
汪鹏 宋晓艳 张瑞萍

【摘要】
目的:对献血者血样HBsAg ELISA(酶联免疫吸附试验)检测为“灰区”的样本进行核酸检测(NAT),分析灰区样本核酸检测的结果以及核酸检测为阳性结果样本酶联免疫检测情况,探讨献血者HBsAg 酶联免疫检测灰区的设置。 方法:先对2016-2017年献血者56794例血样进行HBsAg 酶联免疫检测,再对Cut off值为0.5≤S/CO<1的366例样本进行核酸检测,统计分析检测结果。 结果:366例灰区样本单试剂双孔复检后无反应性147例,有反应性 219例。核酸检测阳性27例,其中24例酶联免疫检测无反应性,2例为单试剂反应性,1例为灰区样本。结论:献血者血液开展核酸检测技术后,HBsAg酶联免疫检测可不设置灰区;核酸技术与酶联免疫技术联合检测,更加保证献血者血液安全。
【关键词】HBV 灰区;酶联免疫吸附试验;核酸检测
【中图分类号】 R365 【文献标识码】B 【文章编号】2095-6851(2020)06-127-01
我国是HBV高感染的国家,“隐匿性”或“窗口期”感染可能是输血传播HBV的主要潜在危险因素。血站系统主要采用两遍酶联免疫和一遍核酸检测对献血者血液进行筛查。由于酶联免疫方法是一种半定量试验,检测的过程会导致检测结果变异系数较大,使得灰区的范围相对较宽,酶联免疫单试剂检测不合格的比例远大于双试剂检测不合格的比例[1]。假阳性检测结果增加血站向献血者解释的难度,同时增加献血者的心里负担,更增加了血液资源的浪费。核酸检测不仅能使输血传播病原体的残余风险降低,还能缩短病毒感染后检测的窗口期,在检测隐匿性HBV感染方面具有重要意义[2]。笔者以本站2016-2017年HBV酶联免疫检测“灰区”样本366例为研究对象,分析灰区样本复查的结果及核酸检测结果,具体如下。
1 资料与方法
1.1 一般资料 选取2016-2017年我站酶联免疫检测为灰区的样本366例为研究对象,所有样本均按照国家法律规范进行HBV酶联免疫双试剂检测,选取单试剂检测灰区的样本进行核酸检测。
1.2 检测仪器和试剂 仪器:HAMILTON STAR全自动加样仪、FAME 24/20全自动酶联免疫仪、HAMILTON STAR 全自动核酸提取仪、DA3000提取仪、AFD9600荧光PCR扩增仪、ABI7500荧光PCR扩增仪。酶联免疫试剂:乙型肝炎病毒表面抗原诊断试剂盒(上海科华)、乙型肝炎病毒表面抗原诊断试剂盒(北京万泰)。核酸检测试剂:达安基因HBV-DNA/HCV-RNA/HIV-RNA(1型)核酸检测试剂(PCR-荧光法);华益美HBV-DNA/HCV-RNA/HIV-RNA(1型+2型)核酸检测试剂(PCR-荧光法)。仪器设备均处于正常使用状态,试剂均在有效期内使用。
1.3 方法
1.3.1 酶联免疫检测 按照血站技术操作规程(2015版)[3]规定对献血者样本进行酶联免疫初复检检测,设定检测值/临界值(S/CO)在0.5~1.0为实验室的灰区检测范围,初次检测处于灰区的样本再用该厂家试剂双孔复检,复检无反应性判为合格,复检有一孔或两孔有反应性的判为不合格。
1.3.2 核酸检测 挑选酶联免疫检测结果无反应性的和HBsAg单试剂检测有反应性的所有样本采用8混样模式进行核酸检测,混检阳性孔样本再进行拆分检测。阳性判断标准:有明显S型扩增曲线且标本检测结果Ct值≤45,则结果判为有反应性;阴性判断标准:无明显S型扩增曲线,标本检测结果的Ct值为“无值”,且相应的内对照结果Ct值≤40,如果检测的是混合样本,则判定组成该初级混合样本的8个样本为阴性。
1.4 统计 采用SPSS13.0统计软件分析
2 结果
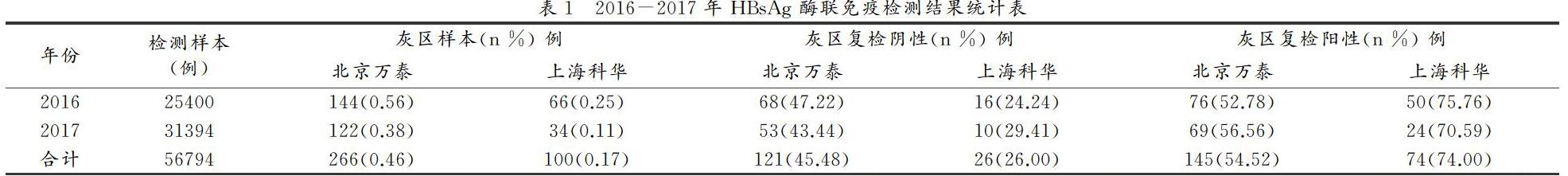
2.1 2016-2017年HBsAg 酶联免疫检测结果(见表1)
2.2 2016-2017年HBV 核酸检测结果(见表2)
2.3 2016-2017年酶联免疫灰区样本核酸检测结果(见表3)
2.4 2016-2017年酶联免疫检测为灰区样本的核酸检测结果(见表4)
3 讨论
3.1 我国是世界人口大国,HBV感染率相对较高,输血传播是主要的感染途径,HBsAg是HBV标志物之一,可以反应HBV感染情况。血站目前采用两遍酶联免疫和一遍核酸模式对献血者血液进行筛查,不同的酶联免疫试剂在血液HBsAg筛查中,表现出不同的灵敏度和特异性,可能是不同试剂厂家的材料来源、检测限、试剂纯度方面差异较大[4],从表1看出,北京万泰HBV试剂初检灰区样本266(0.73)例,高于上海科华100(0.27)例,两者之间比较(P<0.005)有显著性差异,北京万泰试剂复检后无反应性121(45.48)例,有反应性145(54.52)例,上海科华复检后阴性26(26.00),有反应性74(74.00)。
3.2 目前国内对灰区临界设置并无统一的标准,有文献报道设定在0.9-1.1倍CO值区域,也有学者认为可以设置在CO值20%的范围内。统计表1、表2、表3中看出乙肝酶联免疫初次检测为灰区366例的样本,单试剂双孔复检后阴性147例,阳性219例。核酸检测后阳性27例,其中24例酶联免疫检测阴性,2例为酶联免疫检测单试剂阳性,1例为酶联免疫检测灰区样本。卫生部临床检验中心对我们送检的6例核酸检测样本进行了确证,其中3例确证是乙肝感染。
3.3 从表4中可以看出,酶联免疫单试剂复检有反应性样本219例,核酸检测218例无反应性(99.54%),仅有1例酶联免疫复检有反应性,核酸检测阳性。但是单试剂复检有反应性的血液已报废,如果设置有酶联免疫灰区,会导致假阳性率增加(0.38%,218/56794),造成血液的浪费。所以血站开展核酸检测后,灰区的设置是不必要的。
3.4 核酸检测能够缩短乙肝病毒感染的窗口期,其方法的敏感性和特异性优于酶联免疫检测,但是核酸检测对血液标本、检测环境及操作人员技术水平要求较高,如果检测前试剂、样本质量不能保证质量,核酸检测结果也难以保证准确,酶联免疫检测技术成熟,操作相对简单,對设备要求不高,二者联合互补应用,更加能保证临床用血的安全。
参考文献:
[1] 邓雪莲,安万新,梁晓华等.大连市血液中心血清学检测与核酸检测并行的效果观察[J].中国输血杂志,2012,25(1):38-40
[2] 郑剑婷,核酸检测与酶联免疫吸附检测在无偿献血者血液标本乙肝病毒筛查中的应用比较.按摩与康复学,2018,9(3):91-92
[3] 血站技术操作规程(2015版)
[4] 冯娟,血站HBsAg反应性样本的ELISA与PCR法检测结果的相关性.临床输血与检验,2016,18(1):47-50
